Прогнозирование профиля клинических побочных эффектов антидепрессантов из группы ингибиторов обратного захвата серотонина и норадреналина
Автор: Балакин К.В., Лапушкин Г.И., Савилова А.Г., Бовина Е.В., Квашнина Е.А., Воронков А.Э., Васильева Т.М., Скоренко А.В.
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Физико-химическая биология
Статья в выпуске: 1 (33) т.9, 2017 года.
Бесплатный доступ
В работе показана возможность компьютерного прогнозирования профиля побоч- ных эффектов ингибиторов обратного захвата серотонина и норадреналина (ИОЗСН), на основе анализа их мультитаргетного профиля. Были проанализированы побочные эффекты 10 лекарств, ИОЗСН, статистически значимо представленные в базе FDA AERS, а также данные по биомишеням, на которые действуют эти препараты. Расчеты коэффициентов попарного подобия с последующей иерархической кластеризацией по методу Варда позволили разбить соединения на кластеры по профилю подобия по- бочных эффектов, а также по профилю мишень-специфичного действия. Анализ двух иерархических структур выявил выраженное соответствие содержащихся в них кла- стеров. Работа позволяет количественно охарактеризовать профили побочных эффек- тов ИОЗСН, объяснить их существенное различие внутри группы и прогнозировать профиль побочных эффектов для новых ИОЗСН. Результаты работы также создают предпосылки для поиска более общих закономерностей, связывающих пространства побочных эффектов и мишень-специфического действия лекарств, относящихся к раз- личным фармакологическим группам.
Побочные эффекты лекарств, коэффициенты попарного подо- бия, мишень-специфический профиль, кластеризация
Короткий адрес: https://sciup.org/142186176
IDR: 142186176 | УДК: 51.76,
Текст научной статьи Прогнозирование профиля клинических побочных эффектов антидепрессантов из группы ингибиторов обратного захвата серотонина и норадреналина
Прогнозирование побочных эффектов (ПЭ) лекарственных препаратов является актуальной задачей в области разработки и контроля безопасности лекарств. Серьезной проблемой является то обстоятельство, что даже многолетние мультицентровые клинические испытания лекарств, как правило, не приводят к пониманию всех потенциальных опасностей, связанных с применением лекарства. Такое понимание обычно возникает лишь в результате многолетнего клинического применения. Зачастую эти эффекты настолько серьезны, что приводят к необходимости выведения лекарственного препарата с рынка [1]. Отмеченное обстоятельство обуславливает желательность как можно более раннего обнаружения признаков неблагоприятных побочных эффектов.
Появление тех или иных побочных эффектов в основном объясняется действием лекарственного препарата на специфические биомишени, в связи с чем попытки обнаружения системных зависимостей между многочисленными побочными эффектами и сложным профилем мишень-специфичной активности активно обсуждаются в научной литературе [2]– [6]. Однако подобные исследования сопряжены со многими объективными проблемами. Главная из них состоит в недостатке качественных и статистически значимых экспериментальных данных о взаимосвязях между приемом лекарств и конкретными побочными эффектами. В настоящее время эту проблему решают путем создания и многолетнего ведения баз спонтанных отчетов, таких как FDA AERS и другие [7]. Несмотря на очевидную полезность подобных баз, содержащаяся в них информация страдает от многих недостатков, обсуждаемых в литературе [8]. Профиль мишень-специфического действия лекарств оценивают при помощи специализированных баз химико-биологических данных, таких как ChEMBL, PubChem, DrugBank и другие, хотя информация в подобных базах также не лишена недостатков [9].
Ингибиторы обратного захвата серотонина и норадреналина (ИОЗСН) представляют собой группу антидепрессантов, широко используемых в современной фармакологии [10]. Механизм их действия связан с повышением межклеточного уровня указанных нейротрансмиттеров путем ингибирования их обратного захвата пресинаптической ячейкой. Десять исследованных в настоящей работе ИОЗСН (рис. 1) принадлежат пяти структурным хемотипам. Первый хемотип содержит в основе арилоксипропиламиновый фрагмент. Лекарства этого типа проявляют различный профиль селективности по отношению к серотонину и норадреналину в зависимости от заместителя при арилокси-фрагменте. Так, заместители в 2’-положении арилокси-фрагмента (например, Атомоксетин) проявляют предпочтительную активность в отношении норадреналинового, а в 4’-положении (Пароксетин и Флуоксетин) – в отношении серотонинового транспортера. Дулоксетин содержит фенильную группу, конденсированную с положениями 2’- и 3’-арилокси-фрагмента, что обуславливает его двойную селективность к обоим транспортерам. Природа второго ароматического заместителя также имеет существенное влияние на активность и селективность представителей этого хемотипа. 1-(2-Аминоэтил)циклогексональный фрагмент лежит в основе Венлафаксина и Деcвенлафаксина. Величина ингибирующего эффекта и селективность действия этих соединений зависят от заместителей в бензольном кольце. Сертралин, Циталопрам/Эсциталопрам и Трамадол являются представителями еще трех различных структурных хемотипов, обладающих специфическим фармакологическим профилем.
Несмотря на очевидное структурное сходство, а также сходный профиль фармакологической активности, представители ИОЗСН способны проявлять существенно различные побочные эффекты.
В настоящей работе нами была поставлена задача оценить возможности прогнозирования побочных эффектов лекарств, относящихся к группе ИОЗСН, на основе анализа их мишень-специфичного профиля. Эта задача является актуальной на стадии разработки новых антидепрессантов группы ИОЗСН, особенно на этапах клинических испытаний, что потенциально позволяет минимизировать риски для пациентов, а также оптимизировать способ терапевтического применения.
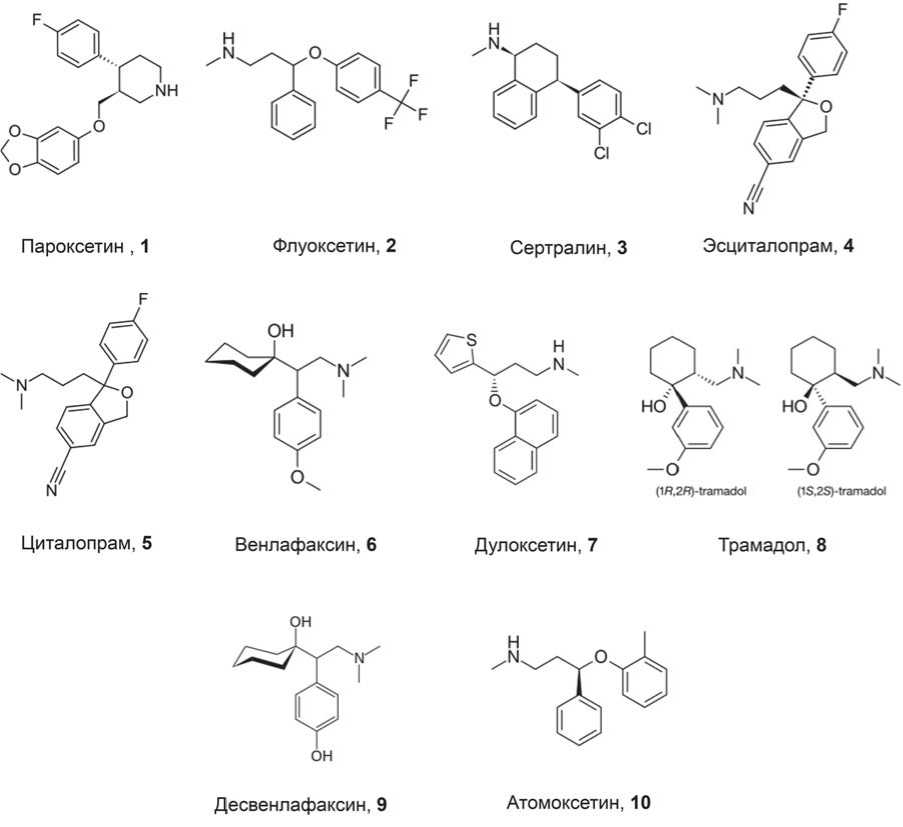
Рис. 1. Структурные формулы ИОЗСН, исследованных в настоящей работе
2. Экспериментальная часть 2.1. Данные по побочным эффектам лекарств
В настоящей работе были использованы данные из базы FDA AERS, находящиеся в публичном доступе [7]. Наименования побочных эффектов соответствуют терминологии международной классификации MedDRA [11]. Для обработки были выбраны данные с 1-го квартала 2009 года по 3-й квартал 2012 года включительно, что в общей сложности составило 2 309 920 отчетов, при этом в 992 246 отчетах было назначено только одно лекарство. Из всех сообщений об одиночных назначениях были отобраны сообщения для 255 наиболее часто встречающихся лекарств; в этих сообщениях находятся данные о 1 458 366 случаях побочных эффектов, что составляет 82% от общей статистики по одиночным назначениям. В числе этих 255 отобранных лекарств находится также группа ИОЗСН (10 лекарств), для которых имеется следующее количество сообщений: Пароксетин – 3060, Флуоксетин – 806, Сертралин – 3288, Эсциталопрам – 1187, Циталопрам – 1190, Венлафаксин – 215, Дулоксетин – 3091, Трамадол – 757, Десвенлафаксин – 5108, Атомоксетин – 660. Лекарства были переименованы в соответствии с международными непатентованными наименованиями (МНН).
2.2. Расчет величин PRR
Коэффициент [12] представляет собой отношение вероятности проявления определённого побочного эффекта в общем наборе побочных эффектов для данного лекарства к вероятности этого побочного эффекта в общем наборе данных, исключая данные по выбранному лекарству. Расчет производился по следующей формуле:
PRR = n 11 ( n 01 + n 00 ) /n oi ( n ii + n 10 ) , (1)
где n 11 – количество случаев данного ПЭ для данного лекарства, n 01 – количество случаев этого же ПЭ для всех прочих лекарств, n 10 – количество случаев всех прочих ПЭ для данного лекарства, n 00 – количество случаев всех прочих ПЭ для всех прочих лекарств. Обычно считается [13], что PRR > 3 указывает на наличие взаимосвязи между приемом лекарства и конкретным побочным эффектом.
2.3. Расчет коэффициентов подобия
Для расчета коэффициентов попарного подобия профиля побочных эффектов лекарств в качестве дескрипторов использовались величины PRR (1), рассчитанные, как указано в предыдущем разделе. Для расчета коэффициентов подобия мишень-специфического профиля использовали полуколичественные данные по in vitro активности соединений по отношению к 28 биомишеням, полученные из базы ChEMBL [14]. Были использованы следующие уровни активности in vitro : 3 – очень высокая ( Ki < 1 нМ), 2 – высокая ( Ki > > 1–100 нМ), 1 – умеренная ( Ki > 100–1000 нМ), 0 – активность низкая или отсутствует ( Ki > 1000 нМ). Коэффициенты подобия рассчитывали с использованием метрик Танимо-то, Эвклида и Ходжкина по формулам непрерывных величин [15].
3. Результаты и обсуждение 3.1. Оценка подобия профиля побочных эффектов
На первом этапе для каждого из 255 лекарственных соединений, отобранных из базы FDA AERS, мы рассчитали значения PRR (1) для побочных эффектов, соответствующих классификации MedDRA. Эта классификация является иерархической и поделена на 4 уровня. Величины PRR были рассчитаны для каждого из этих уровней. В результате мы получили четыре двумерных матрицы, в которых каждому из 255 препаратов соответствовал набор величин PRR длиной от 26 дескрипторов (верхний, 1-й уровень классификации MedDRA) до 6966 дескрипторов (нижний, 4-й уровень классификации MedDRA). Каждая строка в этих матрицах фактически описывает профиль побочных эффектов для соответствующего лекарства. В качестве иллюстрации на рис. 2 приведены профили побочных эффектов Дулоксетина и Флуоксетина на 1-м уровне классификации MedDRA (показаны только побочные эффекты c PRR >2).
Подобная структура данных позволила нам рассчитать для каждого из 255 соединений, отобранных из базы FDA AERS, попарные коэффициенты подобия ПЭ, используя общепринятые метрики подобия – Танимото, Эвклида и Ходжкина [15]. Во всех дальнейших экспериментах были применены коэффициенты Ходжкина, хотя метрики Танимото и Ходжкина являются взаимно высококоррелированными и обеспечивают сопоставимые результаты. Эвклидова метрика оказалась неэффективной вследствие значительного влияния статистического шума: большое количество дескрипторов со случайными малыми значениями в итоге приводит к значительному ослаблению полезного сигнала.
Полученные на первом этапе работы данные являются чрезвычайно полезными в целях количественной оценки подобия ПЭ между любыми парами лекарственных соединений.
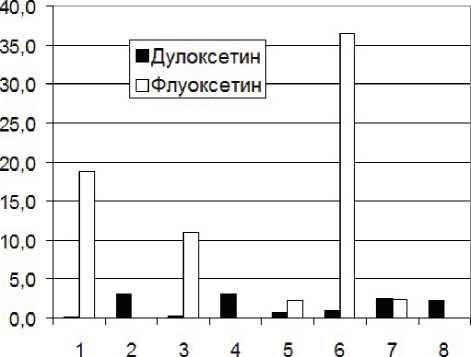
Номер побочного эффекта
Рис. 2. Профили побочных эффектов Дулоксетина и Флуоксетина (уровень 1 классификации MedDRA). Показаны только группы эффектов, для которых расчетные значения критерия PRR для любого из препаратов превышают 2. Соответствие номеров и групп побочных эффектов: 1 – генетические нарушения, 2 – заболевания уха, 3 – эндокринные нарушения, 4 – гепатобилиарные расстройства, 5 – метаболитические нарушения, 6 – патологии, влияющие на нормальное протекание беременности и родов, 7 – психиатрические расстройства, 8 – нарушения, приводящие к хирургическому вмешательству
3.2. Кривые обогащения
На следующем этапе предстояло оценить, насколько качественно полученные коэффициенты подобия ПЭ описывают реальную степень подобия соединений, входящих в родственные по типу фармакологического действия группы. Для этого мы провели модельный эксперимент, позволяющий оценить степень обогащения начальных позиций полученной базы 255 соединений, сортированных по убыванию подобия к отдельным представителям группы ИОЗСН, оставшимися представителями этой же группы. Подобный эксперимент широко применяется для оценки эффективности различных рейтинговых критериев [16].
Для каждого из четырех уровней классификации MedDRA, в каждом из десяти отдельных экспериментов, все 255 соединений были отсортированы в соответствии с убыванием подобия ПЭ к одному из препаратов, представителей группы ИОЗСН (препаратов-«зондов»). На рис. 3 представлены усредненные по 10 экспериментам кривые накопления ингибиторов обратного захвата серотонина для каждого из 4-х уровней классификации MedDRA. Кривые соответствуют графикам накопления хитов, соответствующим каждому из 10 ИОЗСН в качестве «зонда». При сортировке соединений в соответствии с подобием ПЭ к выбранному «зонду», в качестве хитов рассматривались оставшиеся 9 соединений из данной группы. Каждая кривая показывает общий усредненный по 10 экспериментам результат (усреднение проводилось по количеству хитов в каждой позиции ранжированного списка от 1 до 255). Прямая диагональная линия соответствует случайному распределению соединений в несортированной выборке.
Обогащение хитами начальных позиций ранжированных списков наблюдается для всех уровней классификации. В соответствии с рис. 3, начальная скорость обогащения хитами примерно одинакова для уровней 2–4, а самый высокий 1-й уровень (26 дескрипторов) обеспечивает минимальное начальное обогащение. Такой результат кажется вполне логичным, так как очевидна существенная потеря информации при подобном загрублении сигнала на верхнем уровне.
Рис. 4 показывает среднее положение каждого из 10 исследованных представителей группы ИОЗСН в ранжированных списках, по всем четырем уровням классификации
MedDRA. Так, соединения 7–10 условно составляют группу «ранних» хитов, которые в среднем появляются в ранжированных списках на позициях 25–40. Cоединения 1–3 можно отнести к «поздним» хитам, поскольку их типичное положение в ранжированном списке соответствует номерам 90–110. Промежуточное положение, хотя и ближе к «ранним» хитам, занимают соединения 4–6, появляющиеся в типичном случае на позициях 50–55. Очевидно, «поздние» хиты, и в особенности Пароксетин 1, по своему профилю побочных эффектов относятся к атипичным представителям исследуемой группы антидепрессантов, что находит свое отражение в относительно низкой степени их подобия к другим ИОЗСН.
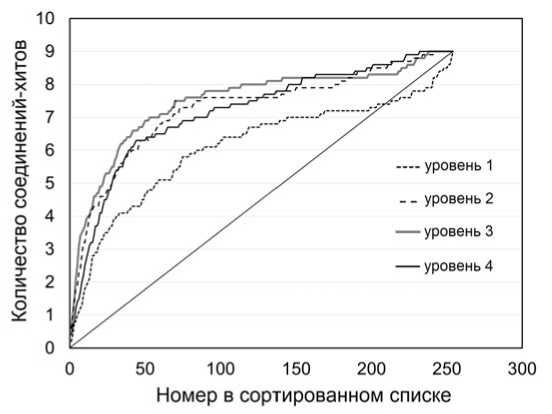
Рис. 3. Усредненные накопительные кривые ИОЗСН для четырех уровней классификации MedDRA
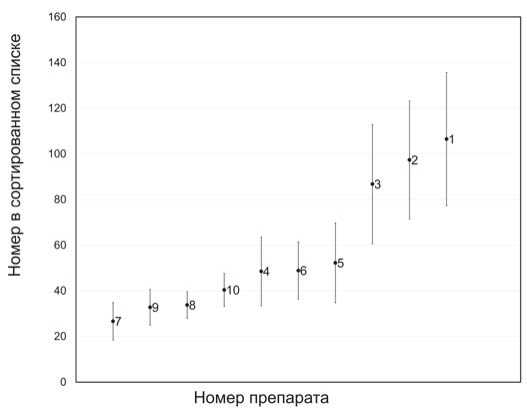
Рис. 4. Позиции хитов в сортировочной выборке для группы ИОЗСН, усредненные по четырем уровням классификации MedDRA. Указаны доверительные интервалы, соответствующие уровню вероятности 95%. Номера соответствуют структурам, представленным на рис. 1
Представляет значительный интерес выяснение причин подобной атипичности отдельных соединений. Для выяснения этих причин, а также в целях объяснения наблюдаемых различий ПЭ фармакологически родственных соединений в целом на следующем этапе исследования мы проанализировали зависимости между профилями ПЭ и профилями муль-титаргетного действия исследуемых лекарств.
3.3. Оценка подобия профилей мишень-специфического действия
Выше было отмечено, что исследуемые препараты принадлежат к пяти различным структурным хемотипам. Несмотря на определенные структурные отличия хемотипов, являясь фармакофорными аналогами серотонина и норадреналина, все 10 соединений обладают сходными особенностями расположения фармакофорных элементов (ароматические и циклоалифатические фрагменты, основная аминогруппа, акцептор водородной связи), обуславливающими высокую аффинность к их основным биомишеням – натрий-зависимым транспортерам серотонина и норадреналина (константа ингибирования Ki в диапазоне от 0,04 нМ до 10–15 нМ). Однако детальный анализ базы ChEMBL, содержащей сведения об активности лекарств по отношению к широкому разнообразию биомишеней, показал, что профиль мишень-специфического действия исследуемых препаратов не исчерпывается двумя основными мишенями и является весьма сложным. Так, в соответствии с данными ChEMBL, суммарно они действуют не менее чем на 28 различных биомишеней, представленных в табл. 1. Кроме основных биомишеней, исследуемые соединения могут также действовать на допаминовый транспортер, гистаминовые рецепторы, альфа-адренорецепторы, мускариновые ацетилхолиновые, опиоидные, серотониновые рецепторы и ряд других. В ряде случаев наблюдается довольно высокая активность по отношению к неосновным биомишеням в диапазоне Ki = 1÷100 нМ. Можно предположить, что наличие подобных активностей способно приводить к появлению специфических побочных эффектов.
Возникает закономерный и интригующий вопрос: в состоянии ли мы обнаружить взаимосвязь между наблюдаемым профилем клинических побочных эффектов лекарств и тонкими различиями в мультитаргетном профиле, представленном в табл. 1. Для ответа на этот вопрос мы воспользовались подходом для количественной оценки подобия мишень-специфичного профиля, аналогичным описанному выше для оценки подобия побочных эффектов. А именно, используя полуколичественные данные для всех 28 мишеней из табл. 1, мы рассчитали попарные коэффициенты подобия мишень-специфического действия (коэффициенты Ходжкина). В данной работе используются следующие уровни in vitro -активности: 3 – очень высокая ( Ki < 1 нМ), 2 – высокая ( Ki = 1÷100 нМ), 1 – умеренная ( Ki = 100÷1000 нМ), 0 – активность низкая или отсутствует ( Ki > 1000 нМ). Использование полуколичественных данных связано с часто встречающейся вариабельностью величин Ki для одного и того же соединения в базе ChEMBL.
Таблица1
Профили in vitro мишень-специфичной активности исследуемых соединений (по данным базы c hem BL)
|
Биомишень (по данным исследования in vitro ) |
Активность in vitro , усл. ед. |
|||||||||
|
к s н Ф С к |
в В <и о И О В Ө |
к к В св л н л <и и |
S о ч св в S' о m |
S св в о в св в У |
в св 'flee в в <и m |
и S Ф У |
в о S св н |
Ф к И Ф ^ |
И S ф О о <1 |
|
|
Натрий-зависимый переносчик серотонина |
3 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
|
Натрий-зависимый переносчик норадреналина |
2 |
0 |
1 |
1 |
0 |
1 |
2 |
1 |
1 |
1 |
|
Натрий-зависимый переносчик дофамина |
0 |
0 |
2 |
1 |
0 |
1 |
1 |
0 |
0 |
0 |
|
Белок множественной лекарственной устойчивости |
1 |
1 |
1 |
0 |
1 |
1 |
0 |
0 |
0 |
0 |
|
АТФ-связывающий кассетный белок |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
0 |
0 |
|
H1-гистаминовый рецептор |
0 |
0 |
0 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
|
H3-гистаминовый рецептор |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
α -1A-адренорецептор |
0 |
0 |
0 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
|
α -1D-адренорецептор |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
|
α -2A-адренорецептор |
0 |
0 |
2 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
Биомишень (по данным исследования in vitro ) |
Активность in vitro , усл. ед. |
|||||||||
|
к s и ф и С у К |
к S н ф is ч Ө |
к к Ч св л н л <и и |
о ч св в S' m |
S св о в св в У |
в К И ф m |
И S ф У |
в о ч: св св н |
ф к И ф Ч |
И S ф О о |
|
|
α -2B-адренорецептор |
0 |
1 |
2 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
α -2C-адренорецептор |
0 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
α - субъединица никотинового ацетилхолинового рецептора |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
|
M1-ацетилхолиновый мускариновый рецептор |
2 |
1 |
1 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
|
M2-ацетилхолиновый мускариновый рецептор |
1 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
M3-ацетилхолиновый мускариновый рецептор |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
|
M4-ацетилхолиновый мускариновый рецептор |
2 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
M5-ацетилхолиновый мускариновый рецептор |
2 |
1 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
δ -опиоидный рецептор |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
|
μ -опиоидный рецептор |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
|
κ -опиоидный рецептор |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
|
σ -опиоидный рецептор |
0 |
1 |
2 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
|
5-HT2A-рецептор |
1 |
2 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
5-HT2B-рецептор |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
|
5-HT2C-рецептор |
0 |
2 |
1 |
0 |
1 |
0 |
0 |
1 |
0 |
0 |
|
5-HT6-рецептор |
0 |
1 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
|
NR1-3a-субъединица глутаматного NMDA-рецептора |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
1 |
0 |
0 |
3.4. Кластеризация на основе коэффициентов попарного подобия
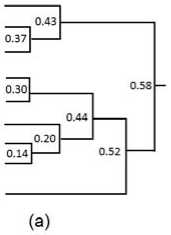
Рассчитанные коэффициенты попарного подобия побочных эффектов и мишень-специфического действия позволяют нам кластеризовать исследуемые молекулы. В настоящей работе для решения этой задачи мы использовали метод иерархической кластеризации (метод Варда) [17]. Использовались коэффициенты подобия ПЭ, рассчитанные на основе величин (1), полученных для 1-го уровня классификации MedDRA, а также коэффициенты подобия мишень-специфического действия, рассчитанные на основе полуколичественных показателей активности по отношению к 28 мишеням (табл. 1). Полученные в результате соответствующие иерархические кластерные структуры представлены на рис. 5.
Несмотря на некоторую условность разделения на «ранние», «промежуточные» и «поздние» группы хитов, далее мы продолжаем пользоваться этой терминологией в целях удобства. Первый вывод, который можно сделать на основе анализа (рис. 5), – это выраженное сходство структур обеих иерархий, соответствующих профилю биомишеней (рис. 5а) и побочных эффектов (рис. 5б). Так, совершенно отчетливо тройка «поздних хитов» (рис. 4), ранее охарактеризованных нами как атипичные представители ИОЗСН, – Пароксетин, Флуоксетин и Сертралин, в обоих случаях образует выраженный кластер, далеко отстоящий от «ранних» и «промежуточных» хитов. Три из четырех представителей «ранних» хитов – Атомоксетин, Десвенлафаксин и Дулоксетин – также в обеих иерархиях занимают выраженный отдельный кластер. Характерно, что «промежуточные» хиты – Циталопрам, Эсциталопрам, Венлафаксин и один представитель «ранних» хитов Трамадол занимают и в полученных иерархиях промежуточные положения, появляясь то в кластере «поздних» (например, Эсциталопрам в профиле побочных эффектов), то в кластере «ранних» (например, Венлафаксин в профиле мишеней) хитов. Указанное обстоятельство указывает на действительно промежуточный характер этой группы соединений, что не позволяет достоверно определить их позицию в условиях проведенного эксперимента.
Показательно, что небольшие модификации в алгоритме кластеризации, а именно использование алгоритма единичной связи (single-linkage) вместо алгоритма усреднения по группе (group-average) в методе Варда, способны приводить к изменениям в структуре иерархий (данные не показаны). По-прежнему в обеих иерархиях имеются отдельные кла- стеры для «поздних» и «ранних» хитов, тогда как «промежуточные» хиты способны попадать как в те, так и другие кластеры. Такая ситуация характерна для случаев, когда межкластерные различия являются минимальными, что и соответствует реальности для представителей «промежуточной» группы. При этом ни в одной из созданных иерархий на рис. 5 не отмечено случаев, чтобы «поздние» и «ранние» хиты попадали в один кластер.
Профиль мишень-специфичной активности
Профиль побочных эффектов
Пароксетин Флуоксетин Сертралин
Циталопрам Эсциталопрам Венлафаксин Дулоксетин Десвенлафаксин Атомоксетин
Трамадол
Пароксетин
Флуоксетин
Сертралин Эсциталопрам
Циталопрам Венлафаксин
Трамадол Десвенлафаксин Дулоксетин Атомоксетин
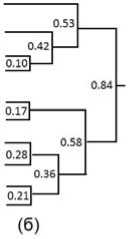
Рис. 5. Иерархическая кластеризация по методу Варда (алгоритм усреднения по группе), основанная на коэффициентах попарного подобия Ходжкина. (а) Профиль мишень-специфичной активности, 28 мишеней. (б) Профиль побочных эффектов, 26 групп (1 уровень классификации MedDRA). Указаны нормированные дистанции (D) между группами, D = 1 – SC, где SC – коэффициент подобия
Наибольшей атипичностью, как и ранее на рис. 4, характеризуется Пароксетин, который во всех экспериментах занимает отдельный кластер, далеко отстоящий как от своих ближайших соседей, Флуоксетина и Сертралина, так и в существенно большей степени от остальных соединений. Причинами подобного поведения являются, по всей видимости, выраженные особенности профиля его мишень-специфичной активности (табл. 1). Так, Пароксетин обладает наивысшей из всех исследованных соединений активностью по отношению к основной мишени – натрий-зависимому транспортеру серотонина с Ki = 0,04 нМ, то есть почти на 2 порядка активнее, чем другие ИОЗСН. Кроме того, Пароксетин отличается высокой активностью по отношению к мускариновым ацетилхолиновым рецепторам М1–М5 ( Ki = 30÷190 нМ). Эти особенности резко выделяют Пароксетин на фоне остальных препаратов.
Можно сделать вывод, что при помощи описанных экспериментов мы обнаружили соответствие расчетных, количественно описанных профилей побочных эффектов и мишень-специфичной активности 10 антидепрессантов, представителей группы ИОЗСН. Мы продемонстрировали подход для оценки особенностей профиля побочных эффектов ИОЗСН на основе анализа in vitro активности на небольшой панели биомишеней.
С точки зрения традиционного QSAR-анализа с помощью разработанного подхода мы можем проводить классификационное отнесение соединений к одной из трех условных групп ИОЗСН – «ранние», «поздние» и «промежуточные» хиты, находя при этом соответствия в профиле побочных эффектов, описываемых первым, самым верхним уровнем классификации MedDRA. При этом соединения, относящиеся к «промежуточному» типу, имеют склонность попадать то в «ранние», то в «поздние» кластеры, в зависимости от варианта используемого алгоритма кластеризации. На основании этих результатов можно предположить, что достигнутая точность прогнозирования является предельной или близкой к таковой для имеющихся в нашем распоряжении информационных массивов. Не исключены, впрочем, возможности для успешного анализа и интерпретации более тонких феноменов, объясняющих появление тех или иных побочных эффектов в зависимости от влияния на конкретные биомишени. В этом смысле разработанный инструментарий может оказаться весьма полезным и наглядным как для разработчиков лекарств, так и для практикующих клиницистов.
С практической точки зрения развитие исследований подобного рода может иметь значительные положительные следствия для разработки лекарственных препаратов.
Например, для новых представителей фармакологической группы ИОЗСН имеет смысл уже на доклинических этапах провести in vitro эксперимент на панели из 28 мишеней (табл. 1). По результатам этого эксперимента соединение можно будет отнести к одному из типов, условно называемых в этой работе «ранними», «промежуточными» и «поздними». Такое отнесение потенциально позволяет прогнозировать профиль его побочных эффектов, что еще на доклинических этапах может способствовать уточнению и корректировке отдельных аспектов безопасности при помощи доклинических моделей. Если учесть, что подобный in vitro анализ можно провести за несколько дней, а выяснение профиля клинических побочных эффектов лекарств занимает годы, если не десятилетия, и сопряжено со значительными рисками для здоровья пациентов, то понятно, что такая возможность является весьма ценной. Уместно отметить, что развитие методов компьютерного прогнозирования эффективности взаимодействия между низкомолекулярными соединениями и белковыми биомишенями, например, основанных на инструментах молекулярного докинга или иных методах, теоретически позволяет обойтись без in vitro эксперимента на мишенях и прогнозировать интересующие нас эффекты в режиме компьютерного, виртуального скрининга.
Следует отметить, что структурный фактор не играет решающей роли в определении потенциального профиля побочных эффектов лекарств. Отсутствие выраженной связи такого рода можно также продемонстрировать на примерах соединений, соответствующих определенным молекулярным скаффолдам. Так, соединения, содержащие в своей структуре арилоксипропиламиновый фрагмент, относятся как к «ранним» (Атомоксетин, Дулоксетин), так и «поздним» (Пароксетин, Флуоксетин) хитам и существенно отличаются по профилям побочных эффектов. Впрочем, в случаях высокого структурного подобия соединений, из которого непосредственно вытекает близкое сходство мишень-специфического профиля, возможно проявление сходного профиля побочных эффектов. Однако это наблюдение лишь подтверждает вывод о том, что решающее значение в проявлении специфических клинических побочных эффектов соединений играет профиль их мультитаргетного действия и лишь опосредованно – структурное сходство.
4. Выводы
В настоящей работе был разработан подход к оценке подобия профиля побочных эффектов лекарств. В его основе лежит расчет параметра PRR, являющегося критерием взаимосвязи между приемом лекарства и побочным эффектом, с дальнейшим использованием традиционных в хемоинформатике метрик подобия. Было обнаружено соответствие количественно описанных профилей побочных эффектов и мишень-специфичной активности 10 антидепрессантов, представителей группы ингибиторов обратного захвата серотонина и норадреналина. Продемонстрирована возможность оценки профиля их побочных эффектов на основе анализа in vitro активности на относительно небольшой панели биомишеней. Следует при этом отметить, что описанный подход не претендует на прогнозирование побочных эффектов лекарств, связанных с индивидуальными гено- и фенотипическими особенностями пациентов.
Мы также ожидаем, что и для больших массивов лекарственных препаратов с известными профилями побочных эффектов и мишень-специфичной активности можно обнаружить выраженные связи, поддающиеся количественной оценке на основе подходов, предложенных в настоящей работе. Подобная возможность будет способствовать более эффективной оценке безопасности новых лекарственных кандидатов.
Список литературы Прогнозирование профиля клинических побочных эффектов антидепрессантов из группы ингибиторов обратного захвата серотонина и норадреналина
- Pharmaceutical data mining: approaches and applications for drug discovery/Ed. by K.V. Balakin. Hoboken: John Wiley & Sons, Inc., 2010.
- Liu X., She Z., Xue Y., Li Z.R., Yang S.Y., Chen Y.Z. In silico prediction of adverse drug reactions and toxicities based on structural, biological and clinical data//Current Drug Safety. 2012. V. 7, N 3. P. 225-237.
- Yamanishi Y., Pauwels E., Kotera M. Drug side-effect prediction based on the integration of chemical and biological spaces//J. Chem. Inf. Model. 2012. V. 52, N 12. P. 3284-3292.
- Lounkine E., Keiser M.J., Whitebread S., Mikhailov D., Hamon J., Jenkins J., Lavan P., Weber E., Doak A.K., Cote S., Shoichet B.K., Urban L. Large-scale prediction and testing of drug activity on side-effect targets//Nature. 2012. V. 486, N 7403. P. 361-367.
- Bowes J., Brown A.J., Hamon J., Jarolimek W., Sridhar A., Waldron G., Whitebread S. Reducing safety-related drug attrition: the use of in vitro pharmacological profiling//Nat. Rev. Drug Discov. 2012. V. 11, N 12. P. 909-922.
- Pan J.B., Ji N., Pan W., Hong R., Wang H., Ji Z.L. High-throughput identification of off-targets for the mechanistic study of severe adverse drug reactions induced by analgesics//Toxicol. Appl. Pharmacol. 2014. V. 274, N 1. P. 24-34.
- Sakaeda T., Tamon A., Kadoyama K., Okuno Y. Data mining of the public version of the FDA Adverse Event Reporting System//Int. J. Med. Sci. 2013. V. 10, N 7. P. 796-803.
- Hazell L., Shakir S.A. Under-reporting of adverse drug reactions: a systematic review//Drug Safety. 2006. V. 29, N 5. P. 385-396.
- Williams A.J., Ekins S., Tkachenko V. Towards a gold standard: regarding quality in public domain chemistry databases and approaches to improving the situation//Drug Discov. Today. 2012. V. 17, N 13-14. P. 685-701.
- Humble M. Noradrenaline and serotonin reuptake inhibition as clinical principles: a review of antidepressant effi//Acta Psychiatr. Scand. 2000. N 101 (Suppl. 402). P. 28-36.
- Bousquet C., Sadou E., Souvignet J., Jaulent M.C., Declerck G. Formalizing MedDRA to support semantic reasoning on adverse drug reaction terms//J. Biomed. Inform. 2014. V. 49, June 2014. P. 282-291.
- Evans S.J., Waller P.C., Davis S. Use of proportional reporting ratios (PRRs) for signal generation from spontaneous adverse drug reaction reports//Pharmacoepidemiol. Drug Safety. 2001. V. 10, N 6. P. 483-486.
- van Puijenbroek E.P., Bate A., Leufkens H.G.M., Lindquist M., Orre R., Egberts A.C.G. A comparison of measures of disproportionality for signal detection in spontaneous reporting systems for adverse drug reactions//Pharmacoepidemiol. Drug Safety. 2002. V. 11, N 1. P. 3-10.
- Bento A.P., Gaulton A., Hersey A., Bellis L.J., Chambers J., Davies M., Kruger F.A., Light Y., Mak L., McGlinchey S., Nowotka M., Papadatos G., Santos R., Overington J.P. The ChEMBL bioactivity database: an update//Nucleic Acids Res. 2014. V. 42, Database issue. P. D1083-D1090.
- Timmerman H., Roberto T., Consonni V., Mannhold R., Kubinyi H. Handbook of Molecular Descriptors. Weinheim: Wiley-VCH, 2002.
- Fawcett T. An introduction to ROC analysis//Pattern Recognition Lett. 2006. V. 27, N 8. P. 861-874.
- Ward J. H. Hierarchical grouping to optimize an objective function//J. Am. Statistic. Assoc. 1963. V. 58, N 301. P. 236-244.


