Прогнозирование развития нежелательных явлений химиотерапии у лиц с впервые выявленным туберкулезом легких
Автор: Данилов А.Н., Морозова Т.И., Докторова Н.П.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Фтизиатрия
Статья в выпуске: 4 т.11, 2015 года.
Бесплатный доступ
Цель: разработка критериев и метода прогнозирования возникновения побочных неблагоприятных эффектов при первом режиме химиотерапии у лиц с впервые выявленным туберкулезом. Материал и методы. У 214 человек, получавших первый режим химиотерапии, проведен анализ побочных реакций (ПР) на противотуберкулезные препараты (ПТП). В ходе лечения у больных оценивались показатель качества жизни по методике САН, состояние межсистемного взаимодействия дыхательной и сердечно-сосудистой систем организма (коэффициент Хильдебранта), вегетативный индекс Кердо. Результаты. Нежелательные эффекты на ПТП развиваются у каждого третьего больного (33,6%). Установлена зависимость развития разных типов ПР от возрастного ценза и наличия сопутствующей патологии. Аллергические реакции достоверно чаще развиваются у пациентов с эндокринной патологией (27,8%), токсические — у больных с поражением нервной системы (56,3%). Степень изменения индекса Кердо 59,4±2,4%, коэффициента Хильдебранта — 48,9±1,6% в первые 4 недели лечения больного соответствует возникновению ПР в первые 3 месяца химиотерапии. Заключение. Динамика коэффициента Хильдебранта, индекса Кердо и показателя САН на начальных этапах лечения в значительной мере ассоциирована с риском развития побочных эффектов химиотерапии и явилась основой компьютерной экспертно-консультативной системы для прогнозирования развития данных осложнений. Прогностическая ценность системы составляет 76,3% чувствительности при 84,7% специфичности.
Лечение, нежелательные явления, побочные реакции, прогноз, туберкулез легких, химиотерапия
Короткий адрес: https://sciup.org/14918202
IDR: 14918202
Prognosis of development of unfavorable phenomena of chemotherapy in patients with for the first time revealed tuberculosis of lungs
Aim: development of criteria and a method of prognosing of emergence of adverse side effects to the first mode of chemotherapy at patients with for the first time revealed tuberculosis. Materials and Methods: The analysis of the collateral reactions (CR) on tubercular preparations has been carried out at 214 patients receiving treatment at the first mode of chemotherapy. During the treatment an indicator of quality of life by a technique the DIGNITY (health, activity, mood), a condition of intersystem interaction of respiratory and cardiovascular systems of an organism (Hildebrant's coefficient), a vegetative index of Kerdo were estimated at patients. Results. Ufavorable effects on PTP develop at every third patient (33,6%). The CR different types depends on the age and availability of the accompanying pathology. Allergic reactions develop at patients with existence of endocrine pathology (27,8%) authentically more often, toxic — at patients with defeats of nervous system (56,3%). Extent of change of an index of Kerdo of 59,4±2,4%, Hildebrant's coefficient 48,9± 1,6% in the first 4 weeks of treatment of the patient corresponds to emergence of CR in the first 3 months of chemotherapy. Conclusion. Dynamics of coefficient of Hildebrant, Kerdo's index and an indicator of treatment, SAN at the initial stages, are considerably associated with the risk of development of side effects of chemotherapy and were a basis of the developed computer system expert for prognosing the development of these complications. The predictive value of system is 76,3% of sensitivity at 84,7% of specificity.
Текст научной статьи Прогнозирование развития нежелательных явлений химиотерапии у лиц с впервые выявленным туберкулезом легких
-
1 Введение. Химиотерапия служит основным методом лечения туберкулеза путем длительного применения оптимальной комбинации лекарственных средств, подавляющих размножение микобактерий туберкулеза или уничтожающих их в организме. Режим химиотерапии выбирается на основании определения лекарственной чувствительности микобактерий туберкулеза, выделенных из патологического материала [1]. Среди сложностей, возникающих в процессе лечения пациентов, особое место занимают неблагоприятные побочные реакции (ПР) применяемых химиотерапевтических средств [2–6]. Наиболее частые нежелательные явления (НЯ): тошнота, рвота, диарея, артралгия, гипокалиемия, гепатит, ототоксические и аллергические реакции. Реже возникают гипотиреоз, нейропсихические расстройства и нефротоксические реакции [7–9]. Важно отметить, что некоторые неблагоприятные побочные реакции могут представлять угрозу жизни пациента, если их своевременно не диагностировать и не купировать. Если ПР не устраняются должным образом, существует высокий риск отрыва от лечения и получения неудовлетворительных результатов от проводимой терапии [10]. Таким образом, разработка надежных методов прогнозирования развития возможных НЯ перед началом химиотерапии является актуальной и несомненно имеет большое практическое значение.
Цель исследования: разработка критериев и метода прогнозирования возникновения побочных нежелательных эффектов при первом режиме химиотерапии у лиц с впервые выявленным туберкулезом.
Материал и методы. Дизайн исследования: проспективное сплошное нерандомизированное. Отбор популяции: больные с впервые установленным диагнозом инфильтративного туберкулеза легких за 2 года в Саратовской области (2013–2014). Формирование выборки больных, включенных в исследование, произведено на основе критериев включения и исключения.
Критерии включения: наличие впервые выявленного инфильтративного туберкулеза органов дыхания; наличие положительного результата микроскопического исследования мокроты на кислотоустойчивые микобактерии, подтвержденного результатами посева на твердые или жидкие питательные среды (BACTEC MGIT™ 960); наличие результата теста на лекарственную чувствительность к противотуберкулезным препаратам (ТЛЧ) с использованием молекулярно-генетических методов (XpertMTB/Rif®; биологические микрочипы); отсутствие лекарственной устойчивости к противотуберкулезным препаратам, подтвержденное в первые две недели наблюдения; отсутствие в анамнезе указаний на прием противотуберкулезных препаратов основного ряда (изониазид, рифампицин, пиразинамид, этамбутол) более одного месяца и на прием фторхинолонов длительностью более одной недели в течение 6 месяцев до момента включения в исследование; проведение интенсивной фазы химиотерапии по первому режиму согласно приказу МЗ РФ от 29.12.14 №951 «Об утверждении методических рекомендаций по совершенствованию диагностики и лечения туберкулеза органов дыхания»: изониазид, рифампицин, пиразинамид, этамбутол [11]; лица обоего пола в возрасте от 18 до 67 лет (включительно). Критерии ис-
ключения: наличие сопутствующей патологии в стадии декомпенсации, наличие ВИЧ-инфекции, объем терапии менее 60 доз.
В исследование включены 214 человек. По гендерному признаку распределение было следующим: мужчин 61,7% (n=132), женщин 38,3% (n=82). Средний возраст больных составил 45,4±20,5 года.
Информация для анализа результатов исследования получена из медицинских документов статистической отчетности, мониторинг возникновения неблагоприятных побочных эффектов осуществлялся в ходе анализа карты лечения больного туберкулезом (учетная форма № 01-ТБ/У). Проведена оценка зависимости развития нежелательных явлений от возраста пациента и наличия сопутствующей патологии, как главных факторов риска, влияющих на переносимость лечения. В последующем все больные были разделены на две группы: 1-я группа — лица с удовлетворительной переносимостью химиотерапии (n=142); 2-я группа — пациенты, лечение которых осложнялось НЯ (n=72).
Известно, что основной причиной развития побочных эффектов противотуберкулезных препаратов является их токсикологическое и аллергологическое воздействие. Указанные процессы развиваются в организме больного не мгновенно, а начинают проявляться в виде клинических симптомов в большинстве случаев после двух недель приема. Однако появлению клинических симптомов всегда предшествуют изменения межсистемного взаимодействия различных органов и функциональных структур организма под управлением вегетативной нервной системы. По данным А. М. Вейна (2003) [12], на ранних этапах эти изменения могут быть зарегистрированы с помощью индекса Кердо, коэффициента Хильде-бранта и показателя САН, в связи с чем они были выбраны в качестве критериев прогнозирования развития нежелательных явлений в исследуемой группе больных туберкулезом. Для оперативной оценки самочувствия, активности и настроения использовалась методика САН [13]. Нормальная оценка состояния испытуемого по этой методике находится в диапазоне 5,0–5,5 балла. Состояние межсистемного взаимодействия дыхательной и сердечно-сосудистой систем организма определяли по формуле с помощью коэффициента Хильдебранта: Q=P/Д , где Р — частота сердечных сокращений (уд. мин), Д — число дыханий в мин. Значения коэффициента в пределах 2,8–4,9 свидетельствуют о нормальных межсистемных взаимодействиях висцеральных систем, отклонение от этих значений — о степени рассогласования в их взаимодействии. Функциональное состояние организма оценивалось по вегетативному индексу Кердо с помощью выражения
ВИ = (1-^)х100 , где Д — величина диастолического давления (мм рт.ст.), Р — частота сердечных сокращений (уд. мин). Положительное значение индекса указывает на активацию симпатического отдела ВНС, а отрицательное — парасимпатического.
Показатели оценивались в двух контрольных точках: перед началом лечения и в динамике через 4 недели химиотерапии.
Для оценки вероятности развития НЯ в первые четыре недели лечения у каждого конкретного больного в зависимости от динамики показателя САН, индекса Кердо и коэффициента Хильдебранта использован Байесовский подход к оценке условных вероятностей. Согласно теореме Байеса, апостериорная вероятность рS/P, то есть вероятность развития побочных эффектов при наличии фактора P может быть определена по формуле pS/P =----PS*pPIS .
.
Статистическую обработку данных выполняли с помощью унифицированных компьютерных программ Excel Microsoft Word и пакета прикладных программ Statistica . Проверку нормальности распределения значений в выборке проводили с помощью теста Колмагорова — Смирнова. Распределение во всех группах было близко к нормальному. Рассчитывали среднее арифметическое (М), среднюю ошибку среднего арифметического (m), среднеквадратичное отклонение (s). Показатель достоверности различий (р) определялся с использованием критерия Стьюдента (t). Различия оценивались как достоверные при вероятности 95% (р<0,05) и выше.
Результаты. Установлено, что побочные реакции различного вида и степени выраженности на ПТП первого ряда были зарегистрированы у 72 больных, что составило 33,6% от общего числа обследованных. При анализе структуры нежелательных явлений, возникших у больных с впервые выявленным инфильтративным туберкулезом с бактериовыделением, установлено преобладание токсических НЯ (65,2%, n=48), аллергические проявления по типу крапивницы зафиксированы у 1/3 пациентов (n=24). В целом среди токсических побочных эффектов пре- валировали изменения со стороны гепатобилиарной системы — у 19 чел. (39,6%). Удельный вес нейротоксических изменений (головная боль, головокружение, раздражительность, бессонница, парестезии) составил 35,4% случаев (n=17). У каждого четвертого больного возникли кардиотоксические проявления в виде сердцебиения и неприятных ощущений за грудиной (12 человек).
Большинство побочных реакций на ПТП развивалось в первые 3 месяца лечения (45,8% больных, n=33), в период с 3-го по 6-й месяц — у 20,8% (n=15) и в более отдаленные сроки в 33,3% случаев (n=24). При проведении корригирующей терапии неблагоприятные симптомы ПТП удавалось купировать в 92,6% случаев.
Распределение больных по частоте встречаемости НЯ на ПТП с учетом особенностей медико-социального статуса больных представлено в табл. 1.
Анализируя представленные в табл. 1 данные, можно отметить, что значимым в развитии нежелательных явлений оказывается возрастной ценз пациента. В возрасте до 30 лет побочные эффекты имели место у 10,9% больных, в то время как после 30 лет этот показатель увеличился в 1,5 раза, р=0,0000. При этом, как следует из табл. 1, у 41,5% больных (n=27) старше 50 лет зарегистрированы побочные эффекты.
Злоупотребление алкоголем и низкая масса тела не являются определяющими параметрами в развитии нежелательных реакций.
Наличие сопутствующей патологии существенно влияет на переносимость противотуберкулезных лекарственных средств. Наименее прогностически
Таблица 1
Частота встречаемости побочных реакций на ПТП первого ряда с учетом медико-социального статуса больных
|
Наименование критерия |
n |
Частота побочных реакций ПТП (абс, %) |
|||
|
нет |
аллергические |
токсические |
токсико-аллергические |
||
Возраст (лет):
|
<30; |
64 |
57 (89,1) |
5 (7,8) |
2 (3,1) |
- |
|
31–50; |
85 |
47 (55,3) |
20 (23,5) |
12 (14,1) |
6 (7,1) |
|
р* |
0,0000 |
0,0147 |
0,0272 |
||
|
>50. |
65 |
38 (58,5) |
12 (18,5) |
10 (15,4) |
5 (7,7) |
|
р* |
0,0002 |
0,0351 |
0,0190 |
||
|
Злоупотребление алкоголем |
54 |
18 (33,3) |
8 (14,8) |
20 (37,0) |
8 (14,8) |
|
Низкая масса тела |
59 |
31 (52,5) |
9 (15,3) |
10 (16,9) |
9 (15,3) |
Наличие сопутствующих заболеваний:
|
нет |
43 |
32 (74,4) |
8 (18,6) |
3 (6,9) |
- |
|
органов пищеварения |
42 |
16 (38,1) ** |
4 (9,5) |
14 (33,3) |
8 (19,0) |
|
р** |
0,0012 |
0,0547 |
0,0035 |
0,0035 |
|
|
мочевыделительной системы |
26 |
7 (26,9) ** |
5 (19,2) |
4 (15,4) |
10 (38,5) |
|
р** |
0,0003 |
0,9355 |
0,2872 |
0,0000 |
|
|
нервной системы |
16 |
3 (18,7) ** |
2 (12,5) |
9 (56,3) ** |
2 (12,5) |
|
р** |
0,0003 |
0,5908 |
0,0001 |
0,0193 |
|
|
эндокринной системы |
18 |
4 (22,2) ** |
5 (27,8) |
8 (44,4) ** |
1 (5,5) |
|
р** |
0,0004 |
0,4395 |
0,0011 |
0,1104 |
|
|
органов дыхания |
69 |
34 (49,3) |
12 (17,4) |
15 (21,7) |
8 (11,6) |
|
р** |
0,0102 |
0,7882 |
0,0386 |
0,0200 |
П р и м еч а н и е : * — достоверность различий с возрастной группой <30 лет; ** — достоверность различий с группой при отсутствии сопутствующих заболеваний.
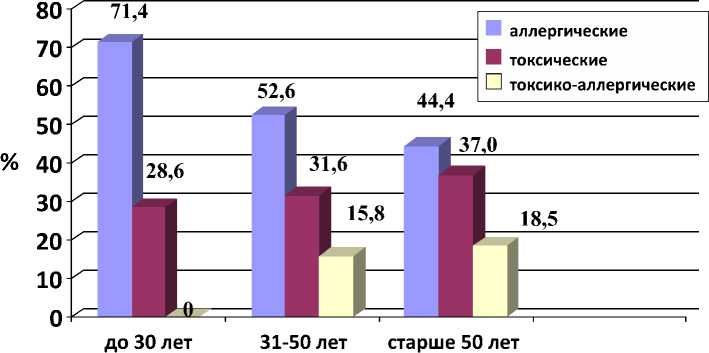
Структура НЯ у больных туберкулезом, получающих лечение по I режиму в зависимости от возраста, %
неблагоприятным фактором в плане развития побочных эффектов химиотерапии у больных туберкулезом является наличие заболеваний органов дыхания, р=0,0102. На фоне патологии органов пищеварения НЯ развивались у 61,9% (п=2б) обследованных. Патология нервной системы у больных инфильтративным туберкулезом легких с бактериовыделением способствует развитию нейротоксических явлений при проведении химиотерапии (81,3%, n=13). Установлено, что аллергические реакции достоверно чаще развиваются у пациентов с наличием эндокринной патологии (27,8%), токсические реакции — у больных с наличием поражения нервной системы (56,3%).
Анализируя структуру НЯ, можно отметить некоторые закономерности в развитии побочных эффектов химиотерапии с учетом факторов риска их развития. В частности, с увеличением возраста аллергические реакции на прием противотуберкулезных препаратов снижаются, а токсико-аллергические повышаются (рисунок).
Аллергические реакции в структуре всех нежелательных явлений при первом режиме лечения туберкулеза у больных до 30 лет встречались у 71,4% (n=5) больных, в то время как после 50 лет в 44,4% (n=12) случаев. Выявлена тенденция к увеличению числа токсических и токсико-аллергических проявлений с увеличением возраста. Статистически значимой достоверности разных типов реакций в зависимости от возраста получено не было.
Учитывая высокий процент побочных эффектов химиотерапии по I режиму у больных туберкулезом легких, необходима разработка четких критериев прогноза возникновения НЯ для проведения превен- тивных мер на более ранних этапах лечения. С этой целью проведено исследование индекса Кердо, коэффициента Хильдебранта и показателя САН в двух группах больных: с наличием и отсутствием побочных эффектов на фоне лечения (табл. 2).
Из табл. 2 следует, что перед началом приема препаратов значения индексов у больных туберкулезом существенно не различались, независимо от наличия или отсутствия побочных эффектов в ходе дальнейшей терапии. У больных с отсутствием неблагоприятных реакций на прием препаратов исходно индекс Кердо составил 13,6±3,1 ед., коэффициент Хильдебранта 3,4±0,2 ед. и показатель САН 5,1±0,9 ед. При развитии побочных эффектов эти показатели составили 16,4±2,2 ед., 4,1±0,6 ед. и 5,4±0,8 ед. соответственно (р>0,05). Однако в динамике этих показателей в первые четыре недели лечения наблюдались существенные различия. В группе больных без побочных эффектов в ходе приема препаратов в течение 9–12 месяцев в первые четыре недели индекс Кердо повысился на l6,1±1,6%, коэффициент Хильдебранта на 26,1±2,2%, а показатель снизился на 11,2±1,8% (р>0,05), но при этом остался в зоне комфортного психоэмоционального состояния, в то время как в группе больных с наличием побочных эффектов изменения перечисленных показателей составили 40,6±2,4%, 46,1±1,9% и 43,2±0,7% соответственно (р<0,05), что свидетельствует о существенном преобладании симпатикотонии, появлении диссонанса в работе кардиореспираторной системы и снижении настроения и самочувствия. Таким образом, выраженная динамика изучаемых показателей в первый месяц лечения с высокой степенью вероят-
Таблица 2
Изменения показателя САН, индекса Кердо, коэффициента Хильдебранта в течение первых четырех недель химиотерапии у больных туберкулезом при наличии и отсутствии побочных эффектов в дальнейшем, ед.
|
Анализируемые показатели |
Группы наблюдения |
|||||
|
Отсутствие побочных эффектов, n=142 |
Наличие побочных эффектов, n=72 |
|||||
|
исходно, ед. |
через 4 недели, ед. |
динамика (%) |
исходно, ед. |
через 4 недели, ед. |
динамика (%) |
|
|
Индекс Кердо |
13,6±3,1 |
16,2±2,7 |
16,1±1,6 |
16,4±2,2 |
27,6±1,4* |
40,6±2,4* |
|
Коэффициент Хильдебранта |
3,4±0,2 |
4,6±0,7 |
26,1±2,2 |
4,1±0,6 |
7,6±0,5* |
46,1±1,9* |
|
Показатель САН |
5,1±0,9 |
4,6±0,6 |
–11,2±1,8 |
5,4±0,2 |
3,1±0,4* |
–43,2±0,7* |
П р и м еч а н и е : * — достоверность различий с исходными значениями (р<0,05).
ности может указывать на возможность развития побочных эффектов в ходе дальнейшего лечения.
Динамика изучаемых показателей на разных сроках возникновения побочных реакций в дальнейшем у больных с наличием НЯ (n=72) представлена в табл. 3.
При анализе данных, представленных в табл. 3, обращает на себя внимание четкая зависимость между степенью изменения индекса Кердо коэффициента Хильдебранта в первые четыре недели химиотерапии и сроками возникновения в дальнейшем побочных эффектов. В частности, степень изменения индекса Кердо 59,4 ± 2,4%, коэффициента Хильдебранта 48,9 ± 1,6% соответствует возникновению осложнений в первые 1–3 месяца лечения. В тех случаях, когда побочные эффекты возникали через 9–12 месяцев, происходило снижение перечисленных показателей, непревышающих 25-30%. Однако указанная зависимость нарушалась при анализе соотношений между динамикой показателя САН в течение первых четырех недель терапии и развитием побочных эффектов в ходе дальнейшего лечения. Как следует из табл. 3, при снижении САН на величину более 50% побочные эффекты могли развиваться на любом этапе лечения в течение 9–12 месяцев.
В результате психологических тест-опросов и мониторинга показателей кардиогемодинамики установлено, что функциональное и психоэмоциональ- ное состояние организма предполагает развитие разных типов нежелательных явлений (табл. 4).
Как следует из табл. 4, чем больше отклонение индекса Кердо во второй контрольной точке от первоначального значения, тем больше вероятность развития у пациентов НЯ в ходе химиотерапии. Следует отметить, что выраженная симпатикотония в большей мере ассоциирована в дальнейшем с возникновением аллергических побочных эффектов, чем токсических и токсико-аллергических. Так, при изменении индекса Кердо с <10 до 30% и более частота аллергических реакций возрастала с 20,4 до 51,2%, т.е. в 2,5 раза, в то время как токсических и токсико-аллергических в 1,6 раза. Серьезные межсистемные кардиореспираторные нарушения, измеряемые с помощью коэффициента Хильдебранта, оказалось более значимыми для возникновения токсических реакций. Увеличение показателя в первый месяц терапии способствовало росту числа аллергических реакций в 1,2 раза, токсических в 2,2 раза. Выраженная динамика показателя САН в первые четыре недели химиотерапии приводила к росту встречаемости аллергических, токсических и токсико-аллергических побочных эффектов практически пропорционально. На фоне изменения САН в указанном диапазоне количество НЯ возросло в среднем в 1,7 раза.
Представленные данные свидетельствуют о том, что изменения индекса Кердо, коэффициента Хиль-дебранта и показателя САН на начальном этапе ле-
Таблица 3
Динамика изменения показателя САН, индекса Кердо, коэффициента Хильдебранта в первые четыре недели химиотерапии при разных сроках возникновения ПР, %
|
Сроки возникновения побочных эффектов (мес.) |
Изменения показателей за первые четыре недели |
||
|
Индекс Кердо |
Коэффициент Хильдебранта |
Показатель САН |
|
|
1–3 |
59,4 ± 2,4 |
48,9 ± 1,6 |
–60,8 ± 2,6 |
|
4–6 |
38,7 ± 1,2 |
31,6 ± 1,4 |
–57,8 ± 1,7 |
|
7–9 |
30,8 ± 0,9* |
31,2 ± 1,6 |
–62,4 ± 2,7 |
|
10–12 |
27,6 ± 2,1* |
26,7 ± 1,1* |
–61,6 ± 2,2 |
П р и м еч а н и е : * — достоверность различий с группой 1–3 месяца (р<0,05).
Таблица 4
Частота встречаемости побочных реакций при различной динамике показателей САН, индекса Кердо, коэффициента Хильдебранта в первые четыре недели лечения больных туберкулезом, %
Таблица 5
Результаты работы компьютерной программы «Эксперт» по оценке рисов развития побочных эффектов
Общий риск развития побочных эффектов
Максимальный риск развития сроки (мес.)
Виды побочных эффектов
73,2%
Через 6,4 месяца Аллергические — 12,1 %
Токсические — 74,2% Токсико-аллергические — 8,6%
Интерпретируя представленные в табл. 5 данные, можно констатировать, что у больного через 6,4 месяца лечения с вероятностью 73,2% могут развиться побочные эффекты от проводимой химиотерапии, причем с вероятностью 74,2% — это токсические реакции.
Оценка надежности компьютерной экспертноконсультативной системы «Эксперт» по прогнозированию развития побочных эффектов химиотерапии у больных с впервые выявленным туберкулезом оценивалась на произвольной выборке из 73 человек.
Результаты исследования показали, что предложенная экспертно-консультативная система обладает 76,3% чувствительностью при 84,7% специфичности для прогнозирования риска развития побочных эффектов химиотерапии, что позволяет рекомендовать ее для практического использования во фтизиатрии.
Обсуждение. Несмотря на несомненные успехи применения противотуберкулёзных препаратов для лечения туберкулёза, развивающиеся побочные действия ограничивают проведение полноценной химиотерапии, что существенно ухудшает приверженность пациентов к лечению и ведет к снижению эффективности оказания противотуберкулезной помощи. В настоящее время существуют субъективные методы прогнозирования возможных нежелательных явлений, основанные на оценке общесоматического состояния в анамнезе. В практической работе фтизиатра объективной необходимостью является прогнозирование возникновения побочных реакций у впервые выявленных больных туберкулезом на начальном этапе лечения.
В процессе работы выявлено, что нежелательные эффекты на ПТП развиваются у каждого тре- тьего больного, и установлена зависимость развития разных типов ПР от возрастного ценза и наличия сопутствующей патологии. Результаты исследования показали, что между изменением межсистемного взаимодействия различных органов и функциональных структур организма под управлением вегетативной нервной системы, зарегистрированного с помощью индекса Кердо, коэффициента Хильдебранта и показателя САН, на начальном этапе I режима терапии и риском развития нежелательных явлений в последующем имеется четкая зависимость. Установленные закономерности были использованы при разработке компьютерной экспертно-консультативной системы «Эксперт» прогнозирования побочных эффектов химиотерапии у больных туберкулезом, которая может быть рекомендована к использованию в практической фтизиатрии.
Выводы:
-
1. При лечении больных с впервые выявленным туберкулезом по I режиму химиотерапии сочетанием четырех основных препаратов (изониазид, рифампицин, пиразинамид, этамбутол) возникновение нежелательных явлений увеличивается с возрастом и зависит от наличия сопутствующей патологии. Аллергические реакции достоверно чаще развиваются у пациентов с наличием эндокринной патологии (27,8%), токсические реакции — у больных с наличием поражения нервной системы (56,3%).
-
2. Изменения коэффициента Хильдебранта, индекса Кердо и показателя САН на начальных этапах лечения у больных с впервые выявленным туберкулезом в значительной мере ассоциированы с риском развития побочных эффектов химиотерапии, в связи с чем они могут быть использованы для прогнозирования развития осложнений химиотерапии.
-
3. Разработанная компьютерная экспертно-консультативная система для прогнозирования побочных эффектов химиотерапии у больных туберкулезом обладает 76,3% чувствительностью при 84,7% специфичности, что позволяет рекомендовать ее для практического применения.
Список литературы Прогнозирование развития нежелательных явлений химиотерапии у лиц с впервые выявленным туберкулезом легких
- Борисов С.E., Соколова Г.Б. Этиотропное лечение туберкулеза при лекарственной устойчивости М. Tuberculosis: взгляды и рекомендации международных организаций. Consilium medicum 2001; (12): 595-602
- Докторова Н.П., Морозова Т.И., Паролина Л.Е. Частота побочных реакций при лечении больных туберкулезом. Фтизиатрия и пульмонология 2013; 1 (6): 19
- Мишин В.Ю. Медикаментозные осложнения комбинированной химиотерапии туберкулеза легких. М.: Мед. информ. агентство, 2007; 248 с.
- Мордык А.В., Лысов А.В., Гапоненко Г.Е. и др. Частота неблагоприятных побочных реакций на противотуберкулезные препараты у впервые выявленных больных туберкулезом органов дыхания старше 18 лет и факторы, влияющие на их развитие. Туберкулез и болезни легких 2010; (2): 40-44
- Панова Л.В., Овсянкина Е.С. Частота развития и виды побочных реакций на химиотерапию у подростков, больных туберкулезом. Проблемы туберкулеза и болезней легких 2003; (1): 28-30
- Иванова Д.А., Борисов С.E., РЫЖОВ A.M. и др. Частота, характер и факторы риска лекарственно-индуцированного поражения печени при лечении впервые выявленных больных туберкулёзом. Туберкулез и болезни легких 2013; (11): 25-31
- Баласанянц Г.С., Суханов Д.С., Айзиков Д.Л. Побочные действия противотуберкулезных препаратов и методы их устранения: учебное пособие. Санкт-Петербург, 2011; 88 с.
- Докторова Н.П., Морозова Т.И., Александрова Е.Н. Спектр нежелательных реакций при лечении больных туберкулезом детей и подростков. Туберкулез и социально-значимые заболевания 2014; (1): 116-117
- Ташпулатова Ф.К. Профилактика побочных реакций противотуберкулезных препаратов при туберкулезе легких у больных с различным генетическим фоном. Проблемы туберкулеза и болезней легких 2003; (6): 17-21
- Чyканов В.И., Каминская Г.О., Ливчане Э. Частота и характер побочных реакций при лечении больных туберкулезом легких противотуберкулезными препаратами резервного ряда. Проблемы туберкулеза и болезней легких 2004; (10): 6-10
- Об утверждении методических рекомендаций по совершенствованию диагностики и лечения туберкулеза органов дыхания: приказ Минздрава РФ № 951 от 29.12.2014 г.: ГАРАНТРУ). http://www.garant.ru/products/ipo/prime/doc/70749840/#ixzz3m7leVL4j
- Вейн A.M. Вегетативные расстройства: клиника, диагностика, лечение. М.: Мед. информ. агентство, 2003; 752 с.
- Доскин В.А. Лаврентьева H.A., Мирошников М.П., Шарай В.Б. Тест дифференцированной самооценки функционального состояния. Вопросы психологии 1973; (6): 141-145.


