Прогнозирование результата патогистологического исследования простаты с помощью искусственной нейронной сети
Автор: Попков В.М., Шатылко Т.В., Фомкин Р.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Материалы III всероссийской недели науки с международным участием. Саратов, 3-6 марта 2014 г.
Статья в выпуске: 2 т.10, 2014 года.
Бесплатный доступ
Цель: оптимизация ведения пациентов с уровнем PSA сыворотки крови в диапазоне 4-10 нг/мл путем проектирования и обучения искусственной нейронной сети (ИНС), прогнозирующей гистологическую картину простаты по имеющимся клиническим, лабораторным и инструментальным данным. Материал и методы. Информация из историй болезни 254 пациентов, которым в период 2012-2013 гг. выполнялась трансректальная биопсия простаты (ТРБ) в онкологическом отделении КБ им. С. Р. Миротворцева, использована для создания нескольких ИНС с различной архитектурой. Внешняя валидация произведена на данных 27 пациентов, которым проводилась ТРБ в январе — феврале 2014 г. Результаты. Однослойная нейронная сеть с 11 входящими, 9 промежуточными и 3 выходными нейронами оказалась наиболее эффективной: в 92,6% случаев давала верное предположение о наличии или отсутствии рака простаты (РПЖ). Определены факторы, влияющие на прогноз, в порядке убывания значимости: объем простаты, PSA, возраст, пальпаторная плотность простаты, скорость прироста PSA, асимметрия простаты, предшествовавшая негативная биопсия, свободная фракция PSA, прием ингибиторов 5-альфа-редуктазы. Заключение. ИНС могут применяться для прогнозирования гистологических находок при ТРБ. Важными клиническими ориентирами, указывающими на вероятное наличие РПЖ, являются высокая PSA-плотность и изменения консистенции простаты при ее пальпации.
Искусственные нейронные сети, рак простаты
Короткий адрес: https://sciup.org/14917959
IDR: 14917959
Текст научной статьи Прогнозирование результата патогистологического исследования простаты с помощью искусственной нейронной сети
-
1Введение. Простатспецифический антиген
(PSA) — один из наиболее эффективных биохимиче-
ских опухолевых маркеров в онкологии. Его определение в сыворотке крове успешно применяется с целью контроля эффективности лечения рака простаты (РПЖ) и для раннего выявления рецидивов. Однако роль PSA в скрининге РПЖ нередко подвергается сомнению, что связано с высокой частотой ложнопо- ложительных результатов и соответственно низкой предиктивной ценностью и специфичностью. Низкая специфичность PSA объясняется тем, что этот фермент, известный также как гамма-семинопроте-ин и калликреин-3, играет важную роль в физиологии репродукции, а значит, синтезируется в большом количестве и здоровой тканью простаты. Благодаря своим протеазным свойствам он катализирует биохимические процессы, приводящие к декоагуляции спермы в женских половых путях, тем самым делая возможным активное передвижение сперматозоидов и непосредственно оплодотворение. Таким образом, свою естественную функцию PSA выполняет в составе семенной жидкости, но в небольших количествах постоянно попадает из ткани простаты в кровь. Любое механическое или функциональное раздражение простаты приводит к интенсивному выбросу PSA в кровь, с чем и связаны ложноположительные результаты, наблюдаемые после пальцевого ректального исследования, клизм, половых контактов, мастурбации. Нарушение функции гистогематиче-ского барьера вследствие длительного хронического простатита или других доброкачественных процессов может привести к персистирующему повышению уровня PSA на значениях выше референсного интервала (>4,0 нг/мл). С этим связан феномен «серой зоны PSA», под которой понимается интервал значений уровня PSA сыворотки от 4 до 10 нг/мл. Такой уровень PSA приводит к закономерным подозрениям относительно РПЖ, но еще не позволяет делать каких-либо выводов.
Вопросы тактики ведения таких пациентов неоднозначны. Трансректальная биопсия простаты с последующим патогистологическим исследованием препарата в большинстве случаев позволяет сделать вывод о характере изменений в органе. Тем не менее это инвазивное вмешательство, чреватое рядом осложнений, таких, как инфекции нижних мочевыводящих путей, острая задержка мочеиспускания, гематурия, гемоспермия, а также ректоррагия, потенциально летальная, особенно при амбулаторном проведении этой процедуры. Необходимо выделять контингент пациентов, которым действительно необходимо проведение трансректальной биопсии простаты. Выполнение биопсии всем пациентам с PSA в интервале «серой зоны» является крайностью, уход от которой позволит снизить число осложнений и повысить экономическую эффективность скрининговой программы. К сожалению, критерии для такого отбора пациентов до сих пор не сформулированы. Другой крайностью является полный отказ от PSA-скрининга, который предлагается, например, Американской урологической ассоциацией.
Одной из претензий в адрес PSA-базированных скрининговых программ для РПЖ является предполагаемая гипердиагностика его малоагрессивных форм, лечение которых не дает существенного увеличения продолжительности жизни у пожилых пациентов с сопутствующими заболеваниями, зато снижает качество жизни ввиду своих побочных эффектов.
Все эти и другие вопросы обсуждались Международным согласительным комитетом в Мельбурне в 2013 г. Итоги заседания комитета были выражены в пяти тезисах, один из которых сформулирован следующим образом: «Анализ крови на PSA должен рассматриваться не самостоятельно, а в рамках мульти-вариабельного подхода к раннему выявлению РПЖ» [1]. К сожалению, итоговые тезисы Международного согласительного комитета не говорят о том, что из себя представляет этот мультивариабельный подход, в чем заключается его принцип и как он реализуется на практике. Четкие рекомендации отсутствуют; предлагаются эвристический анализ клинической ситуации практикующим урологом, использование новых маркеров (PCA3), математических индексов и номограмм. Известна еще одна группа методов, способных помочь в решении этой непростой проблемы, — методы искусственного интеллекта, из которых наиболее применимым является создание искусственных нейронных сетей.
Искусственная нейронная сеть является кибернетической системой, которая способна анализировать большие массивы данных, находить в них закономерности и, обучившись таким образом, давать некий прогноз на основе новых входящих переменных. Нами была произведена попытка создания и обучения искусственной нейронной сети на собственном клиническом материале.
Цель: определение наиболее важных клинических ориентиров, позволяющих прогнозировать результат биопсии простаты, с помощью искусственных нейронных сетей.
Материал и методы. В компьютерной программной среде для работы с искусственными нейронными сетями спроектировано несколько сетей по типу многослойного персептрона с различной архитектурой. Создано три варианта нейронной сети: с одним, двумя и тремя слоями промежуточных нейронов. Количественными входными переменными для искусственных нейронных сетей служили возраст пациента, уровень PSA крови и его свободной фракции, объем простаты, PSA-плотность, параметры PSA-кинетики (скорость прироста и время удвоения PSA). Логическими входными переменными были плотная консистенция и асимметрия простаты, определяемые при пальцевом ректальном исследовании, предшествовавшая биопсия простаты с негативным результатом, прием ингибиторов 5-альфа-редуктазы в анамнезе.
Искусственные нейронные сети имели три выходных переменных, позволяющих дать ответ на три вопроса:
-
1) Ожидается ли обнаружение РПЖ при трансректальной биопсии? (логическая переменная);
-
2) Какое гистологическое заключение ожидается после трансректальной биопсии? (категориальная переменная с 4 вариантами: доброкачественная гиперплазия простаты, простатическая интраэпителиальная неоплазия низкой степени, простатическая интраэпителиальная неоплазия высокой степени, аденокарцинома простаты);
-
3) В случае выявления аденокарциномы простаты — какую сумму баллов Gleason следует ожидать? (количественная переменная).
Для обучения искусственных нейронных сетей использовалась информация из историй болезни 254 пациентов, которым в период 2012–2013 гг. выполнялась трансректальная биопсия простаты в онкологическом отделении КБ им. С. Р. Миротворцева СГМУ. Обучение производилось на протяжении не менее 1 500000 циклов.
Внешняя валидация искусственных нейронных сетей осуществлялась на основании данных 53 пациентов, которым производилась трансректальная биопсия в январе — марте 2014 г. По результатам внешней валидации были подсчитаны чувствительность, специфичность, положительная и отрицатель-
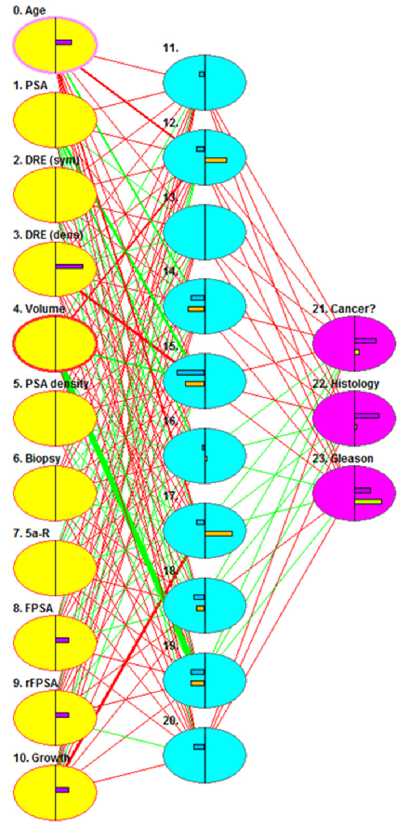
Рис. 1. Схема искусственной нейронной сети с одним слоем скрытых нейронов ная предиктивная ценность, а также коэффициент корреляции Мэтьюса для каждого варианта сети.
Post hoc для проверки возможной диагностической ценности PSA-плотности и пальпаторной консистенции простаты пациенты были разделены на две группы: пациенты с доброкачественной гиперплазией простаты, включая PIN (130 пациентов), и пациенты с обнаруженным РПЖ (124 пациента). Значения PSA-плотности в этих двух группах сравнивались с использованием статистического критерия Манна — Уитни. Сравнение пальпаторной плотности простаты проводилось с помощью критерия согласия Пирсона (хи-квадрат).
Результаты. Наиболее эффективной в прогностическом плане оказалась искусственная нейронная сеть с одним скрытым слоем из 9 нейронов (рис. 1). В 92.5% случаев она давала верное предположение о наличии или отсутствии РПЖ. Чувствительность составила 93,8%, специфичность 91,9%, позитивная и негативная предиктивная ценность 83,3 и 97,1% соответственно. Как интегральный параметр, характеризующий предиктивную ценность, использовался коэффициент корреляции Мэтьюса, составивший 0,83, что соответствует сильной прогностической способности искусственной нейронной сети.
Сравнительная характеристика нейронных сетей с различной архитектурой представлена на графике (рис. 2).
В 77,4% случаев она давала верное гистологическое заключение, делая различие между доброкачественной гиперплазией, раком и разными формами простатической интраэпителиальной неоплазии (PIN). Нейронная сеть оказалась неспособной точно предсказать сумму баллов Gleason (33,3%), при этом отмечена тенденция к занижению степени атипии и гиподиагностике агрессивных форм РПЖ.
В таблице представлена сравнительная точность прогноза нейронных сетей с различным количеством промежуточных слоев.
Частота соответствия морфологической картины прогнозу нейронных сетей с различной архитектурой, %
|
Запрос |
1 скрытый слой |
2 скрытых слоя |
3 скрытых слоя |
|
«Ожидается ли обнаружение РПЖ при трансректальной биопсии?» |
92,5 |
58,5 |
69,8 |
|
«Какое гистологическое заключение ожидается после трансректальной биопсии?» |
77,4 |
47,3 |
52,7 |
|
«В случае выявления аденокарциномы простаты какую сумму баллов Gleason следует ожидать?» |
33,3 |
30,0 |
31,1 |
Определены факторы, влияющие на прогноз сети, и установлена относительная важность каждого из них. Далее они перечислены в порядке убывания значимости: объем простаты, PSA крови, возраст, пальпаторная плотность простаты, скорость прироста PSA, асимметрия простаты, предшествовавшая негативная биопсия, свободная фракция PSA, прием ингибиторов 5-альфа-редуктазы (график на рис. 3).
Учитывая то, что на первых местах находились объем простаты и уровень PSA крови, мы предположили, что важным клиническим ориентиром может являться расчетный параметр — PSA-плотность, определяемая как отношение PSA сыворотки в нг/мл к объему простаты в см3. Медиана PSA-плотности в группе пациентов с доброкачественным поражением простаты составила 0,1503, в группе пациентов с аденокарциномой простаты — 0,5568 (p<0,05).
Довольно важным клиническим ориентиром оказалась также пальпаторная плотность простаты. Повышенная плотность определялась у 9,3% пациентов в группе с доброкачественными процессами в простате и у 75,8% пациентов в группе пациентов с РПЖ (p<0,05).
Обсуждение. Идея создания искусственных нейронных сетей с целью оптимизации скрининга на РПЖ не нова [2]. Многих исследователей привлекает не только ореол новизны, окружающий применение искусственного интеллекта в медицине, но и чисто практические моменты, выгодно отличающие метод нейронных сетей от аналогов. Например, искусственные нейронные сети способны продолжать обучение и совершенствоваться по мере накопления клинического материала. Они могут искать нелинейные взаимосвязи между напрямую не связанными данными, в отличие от регрессионного анализа и основанных на нем номограмм [3].
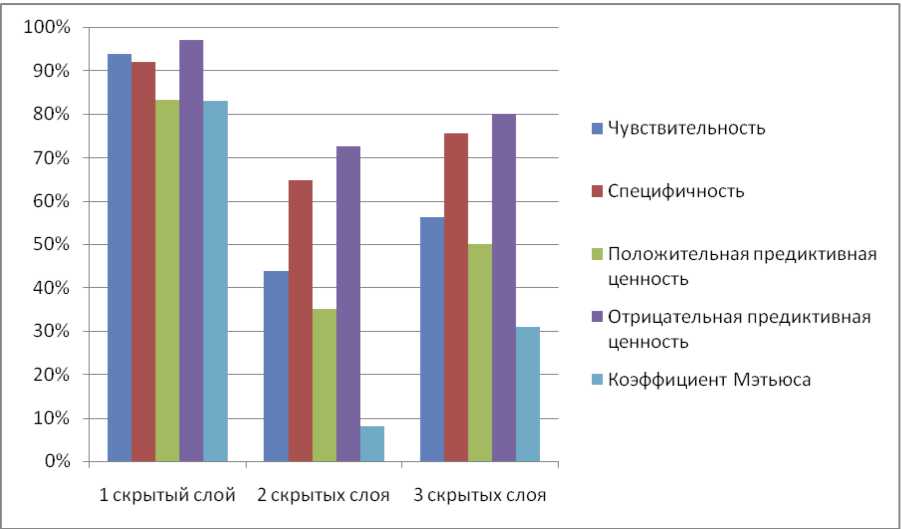
Рис. 2. Сравнение прогностической ценности нейронных сетей с различной архитектурой в отношении рака простаты.
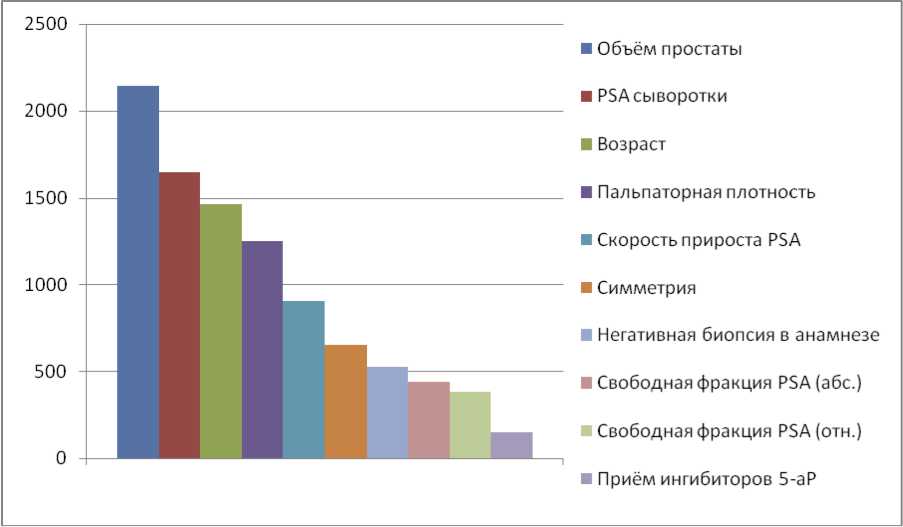
Рис. 3. Относительная прогностическая важность входных переменных
Наиболее эффективной оказалась сеть с одним скрытым нейронным слоем, что подтверждает тезис о том, что избыточная архитектура искусственных нейронных сетей в неточных наборах данных (в частности, биомедицинских) приводит к неадекватному их функционированию.
Ближайшим аналогом созданной нами искусственной нейронной сети является ProstataClass, разработанная немецким научным коллективом Stephan et al. в 2005–2008 гг. Она имеет 5 входных нейронов, 3 скрытых и 1 выходной; основным предназначением ее является разделение пациентов на группы высокого и низкого риска РПЖ. ProstataClass была построена на данных 798 пациентов, что в несколько раз превышает объем нашей базы данных в настоящий момент. Ее валидация также проводилась с большим количеством пациентов — 282 [3]. Тем не менее непосредственные результаты валидации нашей искусственной нейронной сети оказались не хуже. Докладывается о высокой частоте ложноотрицательных результатов (36%) при использовании ProstataClass [4]. Это может объясняться тем, что мы взяли больше клинических ориентиров в качестве входных переменных, а также тем, что все субъективно оцениваемые параметры (данные ультразвукового и пальцевого ректального исследования) определялись одной и той же командой клиницистов на протяжении всего срока сбора клинического материала. В любом случае адекватное сравнение эффективности нашей нейронной сети с аналогами будет возможно лишь по мере накопления клинического материала для обучения и валидации.
Интересно, что искусственная нейронная сеть во многих случаях оказалась способной более тонко прогнозировать результат гистологического исследования биоптата, а именно различать PIN высокой и низкой степени. Казалось бы, простатическая интраэпителиальная неоплазия — термин сугубо патоги-стологический, и на основании клинических данных ее заподозрить нельзя. Тем не менее «искусственная интуиция» нейронной сети, видимо, выявила некоторые нелинейные взаимосвязи, характерные для клинической картины при PIN. Мы с естественным скепсисом относимся к данному наблюдению, но будем обращать внимание на этот аспект по мере дальнейшего накопления и обработки клинического материала.
Что касается суммы баллов Gleason, плохие предиктивные свойства нашей искусственной нейронной сети в ее отношении вполне ожидаемы, так как, по сути, материал для ее обучения в этом плане был ограничен 124 пациентами с РПЖ. Данные остальных 130 пациентов с аденомой простаты ценности здесь не представляли.
С помощью искусственной нейронной сети нами получено представление об иерархии клинических ориентиров, на основании которых можно эвристически определять тактику ведения пациентов с PSA сыворотки крови в так называемой «серой зоне». Методы классической статистики подтвердили возможную диагностическую ценность PSA-плотности. Следующим шагом должно быть определение cut-off value для этого параметра.
Твердая консистенция простаты при ректальном пальцевом исследовании — классический признак РПЖ, незаслуженно забытый некоторыми амбулаторными урологами. Настоящее исследование еще раз обращает внимание на важность пальцевого ректального исследования в онкологическом скрининге.
Заключение. Построение искусственных нейронных сетей — перспективный метод, способный оптимизировать скрининговую программу при поиске РПЖ. Их использование позволяет применять «муль- тивариабельный подход», предложенный Международным согласительным комитетом, интегрируя разнородные клинические и лабораторные данные. В отличие от номограмм и регрессионных уравнений, искусственные нейронные сети поддаются корректировке по мере использования и могут быть адаптированы к специфическим условиям той или иной клиники. Пока не внедрены в практику стандартизованные инструменты на основе искусственных нейронных сетей, тактика ведения пациентов с уровнем PSA сыворотки крови в пределах «серой зоны» остается спорной. Тем не менее ряд клинических и лабораторных ориентиров, таких, как пальпаторная плотность простаты и PSA-плотность, могут оказаться полезными в эмпирическом решении вопроса о необходимости выполнения трансректальной биопсии.
Список литературы Прогнозирование результата патогистологического исследования простаты с помощью искусственной нейронной сети
- Murphy DG, Ahlering T, Catalona WJ, et al. The Melbourne Consensus Statement on the early detection of prostate cancer. BJU lnt2014Feb; 113(2): 186-8
- Ecke TH, Bartel P, Hallmann S, et al.Outcome prediction for prostate cancer detection rate with artificial neural network (ANN) in daily routine. Urol Oncol 2012 Mar-Apr; 30 (2): 139-44
- Ecke TH, Hallmann S, Koch S, et al. External validation of an artificial neural network and two nomograms for prostate cancer detection. ISRN Urol 2012; 2012: 643181
- Meijer RP, Gemen EF, van Onna IE, et al. The value of an artificial neural network in the decision-making for prostate biopsies. World J Urol 2009 Oct; 27 (5): 593-8.


