Пространственная модель анаэробной метакрилатредуктазной системы
Автор: Архипова Оксана Викторовна, Трошина Ольга Юрьевна, Микулинская Галина Викторовна
Журнал: Вестник Тверского государственного университета. Серия: Биология и экология @bio-tversu
Рубрика: Междисциплинарные исследования
Статья в выпуске: 2, 2017 года.
Бесплатный доступ
Компьютерное моделирование пространственной структуры метакрилатредуктазы (Mrd) и цитохрома с (Mcc) метакрилатной редокс системы Geobacter sulfurreducens AM-1 выявило высокое структурное сходство с растворимыми фумаратредуктазами Shewanella. Mrd и по последовательности, и структурно повторяет два С-концевых каталитических домена этих фумаратредуктаз - FAD-связывающий и домен-«зажим». Mcc сходен с малым N-концевым гемсодержащим доменом периплазматических фумаратредуктаз Shewanella. Высказывается предположение о пространственном взаимодействии консервативных аминокислот Mrd, участвующих в катализе и связывании субстрата.
Метакрилатредуктаза (mrd), цитохром с (mcc), флавоцитохромы с, периплазматические фумаратредуктазы
Короткий адрес: https://sciup.org/146278248
IDR: 146278248 | УДК: 577.151.3
Spatial model of anaerobic methacrylate reductase system
The high structural similarities of methacrylate reductase (Mrd) and cytochrome c (Mcc) (of the methacrylate redox system) from Geobacter sulfurreducens AM-1 with the soluble fumarate reductases of Shewanella were revealed by the computer modelling. Mrd repeates two C-terminal catalytic domains of these fumarate reductases - FAD-binding and clamp domains - both sequence and structure. Mcc is similar to small N-terminal heme-containing domain of the periplasmic fumarate reductases of Shewanella. The assumption of spatial interaction of the conservative amino acids from Mrd, involved in catalysis and substrate binding, is discussed.
Текст научной статьи Пространственная модель анаэробной метакрилатредуктазной системы
Введение. Многие анаэробные бактерии используют ненасыщенные органические соединения в качестве терминальных акцепторов восстановительных эквивалентов (Архипова, Акименко, 2005). Детально изучены такие разновидности анаэробного дыхания, как кофеатное и фумаратное (Hägerhäll, 1997; Kröger et al., 2002; Hess et al., 2013; Iverson, 2013). Заключительные стадии этих типов дыхания -восстановление кофеата в гидрокофеат и фумарата в сукцинат – происходят в цитоплазме и/или периплазме. Восстановление осуществляется 1) мономерными редуктазы, 2) редуктазами из 3-4 субъединиц, 3) ферментными системами из нескольких белков с разными каталитиче c кими активностями.
Терминальная стадия кофеатного дыхания Acetobacterium woodii - восстановление производных фенилпропеновой кислоты -
∗ Работа выполнена при частичной поддержке РФФИ (грант № 17-0401068 «Анаэробная ферментная система, восстанавливающая метакрилат»).
- 306 - осуществляется в цитозоле клеток с помощью ферментов, кодируемых опероном carABCDE (Hess et al., 2013). К ним относятся гидрокофеил-CoA:кофеат-CoA трансфераза (CarA), ATP-зависимая ацил-CoA синтетаза (CarB) и трёхсубъединичный ферментный комплекс из кофеил-CoA редуктазы и электрон-транпортного флавопротеина (CarCDE).
В случае фумаратного дыхания клетки бактерий восстанавливают фумарат в цитозоле (например, Wolinella succinogenes и Escherichia coli) или в периплазме (бактерии рода Shewanella). Ферментный комплекс, восстанавливающий фумарат в цитозоле, располагается с внутренней стороны цитоплазматической мембраны и состоит из 3-4 белковых субъединиц (Hägerhäll, 1997; Kröger et al., 2002; Iverson, 2013). Периплазматические фумаратредуктазы бактерий рода Shewanella являются растворимыми мономерами и относятся к семейству флавоцитохромов с (Gordon et al., 1998; Dobbin et al., 1999; Maier et al., 2003).
Анаэробная бактерия Geobacter sulfurreducens АМ-1 использует соединение антропогенной природы – метакрилат – в качестве конечного акцептора редуктазной цепи (Mikoulinskaia et al., 1999). Интерес к представителям рода Geobacter (δ-Proteobacteria) вообще обусловлен высоким разнообразием у них дыхательных цепей: электрон-транспортных компонентов, цитохромов (Methė et al., 2003). Такая особенность микроорганизмов позволяет им быть как электротрофами (Lovley, 2010), принимающими электроны для восстановления терминальных акцепторов электронов напрямую от электрода, так и экзоэлектрогенами (Logan, 2009), переносящими электроны на твёрдые электроды. Бактерии рода Geobacter вовлечены в процессы электробиоремедиации радиоактивных металлов и органических загрязнений (Lovley, 2010). Они играют значительную роль в глобальных круговоротах металлов и углерода: восстанавливают Fe(III) в Fe(II), U(VI) в U(IV), окисляют ацетат и многоуглеродные органические субстраты, участвуют в разложении гумуса. Кроме того, бактерии рода Geobacter способны к фумаратному дыханию (Caccavo et al., 1994; Methė et al., 2003).
Трансформацию метакрилата в изобутират у G. sulfurreducens АМ-1 катализирует периплазматическая метакрилатная редокс система (Mikoulinskaia et al., 1999). Она состоит из двух хромопротеидов: флавинсодержащей метакрилатредуктазы (Mrd; 50 кДа) и её физиологического донора электронов – цитохрома с (Mcc; 30 кДа) (Mikoulinskaia et al., 1999). Недавно нами был секвенирован полный геном G. sulfurreducens АМ-1 (Arkhipova et al., 2015). Гены, кодирующие компоненты метакрилатной редокс сиcтемы, оказались организованными в оперон. Обнаружение генов mrd и mcc в геноме привело к расшифровке аминокислотных последовательностей обоих компонентов.
Подавляющее большинство белковых последовательностей, проявляющих выраженное сходство с Mrd и Mcc, не были получены в чистом виде и охарактеризованы биохимически (Arkhipova et al., 2015). Например, наиближайшие гомологи Mrd и Mcc – гипотетические белки, данные о которых получены на основании анализа последовательностей геномов четырёх представителей класса δ-Proteobacteria и одного представителя класса Deferribacteres (Arkhipova et al., 2015). Гомологи Mrd и Mcc из Anaeromyxobacter sp. K, Anaeromyxobacter dehalogenans 2CP-1, Anaeromyxobacter dehalogenans 2CP-C, Desulfatibacillum alkenivorans AK-01 и Denitrovibrio acetiphilus DSM 12809, по всей видимости, являются компонентами единой редокс системы, поскольку их гены также организованы в одну транскрипционную единицу.
К настоящему моменту были исследованы экспериментально следующие флавопротеины-гомологи Mrd: FccA (WP_011138088) бактерии Wolinella succinogenes (Gross et al., 2001), предполагаемая уроканатредуктаза SO_4620 (WP_011074216) (Bogachev et al., 2012) и периплазматические фумаратредуктазы Fcc 3 (WP_041413240; далее Fcc 3 -f) (Gordon et al., 1998), Ifc 3 (WP_011638036) (Dobbin et al., 1999) и Fcc 3 (WP_011071245; далее Fcc 3 -o) (Maier et al., 2003) бактерий рода Shewanella. Растворимые фумаратредуктазы шеванелл (Fcc 3 -f (WP_041413240), Ifc 3 (WP_011638036), Fcc 3 -o (WP_011071245) являются к тому же гомологами Mcc метакрилатной редокс системы (Arkhipova et al., 2015).. Эти фумаратредуктазы бактерий рода Shewanella - единственные из гомологов Mrd и Mcc, для которых известны кристаллические структуры (Bamford et al., 1999; Leys et al., 1999; Taylor et al., 1999; Doherty et al., 2000).
Целью работы было проанализировать потенциальную пространственную организацию компонентов метакрилатной редокс системы, включая выявление консервативных аминокислот Mrd, участвующих в катализе и связывании субстрата.
Методика. Объектом исследований служила анаэробная бактерия G. sulfurreducens АМ-1 из коллекции культур лаборатории адаптации микроорганизмов Института биохимии и физиологии микроорганизмов им. Г.К.Скрябина РАН (г. Пущино).
Предметом исследований были установленные ранее (Arkhipova et al., 2015). аминокислотные последовательности компонентов метакрилатной редокс системы G. sulfurreducens АМ-1.
Для анализа аминокислотных последовательностей и расчета молекулярных масс использовали программу GENERUNR (http://www.generunner.net). Количество гемов с у гомологичных белков определяли по числу гемсвязывающих участков CXXCH (где C – цистеин, H – гистидин, X – любая аминокислота) (Li et al., 2011).
Множественные выравнивания аминокислотных последовательностей осуществляли с помощью программы BLAST с сервера National Center of Biotechnology Information, National Library of Medicine, USA (NCBI; http://www.ncbi.nlm.nih.gov ).
Построение предполагаемых пространственных структур выполняли с помощью программы Cn3D Viewer, доступной на сервере NCBI, USA ( http://www.ncbi.nlm.nih.gov/structure/CN3D/cn3d/shtml ). При этом аминокислотные последовательности компонентов метакрилатной редокс системы накладывали на известную пространственную структуру фумаратредуктазы Ifc 3 (WP_011638036; 1Q08) бактерии Shewanella frigidimarina NCIMB 400 (Bamford et al., 1999). Флавоцитохром Ifc 3 (WP_011638036) был выбран по принципу наибольшего сходства с Mrd, но результаты аналогичны при выборе флавоцитохромов с Fcc 3 -f (WP_041413240) и Fcc 3 -o (WP_011071245).
Филогенетический анализ аминокислотных последовательностей Mrd, Мсс и гомологичных им белков, а также генов, кодирующих 16S рРНК, был осуществлён с помощью программного пакета MEGA версия 6.0 (Tamura et al., 2013). Дендрограммы аминокислотных последовательностей были построены с использованием метода Maximum Likelihood и модели WAG+G+I. Дендрограмма родства генов 16S рРНК построена с использованием метода Maximum Likelihood и модели Tamura-Nei. Достоверность ветвления оценивали с помощью «bootstrap» анализа 1000 альтернативных деревьев.
Все использованные в работе аминокислотные последовательности белков и нуклеотидные последовательности генов ферментов и 16S рРНК, доступны в базах данных GenBank, Gene, Genome, Nucleotide, Protein с сервера National Center of Biotechnology Information, National Library of Medicine, USA (NCBI; http://www.ncbi.nlm.nih.gov ).
Результаты
Гомологи компонентов метакрилатной редокс системы. Ранее было показано, что самые близкие гомологи метакрилатной редокс G. sulfurreducens АМ-1 системы – гипотетические белки, обнаруженные при аннотации полных геномов бактерий (Arkhipova et al., 2015). Однако, как уже упоминалось во ВВЕДЕНИИ, среди гомологов метакрилатной редокс системы есть и биохимически охарактеризованные. Для представления степени родства хромопротеидов метакрилатной редокс системы и обсуждаемых в статье гомологов были построены филогенетические деревья (рис. 1 и 2). Для этих деревьев были использованы аминокислотные последовательности Mrd (рис. 1) и Mcc (рис. 2) и аминокислотные последовательности как всех биохимически охарактеризованных гомологов из Wolinella succinogenes (Gross et al., 2001), Shewanella oneidensis MR-1 (Maier et al., 2003; Bogachev et al., 2012) и S. frigidimarina NCIMB 400 (Gordon et al., 1998; Dobbin et al., 1999), так и гипотетических, но проявляющих наибольшее сходство (Arkhipova et al., 2015), гомологов из Anaeromyxobacter dehalogenans 2CP-1. Родство самих бактерий представлено на дендрограмме, построенной на основании данных о генах 16S рРНК этих бактерий (рис. 3).
100 Fcc 3 -f Shewanella frigidimarina NCIMB 400
100 Fcc 3 -o Shewanella oneidensis MR-1
58 Ifc 3 Shewanella frigidimarina NCIMB 400
уроканатредуктаза Shewanella oneidensis MR-1
II флавиновая субъединица флавоцитохрома с Wolinella succinogenes DSM 1740
I 100 J Mrd Geobacter sulfurreducens AM-1
флавоцитохром с Anaeromyxobacter dehalogenans 2CP-1
0.2
Р ис . 1 . Дендрограмма родства Mrd Geobacter sulfurreducens AM-1 (AJY71931) и гомологичных белков: гипотетичеcкого флавоцитохрома c (WP_012633122) из Anaeromyxobacter dehalogenans 2CP-1 и исследованных эспериментально флавиновой субъединицы флавоцитохрома с (WP_011138088) из Wolinella succinogenes DSM 1740 , предполагаемой уроканатредуктазы (WP_011074216) из Shewanella oneidensis MR-1, флавоцитохрома с 3 -фумаратредуктазы Ifc 3 (WP_011638036) S. frigidimarina NCIMB 400, флавоцитохрома с 3 -фумаратредуктазы Fcc 3 -f (WP_041413240) S. frigidimarina NCIMB 400 и флавоцитохрома с 3 -фумаратредуктазы Fcc 3 -o (WP_011071245) S. oneidensis MR-1.
97 Fcc 3 -o Shewanella oneidensis MR-1
Ifc 3 Shewanella frigidimarina strain NCIMB 400
Fcc 3 -f Shewanella frigidimarina strain NCIMB 400
Mcc Geobacter sulfurreducens AM-1
предполагаемый цитохром с Anaeromyxobacter dehalogenans 2CP-1 цитохром с Wolinella succinogenes DSM 1740
0.5
Рис . 2. Дендрограмма родства цитохромных доменов Mcc Geobacter sulfurreducens AM-1 (AJY71932, С-концевая область) и соответствующих доменов (N-концевые области гомологичных белков: предполагаемого белка A2cp1_1860 (WP_012633121) из Anaeromyxobacter dehalogenans 2CP-1 и исследованных эспериментально гемовой субъединицы флавоцитохрома с (WP_011138087) из Wolinella succinogenes DSM 1740, флавоцитохрома с 3 -фумаратредуктазы Ifc 3 (WP_011638036) Shewanella frigidimarina NCIMB 400, флавоцитохрома с 3 -фумаратредуктазы Fcc 3 -f (WP_041413240) S. frigidimarina NCIMB 400 и флавоцитохрома с 3 -фумаратредуктазы Fcc 3 -o (WP_011071245) S. oneidensis MR-1.
80 Geobacter sulfurreducens AM-1
Anaeromyxobacter dehalogenans 2CP-1
100 Shewanella frigidimarina NCIMB 400
Shewanella oneidensis MR-1
Wolinella succinogenes DSM 1740
0.05
Рис . 3. Дендрограмма родства по генам 16S рРНК Geobacter sulfurreducens AM-1 и бактерий, имеющих гомологи Mrd и Mcc: Anaeromyxobacter dehalogenans 2CP-1, Wolinella succinogenes DSM 1740, Shewanella frigidimarina NCIMB 400, S. oneidensis MR-1.
Как следует из представленных дендрограмм (рис. 1 и 2) фумаратредуктазы Fcc 3 -f, Fcc 3 -o и Ifc 3 двух видов шеванелл имеют гораздо больше сходства между собой, чем их гомологи из других бактерий. G. sulfurreducens АМ-1 и A. dehalogenans 2CP-1, имеющий гомологи Mrd и Mcc наибольшего сходства, кроме того, и сами являются более близкими родственниками, чем бактерии W. succinogenes DSM 1740 или Shewanella (рис. 3).
Консервативные участки Mrd и Mcc. Для обоих хромопротеидов метакрилатной редокс системы (и для Mrd, и для Mcc) показано сходство c флавоцитохромами с Fcc 3 -f (WP_041413240), Ifc 3 (WP_011638036) и Fcc 3 -o (WP_011071245) (табл.). Сходство с Mrd обнаружено для С-концевых последовательностей этих флавоцитохромов на участке между 140-ым и 590-ым аминокислотными остатками (рис. 4). Сходство с Mcc из G. sulfurreducens AM-1 наблюдается с N-концевыми последовательностями обсуждаемых флавоцитохромов с на участке до 125-ого аминокислотного остатка (рис. 5).
У растворимых периплазматических фумаратредуктаз шеванелл и Mrd обнаружены консервативные последовательности (рис. 4), указывающие на принадлежность к FAD-связывающим белкам. У растворимых периплазматических фумаратредуктаз шеванелл и Mcc обнаружены отщепляемые сигнальные пептиды типа Sec (табл.), а также консервативные последовательности CXXCH (рис. 5), указывающие на принадлежность к цитохромам с.
На рисунке 4 хорошо видно присутствие консервативного фосфатсвязывающего (или динуклеотидсвязывающего мотива – ДСМ) участка, характерного для всех FAD- и NAD(P)H-зависимых оксидоредуктаз: xhxhGxGxxGxxxhxxh(x)8hxhE(D), где x - любая аминокислота, h – гидрофобная аминокислота (Eschenbrenner et al., 2001). В случае Mrd он представлен 69-98 аминокислотными остатками незрелого белка (Arkhipova et al., 2015). В случае растворимых периплазматических фумаратредуктаз шеванелл: 146-175 аминокислотными остатками у Ifc3 и 153-182 аминокислотными остатками у Fcc3-f из Shewanella frigidimarina NCIMB 400 (рис. 4), 152181 аминокислотными остатками у Fcc3-o из Shewanella oneidensis MR-1. Центральная часть консенсуса, GxGxxG, представляет собой глицин-богатую часть петли, соединяющей первую β-складку в укладке Россманна (β1α1β2α2β3) с первой α-спиралью, направленной в сторону остатка пирофосфата для компенсации заряда. В целом этот мотив имеет структуру β-складка-поворот-β-складка и формирует гибкий «зажим», окружающий и «заякоривающий» пирофосфат FAD (Hanks, Hunter, 1995).
Таблица
Флавоцитохромы с бактерий рода Shewanella, гомологичные
цитох
с и
из
M-1
Организм
Белок
№ в базе данных
к S
Я й
с
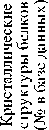
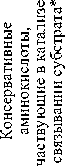
(ссылка)
Shewanella frigidimarina NCIMB 400
Флавоцитохром с 3 -фумаратредуктаза Ifc 3 WP_011638036
53%/36% с Mrd
51%/39% с Mcc
86% (142-582), 3×10-76 с Mrd
40% (27-114), 1×10-09 с Mcc
|
Sec |
H382, R419, H521, |
|||
|
588 амк |
(22 амк) |
4 |
1Q08 |
R561 |
|
63 кДа |
(Bamford et al. |
|
Shewanella |
Флавоцитохром с 3 - |
|
frigidimarina |
фумаратредуктаза Fcc-i-f |
|
NCIMB 400 |
cc 3 - |
|
WP_041413240 |
Shewanella oneidensis MR-1
Флавоцитохром с 3 -фумаратредуктаза Fcc 3 -o
WP_011071245
|
51%/35% с Mrd 53%/38% с Mcc |
84% (164-590), 2×10-63 с Mrd 48% (13-121), 6×10-11 с Mcc |
596 амк 63 кДа |
|
54%/ 38% с Mrd |
86% (149-590), 2×10-72 с Mrd |
596 амк |
|
59%/46% с Mcc |
35% (40-122), 3×10-10 с Mcc |
62.4 кДа |
H390, T402, R427,
|
Sec (25 амк) |
4 |
1QJD |
H529, R569 (Taylor et al. 1999; Doherty et al. 2000) |
|
Sec |
R426, H528, |
||
|
(25 амк) |
4 |
1D4E |
R569 (Leys et al. 1999) |
Примечание. * Номера аминокислотных остатков, участвующих в катализе и связывании субстрата, указаны для незрелых белков растворимых фумаратредуктаз Shewanella, в которых присутствуют отщепляемые сигнальные пептиды типа Sec.
Mrd 65 ---------D--------------ETFDVVVIGSGFAGLAAAAEAAGKGASVVILEKMP 100
Ifc3 128 D--QDKI--Q-KAIAAGPSETTQVLVVGAGSAGFNASLAAKKAGANVILVDKAP176
Fcc3-f 128 -PtIaElAKDKSErQ-AALASAPHDTVDVVVVGSGGAGFSAAISATDSGAKVILIEKEP184
Fcc3-o 130 vP-V-D-A-DKAA-QdKAIAAGVKETTDVVIIGSGGAGLAAAVSARDAGAKVILLEKEP183
* :*::*:::*:*:**::*:::*:::**:*::::*:*
Mrd 101 IYGGNS-IINGGEYNA-WTDGQ[4]TLKLG-DDSAE-WH-KnDTLKGGDFLGYPELVEV155
Ifc3 177 FSGGNS-MISAGGMNAVGTKQQ TAH-GVEDKVE-WFiE-DAMKGGRQQNDIKLVTI228
Fcc3-f 185 VIGGNAKL-AAGGMNAAWTDQQ m KAK-KITDSPELMF-E-DTMKGGQNINDPALVKV236
Fcc3-o 184 IPGGNTKL-AAGGMNAAETKPQ -AKLGIEDKKQIMI-D-DTMKGGRNINDPELVKV235
::***: : ::*::** :*::* :: : :*::: :: : *::***:::::::**::
Mrd 156 LAEGAPKALDWMvEE-GG-L-KLRPI[4]GGHSKYRTH--T--cvEAS-GRGYVEAL-R 206
Ifc3 229 LAEQSADGVQWL-ESLGANLDDLKRS GGARVDRTHRPHGG--KSS-GPEIIDTL-R279
Fcc3-f 237 LSSHSKDSVDWM-TAMGADLTDVGMM GGASVNRAHRPTGG---AGVGAHVVQVLYD288
Fcc3-o 236 LANNSSDSIDWL-TSMGADMTDVGRM GGASVNRSHRPTGG---AGVGAHVAQVLWD287
*::::::::: *: :: *: : ::::: **::::*:* : :: *::::::* :
Mrd 207 RIVDKRGakVRLR-N-EVTWIWRKDtD-GPILGVEVN---TGRRKVNiAvRkGLVLASG259
Ifc3 280 KAAKEQG--IDTRLNSRVVKLVVND-DH-SVVGAVVHGKHTGYYMIG-A-K-SVVLATG231
Fcc3-f 289 N-AVKRN--IDLRMNTRGIEVLK-D-DKGTVKGILVKGMYKGYYWVK-A-D-AVILATG339
Fcc3-o 288 N-AVKRG--TDIRLNSRVVRILE-D-ASGKVTGVLVKGEYTGYYVIK-A-D-AVVIAAG338
: ::::: :::* * ::::::: * : :::*::*: :*::::: * : ::::*:*
Mrd 260 GFSRDvaMRRiyVPYLDET---FNCS--NQKGATGEM-IRYAKAIGAETIHMSYIQLYP312
Ifc3 232 GYGMN--KEM--IAYYRPTMK--DMTssNNITATGDGvL-MAKEIGASMTDIDWVQAHP383
Fcc3-f 340 GFAKN--NER--VAKLDPSLKGFIST--NQPGAVGDG-LDVAENAGGALKDMQYIQAHP391
Fcc3-o 339 GFAKN--NER--VSKYDPKLKGFKAT--NHPGATGDG-LDVALQAGAATRDLEYIQAHP390
*:::: ::: ::::::: ::: *:::*:*:: : :*:::*:::::::::*::*
Mrd 313 -FAdPE-TGTLdV-EAlfpFRGPGvGIVyVTEKGKRFVNELERRDVISNAEMKTGGKKT368
Ifc3 384 TV--GKdSRIL-ISET---VRGVG-AVM-VNKDGNRFISELTTRDKASDAILKQPGQFA434
Fcc3-f 392 TLS-VK-GGVM-VTEA---VRGNG-AIL-VNREGKRFVNEITTRDKASAAILAQTGKSA442
Fcc3-o 391 TYS-PA-GGVM-ITEA---VRGNG-AIV-VNREGNRFMNEITTRDKASAAILQQKGESA441
: :: :::: : *: :**:* ::: *:::*:**::*:::**::*:*:::::*:::
Mrd 369 YSIFNHEmVVNmgsKE-EEVEK--GLarGrFV-KADSIAELAgK--IGID---ADvLVA418
Ifc3 435 WIIFDNQ-LYK---KA-KMVRGYDHL--E-MLYKGDTVEQLA-K-STGM--KvAD-LAK480
Fcc3-f 443 YLIFDDS-V-R---KSLSKIDKYIGL--G-VAPTADSLVKLG-KmE-GIDGK-A--LTE488
Fcc3-o 442 YLVFDDS-I-R---KSLKAIEGYVHL--N-IVKEGKTIEELA-K-QIDVPA--AE-LAK487
:::*::: : : *: ::::: :* : :: :::::::*: * ::* *::
Mrd
Ifc 3
Fcc 3 -f Fcc 3 -o
419 TI-KQHNAYIKNKKDPDYQK-NITdRMVTLEQGPFYAVaQ-WPAVHHTMGGLRINTNAQ 474
481 TV-SDYNGYVASGKDTAFGRADMP---LNMTQSPYYAV-KVAPGIHHTMGGVAINTTAS 534
489 TV-ARYNSLVSSGKDTDFERPNLP-RALN--EGNYYAI-EVTPGVHHTMGGVMIDTKAE 542
488 TVtA-YNGFVKSGKDAQFERPDLP-RELV--VAPFYAL-EIAPAVHHTMGGLVIDTKAE 541
*: ::*::::::**::::: ::: :: ::::**: : :*::******::*:*:*:
Mrd 475 VLDI-WGKI-IPRLYAAGEVTGGVHGSNRLGANAIPDATV-FGRIAGTNAAS-GR-V 526
Ifc 3 535 VLDLQS-KP-IDGLFAAGEVTGGVHGYNRLGGNAIADTVV-FGRIAGDNAAKHALDK 588
Fcc 3 -f 543 VMNAK--KQvIPGLYGAGEVTGGVHGANRLGGNAISD-IITFGRLAGEEAAKYSKKN 596
Fcc 3 -o 542 VKSEKTGKP-ITGLYAAGEVTGGVHGANRLGGNAISD-IVTYGRIAGASAAKFAKDN 596
*::: *: *::*::**********:****:***:* :: :**:**::**: :: :
Р ис . 4 . Множественное выравнивание Mrd Geobacter sulfurreducens AM-1 и периплазматических фумаратредуктаз шеванелл: Ifc 3 (WP_011638036) Shewanella frigidimarina NCIMB 400, Fcc 3 -f - Fcc 3 (WP_041413240) S. frigidimarina NCIMB 400 и Fcc 3 -o - Fcc 3 (WP_011071245) S. oneidensis MR-1. Серым цветом отмечены консервативные аминокислотные последовательности и аминокислоты, участвующие в катализе и связывании субстрата (Bamford et al., 1999; Leys et al., 1999; Taylor et al., 1999; Doherty et al., 2000).
Другой консервативный участок связывания FAD - 11-аминокислотный сегмент T(S)xxxxxF(Y)hhGD(E) (Eggink et al., 1990) -присутствует в аминокислотных последовательностях Mrd (Arkhipova et al., 2015) и флавоцитохромов с шеванелл в усечённом виде (рис. 4): без первого остатка треонина обсуждаемого участка. Данному участку соответствуют 487-491 аминокислоттные остатки Mrd, 547-551
аминокислотные остатки Ifc 3 , 555-559 аминокислотные остатки Fcc 3 -f, 555-559 аминокислотные остатки Fcc 3 -o.
Mcc 1 [112]IGKPADEDLEATTRIMAGMS GATFMASG HYAQGVPCSGCHGA154
Ifc3 1 M---KLKYLVSAMALVVLSS GTAMAKTPDMGSFHADMGSCQSCHAK43
Fcc 3 -f 1 -----MKKMNLAVCIATLMG[5]GTAVAADN-LAEFHVQNQECDSCHTP 44
Fcc3-o 1 MFTRKIQKTALAMLISGAMA GTAYAAPEVLADFHGEMGGCDSCHVS46
::::::::::::::: *::::::: :::::::*::**::
Mcc 155 G---FPAIGDTVENDKCLACHGSYDKLAETTKPKtayEPNPHRSHL-GDIACT 203
Ifc 3 44 P--IKVTDSETHENAQCKSCHGEYAELAN--DKL---QFDPHNSHL-GDINCT 88
Fcc 3 -f 45 D-GELSNDSLTYENTQCVSCHGTLAEVAETTKHE---HYNAHASHFPGEVACT 94
Fcc 3 -o 47 DkGGVTNDNLTHENGQCVSCHGDLKELAAAAPKD---KVSPHKSHLIGEIACT 96
Mcc 204 ACHYGHQKSVLYCKDCHpKFTIT-IPFGK------------------------ 231
Ifc 3 89 SCHKGHEEPKFYCNECH-SFDIKpMPFSDAK---KKKSWDDGWDQDKIQKAIA 137
Fcc 3 -f 95 SCHSAHEKSMVYCDSCH-SFDFN-MPYAKKWlrdEPTIAELAKDKSERQAALA 145
Fcc 3 -o 96 SCHKGHEKSVAYCDACH-SFGFD-MPFGGKW---ERKFVPVDADKAAQDKAIA 144 :**::*:::::**::** :*::: :*:::
Рис . 5 . Множественное выравнивание Mcc Geobacter sulfurreducens AM-1 и периплазматических фумаратредуктаз шеванелл: Ifc 3 (WP_011638036) Shewanella frigidimarina NCIMB 400, Fcc 3 -f - Fcc 3 (WP_041413240) S. frigidimarina NCIMB 400 и Fcc 3 -o - Fcc 3 (WP_011071245) S. oneidensis MR-1.
Кроме того, Mrd содержит консервативные для фумаратредуктаз аминокислотные остатки, участвующие в катализе (Bamford et al., 1999; Leys et al., 1999; Taylor et al., 1999; Doherty et al., 2000), а именно – гистидин-461 и аргинины – R501 и R353 (рис. 4) (Arkhipova et al., 2015).
Пространственная структура Mrd и Mcc. Мы осуществили компьютерное моделирование пространственной структуры Mrd и Mcc G. sulfurreducens AM-1 (рис. 6 и 7). Оба хромопротеида метакрилатной редокс системы проявляют высокое структурное сходство с флавоцитохромом Ifc 3 (WP_011638036) S. frigidimarina NCIMB 400; при этом Mcc сходен с малым N-концевым гемсодержащим доменом белка, а Mrd – с большим С-концевым FAD-связывающим.
Mcc G. sulfurreducens AM-1 структурно сходен с N-концевым гемсодержащим доменом фумаратредуктаз бактерий рода Shewanella. Но нужно отметить, что с N-конца он удлинен относительно этого домена. За счет этого в его аминокислотной последовательности можно найти не 4, как у этих белков, а 7 гем-связывающих участков, хотя Mcc – тетрагемовый, как было показано экспериментально (Mikoulinskaia et al., 1999).
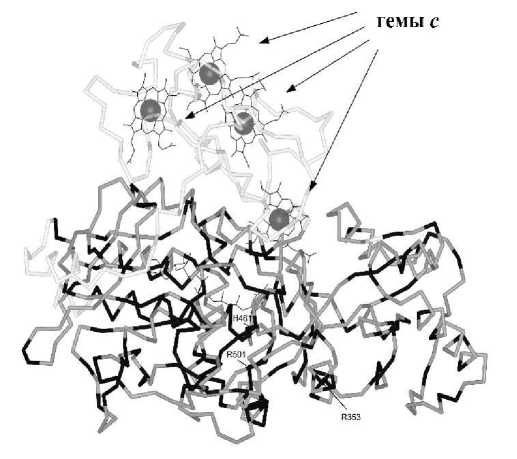
Р ис . 6 . Результат пространственного наложения первичной структуры
Mrd Geobacter sulfurreducens AM-1 на известную трехмерную структуру фумаратредуктазы Ifc 3 (WP_011638036) из Shewanella frigidimarina NCIMB 400. Чёрным цветом выделены консервативные аминокислоты; насыщенным серым цветом окрашены участки одинаковой вторичной структуры.
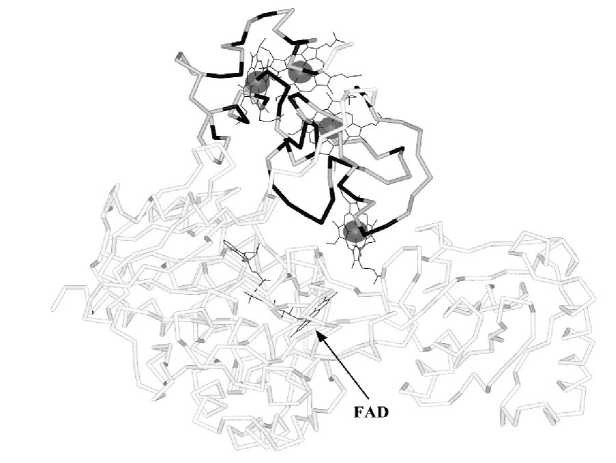
Р ис . 7 . Результат пространственного наложения первичной структуры
Mcc Geobacter sulfurreducens AM-1 на известную трехмерную структуру фумаратредуктазы Ifc 3 (WP_011638036) из Shewanella frigidimarina NCIMB 400. Чёрным цветом выделены консервативные аминокислоты; насыщенным серым цветом окрашены участки одинаковой вторичной структуры.
Обсуждение
Гомологи Mrd и Mcc - растворимые трёхдоменные фумаратредуктазы. Ненасыщенные органические соединения используются анаэробными бактериями в качестве терминальных акцепторов дыхательных цепей анаэробных бактерий (Архипова, Акименко, 2005). Среди всех известных ферментных систем, которые восстановливают двойные связи (Hägerhäll, 1997; Gordon et al., 1998; Dobbin et al., 1999; Mikoulinskaia et al., 1999; Kröger et al., 2002; Maier et al., 2003; Архипова, Акименко, 2005; Hess et al., 2013; Iverson, 2013), фумаратредуктазы S. frigidimarina и S. oneidensis и метакрилатная редокс система G. sulfurreducens AM-1 имеют ряд общих черт: 1) они локализуются в периплазме, 2) в качестве коферментов имеют гемы с и нековалентно связанный FAD (Gordon et al., 1998; Dobbin et al., 1999; Mikoulinskaia et al., 1999; Maier et al., 2003; Архипова, Акименко, 2005). Метакрилат восстанавливает двухкомпонентная система, включающая флавопротеин Mrd и четырёхгемовый цитохром с Mcc. Эта система не восстанавливает фумарат (Mikoulinskaia et al., 1999). Периплазматические фумаратредуктазы бактерий рода Shewanella мономерны (Gordon et al., 1998; Dobbin et al., 1999; Maier et al., 2003).
Наибольшим сходством (E=3·10-76) с Mrd среди этих фумаратредуктаз обладает периплазматический флавоцитохром с Ifc 3 (WP_011638036) из S. frigidimarina NCIMB 400 (табл.). Если для двух других флавоцитохромов c-фумаратредуктаз Fcc 3 -f из S. frigidimarina NCIMB 400 (Gordon et al., 1998) и Fcc 3 -o из S. oneidensis MR-1 (Maier et al., 2003)] главной физиологической функцией является восстановление фумарата, то Ifc 3 проявляет фумаратредуктазную активность только in vitro (Dobbin et al., 1999). Флавоцитохром с Ifc 3 экспрессируется в анаэробно растущих клетках, когда единственными терминальными акцепторами восстановительных эквивалентов служат цитрат или пирофосфат железа, но не фумарат. Согласно результатам исследований пространственной структуры, флавоцитохром с Ifc 3 – асимметричный октагемовый дифлавиновый гомодимер с нативной молекулярной массой 130 кДа (Bamford et al., 1999).
Мономерные фумаратредуктазы шеванелл, для которых известны кристаллические структуры (Bamford et al., 1999; Leys et al., 1999; Taylor et al., 1999; Doherty et al., 2000) – трехдоменные белки. Например, полипептидная цепь в каждой субъединице димера Ifc3 содержит 1) N-концевой домен (2-95 аминокислотные остатки), связывающий ковалентно 4 гема с, 2) каталитический FAD-связывающий домен (100-359 аминокислотные остатки и 498-565 аминокислотные остатки) и 3) каталитический домен-«зажим» (360497 аминокислотные остатки) (Bamford et al., 1999). Последний вследствие своей подвижности играет важную роль в конформационном переходе молекулы фермента из открытой в закрытую конформацию и обратно, обеспечивая таким образом доступ субстрата и выход продукта (Bamford et al., 1999).
Mrd и по последовательности (рис. 4), и структурно (рис. 6) повторяет оба каталитических домена растворимых фумаратредуктаз шеванелл. Mcc (рис. 5 и 7) проявляет сходство с N-концевым доменом этих белков. Таким образом, пространственная модель метакрилатной редокс системы, вероятно, аналогична таковой растворимых фумаратредуктаз рода Shewanella. Флавоцитохромы с-фумаратредуктазы бактерий рода Shewanella, очевидно, имеют модулярную структуру: N-концевой модуль выполняет функцию передачи восстановительных эквивалентов, а С-концевой - обладает ферментативной активностью.
Mrd и его гомологи из шеванелл - представители семейства FAD-связывающих белков глутатионредуктаз. Результаты пространственного наложения (рис. 6 и 7) показывают, что структура Mrd имеет черты, характерные для FAD-связывающих белков. Ранее было показано, что моно- и динуклеотидсвязывающие белки имеют сходную трехмерную структуру, содержащую консервативные участки, критичные для связывания кофактора, при значительной общей вариабельности аминокислотной последовательности. Впервые подобная укладка была описана Россманном (Rossmann et al., 1974). В ее основе лежит мононуклеотид-связывающий структурный мотив βαβαβ. Согласно классификации, основанной на вторичной структуре (Dym, Eisenberg, 2001), Mrd и его гомологи Ifc 3 (WP_011638036), Fcc 3 -f (WP_041413240) и Fcc 3 -o (WP_011071245) можно отнести к семейству FAD-связывающих белков GR (глутатионредуктаз). Для строения домена связывания FAD у белков этого семейства характерно наличие укладки Россманна (β1α1β2α2β3). В целом белки семейства имеют пять центральных параллельных β-складок, окруженных α-спиралями с одной стороны и тремя антипараллельными β-складками – с другой (Dym, Eisenberg, 2001). FAD у белков семейства имеет вытянутую конформацию, в которой остатки аденина и изоаллоксазина расположены дистально друг от друга. Кроме того, у членов семейства консервативно расположение FAD: кольцо аденина направлено внутрь FAD-связывающего домена, кольцо изоаллоксазина – наружу (Dym, Eisenberg, 2001). Для Mrd, таким образом, свойственна подобная структура и подобное расположение FAD.
Роль консервативных аминокислот в катализе. Как уже упоминалось в РЕЗУЛЬТАТАХ, в последовательности Mrd выявлены консервативные аминокислоты: гистидин-461 и аргинины – R501 и R353 (рис. 4). Работы по кристаллическим структурам растворимых фумаратредуктаз Shewanella (Bamford et al., 1999; Leys et al., 1999;
Taylor et al., 1999) появились одновременно - в 1999 году. По мнению Bamford et al. (1999), аргинины Ifc 3 S. frigidimarina, аналогичные R501 и R353 метакрилатредуктазы, ориентируют субстрат внутри активного центра фермента и способствуют его движению к кофактору FAD и предполагаемому участку восстановления фумарата. Кроме того, H388 у Ifc 3 участвует в связывании субстрата (Bamford et al., 1999). Донором протона при катализе, как предполагалось, является H521 (аналог H461 метакрилатредуктазы) (Bamford et al., 1999). Однако, по мнению исследователей кристаллической структуры Fcc 3 -o (Leys et al., 1999), донором протона служит R426 (аналог R353 метакрилатредуктазы). К такому же выводу пришли и исследователи мутантной формы кристаллов Fcc 3 -f (Doherty et al., 2000): донор протона для карбаниона - R427 (аналог R353 метакрилатредуктазы).
Консервативные аминокислоты Mrd (H461, R501 и R353), вероятно, как и в случае фумаратредуктаз шеванелл, стабилизируют переходное состояние во время катализа, обеспечивая делокализацию отрицательного заряда промежуточного карбаниона (Leys et al., 1999). Аргинин, аналогичный R501 Mrd, у фумаратредуктаз взаимодействует двумя боковыми аминогруппами с обоими атомами кислорода первой карбоксильной группы сукцината, ориентируя субстрат параллельно изоаллоксазиновому кольцу (Leys et al., 1999). Один атом кислорода этой карбоксильной группы образует водородную связь с расположенным рядом консервативным глицином (у Mrd это G503). Близкое пространственное расположение двух консервативных аргининов стабилизируется либо карбоксильной группой субстрата, либо (в отсутствие субстрата в активном центре) взаимодействием с консервативным остатком глутаминовой кислоты (у Mrd - E324). Атом азота этого аминокислотного остатка также образует водородную связь со второй карбоксильной группой сукцината (Leys et al., 1999). Можно предположить, что такие же связи образует метакрилат. Двух других консервативных остатков растворимых фумаратредуктаз шеванелл (гистидина и серина/треонина) (Bamford et al., 1999; Leys et al., 1999; Taylor et al., 1999 также взаимодействующих с сукцинатом или фумаратом, у Mrd нет: в положении 311 вместо гистидина находится триптофан, в положении 323 вместо серина или треонина – валин. Поскольку эти аминокислоты также участвуют в связывании субстрата, можно предположить, что их отсутствие связано с субстратной специфичностью Mrd G. sulfurreducens AM-1.
На основании структурного наложения Mcc можно предположить, что имидазольные группы двух гемов цитохрома имеют параллельное и двух – перпендикулярное расположение друг относительно друга, аналогично Fcc 3 -o (Leys et al., 1999), что
Вестник ТвГУ. Серия "Биология и экология". 2017. № 2. обеспечивает тонкую «настройку» уменьшения потенциала гемов (Taylor et al., 1999).
Пространственное взаимодействие консервативных аминокислот при связывании субстрата. Критичным для молекулярного узнавания FAD является остаток пирофосфата, в то время как кольцо изоаллоксазина участвует в катализе, а кольцо аденина стабилизирует связывание кофактора (Mathews, 1991). Как результат, изоаллоксазин и аденин могут взаимодействовать с различными аминокислотами в разных FAD-связывающих белках, а вот участки связывания пирофосфата гораздо более консервативны (Dym, Eisenberg, 2001).
Можно выделить два консервативных участка: ДСМ (xhxhGxGxxGxxxhxxh(x) 8 hxhE(D), где x - любая аминокислота, h – гидрофобная аминокислота) и 11-аминокислотный сегмент T(S)xxxxxF(Y)hhGD(E). Оба консервативных участка присутствуют у Mrd (рис. 4, РЕЗУЛЬТАТЫ). Эти участки, широко разнесенные по аминокислотной последовательности, тем не менее расположены в пространственной близи (рис. 6).
ДСМ характерен для всех FAD- и NAD(P)H-зависимых оксидоредуктаз и обычно имеет N-концевое расположение (Eschenbrenner et al., 2001). Как уже говорилось в РЕЗУЛЬТАТАХ, центральная часть ДСМ - GxGxxG - соединяет первую β-складку в укладке Россманна (β1α1β2α2β3) с первой α-спиралью и образует «зажим» для удержания пирофосфата FAD (Hanks, Hunter, 1995). Роль каждого консервативного остатка глицина хорошо изучена (Wierenga et al., 1986): первый строго консервативный остаток глицина обеспечивает поворот белковой цепи, важный для расположения второго остатка глицина. Второй остаток глицина, благодаря отсутствию боковой цепи, обеспечивает близкий контакт белковой цепи с пирофосфатом, особенно атомами O P1 и O P2 . Третий остаток глицина расположен в начале альфа-спирали и позволяет близкий контакт α-спирали с β-складкой. Гидрофобные остатки обеспечивают гидрофобные взаимодействия α-спирали с β-складкой. Консервативный отрицательно заряженный остаток глутаминовой или аспарагиновой кислоты (Е97 Mrd) образует водородные связи со вторым гидроксилом рибозы остатка аденозина (Wierenga et al., 1986). Последний консервативный остаток глицина и его аминогруппа образует водородную связь с молекулой воды (Bottoms et al., 2002). Молекула воды не только стабилизирует конформацию петли (за счёт образования водородных связей по крайней мере с двумя остатками глицин-богатой петли), но и поддерживает конформацию кофактора (Wierenga et al., 1986).
Другой высококонсервативный участок связывания FAD был впервые идентифицирован у рубредоксинредуктазы (Eggink et al., 1990), и представляет собой 11-аминокислотный сегмент T(S)xxxxxF(Y)hhGD(E). В аминокислотной последовательности Mrd отсутствует первый треонин обсуждаемого участка, остальные же аминокислоты – в наличии (487-491). Консервативные остатки глицина и отрицательно заряженной аминокислоты (в нашем случае – глутаминовой) являются частью петли, связывающей O P1 и O P2 атомы остатка пирофосфата FAD. Ее расположение видно на рисунке 6.
Заключение. Изложенные в статье результаты получены пространственным наложением аминокислотных последовательностей белков метакрилатной редокс системы G. sulfurreducens AM-1 на известные кристаллические структуры растворимых фумаратредуктаз бактерий рода Shewanella. Показано, что Mrd и растворимые фумаратредуктазы шеванелл относятся к семейству FAD-связывающих белков GR (глутатионредуктаз). Для Mrd и таких фумаратредуктаз обнаружены наличие укладки Россманна (β1α1β2α2β3) и консервативных участков связывания пирофосфата: динуклеотидсвязывающий мотив (ДСМ) и усечённый 11-аминокислотный сегмент. Кроме того, полученные сведения указывают на участие в катализе консервативных аминокислот Mrd: H461, R501 и R353. Наиболее вероятным донором протона для карбаниона является аргинин R353.
Белки даже с не очень схожими аминокислотными последовательностями часто обладают большим структурным сходством, обусловленным их функцией (Dym, Eisenberg, 2001). Так, известные трёхмерные структуры 32 разных флавопротеинов и их укладки показывают более высокое сходство, чем можно было бы ожидать, сравнивая их первичные структуры (Dym, Eisenberg, 2001). Выраженное сходство структур фумаратредуктаз S. frigidimarina и S. oneidensis и метакрилатной редокс системы G. sulfurreducens AM-1 свидетельствует об их общих происхождении и физиологической роли (или функциональной нагрузке). Не исключено, что основной функцией этих ферментов может оказаться восстановление природного аналога синтетического метакрилата – акрилата (Arkhipova et al., 2015).
Авторы искренне признательны нс, кбн Института математических проблем биологии РАН, Пущино, М.С. Романову за помощь в подготовке рисунков.
Об авторах:
Архипова О.В. Пространственная модель анаэробной метакрилатредуктазной системы / О.В. Архипова, О.Ю. Трошина, Г.В. Микулинская // Вестн. ТвГУ. Сер.: Биология и экология. 2017. № 2. С. 306-323.
Список литературы Пространственная модель анаэробной метакрилатредуктазной системы
- Архипова О.В., Акименко В.К. 2005. Ненасыщенные органические кислоты -терминальные акцепторы редуктазных цепей анаэробных бактерий//Микробиология. Т. 74. С. 725-737.
- Arkhipova O.V., Meer M., Mikoulinskaia G.V., Zakharova M.V., Galushko A.S., Akimenko V.K., Kondrashov F.A. 2015. Recent origin of the methacrylate redox system in Geobacter sulfurreducens AM-1 through horizontal gene transfer//PLoS ONE. 10(5):e0125888 DOI: 10.1371/journal.pone.0125888
- Bamford V., Dobbin P.S., Richardson D.J., Hemmings A.M. 1999. Open conformation of a flavocytochrome c3 fumarate reductase//Nat. Struct. Biol. V. 6. P. 1104-1107.
- Bogachev A.V., Bertsova Y.V., Bloch D.A., Verkhovsky M.I. 2012. Urocanate reductase: identification of a novel anaerobic pathway in Shewanella oneidensis MR-1//Mol. Microbiol DOI: 10.1111/mmi.12067
- Bottoms C.A., Smith, P.E., Tanner J.J. 2002. A structurally conserved water molecule in Rossmann dinucleotide-binding domains//Protein Sci. Vol. 11. P. 2125-2137.
- Caccavo F.J.R., Lonergan D.J., Lovley D.R., Davis M., Stolz J.F., McInerney M.J. 1994. Geobacter sulfurreducens sp. nov., a hydrogen-and acetate-oxidizing dissimilatory metal-reducing microorganism//Appl. Environ. Microbiol. Vol. 60. P. 3752-3759.
- Dobbin P.S., Butt J.N., Powell A.K., Reid G.A., Richardson D.J. 1999. Characterization of a flavocytochrome that is induced during the anaerobic respiration of Fe3+ by Shewanella frigidimarina NCIMB 400//Biochem. J. Vol. 342. P. 439-448.
- Doherty M.K., Pealing S.L., Miles C.S., Moysey R., Taylor P., Walkinshaw M.D., Reid G.A., Chapman S.K. 2000. Identification of the Active Site Acid/Base Catalyst in a Bacterial Fumarate Reductase: A Kinetic and Crystallographic Study//Biochemistry. Vol. 39. P. 10695-10701.
- Dym O., Eisenberg D. 2001. Sequence-structure analysis of FAD-containing proteins//Protein Sci. Vol. 10. P. 1712-1728. Review.
- Eggink G., Engel H., Vriend G., Terpstra P., Witholt B. 1990. Rubredoxin reductase of Pseudomonas oleovorans. Structural relationship to other flavoprotein oxidoreductases based on one NAD and two FAD fingerprints//J. Mol. Biol. Vol. 212. P. 135-142.
- Eschenbrenner M., Chlumsky L.J., Khanna P., Strasser F., Jorns M.S. 2001. Organization of the multiple coenzymes and subunits and role of the covalent flavin link in the complex heterotetrameric sarcosine oxidase//Biochemistry. Vol. 40. P. 5352-5367.
- Gordon E.H.J., Pealing S.L., Chapman S.K., Ward F.B., Reid G.A. 1998. Physiological function and regulation of flavocytochrome c3, the soluble fumarate reductase from Shewanella putrefaciens NCIMB 400//Microbiology. Vol. 144. P. 937-945.
- Gross R., Simon J., Kröger A. 2001. Periplasmic methacrylate reductase activity in Wolinella succinogenes//Arch. Microbiol. Vol. 176. V. 310-313.
- Hanks S.K., Hunter T. 1995. Protein kinases 6. The eukaryotic protein kinase superfamily: kinase (catalytic) domain structure and classification//FASEB J. Vol. 9. P. 576-596.
- Hess V., González J.M., Parthasarathy A., Buckel W., Müller V. 2013. Caffeate respiration in the acetogenic bacterium Acetobacterium woodii: a coenzyme A loop saves energy for caffeate activation//Appl. Environ. Microbiol. Vol. 79. P. 1942-1947.
- Hägerhäll C. 1997. Succinate: quinone oxidoreductases. Variations on a conserved theme//Biochim. Biophys. Acta. Vol. 1320, P. 107-141.
- Iverson T. 2013. Catalytic mechanisms of complex II enzymes: A structural perspective//Biochim. Biophys. Acta. Vol. 1827, P. 648-657.
- Kröger A., Biel S., Simon J., Gross R., Unden G., Lancaster C.R.D. 2002. Fumarate respiration of Wolinella succinogenes: enzymology, energetics and coupling mechanism//Biochim. Biophys. Acta. Vol. 1553. P. 23-38.
- Leys D., Tsapin A.S., Nealson K.H., Meyer T.E., Cusanovich M.A., Van Beeumen J.J. 1999. Structure and mechanism of the flavocytochrome c fumarate reductase of Shewanella putrefaciens MR-1//Nat. Struct. Biol. Vol. 6. P. 1113-1117.
- Li T., Bonkovsky H.L., Guo J. 2011. Structural analysis of heme proteins: implications for design and prediction//BMC Struct. Biol. Vol. 11 DOI: 10.1186/1472-6807-11-13
- Logan B. 2009. Exoelectrogenic bacteria that power microbial fuel cells//Nature Rev. Microbiol. V. 7. P. 375-383. 2113 DOI: 10.1038/nrmicro
- Lovley D.R. 2010. Powering microbes with electricity: direct electron transfer from electrodes to microbes//Environ. Microbiol. Rep DOI: 10.1111/j.1758-2229.2010.00211.x
- Maier T.M., Myers J.M., Myers C.R. 2003. Identification of the gene encoding the sole physiological fumarate reductase in Shewanella oneidensis MR-1//J. Basic Microbiol. Vol. 43. P. 312-327.
- Mathews F.S. 1991. New flavoenzymes//Curr. Opin. Struct. Biol. V. 1. P. 954-967.
- Methė B.A., Nelson K.E., Eisen J.A., Paulsen I.T., Nelson W. et al. 2003. Genome of Geobacter sulfurreducens: metal reduction in subsurface environments//Science. Vol. 302. P. 1967-1969.
- Mikoulinskaia (Arkhipova) O., Akimenko V., Galushko A., Thauer R., Hedderich R. 1999. Cytochrome c-dependent methacrylate reductase from Geobacter sulfurreducens AM-1//Eur. J. Biochem. Vol. 263. P. 346-352.
- Rossmann M.G., Moras D., Olsen K.W. 1974. Chemical and biological evolution of a nucleotide-binding protein//Nature. V. 250. P. 194-199.
- Tamura K., Stecher G., Peterson D., Filipski A., Kumar S. 2013. MEGA6: Molecular Evolutionary Genetics Analysis version 6.0//Mol. Biol. Evol. Vol. 30. P. 2725-2729.
- Taylor P., Pealing S.L., Reid G.A., Chapman S.K., Walkinshaw M.D. 1999. Structural and mechanistic mapping of a unique fumarate reductase//Nat. Struct. Biol. Vol. 6. P. 1108-1112.
- Wierenga R.K., Terpstra P., Hol W.G. 1986. Prediction of the occurrence of the ADP-binding beta alpha beta-fold in proteins, using an amino acid sequence fingerprint//J. Mol. Biol. Vol. 187. P. 101-107.


