Протеасомы и экзосомы при раке яичников: связь с особенностями клинического течения и прогнозом
Автор: Юнусова Наталья Валерьевна, Кондакова Ирина Викторовна, Коломиец Лариса Александровна, Молчанов Сергей Валерьевич
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Обзоры
Статья в выпуске: 4 (64), 2014 года.
Бесплатный доступ
Обсуждается роль циркулирующих протеасом (С-протеасом) - мультисубъединичных структур, обладающих несколькими протеолитическими активностями, и экзосом - внеклеточных везикул, осуществляющих межклеточный и межтканевой перенос биологически важных молекул (белков и микроРНК) в патогенезе рака яичников. В настоящее время имеются предпосылки для дальнейшего изучения роли С- протеасом и экзосом не только в качестве прогностических маркеров, но и как предикторов эффективности неоадъювантной химиотерапии и оптимальной циторедукции.
Циркулирующие протеасомы, экзосомы, рак яичников, прогноз, неоадьювантная химиотерапия
Короткий адрес: https://sciup.org/14056449
IDR: 14056449 | УДК: 618.11-006.6-036.1-037:577.112
Proteasomes and exosomes in ovarian cancer: ralation with disease prognosis and clinical outcome
The role of circulating proteasomes (C-proteasomes) representing a multisubunit complex with several proteolytically active sites, and exosomes, which are extracellular vesicles providing intracellular and interstitial transfer of biologically important molecules (proteins and miRNAs) in the pathogenesis of ovarian cancer, has been described. Currently, there are prerequisites for further study of the role of C-proteasome and exosome not only as prognostic markers, but also as predictors of the effectiveness of neoadjuvant chemotherapy and optimal cytoreduction.
Текст обзорной статьи Протеасомы и экзосомы при раке яичников: связь с особенностями клинического течения и прогнозом
В большинстве случаев рак яичников (РЯ) выявляется на III–IV стадии процесса. Так, в Российской Федерации в общей структуре РЯ удельный вес III стадии составляет 40,5 %, а IV стадии – 22,2 % [1]. Стандартная терапия диссеминированного РЯ состоит из циторедуктивной операции и химиотерапии с включением препаратов платины и таксанов, последовательность которых может быть различной [8, 21].
Одним из основных прогностических факторов эффективности лечения диссеминированного РЯ является объем остаточной опухоли (ОО) после циторедуктивной операции. Результаты опубликованного метаанализа, включающего 81 клиническое исследование, показали, что продолжительность жизни данной категории больных обратно пропорциональна размеру остаточной опухоли. При отсутствии макроскопически определяемой остаточной опухоли медиана выживаемости составляет 64 мес, при размерах ОО от 1 до 50 мм – 30 мес, более 50 мм – 19 мес [9]. Аналогичные результаты получены и в другом крупном проспективном рандомизированном исследовании, его авторами было показано, что в группе пациенток без остаточной опухоли медиана выживаемости составила 99,1
мес, при остаточной опухоли от 1 до 10 мм – 36,2 мес, более 10 мм – 29,6 мес [12].
При отсутствии условий для оптимальной первичной циторедуктивной операции у больных диссеминированным РЯ возможно проведение неоадъювантной химиотерапии (НАХТ), в отношении которой в литературе нет однозначного мнения. Ряд авторов видят преимущество этого метода лечения в том, что после НАХТ возможно увеличение числа оптимальных циторедуктивных операций по сравнению с первичной циторедукцией, кроме того, выполняется меньший объем операции, соответственно, наблюдаются меньшие кровопотеря и количество послеоперационных осложнений, более короткий период госпитализации, лучшее качество жизни больных [28, 33]. Другие исследователи считают, что НАХТ не приносит положительного результата при лечении распространенного РЯ [9]. Возможно, это обусловлено тем, что у пациенток, получавших НАХТ, были большая распространенность опухолевого процесса и более тяжелое состояние по сравнению с больными, подвергшимися первичному циторедуктивному вмешательству [24].
Неоднозначность мнения авторов выражается не только в целесообразности проведения НАХТ, но и в отношении схем терапии, количестве курсов, критериев оценки эффективности. Общепринятым опухолевым маркером для РЯ, который включен в стандарты обследования и динамического наблюдения, является СА-125. В то же время значение СА-125 как предиктора эффективности НАХТ и оптимальной циторедукции ограничивается низкой чувствительностью и специфичностью [17, 28]. Большие перспективы связывают с использованием нового опухолевого маркера – HE4 [30]. Показано, что предоперационный уровень сывороточного HE4 в большей степени, чем СА-125, может предсказывать оптимальную циторедукцию у больных с распространенным РЯ. В качестве наилучшей комбинации предикторов оптимальной циторедукции рассматривается сочетание HE4 с объемом асцита, чувствительность которой составила 100 %, специфичность – 89 % [7]. Эти данные хорошо коррелируют с результатами исследования J. Hynninen et al. [16], где сывороточный профиль HE4 при проведении НАХТ у больных с распространенным РЯ был связан с клиническим ответом.
В связи с этим перспективным направлением является поиск новых объективных предикторов эффективности НАХТ и оптимальной циторедукции, а также критериев прогноза течения диссеминированного РЯ. Наиболее перспективно изучение надмолекулярных полифункциональных систем, находящихся в кровотоке и других биологических жидкостях, к числу которых относятся циркулирующие протеасомы – мультисубъединичные белковые структуры, обладающие несколькими протеолитическими активностями, и экзосомы – внеклеточные везикулы, осуществляющие межклеточный и межтканевой перенос биологически важных молекул.
Циркулирующие протеасомы как возможные предикторы прогноза у больных раком яичников
Циркулирующие 20S протеасомы (С-протеасомы) – экстраклеточные формы протесом, обнаруженные в сыворотке и плазме крови, альвеолярной и цереброспинальной жидкости [15, 23]. Действуя в основном внутриклеточно, убиквитин-протеасомная система регулирует уровень биологически важных молекул, принимающих участие в пролиферации, апоптозе, миграции и дифференцировке клеток [3]. Одним из наиболее значимых этапов многих физиологических и патологических процессов является внутриклеточная деградация белков в протеасомах, в связи с чем протеасомам придается важное значение в онкогенезе [2, 4]. Основным компонентом убиквитин-протеасомной системы являются протеасомы – мультисубъединичные комплексы, включающие каталитическое ядро 20S, к которому присоединена одна или две регуляторные частицы [31]. Показано, что С-протеасомы, выделенные из плазмы здоровых доноров, по форме и размеру сходны с 20S протеасомами, выделенными из эритроцитов, обладают протеолитической активностью, содержат стандартные и иммунные субъединицы [34]. Повышенная концентрация циркулирующих протеасом выявлена в плазме больных острым лейкозом, миелопролиферативыми и некоторыми аутоиммунными заболеваниями, а также при некоторых солидных опухолях, таких как светлоклеточная карцинома почки, рак молочной железы, эпителиальный РЯ [10, 14, 15]. Показано, что эффективная химиотерапия острого лейкоза приводит к снижению и даже нормализации уровня
С-протеасом. Больные с хроническими лейкозами имеют субоптимальные уровни С-протеасом, однако при прогрессировании заболевания уровень циркулирующих протеасом значительно возрастает [34]. Больные светлоклеточным раком почки, отвечающие на сунитиниб, имели более низкие показатели С-протеасом по сравнению с рефрактерными к этому препарату новообразованиями [10]. Таким образом, начальный уровень и динамика изменения С-протеасом в сыворотке или плазме крови, по-видимому, могут отражать различные аспекты канцерогенеза как лейкозов, так и солидных опухолей, ассоциированы с чувствительностью опухолей к традиционных цитостатическим и таргетным препаратам.
Показано, что при эпителиальном РЯ концентрация C-протесом до лечения была выше, чем у здоровых доноров, а после завершения первичного лечения выше, чем до лечения, и ассоциировалась с объемом остаточной опухоли и общей выживаемостью [14]. Поскольку уровень С-протеасом коррелировал с объемом остаточной опухоли, то С-протеасомы могут рассматриваться в качестве прогностического маркера. Однако другие клинические ассоциации С-протеасом (как предикторов эффективности НАХТ и предикторов оптимальной циторедукции) ранее не изучались.
Экзосомы при раке яичников: функции и возможные перспективы исследования
Экзосомы представляют собой микроскопические внеклеточные везикулы диаметром 30–100 нм, секретируемые различными клетками и способные нести белковые маркеры и генетическую информацию, таким образом участвуя в межклеточной коммуникации. Полагают, что, кроме этой важной функции, экзосомы участвуют в горизонтальном переносе РНК и белков, облегчают иммунный ответ, участвуют в презентации антигенов и неклассической секреции белков, транспорте лекарств, в патогенезе болезней, связанных с расстройствами метаболизма и развитии злокачественных опухолей [5, 18, 26, 29]. Экзосо-мы могут играть важную, но пока недооцененную роль в восстановлении структуры и функции поврежденных органов. Экзосомы, секретируемые гемопоэтическими стволовыми клеткам, муль-типотентными клетками стромы и стволовыми клетками сердца, способны защитить от апоптоза клетки, уцелевшие в поврежденных тканях, стиму- лировать их пролиферацию и образование сосудов. Эти свойства экзосом связывают с тем, что они несут антиапоптотические и про-пролиферативные ростовые факторы и цитокины [20]. Экзосомы имеют цитоплазматическое происхождение и содержат определенный набор белков и РНК. Белковый состав экзосом отражает их происхождение. К числу белков-маркеров экзосом относят белки высококонсервативного семейства тетраспанинов, необходимые для связывания и транспортировки микроРНК (СD63, CD81 и СD9), Alix и Tsg101 – компонента эндосомного белкового комплекса сортировки, необходимого для транспортировки и биогенеза экзосом. Экзосомы богаты белками цитоскелета и актинсвязывающими белками, несут ГТФ-азы семейства Rab и аннексины, которые способствуют слиянию мембран. Также в экзосомах найдены белки теплового шока HSP60, HSP70, HSP90. Экзосомы, происходящие от клеток иммунной системы, богаты белками комплекса гистосовместимости II класса. Кроме того, экзо-сомы несут комплекс протеаз и их активаторов (активную форму металлопротеиназы ADAM10), ассоциированный с беременностью белок PAPP-A, прогепараназу, extracellular matrix metalloprotease inducer (EMMPRIN), urokinase-type plasminogen activator (uPA), матриксные металлопротеиназы (MMP-2,-9) [13, 18, 25]. При изучении экзосом, полученных в культуре мезенхимальных стволовых клеток методом масс-спектрометрии, были детектированы 7 альфа- и 7 бета-цепей 20S про-теасом. Полагают, что протеазы данных экзосом, главным образом 20S протеасом, ответственны за уменьшение повреждения клеток культуры кардиомиоцитов (моделирование ишемии и инфаркта миокарда) [20]. По сравнению с клетками экзосо-мы содержат значительное количество микроРНК, однако в них мало или совсем нет рибосомальной РНК. Важно, что экзосомальные микроРНК защищены от деградации, функциональны и могут влиять на экспрессию генов в клетках-мишенях. Набор микроРНК в экзосомах не вполне отражает их содержание в родительских клетках, вероятно, существуют механизмы избирательной упаковки микроРНК в экзосомы [5, 18, 25].
Экзосомы были найдены в сыворотке крови, моче, амниотической жидкости, а также в канце-роматозных асцитах [5, 18, 25, 27]. Показано, что процесс образования экзосом наиболее интенсивно
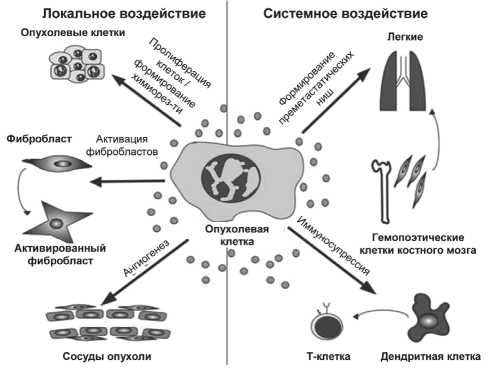
Рис. 1. Протуморогенный потенциал экзосом, происходящих из опухолевых клеток происходит в активно пролиферирующих, например в раковых, клетках. Если размер опухоли мал, то полагают, что экзосомы действуют преимущественно локально, на более поздних стадиях экзо-сомы попадают в кровь и становятся системными. Протуморогенный потенциал экзосом, происходящих из опухолевых клеток, представлен на рис. 1. При эпителиальном РЯ экзосомы, по-видимому, продуцируются клетками первичной опухоли и опухолевыми клетками интраперитонеальных метастазов и накапливаются в асците. Это предположение сделано на основании анализа уровня 8 специфических микроРНК в ткани РЯ и экзосо-мальных микроРНК из асцитической жидкости этих же больных [18]. Показано, что профили микроРНК при РЯ и доброкачественных заболеваниях яичников существенно различаются [32].
В работе S. Runz et al. [25] показано наличие экзосом в асците у большинства больных РЯ, однако примерно у пятой пациентки экзосомы не определялись. В экзосом-позитивных образцах количество экзосом значительно варьировало. Анализ парных образцов асцитической жидкости и сыворотки крови больных с распространенным РЯ показал одновременное присутствие экзосом примерно в 50 % наблюдений. В остальных случаях экзосомы определялись только в асците. Показано, что фенотипически сывороточные экзосомы были сходны с образцами экзосом, полученных из асцитической жидкости, и содержали СD24, ADAM10 и СD9 (белок семейства тетраспанинов – маркер экзосом). Экзосомы, полученные из асцитической жидкости, стимулируют опухолевый рост, содержат широкий спектр протеаз и их активаторов. Полагают, что выраженный протеолитический компонент экзосом, с одной стороны, может в значительной степени определять опухолевый рост и диссемина-цию, модифицируя локальное микроокружение и делая доступными заключенные в мактрикс ростовые факторы, и, с другой стороны, растворять компоненты экстраклеточного матрикса и повышать миграционную и инвазивную активность опухолевых клеток [18]. В этой же работе показано, что экзозомы, полученные из асцитической жидкости больных РЯ, эффективно поглощаются натуральными киллерами (клеточная линия NK-92-C1) и практически не поглощаются опухолевыми клетками (Jurkat T cells). Однако детальные механизмы поглощения экзосом клетками изучены очень слабо. А феномен избирательного поглощения экзосом определенными типами клеток (клетками иммунной системы, эндотелиальными клетками) в настоящее время интенсивно изучается [11, 22]. Кроме того, в отдельных случаях рака яичников эк-зосомы, полученные из асцитической жидкости не поглощаются NK-клетками, что может быть одним из гипотетических механизмов, объясняющих наличие экзосом в сыворотке крови у одних больных и их отсутствие у других [19].
Таким образом, экзосомы обеспечивают связь опухолевых клеток с протуморогенными клетками иммунной системы и эндотелиальными клетками, что, по-видимому, играет роль в инвазии опухоли, неоангиогенезе и метастазировании. Однако, вследствие значительной вариабельности секреции, поглощения, белкового и нуклеинового состава эк-зосом, малой изученности механизмов поглощения экзосом клетками и их выхода в кровеносное русло, вопросы, касающиеся связи асцитических и сывороточных экзосом с особенностями клинического течения и прогноза при РЯ, в настоящее время практически не рассматриваются. Значимость изучения экзосом в таких биологических жидкостях, как асцит и сыворотка крови, объясняется их относительной доступностью для исследования, а также современными методологическими подходами, позволяющими получить высокоочищенную фракцию экзосом без ультрацентрифугирования (наборы для преципитации экзосом «ExoQuick Exosome Precipitation Solution» (System Biosciences); хрома- тографические колонки для выделения экзосом из крови (Cell Guidance Systems).
Асцитическая жидкость как перспективная среда поиска новых прогностических факторов при раке яичников
Эпителиальный РЯ, как правило, характеризуется быстрым ростом, диссеминацией по брюшине, поражением большого сальника и накоплением асцита [8, 19]. Причем более половины больных РЯ к моменту постановки диагноза имеют асцит и практически все больные с рецидивами РЯ страдают от канцероматозных асцитов и/или плевритов [9]. Асцитическая жидкость рассматривается как биологическое микроокружение, способствующее миграции, выживаемости и повышенной инвазивной активности опухолевых клеток (через ингибирование рецептор-индуцированного апоптоза, через формирование компактных клеточных сфероидов). Это объясняется значительным количеством ростовых факторов, цитокинов и фибронектина в асцитической жидкости при РЯ. Доказана связь накопления асцитической жидкости при РЯ с химиорезистентностью, развитием перитонеального канцероматоза, с дальнейшим прогрессированием процесса. Доступность асцитической жидкости для исследования, ее богатейший состав, где, кроме клеточных популяций, также выделяют секреторный компонент (интерлейкины и экзосомы), делают эту биологическую среду уникальным объектом для трансляционных исследований [6].
Таким образом, в настоящее время имеются определенные предпосылки для дальнейшего изучения роли циркулирующих протеасом и экзосом не только в качестве диагностических и прогностических маркеров, но и как предикторов эффективности НАХТ и оптимальной циторедукции.


