Противоопухолевая цитотоксическая активность лимфокин-активированных киллеров
Автор: Велижева Н.П., Жукова О.С., Лебединская О.В., Шубина И.ж, Лебединская Е.А., Киселевский М.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Экспериментальные исследования
Статья в выпуске: 1 (25), 2008 года.
Бесплатный доступ
Изучена цитотоксическая активность лимфокин-активированных киллеров (ЛАК) по отношению к различным опухолевым линиям. Показано, что ЛАК обладают действием, подобным натуральным киллерам, и способны избирательно воздействовать на опухолевые клетки. Они обладают высокой киллерной способностью и широким спектром цитотоксической активности к различным видам трансформированных клеток. Эти данные имеют значение как для расширения области применения ИЛ-2/ЛАК терапии при различных нозологических формах, так и для подтверждения целесообразности использования её в биотерапии злокачественных новообразований.
Лимфокин-активированные киллеры, мононуклеарные клетки периферической крови, клетки опухолевых линий, цитотоксическая активность
Короткий адрес: https://sciup.org/14054826
IDR: 14054826 | УДК: 615.277.3:
Anti-tumor cytotoxic activity of lymphokine-activated killers
Cytotoxic activity of lymphokine-activated killers (LAK) with respect to various tumor lines has been studied. It has been shown that LACs act like natural killers and they are able to effect selectively on tumor cells. They have a high killer ability and wide spectrum of cytotoxic activity towards various types of transformed cells. These findings are of great importance for administering IL-2/LAK therapy for various nosological forms and for cancer biotherapy as well.
Текст научной статьи Противоопухолевая цитотоксическая активность лимфокин-активированных киллеров
Цитотоксические лимфоциты и натуральные киллеры (НК) играют ключевую роль в системе противоопухолевого иммунитета. НК относятся к неспецифическому звену иммунитета и не требуют каскада реакций антигенной презентации в отличие от Т-киллеров. Характерным признаком натуральных киллеров является то, что они могут действовать независимо от наличия специфического антигена и молекул главного комплекса гистосовместимости (Major Histocompatibility Complex – МНС) на мембране измененной клетки. Сигналом на киллинг может быть изменение или отсутствие экспрессии молекул МНС либо их ассоциация с чужеродным белком (в случае вирус-индуцированной трансформации клетки). С одной стороны, имеются сведения о способности избирательного действия НК на опухолевые клетки, но с другой – существуют данные о возможности этих клеток поражать неизменённый эндотелий [1, 2].
К сожалению, высокоактивная субпопуляция натуральных киллеров малочисленна. Киллер-ная активность этих эффекторов иммунобиологического надзора может быть существенно повышена различными модулирующими факторами. С этой целью успешно применяется интерлейкин-2 (ИЛ-2) [4, 5, 7–9]. Генерация ex vivo лимфокин-активированных киллеров (ЛАК) – клеток с высокой степенью цитотоксичности – позволяет преодолеть природную малочисленность НК [1, 6, 11]. Адоптивная иммунотерапия с использованием ЛАК-клеток в настоящее время находит все более широкое применение [7, 10].
В связи с этим целью данной работы явилась оценка специфики лизиса различных клеточных опухолевых линий лимфокин-активированными киллерами и оценка степени их цитотоксической активности.
Материал и методы
Культивирование клеток опухолевых линий.
В качестве объекта исследования использовали линии опухолевых клеток человека: немелкоклеточный рак легкого А549, карцинома яичников человека линии SCOV3, рак молочной железы человека MCF7 и эритробластный лейкоз человека К562 (American Type Culture Collection).
Выделение мононуклеарных лейкоцитов (МЛ). Мононуклеарные лейкоциты выделяли из стабилизированной гепарином (25 ед/мл) периферической крови 30 здоровых доноров на одноступенчатом градиенте фиколла (Pharmacia, плотностью 1,077 г/см3) центрифугированием при 400 g в течение 30 мин. Мононуклеарные клетки (МНК), образовавшие интерфазное кольцо, собирали пипеткой и трехкратно отмывали в среде 199 (Институт полиомиелита и вирусных энцефалитов РАМН, Москва). После каждой отмывки в 10-кратном объёме среды клетки осаждали центирифугированием при 200 g.
Генерация ЛАК. Выделенные из периферической крови МНК ресуспендировали в полной культуральной среде (среда RPMI 1640, 10 % эмбриональной телячьей сыворотки, глютамин, гентамицин) в концентрации 1х106 в 1 мл среды. Затем добавляли ИЛ-2 (Proleukine, Chiron, Голландия) в концентрации 10000 МЕ/мл. Клетки инкубировали при 4,5 % СО2 и 37°С в течение 11 сут.
Определение цитотоксической активности – MTT тест. Цитотоксическую активность лимфоцитов определяли на NK-чувствительной линии клеток эритробластного лейкоза человека К-562, немелкоклеточного рака легкого А-549, рака яичника SKOV-3, нормальных клетках легкого эмбриона теленка VER и на фибробластах, полученных из фрагментов кожи донора в тесте восстановления 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида. Опухолевые и нетрансформированные аллогенные клетки (1x104 в 1 мл) инкубировались в культуральной среде с МНК (в соотношениях клетки-мишени/ эффекторы 1:5; 1:2; 1:1 и 1:0,5) в плоскодонных 96-луночных микропланшетах (Costar, Франция) 18 ч. Затем в лунки добавлялся витальный
Таблица
Цитотоксическая активность мононуклеарных клеток крови и лимфокин-активированных киллеров по отношению к клеткам различных опухолевых линий (%)
|
Соотношение кл.мишень / кл.эффектор |
Немелкоклеточный рак легкого А-549 |
Эритробластный лейкоз человека К-562 |
Рак яичника SKOV-3 |
Рак молочной железы человека MCF7 |
||||
|
МНК (контр.) |
ЛАК |
МНК (контр.) |
ЛАК |
МНК (контр.) |
ЛАК |
МНК (контр.) |
ЛАК |
|
|
1:5 |
58 ± 4,5 |
77 ± 5,8* |
68 ± 9,7 |
86 ± 5,1* |
28 ± 9,2 |
51,5 ± 10,1* |
10 ± 5,2 |
62,5 ± 5,8* |
|
1:2 |
53 ± 5,2 |
60 ± 6,4 |
41 ± 5,3 |
69 ± 6,3* |
25 ± 8,9 |
40 ± 9,2* |
7,5 ± 2,4 |
35,5 ± 4,6* |
|
1:1 |
42 ± 3,1 |
58 ± 6,2 |
33 ± 3,4 |
57 ± 2,7* |
20 ± 5,4 |
30 ± 7,6 |
6 ± 3,1 |
27 ± 6,7* |
Примечание: * – достоверность различий между МНК и ЛАК (p < 0,05)
краситель МТТ (Sigma, США) и по оптической плотности, измеряемой на мультискане МСС-340 (Labsystem, Финляндия), рассчитывался процент лизиса опухолевых клеток (процент цитотоксичности).
Морфо-гистохимическое исследование. Через 5 сут после начала культивирования из центрифугата надосадочной жидкости культур, содержащих мононуклеарные клетки крови донора, активированные ИЛ-2, делали мазки, которые окрашивали азуром II-эозином по Романовскому-Гимза.
Анализ фенотипа ЛАК. Фенотип генерированных клеток исследовали с использованием моноклональных антител (Caltag Laboratories, США) против соответствующих антигенов. Клетки отмывали холодным фосфатно-солевым буфером (ФСБ) и окрашивали FITC-(флюорес-циинизотиоционат) и P- (фикоэритрин) мечеными антителами согласно инструкции производителя. Результаты учитывали на проточном цитометре FacsCalibur (Becton Dickinson). Гейт (окно) популяции клеток устанавливали на основе комбинации прямого и бокового светорассеяния и размера клеток. При учете результатов подсчитывали 10000 событий в гейте. Статистическая обработка материала проведена при помощи программного пакета WINMDI 2.8.
Результаты и обсуждение
Как следует из данных, представленных в таблице, лимфокин-активированные киллеры обладают высокой степенью цитотоксичности по отношению к трансформированным клеточным линиям рака яичника SKOV-3, немелкоклеточного рака легкого А-549, рака молочной железы человека MCF7 и эритробластного лейкоза К-562. При этом уровень цитотоксической активности достоверно повышается при уменьшении соотношения клетка-мишень/клетка-эффектор. Максимальные значения киллерной активности (63, 77 и 86 % соответственно) по сравнению со спонтанной цитотоксической активностью МЛ (58–68 %) достигаются при соотношении мишень–эффектор 1:5. Рис. 1–3 наглядно демонстрируют активный лизис клеток различных опухолевых линий под действием активированных ИЛ-2 мононуклеарных лейкоцитов.
В наших предыдущих исследованиях [3] при цитологическом изучении мазков, полученных из взвеси МЛ, активированных ИЛ-2, показано, что на 5-е сут инкубации существенно возрастает количество лимфоцитов на фоне резкого уменьшения содержания гранулярных лейкоцитов. В эти сроки наблюдается большое количество бластных форм с преобладанием крупных клеток типа пролимфоцитов (рис. 4). В культуре часто встречаются клетки в состоянии митотического деления, что говорит об их высокой пролиферативной активности.
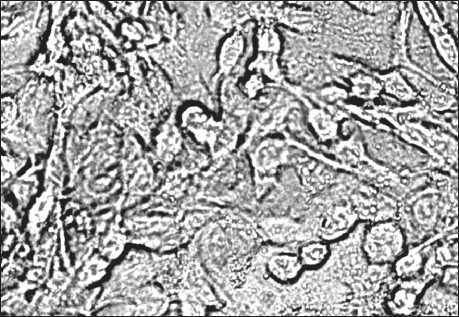
а
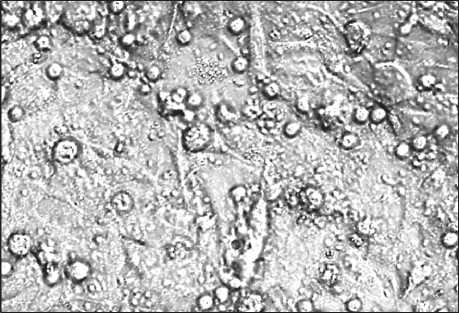
б
Рис. 1. Клетки немелкоклеточного рака легкого А-549 в культуре до (а) и после (б) добавления лимфокин-активированных киллеров. Соотношение клетка-мишень/клетка-эффектор – 1:5. Микрофотографии культуральной взвеси. Фазовоконтрастная микроскопия в светлом поле. Ок. 10, об. 20
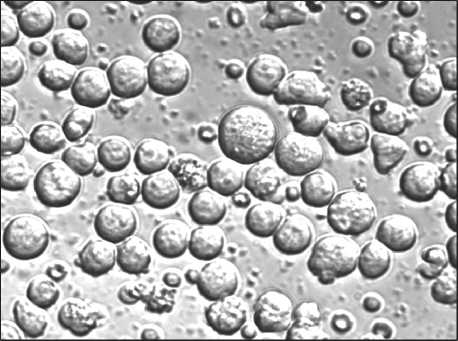
а
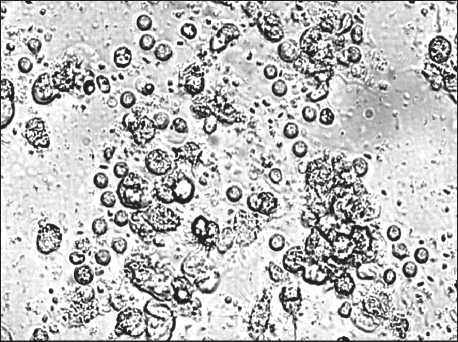
б
Рис. 2. Клетки эритробластного лейкоза К-562 в культуре до (а) и после (б) добавления лимфокин-активированных киллеров.
Соотношение клетка-мишень/клетка-эффектор – 1:5. Микрофотографии культуральной взвеси. Фазовоконтрастная микроскопия в светлом поле. Ок. 10, об. 20
б
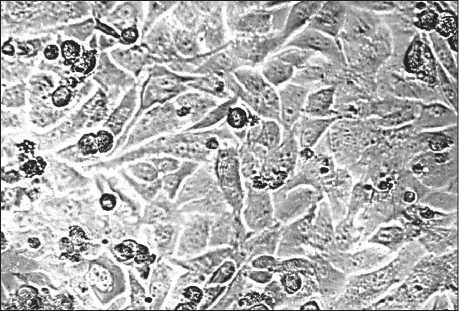
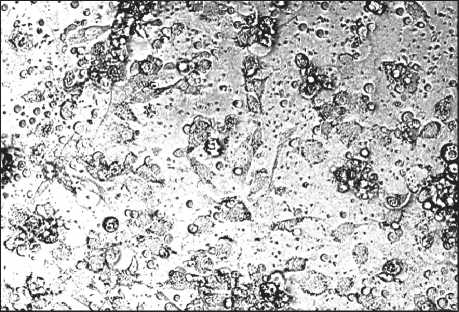
Рис. 3. Клетки рака яичника SKOV-3 в культуре до (а) и после (б) добавления лимфокин-активированных киллеров.
Соотношение клетка-мишень/клетка-эффектор – 1:5.
Микрофотографии культуральной взвеси. Фазовоконтрастная микроскопия в светлом поле. Ок. 10, об. 20
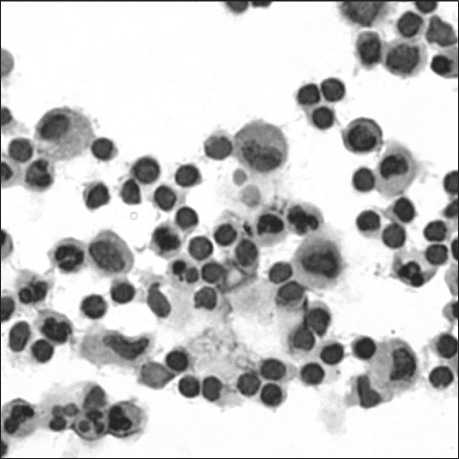
Рис. 4. Лимфокин-активированные киллеры, генерированные из мононуклеарных лейкоцитов периферической крови здоровых доноров (5-й день инкубации). Микрофотография ЛАК в мазке культуральной взвеси. Окраска азуром II-эозином. Ок. 10, об. 40
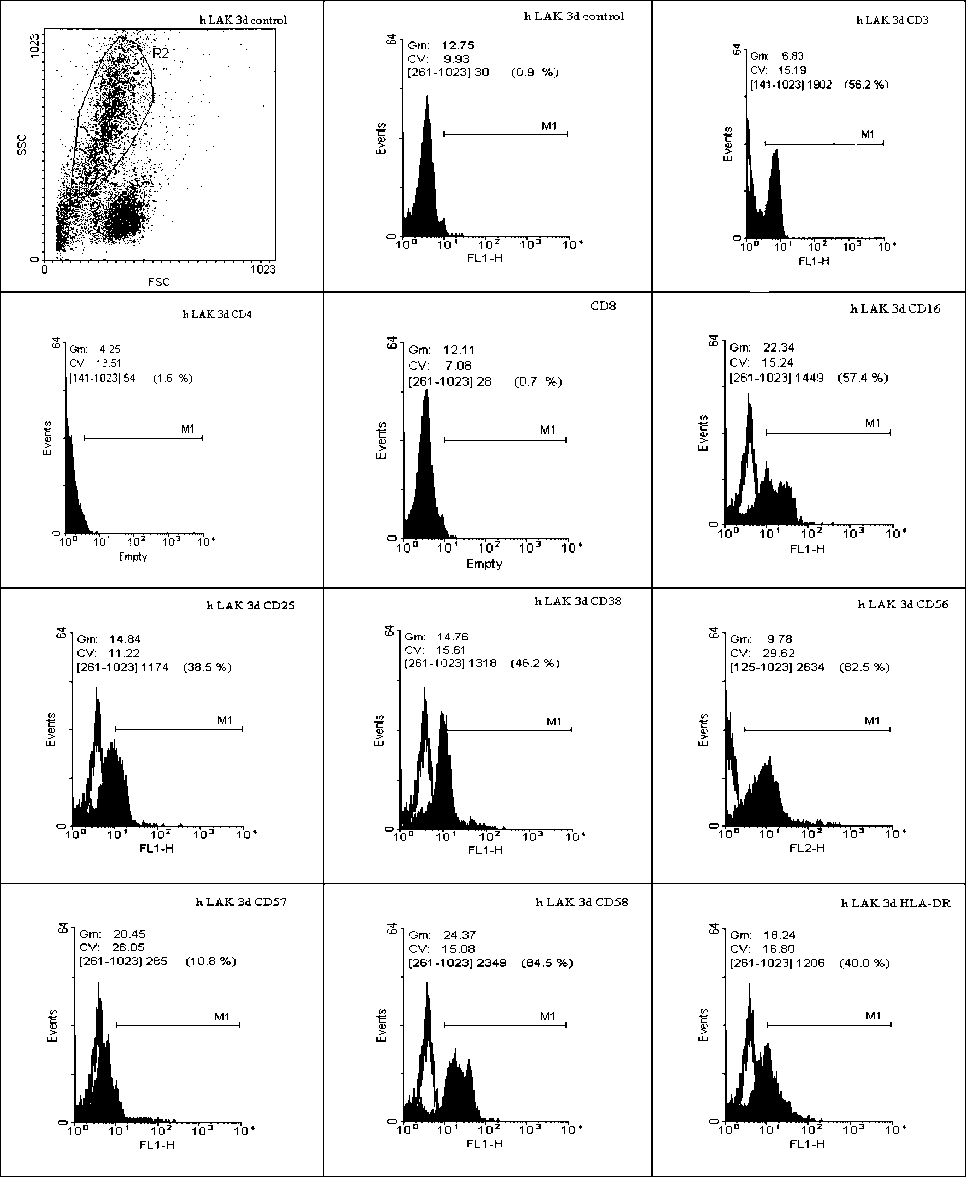
Рис. 5. Гистограммы, отражающие уровень экспрессии поверхностных молекул (кластеров детерминации) лимфокин-активированных киллеров (ЛАК), генерированных из мононуклеарных лейкоцитов периферической крови доноров (3-и сут инкубации с ИЛ-2).
Верхний ряд, дотплот – светорассеяние (популяция ЛАК-клеток в очерченной области), на гистограммах левый пик – аутофлюоресценция клеток при использовании изотипического контроля, правый – флюоресценция (FITC – флюоресциинизотиоционат и R-PE фикоэритрин) после окрашивания соответствующими антителами.


