Противотуберкулёзные терапевтические вакцины и иммунологические методы диагностики (литературный обзор)
Автор: Тарасов Р.В., Титова М.А., Чумоватов Н.В., Комиссарова О.Г.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Проведён систематический обзор литературных источников, содержащихся в базах данных РИНЦ, PubMed, Scopus c 1947 по 2025 гг., используя ключевые слова: «БЦЖ», «иммунопрофилактика туберкулёза», «противотуберкулёзная вакцина», «иммунодиагностика туберкулёза». В исследование вошло 100 наиболее значимых в данном вопросе публикаций. Профилактика туберкулёзной инфекции является одним из наименее используемых, но важнейшим компонентом сдерживания эпидемии туберкулёза. Вакцинация, скрининг на туберкулёзную инфекцию и предоставление профилактического лечения являются ключевыми элементами профилактики туберкулёза среди населения. В данной работе мы рассмотрели историю создания вакцины БЦЖ и её текущую значимость в клинической практике, а также новые перспективные противотуберкулёзные вакцины. Кроме того, большое внимание уделено возможностям иммунологической диагностики на туберкулёзную инфекцию в современных условиях.
Туберкулез, вакцинация, БЦЖ, терапевтические вакцины, иммунологическая диагностика, иммунный ответ, вакцинные кандидаты, противотуберкулезный иммунитет
Короткий адрес: https://sciup.org/143185446
IDR: 143185446 | УДК: 616.24-002.5-084:615.371+616.24-002.5-07:612.017 | DOI: 10.20340/vmi-rvz.2025.6.CLIN.6
Anti-tuberculosis therapeutic vaccines and immunological diagnostic methods (literature review)
A systematic review of the literature sources contained in the RSCI, PubMed, and Scopus databases from 1947 to 2025 was conducted using the keywords: "BCG", "tuberculosis immunoprophylaxis", "tuberculosis vaccine", "tuberculosis immunodiagnostics". The study included 100 of the most significant publications on this issue. Tuberculosis infection prevention is one of the least used, but an essential component of curbing the tuberculosis epidemic. Vaccination, screening for tuberculosis infection and the provision of preventive treatment are key elements of tuberculosis prevention among the population. In this paper, we reviewed the history of the BCG vaccine and its current importance in clinical practice, as well as promising new TB vaccines. In addition, much attention is paid to the possibilities of immunological diagnosis of tuberculosis infection in modern conditions.
Текст научной статьи Противотуберкулёзные терапевтические вакцины и иммунологические методы диагностики (литературный обзор)
Туберкулёз в настоящее время является самым распространённым инфекционным заболеванием в мире, что заставляет как отечественных, так и международных экспертов уделять значительное внимание вопросам профилактики и своевременной диагностики заболевания [1]. В Российской Федерации профилактическое направление в здравоохранении особенно заметно в сфере борьбы с туберкулёзом, где ключевое место в общей системе профилактических мероприятий занимает вакцинация «Бацилла Кальметта — Герена» (Bacillus Calmette — Guérin, BCG) (БЦЖ).
Успешная профилактика инфекционных заболеваний возможна при условии, что вакцинация охватит 90% населения, а у 95% из них выработается необходимый иммунный ответ. Именно это определили международные организации как один из основных методов профилактики туберкулёзной инфекции [2].
В современном обществе растёт число родителей, отвергающих вакцинацию своих детей, что порождает острые дискуссии о целесообразности иммунизации [3]. Подобный отказ представляет серьёзную угрозу и повышает риск развития тяжёлых генерализованных форм туберкулёза. Противотуберкулёзная вакцинация не исключает возможность инфицирования, но обеспечивает более благоприятное течение болезни [4]. Клинические данные свидетельствуют о том, что невакцинированные дети подвержены риску заражения туберкулёзом в 15 раз больше, чем их сверстники, получившие своевременную иммунизацию.
Эти методики обладают двумя ключевыми преимуществами:
-
- позволяют различать инфекционную и поствакцинную аллергию у детей;
-
- обеспечивают надёжную диагностику туберкулёза.
Грамотный подбор иммунологического теста существенно повышает эффективность выявления заболевания. На ранних стадиях, а также при возникновении типичных клинико-рентгенологических признаков, точность диагностики достигает 91,4 %.
ЦЕЛЬ ИССЛЕДОВАНИЯ – проанализировать актуальные данные литературы, посвящённые иммунопрофилактике туберкулёза от самой первой вакцины (БЦЖ) до современных реалий, оценить методы диа- гностики туберкулёза и изучить современное состояние создания новых вакцин против туберкулёза.
МАТЕРИАЛЫ И МЕТОДЫ
Проведён систематический обзор литературных источников, содержащихся в базах данных РИНЦ, PubMed, Scopus c 1947 года по 2025 год, используя ключевые слова: «БЦЖ», «иммунопрофилактика туберкулёза», «противотуберкулёзная вакцина», «иммунодиагностика туберкулёза».
В системах Google Scholar, PubMed, Scopus по текущему запросу найдено 89 публикаций. В системе РИНЦ найдено 244 публикации. Всего найдено 333 публикации.
Критерием включения публикации в обзор являлся факт рассмотрения вопроса иммунопрофилактики туберкулёза лёгких, описание клинических испытаний и особенностей препаратов и методов диагностики. Критерием невключения являлись публикации с дублирующими названиями или несоответствующими названиями (n=54), тезисы конференций (n=33), идентичные статьи (n=4), учебные пособия (n=38), авторефераты (n=29), несоответствие темы поиска (n=75).
На рисунке 1 представлена схема отбора публикаций по стандарту PRISMA.
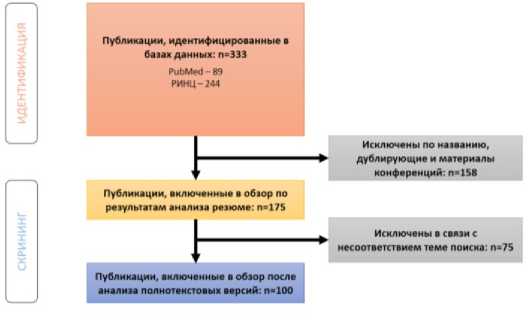
Рисунок 1. Схема отборка публикаций по стандарту PRISMA Figure 1. Scheme of publication selection according to the PRISMA standard
Как видно из схемы на рисунке 1, итого в исследование вошло 100 наиболее значимых в данном вопросе, по нашему мнению, публикаций.
РЕЗУЛЬТАТЫ
История создания вакцины
История разработки противотуберкулёзной вакцины представляет собой длительный и сложный процесс научных изысканий, начавшийся в XIX столетии. Значительный вклад в изучение данной проблематики внес Роберт Кох, который первоначально занимался разработкой противотуберкулёзной вакцины. Изучая коровью оспу в 1890 году, он обнаружил, что существует бактерия, вызывающая туберкулёз у коров — M. bovis. Она сильно отличалась от ранее открытой им человеческой туберкулёзной палочки, но имела с ней и ряд сходств. Кох предположил, что можно ввести эту бактерию человеку, и она будет способствовать выработке иммунитета против M. tuberculosis, не вызывая при этом активного заболевания. К сожалению, испытания этой вакцины обернулись катастрофой — M. bovis оказалась такой же опасной для человека, как и M. tuberculosis [5, 6].
Э.А. фон Беринг, выдающийся немецкий бактериолог, предпринял попытку создания антитуберкулёзной сыворотки посредством экспериментальных исследований на животных. Несмотря на многочисленные попытки, желаемый результат не был достигнут. Основываясь на работах Р. Коха, касающихся исследований микобактерий у крупного рогатого скота, фон Беринг разработал методику профилактических прививок для телят [7].
Существенный прорыв в разработке противотуберкулёзной вакцины был достигнут позже благодаря совместным усилиям французских учёных – микробиолога и гигиениста А. Кальметта и ветеринарного врача, бактериолога и иммунолога К. Герена. В 1908 году исследователи успешно получили иммунологически активный препарат на основе авирулентного ослабленного, но жизнеспособного штамма крупного рогатого скота (Mycobacterium bovis), который был аттенуирован путём последовательных пассажей в ломтиках картофеля, пропитанных глицерином, в течение 13 лет [8]. Наименование «БЦЖ» (BCG) было присвоено препарату в 1921 году после первого клинического применения у новорождённого ребенка, чья мать скончалась от туберкулёза после родов [5, 7, 9, 10]. Данный исторический момент ознаменовал начало масштабной вакцинации населения против туберкулёза во всём мире, а последовавшие за этим клинические испытания во Франции и Бельгии показали, что вакцина очень эффективна для детей.
В 1925 году Кальметт передал штамм БЦЖ в СССР профессору Льву Александровичу Тарасевичу. Штамм БЦЖ, полученный в ходе работы группы Л.А. Тарасевича, был назван BCG-1 Russia. Тем не менее вплоть до окончания Второй Мировой войны эта вакцина практически не использовалась. С середины 1950-х годов вакцинация новорождённых прививкой БЦЖ стала обязательной не только в Советском союзе, но и во многих странах мира. До 1962 года БЦЖ вводили новорождённым перорально (через рот), позже был принят внутрикожный метод введения, поскольку в этом случае может сфор- мироваться более устойчивая иммунологическая память [4, 11].
Сегодня иммунизация БЦЖ обязательна в районах, эндемичных по туберкулёзу, и БЦЖ является наиболее широко используемой вакциной в мире. С 1960-х годов прошлого столетия вакциной было иммунизировано более 4 миллиардов человек. Успех БЦЖ в первую очередь обусловлен её эффективностью в профилактике туберкулёзного менингита у детей [12, 13, 15], который часто встречается в эндемичных по туберкулёзу районах, а также её безопасностью для использования у людей. Кроме того, она экономична и поэтому может быть легко использована во многих частях мира. В настоящее время БЦЖ остаётся основным средством противотуберкулёзной иммунизации в большинстве стран мира, за исключением Соединенных Штатов Америки, Королевства Нидерландов и Германии [16]. Согласно современным статистическим данным, ежегодная вакцинация охватывает не менее 80% детского населения планеты [13, 15, 17].
БЦЖ: механизм, осложнения, эффективность
До середины XX столетия отсутствовали эффективные способы длительного хранения микроорганизмов. В связи с этим различные лаборатории были вынуждены либо самостоятельно выращивать вакцину на основе ранее существовавших штаммов БЦЖ (в том числе BCG-1 Russia), либо разрабатывать её заново. Такая практика привела к возникновению новых разновидностей БЦЖ-штаммов, получивших названия в соответствии с местом их создания. В настоящее время в различных регионах мира преимущественно применяются шесть основных штаммов: BCG-1 Russia — наиболее близкий к оригинальному штамму, созданному Кальметом и Гереном; BCG Pasteur 1173 P2; BCG Danish 1331; BCG Glaxo 107; BCG Tokyo 172-1; BCG Brazil. Каждый из этих штаммов характеризуется различной реактогенно-стью, то есть способностью вызывать иммунный ответ разной интенсивности, что отражается на частоте и характере побочных эффектов. Исследования показывают, что штаммы Pasteur 1173 P2 и Danish 1331 вызывают более выраженные побочные реакции по сравнению с Glaxo 1077, Tokyo 172-1, BCG-1 Russia и Moreau RDJ. Важным параметром вакцин является количество живых бактерий в одной дозе, которое варьируется от 50 тысяч до 3 миллионов бактериальных клеток [4, 11, 14].
В современной российской практике вакцинации применяется исключительно штамм BCG-1 Russia. Данный штамм характеризуется оптимальным сочетанием высокой иммуногенности и низкой реакто-генности. Это означает, что при введении вакцины иммунная система организма демонстрирует адекватный ответ, при этом частота развития побочных реакций остаётся на минимальном уровне. Отечественные вакцинные препараты — БЦЖ и БЦЖ-М, производимые научно-производственным объединением «Микроген», представляют собой лиофилизированные живые микобактерии. Процесс лиофилизации осуществляется в 1,5%-м растворе глутамата натрия. Важно отметить, что оба препарата базируются на идентичных микроорганизмах, однако существуют количественные различия в содержании живых микобактерий. В вакцине БЦЖ концентрация микобактерий составляет 0,05 мг, что в два раза превышает их содержание в БЦЖ-М. Именно это количественное различие обуславливает более низкую реактогенность вакцины БЦЖ-М и, как следствие, меньшую вероятность развития побочных эффектов [18].
Механизм действия вакцин БЦЖ/БЦЖ-М характеризуется специфической направленностью. В процессе иммунного ответа, индуцированного вакцинацией, в организме формируются специализированные Т-лимфоциты с памятью к антигенам возбудителя туберкулёза (Mycobacterium tuberculosis). Данные клетки, известные как Т-клетки памяти, подразделяются на две основные категории: долгоживущие центральные и относительно короткоживущие эффекторные субпопуляции. Эффекторные Т-клетки памяти преимущественно выполняют роль мессенджеров, обеспечивая быструю передачу сигнала об инвазии патогена другим компонентам иммунной системы и инициируя каскад иммунных реакций. В свою очередь, центральные Т-клетки памяти обладают способностью к непосредственной элиминации патогенного агента. Иммунологические исследования демонстрируют, что при вакцинации или естественной инфекции, вызванной микобактериями туберкулёза, преимущественно формируются эффекторные Т-клетки памяти. Формирование центральных Т-клеток памяти при туберкулёзной инфекции не получило достоверного подтверждения в современных исследованиях. Хотя препарат не обеспечивает защиту взрослых от лёгочной формы туберкулёза и не предотвращает инфицирование микобактериями, он эффективно предупреждает развитие наиболее опасных клинических форм заболевания у детей, таких как милиарный туберкулёз и туберкулёзный менингит. Подавление гематогенного распространения возбудителей существенно снижает риск развития заболевания или его реактивации [13, 15]. Защитная эффективность вакцин БЦЖ/БЦЖ-М демонстрирует вариабельность в зависимости от клинической формы туберкулёза:
-
- против первичного туберкулёзного комплекса и лимфаденита — 32%;
-
- против туберкулёза костей — 39%;
-
- против туберкулёзного менингита — 50%;
-
- против диссеминированного туберкулёза — до 80% [19].
Вакцинация БЦЖ/БЦЖ-М включена в Национальный календарь профилактических прививок Российской Федерации согласно приказу Минздрава РФ от 21 марта 2014 года №125н. При этом вакцинация носит добровольный характер, что даёт родителям право отказа от иммунизации. Основными причинами отказа являются медицинские противопоказания или страх родителей перед возможными поствакцинальными осложнениями.
К противопоказаниям вакцинации БЦЖ относятся [4]:
-
- недоношенность (масса тела менее 2500 г);
-
- острые заболевания, такие как внутриутробная инфекция, гнойно-септические заболевания, гемолитическая болезнь новорождённых среднетяжёлой и тяжёлой формы, тяжёлые поражения нервной системы с выраженной неврологической симптоматикой, генерализованные кожные поражения и т.п. Вакцинация откладывается до окончания острых проявлений заболевания и обострения хронических заболеваний;
-
- ВИЧ-инфекция матери (от введения БЦЖ следует воздержаться до возраста 18 месяцев, когда будет уточнён ВИЧ-статус младенца);
-
- злокачественные новообразования;
-
- иммунодефицитные состояния;
-
- генерализованная БЦЖ-инфекция, включая лимфаденит и остит БЦЖ-этиологии, выявленные у других детей в семье.
Поствакцинальные осложнения после первичной вакцинации БЦЖ/БЦЖ-М у новорождённых регистрируются примерно в 10 раз чаще, чем при ревакцинации [20]. К ним относятся:
-
- усиленные местные реакции с возможным некрозом кожи;
-
- холодные абсцессы, язвы, инфильтрат в месте введения вакцины;
-
- регионарные лимфадениты с нагноением;
-
- келоидные рубцы;
-
- оститы и остеомиелиты [21-24];
-
- генерализованная БЦЖ-инфекция [18].
Важно отметить, что большинство осложнений связано с нарушением техники введения вакцины или использованием неадекватных доз препарата. Именно поэтому инъекцию БЦЖ выполняет специально обученный средний медицинский персонал – внутрикожно в районе дельтовидной мышцы.
Современные аспекты эффективности противотуберкулёзной вакцинации требуют детального рассмотрения существующих ограничений БЦЖ. Клинические наблюдения свидетельствуют о том, что развитие активного туберкулёзного процесса в настоящее время регистрируется не только среди лиц с недостаточной или отсутствующей вакцинацией, но и в группе пациентов, получивших эффективную БЦЖ-иммунизацию [25].
На формирование поствакцинального иммунитета при иммунизации БЦЖ особое влияние оказывают экзогенные факторы [31, 32]. Современные гипотезы формирования иммунного ответа выделяют два основных механизма.
Гипотеза маскирования предполагает, что вакцинация БЦЖ не способна существенно улучшить иммунный ответ у индивидуумов, сенсибилизированных микобактериями окружающей среды. Таким образом, БЦЖ, которая вводится сразу после рождения, эффективно защищает новорожденных и грудничков, поскольку не происходит предварительной сенсибилизации к микобактериям окружающей среды. И наоборот, вакцинация БЦЖ неэффективна у взрослых, поскольку она не обеспечивает дополнительного иммунного ответа у населения, уже подвергшегося воздействию микобактерий окружающей среды [33].
Гипотеза блокирования предполагает, что предварительная сенсибилизация микобактериями окружающей среды индуцирует уровень антимико-бактериального иммунитета, который не обеспечивает существенной защиты от инфекции M. tuberculosis, но ухудшает способность БЦЖ сохраняться в тканях хозяина после иммунизации, и, как следствие, активность БЦЖ снижается [34].
При анализе факторов, влияющих на эффективность противотуберкулёзной вакцины БЦЖ, исследователи выделяют следующие ключевые аспекты:
-
• Роль внешней микобактериальной микрофлоры [39, 40].
-
• Дисбаланс иммунокомпетентных клеток, проявляющийся в неспособности вакцины достичь оптимального соотношения популяций CD4+ и CD8+ T-клеток [43, 44].
-
• Отсутствие формирования долгоживущих центральных Т-клеток памяти [45].
-
• Генотипическая гетерогенность штаммов M. bovis БЦЖ [46, 47].
-
• Гетерогенность вакцинных штаммов БЦЖ, используемых при производстве препарата [48, 49].
Данные факторы определяют вариабельность иммунного ответа на вакцинацию и требуют дальнейшего изучения для совершенствования противотуберкулёзной иммунопрофилактики. Формирование защиты против туберкулёза зависит от взаимодействия CD4+ и CD8+ Т-клеток. Ограничением БЦЖ является же преимущественная индукция CD4+ Т-клеток [43]. Результаты исследований последних лет показали, что негативное влияние на эффективность БЦЖ может оказывать даже паразитарная инвазия (на примере в тропических регионах и стран Африки) через поляризацию иммунного ответа в сторону Th2-звена, активацию регуляторных Т-клеток (Treg), секрецию TGF-β и ИЛ-10 — ключевых факторов супрессии иммунного ответа [39, 40].
Существенным ограничением применения вакцины БЦЖ выступает прогрессирующее снижение напряжённости поствакцинального иммунитета, которое наблюдается в период от 3 до 7 лет после проведения вакцинации [26, 27]. Результаты контролируемых исследований демонстрируют практически полное нивелирование защитного эффекта спустя десятилетие после первичной иммунизации [28]. А согласно исследованию, проведённому в Бразилии, в которое вошло более 300 000 детей в возрасте с 7 до 14 лет, – ревакцинация не обеспечивает существенной дополнительной защиты и не должна рекомендоваться [30]. Это подтверждается и результатами исследований Всемирной организации здравоохранения [29].
Главным недостатком БЦЖ вакцины остаётся длительность сохранения иммунного ответа, а эффективность ревакцинация БЦЖ до сих пор вызывает дискусии и не доказана. Авторы [35] из Бразилии показали на 2568 взрослых пациентах, что ревакцинации БЦЖ не снизила первоначальный риск конверсии теста QuantiFERON-TB Gold (QFT) Plus, что лишь подчёркивает важность изучения методов профилактики туберкулёза. С ними согласна и группа авторов из разных стран мира [36], которые провели рандомизированное исследование на 1836 пациентах и показали неэффективность ревакцинации БЦЖ у пациентов.
Таким образом необходимость создания новых эффективных противотуберкулёзных вакцин несомненна и по-прежнему актуальна.
Терапевтические вакцины
На сегодняшний день продолжается активная борьба с туберкулёзом, и в последнее время всё чаще используется термин «терапевтическая вакцина». Терапевтическая вакцинация – введение иммуномодулирующего средства (вакцина) при наличии активного заболевания с целью повышения эффективности лечения и сокращения продолжительности терапии [50]. Современный подход к противотуберкулёзной иммунизации базируется на методике, основанной на принципе гетерологичной вакцинации, известной как стратегия «prime-boost» (запуск-усиление), получившей признание специалистов по всему миру. Механизм действия этой схемы построен на этапном воздействии на защитные силы организма и начинается с первичной иммунизации путём применения вакцины БЦЖ; модифицированных вариантов БЦЖ; ослабленных штаммов Myc. tuberculosis. На следующем этапе осуществляется вторичная иммунизация (ревакцинация) с примене- нием: субъединичных вакцинных препаратов; векторных вакцин; иммунобиологических средств, содержащих защитные антигены микобактерий. Данный методологический подход обеспечивает последовательное усиление иммунного ответа и формирование более надёжной защиты против туберкулёзной инфекции. Стратегия позволяет комбинировать различные типы вакцинных препаратов для достижения максимального профилактического эффекта [51]. В настоящее время терапевтические противотуберкулёзные вакцины находятся на стадии клинических разработок [52].
В таблице 1 представлены основные вакцинные кандидаты, разделённые по методу создания, новизне разработке и эффективности.
Таблица 1. Вакцинные кандидаты
Table 1. Vaccine candidates
|
Название |
Год создания |
Стадия клинического исследования |
Эффективность |
Описание |
|
1. На основе живых модифици |
рованных штаммов m.bovis БЦЖ |
|||
|
VPM 1002 [52, 53, 54, 55] |
2004 |
III |
Показала высокий уровень безопасности и эффективности в индукции иммунного ответа с участием CD8+-Т-клеток |
Рекомбинантный штамм БЦЖ Prague, экспрессирующий N-терминальную область антигена 85B и листериолизин; с делецией гена, кодирующего уреазу |
|
rBCG30 [56] |
2005 |
Испытания были прекращены, так как вакцина содержала ген устойчивости к антибиотикам |
Повышение иммунных реакций, специфичных к антигену 85B |
Рекомбинантный штамм БЦЖ Tice, экспрессирующий антиген 85B |
|
Aeras – 422 [57] |
2009 |
Испытания остановлены ввиду нежелательных явлений у добровольцев |
Сочетание подходов VMP 1002 b rBCG30 |
Рекомбинантный штамм БЦЖ, экспрессирующий перфринголизин и антигены 85А, 85B, Rv3407 |
2. Вакцинные кандидаты на основе живых аттенуированных штаммов M.tuberculosis
|
MTBVAC01Δ phoP Δ fad26 (DIM) [60, 61, 62] |
2001 |
III |
Содержит все антигены, присутствующие в штаммах, которые заражают людей |
Живая вакцина на основе аттенуированного штамма M. tuberculosis с инактивацией генов phoP и fadD26 |
|
MTB (Δ lysA, Δ panCD, Δ secA2) |
2007 |
Доклинические исследования |
Вызывает усиление апоптоза инфицированных макрофагов путем уменьшения секреции микобактериальной супероксид-дисмутазы |
Нерепликативный ауксотрофный по лизину и пантотенату штамм M. tuberculosis, аттенуированный за счет удаления гена secA2 |
3. Вакцинные кандидаты на основе рекомбинантных белков с адъювантом
|
HybridI+CAF01 [64] |
2008 |
I |
Разрабатывается метод введения, преимущественно аэрозольный |
Белки 85B и ESAT-6 с адъювантом CAF01 |
|
HybridI + IC31 [65] |
2008 |
I |
Безопасна и иммуногенна у взрослых, вакцинированных БЦЖ, с инфекцией или без нее |
Белки 85B и ESAT-6 с адъювантом IC31 |
|
Hybrid 56+CAF01 |
2008 |
Доклинические исследования |
Безопасен и иммуногенен после ин-траназальной первичной и/или усиленной иммунизации (на мышах) |
Белки 85B, ESAT-6 и Rv2660с с адъювантом CAF01 |
|
M72+AS02 или AS01 [66] |
Начало 2000-х |
IIb |
~50% Способна защищать от туберкулёзной инфекции |
Белки Rv1106 и Rv0125 с адъювантом |
|
HyVACIV/ Aeras-404+IC31 |
2014 |
I |
Вакцина хорошо переносилась, в основном наблюдались легкие и умеренные самоограничивающиеся боли в месте инъекции, миалгия, артралгия, лихорадка и поствакцинальная воспалительная реакция |
Белки 85B и TB10.4 с адъювантом IC31 |
|
GamTBvac [69, 70] |
2021 |
III |
Безопасна и хорошо переносилась при различных дозах используемых антигенов |
Содержит антигены Ag85A и ESAT-6-CFP-10 вместе с адъювантом CpG ODN |
4. Вакцинные кандидаты на основе рекомбинантных вирусных векторов
|
MVA85A/ Aeras-485 [54, 71, 72, 73] |
2002 |
II |
Неэффективна при вакцинации детей Перспективна для предотвращения распространения ТБ среди взрослого населения |
Модифицированный вирус Vaccinia штамм Ankara, экспрессирующий антиген 85А |
|
Ad35/Aeras 402 [54, 73] |
2004 |
II |
Показала безопасность и широкий иммунный ответ |
Репликативно-дефектный вирусный вектор на основе аденовируса 35 серотипа, экспрессирующий антигены 85А, 85B, TB10.4 |
|
Название |
Год создания |
Стадия клинического исследования |
Эффективность |
Описание |
5. Инактивированные цельноклеточные вакцины
|
RUTI [53, 54, 74, 75] |
2010 |
II |
Показала способность к защите от осложнений Продемонстрировала способность к иммунотерапевтическому эффекту различных доз, используемых в исследовании |
Детоксифицированный фрагмент M. tuberculosis, транспортируемый в липосомах |
||
|
DAR-901 [53] |
2016 |
IIb |
Показала эффективность применения SRL172 у взрослых с ВИЧ-инфекцией |
Инактивированная M. obuense |
||
Как видно из таблицы 1, изучение терапевтических противотуберкулёзных вакцин активно продолжается, и многие вакцины показывают хорошую эффективность на разных этапах клинических испытаний.
Вакцинные кандидаты на основе живых модифицированных штаммов M. bovis БЦЖ Вакцина VPM 1002 на основе генетически модифицированного штамма Mycobacterium bovis (HLY+rBCG) показала высокую эффективность в доклинических исследованиях, в II фазе клинических исследований – высокую безопасность и иммуногенность у ВИЧ-инфицированных и здоровых новорождённых. Испытания показали, что протективная эффективность этой вакцины существенно выше по сравнению с родительской БЦЖ благодаря лучшей индукции CD4+ и СD8+ клеток, а также IFN-y, IL-18,12 и других цитокинов, ответственных за функцию клеточного иммунитета против M. tuberculosis. В настоящий момент вакцина находится на III фазе клинических исследований в Индии, в которой участвуют 5000 детей [52–55].
Особенности разработки рекомбинантных вакцин rBCG30 [56] и Aeras-422 [57] демонстрировали неоднозначные результаты при экспериментальной и клинической оценке препаратов. Экспериментальные исследования на лабораторных животных (мышах и морских свинках) продемонстрировали повышенную протективную активность штамма в сравнении со стандартной вакциной БЦЖ при инфицировании вирулентными микобактериями. Клиническая апробация вакцинного препарата rBCG30, характеризующегося экспрессией антигена 85B, была проведена на группе из 30 здоровых добровольцев. Исследование подтвердило благоприятный профиль безопасности вакцинного препарата. Иммунологическая оценка же, напротив, показала, что иммуногенная активность rBCG30 не соответствовала первоначальным ожиданиям исследователей. Дальнейшие испытания был прекращены, что было обусловлено обнаружением в составе вакцины гена, обеспечивающего устойчивость к антибиотикам, что стало критическим фактором для продолжения исследования.
Используя сочетание двух перечисленных выше инновационных подходов, разработан рекомбинантный штамм БЦЖ, экспрессирующий белковые компоненты Аg85A, Аg85B и Rv3407 совместно с перфринголизином. Функциональные характеристики рекомбинантного штамма определяются уникальными свойствами перфринголизина, который демонстрирует расширенный спектр гемолитической активности в сравнении с листериолизином. Существенным биохимическим преимуществом является способность перфринголизина проявлять каталитическую активность в более широком диапазоне значений pH среды, что обеспечивает оптимизацию иммуномодулирующего потенциала рекомбинантного штамма [58]. В ходе клинического исследования вакцины AERAS-422 у двух добровольцев были зарегистрированы нежелательные явления (реактивация Herpes zoster) тяжёлой степени выраженности, что послужило основанием для преждевременного прекращения исследования.
Таким образом среди вакцинных кандидов на основе живых модифицированных штамов в настоящее время перспективным является лишь препарат VMP 1002, проходящий последнюю фазу клинических испытаний. О подробных результатах исследования в научных кругах пока не говорится.
Вакцинные кандидаты на основе живых аттенуированных штаммов M. Tuberculosis
Ещё один подход к созданию живых аттенуированных противотуберкулёзных вакцин заключается в разработке штаммов M. tuberculosis с отсутствием связи между восстановлением вирулентности и метаболитами макроорганизма-хозяина.
Исследования эффективности профилактической иммунизации показали перспективность применения вакцинных штаммов с модифицированным геном secA2. Генетический компонент secA2 играет ключевую роль в системе секреции бактериальных белков, непосредственно связанной с патогенностью микобактерий. Мутация данного гена приводит к модификации секреторной активности микобактерий, индукции апоптоза в инфицированных макрофагах и снижению продукции супероксиддисму-тазы бактериального происхождения. Механизмы действия вакцинных штаммов с мутантным secA2
основаны на целенаправленном воздействии на ключевые звенья патогенеза туберкулёзной инфекции. Ограничение секреции супероксиддисмутазы способствует усилению апоптотической гибели инфицированных клеток, что является важным фактором в формировании защитного иммунного ответа. Полученные результаты свидетельствуют о потенциальной возможности использования штаммов с модифицированным secA2 в качестве основы для разработки новых поколений противотуберкулёзных вакцин [59].
Значительный прогресс в данной области достигнут благодаря всестороннему изучению вакцинного кандидата MTBVAC, который прошёл комплексную доклиническую оценку, соответствует критериям Женевского консенсуса и демонстрирует высокую степень безопасности. Штамм характеризуется наличием двух стабильных делеций в ключевых генах вирулентности — phoP и fadD26 и не имеет маркеров устойчивости к антибиотикам [60, 61, 62]. На сегодняшний день MTBVAC — представляет собой уникальный вакцинный препарат, созданный на основе аттенуации M. tuberculosis, не имеющий аналогов в современной противотуберкулёзной вакцинологии. Клиническая оценка безопасности и эффективности вакцины осуществляется в рамках программы South African Tuberculosis Vaccine Initiative (SATVI), где проводятся исследования II фазы. Исследования включают два независимых клинических испытания:
-
• исследование NCT02933281: оценка дозировки у взрослых участников с различным статусом контакта с M. tuberculosis (завершено в сентябре 2021 года);
-
• исследование NCT03536117: изучение безопасности и переносимости у здоровых новорождённых (завершено в марте 2022 года) [63].
О начале III фазы исследования в настоящее время в литературе не сообщается.
Вакцинные кандидаты на основе рекомбинантных белков с адъювантом
Ключевым фактором успешности создания субъединичных противотуберкулёзных вакцин является корректный подбор специфического антигена, способного обеспечить выраженный протективный эффект иммунизации. Современные разработки в области вакцинологии характеризуются активным исследованием адъювантных систем. На текущий момент в стадии разработки находятся четыре перспективных комбинированных адъюванта, представляющих собой комплексные системы, включающие мультикомпонентные структуры, вещества с разнонаправленным действием и компоненты с различной биологической активностью. Комбинационный подход к конструированию адъювантных систем позволяет оптимизировать иммуномодулирующий потенциал вакцин и повысить их эффективность в формировании защитного иммунитета против туберкулёзной инфекции.
CAF01 (торговое название — LipoVac) представляет собой синтетический иммуномодулирующий препарат, созданный на основе трихалозы и обладающий микобактериальной активностью. Механизм действия данного адъюванта характеризуется провоспалительным эффектом, TLR-независимой активацией продукции цитокинов, стимуляцией выработки цитокинов Tх1-типа. Уникальная особенность CAF01 заключается в альтернативном пути индукции иммунного ответа, что позволяет расширить терапевтические возможности в области противотуберкулёзной вакцинации и усилить формирование защитного иммунитета [64]. Данный препарат проходит I фазу испытаний.
Адъювантная система IC31 представляет собой многокомпонентный препарат, включающий в себя синтетический пептид KLKL5KLK, обладающий антимикробной активностью и улучшающий взаимодействие между антигенпрезентирующими клетками и антигенами, и TLR9-лиганд ODN1a, обладающий выраженным иммуностимулирующим эффектом. Клинические исследования показали высокую эффективность при внедрении адъюванта IC31 в состав вакцин Hybrid 1 и HyVAC IV. Иммунологический ответ, вызванный этой комбинацией, характеризовался формированием выраженного Т-клеточного ответа, развитием смешанного цитокинового профиля Tх1/Tх2, высоким иммунным ответом у пациентов всех возрастных групп [65].
Адъювантные системы AS01 и AS02 включают активные компоненты: монофосфорил липид А и дериват сапонина QS-21, которые различаются способом доставки – липосомальной (AS01) или эмульсионной «масло/вода» (AS02) форме. Принцип действия основан на синергетическом эффекте компонентов, что обеспечивает усиление иммунного ответа, повышение иммуногенности вакцинных препаратов, оптимизацию формирования защитного иммунитета [66].
Вакцина M72/AS01E показала общую эффективность ~50% для профилактики ТБ в рандомизированном плацебо-контролируемом исследовании фазы IIb после примерно трёх лет испытаний. Описано, что она эффективна в профилактике активного ТБ у взрослых с латентной туберкулёзной инфекцией. Получатели вакцины в Кении, Замбии и Южной Африке получили 2 дозы вакцины M72/AS01E с интервалом в 1 месяц и, в течение среднего периода наблюдения в 36 месяцев, имели на 50% меньше случаев бактериологически подтвержденного активного ТБ, чем в контрольной группе. Вакцина хорошо переносилась и была безопасна [52, 53, 67, 68].
Все вышеперечисленные вакцины на основе ре-комбинатных генов проходит либо доклинические, либо клинические испытания I фазы. В настоящее время можно лишь говорить об их перспективности, но до клинического использования ещё далеко.
Вакцина GamTBvac представляет собой субъединичную вакцину, в состав которой входят антигены ESAT6-CFP10. В ходе исследований было установлено, что препарат обладает высоким уровнем безопасности. При этом он способен вызывать устойчивый и продолжительный иммунный ответ двух типов: клеточный (Th1) и гуморальный. Особенность клеточного иммунного ответа заключается в том, что он реализуется через интерферон-гамма (IFN- γ ). При использовании средних дозировок наблюдается оптимальный эффект: отмечается постепенное нарастание выработки IFN- γ , при этом уровень цитокинов остаётся стабильно высоким на протяжении длительного времени без существенного снижения. Эта противотуберкулёзная субъединичная вакцина в настоящее время проходит исследования III фазы [70, 80] и наиболее близка к началу клинического применения.
Вакцинные кандидаты на основе рекомбинантных вирусных векторов
В современной иммунологии разработан подход к активизации защитных сил организма против возбудителей туберкулёза без привлечения традиционных иммуностимуляторов (адъювантов), заключающийся в использовании специально модифицированных инфекционных агентов — ослабленных вирусов и бактерий, выполняющих функцию биологических транспортеров. Эти природные носители, известные как векторные системы, выступают своеобразными курьерами, которые не только доставляют необходимые антигены в организм человека, но и обеспечивают их активное проявление на клеточном уровне. Однако для безопасного применения таких векторных вакцин на людях необходимо соблюдение важного условия: вакцинный штамм должен быть тщательно ослаблен (аттенуирован) и гарантированно безопасен для человека. Это ключевой фактор, определяющий возможность использования живых векторных вакцин в медицинской практике.
Вакцина MVA85A показала свою безопасность, но в случае применения у детей (клинические испытания фазы II) обеспечивала защиту от инфекции не больше, чем БЦЖ. У взрослых вакцина показала перспективность для предотвращения распространения ТБ среди взрослого населения в виде увеличения численности полифункциональных Ag85А-специфичных CD4+ и CD8+ Т-клеток, а также клеток памяти. CD4+ Т-клеточный ответ на Аg85А у взрослых пациентов, вакцинированных MVA85А, обнаруживался даже спустя 6 лет после вакцинации [54, 71, 72, 73].
Вакцина Ad35/Aeras 402 показала безопасность и широкий иммунный ответ по типу Th1, за исключением одного, но важного маркера – интерлейкина-17. В настоящий момент проходит II фазу клинических испытаний [54, 73].
Инактивированные цельноклеточные вакцины
Состав вакцины RUTI базируется на компонентах клеточной стенки возбудителя M. tuberculosis, которые заключены в специальную липосомную суспензию. Данная вакцина позиционируется как терапевтическое средство, которое целесообразно применять на этапе интенсивной химиотерапии. Фаза I клинических исследований проводилась у здоровых добровольцев, что позволило оценить базовую безопасность препарата. Фаза II проводилась на пациентках с подтверждённой туберкулёзной инфекцией. Вакцина продемонстрировала выраженный защитный эффект против возможных осложнений и проявила значимый иммунотерапевтический потенциал при использовании различных дозировок. В настоящее время вакцина готовятся к III, завершающему, этапу клинических исследований для оценки клинической эффективности комбинированного лечения в отношении латентной туберкулёзной инфекции [53, 54, 74, 75].
В состав вакцины DAR-901 входят нетуберкулёзные штаммы микобактерий, полученные из сертифицированного банка клеток Master Cell Bank SRL-172. Данный штамм уже доказал свою эффективность в ходе успешных клинических испытаний III фазы, проведённых на территории Танзании. Особенно значимыми являются результаты применения вакцины у пациентов с ВИЧ-инфекцией, где была продемонстрирована высокая терапевтическая эффективность. В настоящее время проводится рандомизированное исследование фазы IIb, в рамках которой осуществляется трёхкратная вакцинация подростков в возрасте 13–15 лет, ранее вакцинированных БЦЖ [53].
В основе препарата MIP лежит термически инактивированная культура непатогенной микобактерии Mycobacterium indicus pranii, которая генетически близка к Mycobacterium avium [76]. Результаты клинических испытаний III фазы убедительно доказали перспективность использования MIP в роли дополнительного (бустерного) компонента к вакцине БЦЖ [77].
Таким образом на III фазе клинических испытаний находятся MTBVAC, VPM1002, GamTBvac, Immuvac (MIP), а также ревакцинация БЦЖ [78]. Однако большинство исследований всё ещё продолжается, некоторые вакцины находятся только в начале испытаний.
Иммунологические методы диагностики туберкулёзной инфекции
Далее проведён анализ литературы на тему диагностики туберкулёзной инфекции в социуме с целью поиска наиболее чувствительного и специфического метода.
Проба Манту и проба АТР
Проба Манту используется уже более 110 лет как способ иммунологического скрининга на туберкулёзную инфекцию. Но интерпретация результатов массовой туберкулинодиагностики объективно затруднена вследствие иммунизации детского населения против туберкулёза применением вакцины БЦЖ/БЦЖ-М; специфичность внутрикожной пробы Манту значительно снизилась из-за большого числа «ложноположительных реакций» [79]. В 2008 году в России был внедрён новый метод диагностики туберкулёза – внутрикожная проба с АТР «Диаскин-тест®». По сравнению с традиционной пробой Манту, новый метод диагностики пробы с АТР «Диаскин-тест®» показывает более высокую чувствительность и специфичность [80, 81].
В одном из исследований авторы оценивали результаты скрининга 1267 детей при помощи пробы Манту и АТР «Диаскинтест». Положительная реакция пробы Манту наблюдалась у 753 детей (59,4%), сомнительная реакция – у 293 детей (23,1%), отрицательная реакция – у 221 ребенка (17,4%); положительная реакция АТР «Диаскинтеста» наблюдалась у 11 детей (0,9%), сомнительная реакция – у 21 ребенка (1,7%), отрицательная реакция – у 1235 детей (97,4%) [82], то есть авторами отмечена высокая частота «ложноположительных» реакций, что значительно усложняет диагностику туберкулёзного процесса.
В другом исследовании авторы сравнивали результаты пробы Манту и АТР «Диаскинтест» у 165 детей с активным туберкулёзным процессом и у 95 детей, инфицированных МБТ [83]. Исследование показало, что «Диаскинтест» обладает крайне высокой чувствительностью (94,6%) по сравнению с пробой Манту (50,3%) у пациентоа с активным туберкулёзом. При этом у пациентов, инфицированных МБТ, «Диаскинтест» показывал высокую специфичность и дал положительный результат в 25,3% случаев, в том время как проба Манту показала высокий результат в 24,2% случаев.
Проводилось ещё одно исследование, в котором массово обследовали 39 983 ребенка с применением пробы Манту и АТР «Диаскинтеста». У 39 371 ребенка (98,5%) реакция на АТР «Диаскин-тест» была отрицательная, у 252 детей (0,6%) – сомнительная, у 360 детей (0,9%) – положительная.
Среди ранее инфицированных детей без нарастания чувствительности к туберкулину отмечены положительные реакции на АТР «Диаскинтест» у 57,7% из числа всех положительных реакций на АТР «Диа-скинтест». У 22,5% положительную реакцию на АТР «Диаскинтест» выявили при нарастании чувствительности к туберкулину среди ранее инфицированных, у 19,7% – в раннем периоде первичной туберкулёзной инфекции. Сомнительные реакции на АТР «Диаскинтест» у 48,8% из числа всех сомнительных реакций были выявлены у ранее инфицированных детей без нарастания чувствительности к туберкулину. У 41,7% сомнительные реакции на АТР «Диаскинтест» выявляли при нарастании чувствительности к туберкулину или в раннем периоде первичной туберкулёзной инфекции [84].
В исследовании [85] авторы показали низкую эффективность пробы Манту с 2 ТЕ в качестве метода ранней диагностики заболевания. Авторы сделали вывод, что применение пробы Манту с 2 ТЕ приводит к гиподиагностике ЛТИ при низкой чувствительности (10%) и средней (50%) чувствительности к туберкулину при использовании пробы с АТР, QFR и T-SPOT.TB, т.е. дети не направляются к фтизиатру своевременно, тогда как при высокой чувствительности отмечается гипердиагностика данного состояния в 75,9% случаев. Также авторами отмечено, что в случае наличия сопутствующей патологии необходимо учитывая и возможность ложноположительного результата по пробе с АТР, в особенности у детей с аллергической патологией и ожирением, которым рекомендовано применение ELISРОT и QFT.
Таким образом, опираясь на четыре выше приведённые работы, можно сделать вывод, что проба «Дискинтест» лучше подходит для диагностики у уже инфицированных пациентов, по сравнению с пробой Манту, которая во всех работах показала высокий «ложноположительный» результат в данной категории пациентов.
В 2012 году в Российской Федерации, помимо кожных тестов, стали применять иммунологический метод T-SPOT.TB. Однако эта проба не нашла пока широкого применения ввиду необходимости специального оборудования, поэтому применяется лишь в случаях отказа родителей на проведение кожных иммунологических проб детям. Но этот метод диагностики показал высокую эффективность в выявлении туберкулёзной инфекции [86–88]. Было проведено исследование, в котором 23 людям выполнялся тест T-SPOT.TB для подтверждения латентной туберкулёзной инфекции (ЛТИ) и активного туберкулёзного процесса. Положительный результат Т-SPOT.TB был получен у 7 пациентов (30,5%), сомнительный – в 4,3%, отрицательный – в 65,2% случаев. Среди положительно реагирующих на Т-SPOT.ТВ был 1 ребенок с подозрением на туберкулёз внутригрудных лимфатических узлов и 6 взрослых, среди которых ½ – с внелёгочной локализацией [87]. Было проведено другое исследование, в котором 52 ребенка были с изменённой чувствительностью к кожным пробам, из них 51 ребёнок был вакцинирован БЦЖ-М. Положительный результат T-SPOT.TB установлен у 13 детей (25%), сомнительный – у 10 детей (19,2%), отрицательный – у 29 (55,8%) детей [88].
Ещё в одном исследовании была разработана специальная модель для анализа эффективности диагностических тестов, что позволяет проводить комплексную оценку полученных результатов. Для сравнения был рассмотрен гипотетический идеальный диагностический метод с максимальными показателями точности (100% чувствительность и специфичность). При распространённости латентной туберкулёзной инфекции (ЛТИ) на уровне 20% такой тест продемонстрировал бы 20 положительных и 80 отрицательных результатов из 100 обследованных пациентов. Однако при клиническом использовании пробы Манту, характеризующейся относительно невысокими показателями (36% чувствительность и 59% специфичность), из 100 обследованных детей положительный результат зафиксирован у 40 человек, при этом только у 7 из них действительно присутствовала ЛТИ, что указывает на значительное количество ложноположительных результатов. Существенно более высокие показатели в данной модели продемонстрировал тест T-SPOT.TB, обладающий чувствительностью 73% и специфичностью 93%. Положительные результаты были получены у 19 человек, у 14 выявлено ЛТИ, а у 5 получен неопределенный результат [89].
Таким образом можно сделать вывод, что в случае ЛТИ применение T-SPOT.TB позволяет выявить гораздо больше случаев реального инфицирования ЛТИ, особенно для детей из групп риска, чьи родители отказываются от скрининговой иммунодиагностики или при наличии медицинских отводов или противопоказаний для проведения кожных проб.
QuantiFERON-TB тест
QuantiFERON-TB Gold In-Tube и QuantiFERON-TB Gold Plus являются тест-системами последнего поколения для диагностики активной и латентной туберкулёзной инфекции in vitro. Квантифероновые тесты имеют ряд преимуществ: отсутствуют противопоказания, побочные реакции, отсутствие перекрёстной реактивности с БЦЖ и другими видами микобактерий, более объективная оценка получен- ных результатов, не зависящая от кожной чувствительности [90–92].
В исследовании Васильевой Е.В. у 47 пациентов с верифицированным туберкулёзом тест QuantiFERON-TB Gold In-Tube был положительным у 36 из 47 обследованных [93]. У больных с бактериовыделением по сравнению с больными без бактериовыделения частота положительных результатов в тесте достоверно не различалась (78% против 73%). Ложноотрицательные результаты получены в 11 случаях, из них у 2 пациентов в возрасте более 70 лет, у 2 пациентов с хроническим вирусным гепатитом С, у одного больного казеозной пневмонией и у 6 лиц с различными формами туберкулёза (инфильтративный – 3, диссеминированный – 1, очаговый – 2). В группе больных с другой лёгочной патологией число истинно отрицательных результатов составило 70%.
В Японии в 2012 году авторами К. Хигучи и И. Секия [94] проведено сравнение специфичности между T-SPOT.TB и QuantiFERON®-TB Gold. Из общего числа 111 субъектов, вакцинированных БЦЖ, один положительный результат и 110 отрицательных результатов были получены с использованием обоих тестов на основе глобальных порогов. Хотя некоторые метаанализы сообщили о более высокой специфичности для QuantiFERON®-TB Gold по сравнению с T-SPOT.ТВ, их исследование показывает одинаково высокую специфичность для обоих тестов в популяции с действительно низким риском заражения туберкулёзом.
В работе Danilo Buonsenso в 5 исследованиях чувствительность QuantiFERON-TB Gold Plus оценивалась по отношению к «окончательному диагнозу» микробиологически подтвержденного туберкулёза [95]. Общая чувствительность анализа QuantiFERON-TB Gold Plus для инфекции МБТ по сравнению со стандартом микробиологически подтверждённого туберкулёза составила 54,5–87,3%. Самая высокая чувствительность была в исследовании детей/ подростков с клинически/рентгенологически подозрением на туберкулёз (впоследствии подтвержденным активным заболеванием), а самая низкая чувствительность была в популяции, из которой 42,4% имели внелёгочный туберкулёз или лёгочный туберкулёз с сопутствующим внелёгочным туберкулёзом.
В работе Telisinghe L. авторы сравнивали чувствительность QuantiFERON-TB Gold Plus и QuantiFERON-TB Gold In-Tube у пациентов с коинфекцией ВИЧ и туберкулёз [96]. Исследование, проведённое в Замбии, показало 85% чувствительности с QuantiFERON-TB Gold Plus среди пациентов с положительным результатом посева, активных пациентов с туберкулёзом, которые были ВИЧ- положительными (68 человек). Хотя исследование не включало прямое сравнение с QuantiFERON-TB Gold In-Tube, авторы утверждали, что QuantiFERON-TB Gold Plus имеет более высокую чувствительность, чем QuantiFERON-TB Gold In-Tube у пациентов с ВИЧ-инфекцией.
В исследовании [97] сравнивалась чувствительность тестов QuantiFERON-TB Gold Plus и QuantiFERON-TB Gold In-Tube у детей с туберкулёзом. Это небольшое исследование, проведённое в Эсватини, показало одинаковую чувствительность между QuantiFERON-TB Gold Plus и QuantiFERON-TB Gold In-Tube среди детей с активным туберкулёзом на основе микробиологических и клинических эталонных стандартов. Несколько исследований сравнили специфичность QuantiFERON-TB Gold Plus со специфичностью QuantiFERON-TB Gold In-Tube в группах населения с низким риском в Америке у 262
людей, среди которых был 51 человек с нетуберкулёзным микобактериозом (98,1% против 98,9%).
Авторами [98] в своей работе отмечен очень важный факт того, что защита от заражения M. tuberculosis после вакцинации БЦЖ, измеряемая по результатам теста QuantiFERON, неодинакова в разных группах. В группах, члены которых недавно контактировали с больным, результаты теста QuantiFERON свидетельствуют о защите от заболевания и могут использоваться в качестве косвенного показателя заболевания при испытаниях противотуберкулёзных вакцин. Авторами отмечено, что туберкулиновая проба не подходит для профилактики в рамках экспериментальных исследований фазы 2b.
Все данные сравнительной оценки чувствительности и специфичности методов диагностики туберкулёза из описанных выше работ представлены в таблице 2.
|
Сравнение методов диагностики туберкулёза |
|||||
|
Манту |
Диаскинтест |
T-SPOT.TB |
QuantiFERON-TB Gold In-Tube |
QuantiFERON-TB Gold Plus |
|
|
Чувствительность к туберкулину |
50,3% [83] – 59,4% [82] |
94,6% [83] |
73% [89] |
78% [93] |
54,5%–87,3% [95] |
|
Специфичность |
17,4% [82] – 20% [83] |
93,7% [99] |
93% [89] |
98,9% [97] |
98,1% [97] |
Как видно из данных таблицы 2, чувствительность Диаскинтеста, T-SPOT.TB, QuantiFERON-TB Gold In-Tube и QuantiFERON-TB Gold Plus существенно больше, чем у Манту. По результатам сравнения специфичности методов диагностики туберкулёза заметно, что Диаскинтест, T-SPOT.TB, QuantiFERON-TB Gold In-Tube и QuantiFERON-TB Gold Plus показывают более высокие значения. Несмотря на то, что в исследованиях был разный объём выборки, предпочтение по эффективности в большей степени отдается именно им. Эти методы являются более надежным выбором для диагностики туберкулёза, нежели Манту, так как при их применении наблюдается гораздо меньшее число ложноположительных результатов, что является важным фактором при диагностике туберкулёза. В случае отказа от проведения кожных проб T-SPOT.TB, QuantiFERON-TB Gold In-Tube и QuantiFERON-TB Gold Plus являются преимущественным выбором диагностики у пациентов с латентной туберкулёзной инфекцией.
Однако, несмотря на высокие показатели, необходимо просчитать экономическую целесообразность каждого метода, особенно учитывая дороговизну оборудования и лаборатории для их выполнения, что наиболее важно в современных реалиях.
ВЫВОДЫ
Таким образом в данном обзоре оценены и проанализированы основные публикации, связанные с иммунопрофилактикой и иммунодиагностикой туберкулёза.
На основании проанализированного материала можно сделать вывод, что в современенных реалиях, несмотря на то, что клинические испытания терапевтических вакцин против туберкулёза продолжаются, потребуется ещё много времени и средств, чтобы внедрить эти препараты в массовое производство. Наиболее перспективные кандидаты в настоящее время проходят испытания на эффективность в странах с высоким уровнем заболеваемости. Создание испытательных центров для проверки эффективности представляет собой серьёзную проблему для исследователей. Для проведения испытаний IIb и III фаз требуется надёжная клиническая и лабораторная среда с налаженными ресурсами на местах, где можно набирать очень большие группы участников и наблюдать за ними в течение длительного времени [100]. Усовершенствованный режим вакцинации против туберкулёза является важной составляющей эффективной борьбы с туберкулёзом во всём мире и достижения целей программы «Остановить туберкулёз». В настоящее время эффективной вакциной является БЦЖ, которая снижа- ет риски развития тяжёлых распространённых форм туберкулёзного процесса, в том числе внелёгочной локализации. Безусловно, в будущем альтернативой БЦЖ могут быть и другие вакцины, которые находятся на стадии клинических испытаний. Каждая из данных вакцин обладает различными механизмами действия по отношению к туберкулёзной инфекции, что в теории может послужить к сокращению времени проведения противотуберкулёзного лечения, а также повысить вероятность благоприятного исхода после химиотерапии. Анализ литературы показал, что ближе всего к внедрению и окончанию испытаний (а именно факт нахождения в III фазе) находятся препараты MTBVAC, VPM1002, GamTBvac, Immuvac (MIP), что безусловно даёт надежду на повышение эффективности профилактики туберкулёза.
На основании анализа иммунологических методов диагностики нельзя не отметить высокую значимость применения данных методов среди взрослого и детского населения. Проба Манту остаётся наиболее распространённым методом диагностики среди детского населения в настоящее время, однако всё чаще сообщаются данные о частом разви- тии «ложноположительных» результатов. В связи с этим требуется активное внедрение более современных иммунологических методов диагностики туберкулёзной инфекции в клиническую практику. Результаты проанализированных исследований доказывают высокую значимость применения современных методов диагностики, к которым относится проба с АТР «Диаскинтест», T-SPOT и квантиферо-новый тест. По данным различных авторов, эффективность данных иммунологических методов диагностики достигает 90% среди людей различных популяций. В связи с чем применение данных методов имеет высокую значимость в клиническом применении как в общей лечебной сети, так и противотуберкулёзных учреждениях. Стоит отметить, что согласно проанализированным публикациям наиболее специфичным методом диагностики явился QuantiFERON-TB Gold In-Tube, однако не с самой высокой чувствительностью. При этом «Диаскин-тест» в исследованиях показывает самую высокую чувствительность, но при этом и довольно высокую специфичность.


