Пучково-плазменные технологии переработки целлюлозы и лигнинов
Автор: Кхин Маунг Хтау, Хтет Вэй Ян Чжо, Васильева Т.М.
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Физика
Статья в выпуске: 1 (41) т.11, 2019 года.
Бесплатный доступ
Рассмотрена возможность применения неравновесной низкотемпературной плазмы для обработки биополимеров (целлюлозы, лигнина и его производных). Разработаны следующие методики, основанные на плазменно-стимулированных процессах: - деструкция твердых порошков биополимеров в электронно-пучковой плазме (ЭПП), генерируемой при инжекции электронного пучка в плотные газообразные среды; - функционализация полисахаридных материалов и лигнинов в гибридной плазме (ГП), которая генерируется при инжекции электронного пучка в ВЧ газоразрядную плазму. При ЭПП-стимулированной деструкции целлюлозы наблюдалось образование олигосахаридов с молекулярной массой 800-2000 Да и степенью полимеризации, варьирующейся от димеров до гептамеров, также показана частичная деструкция лигниновых порошков. Обработка ЭПП и ГП полисахаридных губок изменяла морфологию поверхностей, улучшала гидрофильность и приводила к образованию химически активных полярных кислородсодержащих групп. В ГП была выполнена прививка белка крови тромбина и молочной кислоты на поверхность из целлюлозных губок, гидролизованного лигнина и лигносульфонатов соответственно.
Целлюлоза, лигнин, порошки, модифицирование поверхности, электронно-пучковая плазма, гибридная плазма
Короткий адрес: https://sciup.org/142220467
IDR: 142220467 | УДК: 544.558;544.528
Beam plasma technologies for processing cellulose and lignins
Applications of nonequilibrium low temperature plasmas for the processing of biopolymers (cellulose, lignin and its derivatives) are described. The techniques based on plasma-assisted processes are developed, viz. destruction of biopolymers solid powders in electron beam plasma (EBP), generated by the injection of the electron beam into dense gaseous media; functionalization of polysaccharides materials and lignins in hybrid plasma produced by an electron beam injection into RF gas discharge plasma.The formation of oligosaccharides with molecular weight 800-2000 Da and polymerization degree varying from dimers to heptamers during the EBP-stimulated destruction of cellulose, chitin, and chitosan powders is observed. The EBP- and HP- treatment of polysaccharides sponges were found to change the surfaces morphology, improve hydrophilicity and cause the formation of chemically active groups. Further grafting of the blood clotting protein thrombin and lactic acid is performed in HP modified surfaces of cellulose sponges, hydrolyzed lignin and lignosulfonates.
Текст научной статьи Пучково-плазменные технологии переработки целлюлозы и лигнинов
В последнее время во всем мире отмечается увеличение использования биоматериалов в качестве недорогих и возобновляемых источников для создания новых функциональных полимерных биокомпозитов. Самым распространенным возобновляемым биоматериалом на Земле является лигноцеллюлозная биомасса, которая состоит из трех основных биологических полимеров: целлюлозы, гемицеллюлозы и лигнина. В свою очередь целлюлоза (главным образом, в виде растительных волокон) представляет собой наиболее распространенный природный полимер, а лигнин - второе по распространенности вещество в природе после целлюлозы. Структурные формулы целлюлозы и лигнина представлены на рис. 1. В отличие от кристаллических полисахаридов лигнин обладает нелинейной аморфной структурой и состоит из метоксилированных пропиловых фениловых блоков.
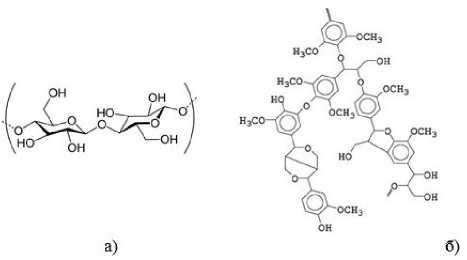
Рис. 1. Структурные формулы целлюлозы (а), лигнина, (б)
Интерес к использованию целлюлозы и лигнинов в различных сферах деятельности человека. связан не только с их широким распространением в природе и вознобновляемостью их сырьевых источников, но и с уникальным комплексом физико-химических, механических и биологических особенностей: прочностью, низкой токсичностью, высокой комплексообразующей активностью, возможностью химической модификации, хорошей совместимостью с тканями организма, способностью к биодеградации, возможностью получения наноструктур (например, наноцеллюлозы) [1-4]. Среди областей, где применяется целлюлоза, можно назвать целлюлозно-бумажную промышленность, текстильное производство, энергетику, сельское хозяйство, биотехнологию и медицину. Лигнин, являясь ароматическим соединением, представляет собой ценное перспективное сырье для органического синтеза и получения биотоплива, что делает его перспективной альтернативой нефти.
Традиционным методом переработки целлюлозы является химический гидролиз, которому присущ целый ряд ограничений и недостатков [1]: многостадийность, длительность, образование значительных количеств побочных продуктов, что требует весьма трудоемкого выделения целевых соединений, применения концентрированных растворов кислот и щелочей, необходимости обезвреживания отходов, высокой температуры процесса. Лигнин вообще трудно подвергается какой-либо химической переработке и модификации и поэтому в основном используется в качестве топлива, несмотря на. наличие большого количества, потенциальных коммерческих применений [5]. Таким образом, разработка, новых экологически чистых методов переработки природных полимеров, основанных на. нетрадиционных воздействиях на. вещество, остается крайне актуальной задачей.
Плазмохимическая модификация/предобработка природного сырья позволяет не только сократить экономические и временные затраты на. следующих этапах его переработки, но и добиться увеличения выхода, целевых продуктов (например, низкомолекулярных водорастворимых олигосахаридов, мономерных ароматических веществ, биотоплива), способных улучшить качество и технологические свойства, производимых из них материалов.
Цель работы - прямое экспериментальное доказательство возможности управляемой деструкции целлюлозы и модификации лигнина в низкотемпературной неравновесной плазме, а именно электронно-пучковой плазме (ЭПП) и гибридной плазме.
2. Экспериментальная установка
В настоящей работе для обработки целлюлозы использовалась ЭПП, которая генерируется при инжекции электронного пучка в плотные газообразные среды [6]. Получаемая ЭПП сильно неравновесна: в ее составе присутствуют молекулы, атомы, радикалы и ионы в основном и в возбужденном состояниях, а также электроны плазмы и электроны инжектируемого пучка. Концентрации тяжелых частиц плазмы существенно превышают их равновесные значения, что и определяет высокую химическую активность ЭПП. Экспериментально доказано, что температуру в процессе модификации материалов удается поддерживать на уровне 300-400 К без потери высокой химической активности ЭПП, что позволяет работать с термолабильными соединениями, в том числе и с полисахаридами.
Деструкция порошков целлюлозы проводилась в электронно-пучковом плазмохимическом реакторе, устройство и принцип действия которого представлены в [6]. С целью увеличения массы обрабатываемого порошка были разработаны специальные дополнительные устройства, в реакционном объеме которых организовано перемешивание значительного количества порошка в процессе обработки. Рисунок 2а иллюстрирует процесс ЭПП-обработки. Сформированный в высоком вакууме (~ 10—5 Торр) электронный пучок (ЭП) (3) инжектировался в заполненную плазмообразующей средой реакционную камеру (6) через газодинамическое выводное окно (4), при этом формировалось облако химически активной ЭПП (7). ЭП сканировали в круглый растр с помощью электромагнитной системы (5), что повышало равномерность обработки материала (8).
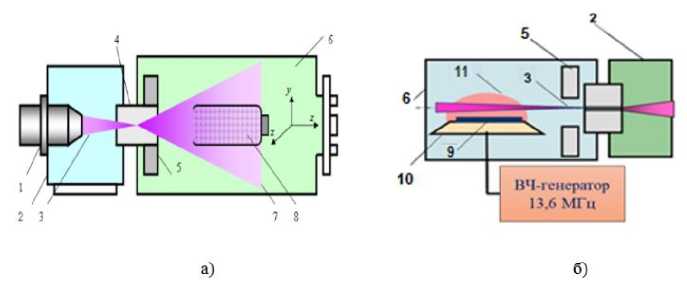
Рис. 2. Схема, плазмохимического реактора, и процедура, (а) генерации электронно-пучковой плазмы и (б) генерации гибридной плазмы-стимулированной деструкции порошков целлюлозы: 1 - электронная пушка; 2 - высоковакуумная камера; 3 - электронный пучок; 4 - выводное устройство;
5 - электромагнитная отклоняющая система; 6 - рабочая камера; 7 - облако ЭПП; 8 - кварцевая труба; 9 - обработанный субстрат, 10 - ВЧ-генератор, 11 - ВЧ-разряда
Температура, образцов измерялась оптическим пирометром Optris LS (Optris GmbH, Германия) и не превышала 50 °C. Сила тока пучка 1ъ подбиралась таким образом, чтобы поддерживать постоянным указанное значение температуры и варьировалась в пределах 1 < 1ь < 100 мА. Энергия электронов на входе в реакционную камеру была постоянной и составляла 30 кэВ. В экспериментах в качестве плазмообразующего газа использовались кислород, аргон и аммиак. Величины давления плазмообразующих газов варьировались в пределах 1-10 Торр.
Гибридную плазму получали путем инжекции ЭП в область ВЧ-разряда, для генерации которого использовали ВЧ-генератор GenesisGHW-12 (MKSInstruments, Великобритания) с частотой 13,6 МГц и эффективной мощностью 20 Вт. В качестве плазмообразующей среды использовали химический чистый кислород и гелий при давлении 0,5 Торр.
В работе были использованы порошок микрокристаллической целлюлозы (средневязкостная масса 1000 кДа), а также полученные на ее основе губки, гидролизный лигнин и лигносульфонаты.
3. Результаты
Обработка целлюлозы в ЭПП придавала исходным соединениям новые физикохимические свойства. Отмечалось снижение степени кристалличности целлюлозы и формирование водорастворимых продуктов. По данным гельпроникающей ВЭЖХ, молекулярная масса для наибольшего пика у соединений, полученных в процессе ЭПП-деструкции целлюлозы, варьировалась в пределах 800-2000 Да. Таким образом происходило образование олигосахаридов со степенью полимеризации от димеров до гептамеров, что связано с действием активных форм кислорода на 3 — 1, 4 гликозидные связи биополимера. При этом следует особо отметить два фундаментальных результата [6]:
-
1) пороговый характер зависимости, связывающей степень деструкции полимера с длительностью пучково-плазменного воздействия;
-
2) вероятность появления побочных, не растворимых в воде соединений в составе продуктов пучково-плазменной модификации биополимеров - эффекта, обусловленного обратной полимеризацией образующихся низкомолекулярных продуктов при неоптимальном выборе условий обработки.
В то же время обработка в ЭПП лигнина практически не влияла на размер макромолекул.


а) б)
SEM-фотографии поверхности губки до и после модификации в ЭПП, увеличение х100 : а) - исходный образец, б) - образец, обработанный в ЭПП кислорода.


а) б)
SEM-фотографии поверхности губки до и после модификации в ЭПП, увеличение х5000 : а) - исходный образец, б) - образец, обработанный в ЭПП кислорода.
Рис. 3. Обработка, губок целлюлозы в ЭПП
В гибридной плазме удалось реализовать прочное ковалентное связывание полисахаридной основы губки и белка тромбина, который является естественным активатором свертывания крови. Плазменно-стимулированный синтез проводили по следующей схеме:
1. Активация и функционализация поверхности полисахаридной губки посредством ее обработки в течение 10 мин в гибридной плазме кислорода (0,5 Торр) при эффективной мощности ВЧ-разряда 50 Вт, ток ЭП варьировали в пределах І^, = 0,4 — 0, 6 мA, U = 30 кэВ.
2. Нанесение на активированную поверхность губки раствора тромбина (активность 500 NIH), которое производили сразу же после ее извлечения из реакционной камеры.
3. Обработка губки с нанесенным тромбином в плазме ВЧ-разряда (эффективная мощность 20 Вт, плазмообразующий газ - гелий при давлении 0,5 Торр) в течение 10 мин и Ts = 30 °C. Предполагалось, что данный этап будет способствовать формированию прочных ковалентных связей между активными группами функционализированного полисахарида и тромбина.
4. Выводы
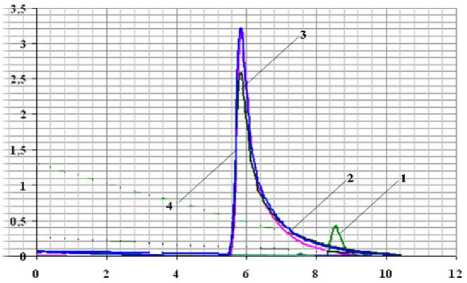
Рис. 4. Гель-пропикающая хроматография биополимерных материалов, полученных в гибридной плазме: 1 - тромбин; 2 - целлюлозная губка, обработанная в гибридной плазме О2; 3 - целлюлозная губка с привитым тромбином, полученная в гибридной плазме О2; 4 - целлюлозная губка с привитым тромбином, полученная в гибридной плазме аммиака.
На хроматограмме коммерческого препарата, тромбина, определялся пик, соответствующий его молекулярной массе (~ 40 кДа) со временем элюирования 8,58 мин. В то же время на. хроматограмме образцов, полученных в ходе плазмохимического синтеза, пик индивидуального тромбина, отсутствовал, что свидетельствует о прочном связывании белка, с полисахаридной матрицей. В дальнейших экспериментах методика, была, использована, для прививки молочной кислоты на. поверхность гидролизного лигнина, и лигносульфонатов.
Экспериментально доказана, возможность получения низкомолекулярных водорастворимых олигосахаридов целлюлозы в ЭПП кислорода. При этом наблюдается пороговый характер зависимости, связывающей степень деструкции полимера, с длительностью пучковоплазменного воздействия, что позволяет оптимизировать процесс обработки и исключить непроизводительные энергозатраты.
В гибридной плазме возможно осуществлять ковалентное связывание биологически активных молекул с биополимерным субстратом. Полученные материалы в дальнейшем могут служить основой для создания эффективных сорбентов, гемостатических средств, нанобиосенсоров и т.п.
Работа, выполнена, при поддержке Минобрнауки, проект № 10А.100.
Список литературы Пучково-плазменные технологии переработки целлюлозы и лигнинов
- Zargar V., Asghari M., Dashti A. A Review on Chitin and Chitosan Polymers: Structure, Chemistry, Solubility, Derivatives, and Applications//Chem. Bio Eng. Reviews. 2015. V. 2. P. 226.
- Biederman H. Plasma polymers and some biomedical applications//European Cells and Materials 2003. V. 6. P. 28.
- Klemm D., Heublein B., Fink H.P., Bohn A. Cellulose: fascinating biopolymer and sustainable raw material//Angew. Chem. Int. Edit. 2005. V. 44. P. 3393.
- Yan Xue, Zihao Moua, Huining Xiao. Nanocellulose as a sustainable biomass material: structure, properties, present status and future prospects in biomedical applications//Nanoscale. 2017. V. 9. P. 14758.
- Patel M., Zhang X., Kumar A. Techno-economic and life cycle assessment on lignocellulosic biomass thermochemical conversion technologies: A review//Renewable and Sustainable Energy Reviews. 2016. V. 53. P. 1499.
- Vasilieva T., Chuhchin D., Lopatin S., Varlamov V., Sigarev A., Vasiliev M. Chitin and cellulose processing in low-temperature electron beam plasma//Molecules. 2017. V. 22. P. 1908. 22111908 DOI: 10.3390/molecules


