Пути улучшения диагностики и лечения раннего рака толстой кишки: литературная справка и клинический случай
Автор: Гаулика В.О., Парсаданян А.М., Костанян К.К.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Обзоры
Статья в выпуске: 3 т.24, 2025 года.
Бесплатный доступ
Разработка эффективных, высокочувствительных и высокоспецифичных подходов к ранней диагностике рака толстой кишки является основой для своевременного применения различного рода целенаправленных вмешательств, способных эффективно разрешить задачу с сохранением приемлемого качества жизни пациента. Эндоскопические методы диагностики и лечения по-прежнему играют решающую роль в улучшении онкологических исходов и постоянно совершенствуются для повышения выявляемости колоректального рака. Цель исследования – проанализировать и обобщить современную научную литературу, описывающую пути улучшения ранней диагностики и лечения рака толстой кишки; описать клинический случай из собственной практики, демонстрирующий важность качественной диагностики для подбора стратегии при лечении рака толстой кишки. Материал и методы. Для написания обзорной части статьи был произведен поиск публикаций в системе Pubmed, в базах Google Scholar, elibrary.ru по ключевым словам: колоректальный рак, рак толстой кишки, КТ-колонография, колоноскопия. Приоритет был отдан работам, описывающим совершенствование инструментальных методик выявления новообразований толстой кишки. Было изучено более 100 публикаций отечественных и зарубежных авторов за 2016–25 гг., из них 41 была отобрана для настоящего обзора. Результаты. В качестве наиболее перспективного подхода в современной литературе представляется точная оптическая диагностика, с возможностью информативного эндоскопического прогнозирования гистологии полипов в режиме реального времени, в том числе с высокой чувствительностью к выявлению новообразований малых размеров. Подобный подход позволит отказаться от щипцовой биопсии, снизив частоту ошибочных диагнозов (что продемонстрировано в описанном клиническом случае), в том числе по причине неправильного отбора образцов. Заключение. При разработке стратегий улучшения раннего выявления и лечения рака толстой кишки необходимо учитывать, что кадровый, диагностический и терапевтический потенциал в различных регионах России значительно различается. Отечественным исследователям необходимо формировать собственный опыт в проведении комплексных диагностических мероприятий, устранении экономических препятствий для эффективного выявления рака толстой кишки, а также разрабатывать рациональные пути улучшения терапевтических подходов, исходя из возможностей регионального здравоохранения.
Рак толстой кишки, колоректальный рак, колоноскопия, щипцовая биопсия, искусственный интеллект, узкоспектральная эндоскопия
Короткий адрес: https://sciup.org/140310579
IDR: 140310579 | УДК: 616.345-006.6-07-08 | DOI: 10.21294/1814-4861-2025-24-3-114-123
Ways to improve the diagnosis and treatment of early colorectal cancer: a literature review and a clinical case study
The development of effective, highly sensitive and highly specific approaches to early detection of colorectal cancer is the basis for the timely use of various targeted interventions that can effectively solve patients’ problems, minimizing the impact on their quality of life. Endoscopic diagnostic and therapeutic techniques continue to play a critical role in improving cancer outcomes and are continually being reviewed and improved to increase detection rates of colorectal cancer. The aim of the study was to analyze and summarize the current scientific literature describing promising developments in early diagnosis and treatment of colorectal cancer, as well as to describe a case report demonstrating the importance of high-quality diagnostics for selecting a therapeutic strategy for colorectal cancer. Material and Methods. The literature search was conducted in Pubmed, Google Scholar, and Elibrary.ru databases, focusing on articles published between 2016 and 2025, using the key words “colorectal cancer”, “colorectal cancer”, “CT-colonography”, “colonoscopy”. Priority was given to the studies describing the improvement of screening tools for detecting colorectal neoplasia. Of the 100 publications, 41 were selected for this review. Results. Precise optical diagnosis of colorectal polyps, including the ability to predict polyp histology in real time during colonoscopy, appears to be the most promising approach for detecting even small colorectal lesions. This approach can potentially allow for the abandonment of forceps biopsy reducing the incidence of misdiagnosis (as demonstrated in the described case report). Conclusion. To develop strategies for improving early detection and treatment of colorectal cancer, it is necessary to take into account the fact that the human, diagnostic and therapeutic potential in different regions of Russia varies significantly. Researchers should prioritize developing their own diagnostic experience, removing economic barriers to effective colorectal cancer detection, and developing rational ways to improve therapeutic approaches within regional health care settings.
Текст научной статьи Пути улучшения диагностики и лечения раннего рака толстой кишки: литературная справка и клинический случай
Рак толстой кишки является одной из лидирующих патологий, на протяжении уже нескольких десятков лет показывающий значительный рост заболеваемости и смертности. Колоректальный рак (под этим термином подразумевается злокачественная опухоль всей толстой кишки, включая прямую) по распространенности среди онкологических заболеваний во всем мире занимает третье место у мужчин и второе место – у женщин [1]. Согласно данным ВОЗ, в мире ежегодно регистрируется 1,93 млн случаев колоректального рака (КРР). В России распространенность заболевания демонстрирует неуклонный рост; с постепенным «омоложением» контингента онкологических больных [2]. При этом в развитых странах отмечается некоторая тенденция к снижению смертности от КРР, которую связывают с реализацией программ скрининга рака и разработкой более эффективных стратегий для лечения ранней стадии заболевания в виде удаления очагов КРР и аденоматозных полипов. Раннее обнаружение предраковых заболеваний и рака толстой кишки остается оптимальным методом снижения заболеваемости и улучшения онкологических исходов при КРР [3].
Для обнаружения ранних злокачественных изменений толстой кишки, выявления признаков инвазии и получения тканей для дополнительного гистологического исследования используется колоноскопия. Для повышения диагностической эффективности исследования внедряются в практику эндоскопы с высокой разрешающей способностью, с возможностью оптического увеличения, проведения осмотра в HD-качестве, применения узкоспектрального режима, аутофлуоресценции, хромоскопии или использования витальных красителей [4]. Сегодня сохраняется вариативность в определении наиболее предпочтительной диагностической стратегии раннего обнаружения КРР. Низкое качество ранней диагностики связано с повышенным риском развития запущенных случаев КРР и ростом смертности; при этом качество существенно варьирует в зависимости от индивидуального подхода к скрининговым обследованиям различных медицинских учреждений, опыта и квалификации эндоскопистов и полноты обследования [5].
Цель исследования – проанализировать современную научную литературу, посвященную улучшению ранней диагностики и лечения рака толстой кишки; и описать клинический случай из собственной практики, демонстрирующий важность качественной диагностики для подбора стратегии при лечении рака толстой кишки.
Материал и методы
Для написания обзорной части статьи был произведен поиск публикаций в системе Pubmed, в базах Google Scholar, elibrary.ru по ключевым словам: колоректальный рак, рак толстой кишки, КТ-колонография, колоноскопия. Приоритет был отдан работам, описывающим совершенствование инструментальных методик выявления новообразований толстой кишки.
Приложения на основе искусственного интеллекта в диагностике ноовообразований толстой кишки
Для ликвидации ограничений в работе врачей-эндоскопистов, числа пропущенных новообразований и оптимизации диагностического и терапевтического результатов, связанных с квалификацией и опытом врача, все чаще рассматриваются современные технологии. К ним относятся приложения искусственного интеллекта (ИИ), которые способны повышать точность выявления онкологических изменений толстой кишки путем автоматизированного обнаружения и характеристики поражений [6].
В недавней работе К.И. Кулаева и соавт. [2] предпринята попытка снизить частоту пропущенных случаев КРР при проведении диагностической колоноскопии путем привлечения возможностей искусственного интеллекта к детекции новообразований толстой кишки. Чувствительность детекции новообразований с помощью системы принятия решения на основе ИИ составила 80,7 %, при этом наибольшая эффективность детекции новообразований с помощью ИИ зарегистрирована при обнаружении новообразований менее 1,0 см в диаметре [2].
В крупном рандомизированном исследовании, включающем 3 059 бессимптомных пациентов, оценивали эффективность ИИ для улучшения результатов обследования толстой кишки опытными врачами-эндоскопистами и специалистами с ограниченным опытом работы. По результатам исследования колоноскопия с использованием ИИ продемонстрировала значительное преимущество в выявлении новообразований, вне зависимости от их локализации, размера (>10 мм или <5 мм) и опыта врача-эндоскописта. Помимо этого, колоноскопия с ИИ позволила несколько уменьшить влияние недостаточной подготовки кишечника на результат исследования. В качестве недостатка использования ИИ отмечается более длительное время интубации и извлечения эндоскопа, чем при обычной колоноскопии (вероятно, для подтверждения подозрений на полипы ИИ требуется больше времени, чем эндоскописту) [5].
В другой работе колоноскопия, дополненная ИИ, привела к 2-кратному снижению частоты пропущенных случаев при колоректальной неоплазии, в том числе небольших поражений (диаметром <10 мм), как в проксимальном, так и в дистальном отделах толстой кишки, не идентифицированных посредством стандартной колоноскопии [7]. Анализ нескольких аналогичных клинических исследований при колоноскопии с ИИ в отношении колоректальной неоплазии показал чувствительность, равную 95 %, специфичность – 88 % [8]. Эффективность машинного обучения показана в ряде рандомизированных контролируемых исследований; использование ИИ привело к увеличению частоты выявления аденом на 44 % [9, 10].
В других исследованиях также продемонстрирована эффективность системы на основе ИИ, обученной обрабатывать изображения, полученные при колоноскопии, путем наложения эндоскопического изображения на предполагаемые поражения из базы данных в режиме реального времени [11]. Системы компьютерного обнаружения используются для гистологического прогнозирования колоректальных полипов без применения биопсии тканей. При этом машинный диагноз совпадал с диагнозом врача-эндоскописта в 97,5 %; а гистологический прогноз колоректального поражения системы распознавания изображений в режиме реального времени с гистологическим результатом – в 93,3 % случаев [12].
Определенно внедрение автоматизированных технологий в диагностику колоректальных новообразований может быть рассмотрено в качестве потенциального механизма стандартизации диагностического процесса и позволит оптимизировать результаты эндоскопического обследования, снижая количество диагностических ошибок. Низкий риск применения автоматизированных систем позволяет внедрить их в скрининговые программы либо использовать в качестве инструмента контроля качества или облегчения принятия решений. Системы компьютерного обнаружения новообразований на основе ИИ и гистологическое прогнозирование могут послужить безопасным инструментом, дополняющим рутинные обследования. Однако методика с применением ИИ требует оснащения современным эндоскопическим оборудованием, отличается высокой стоимостью и пока не способна заменить опытного врача-эндоскописта.
Совершенствование подходов к эндоскопической визуализации
Одним из эффективных направлений качественной диагностики колоректальных поражений является улучшение качества изображения совре- менного оборудования. Передовой технологией эндоскопической визуализации является узкоспектральная эндоскопия (NBI), которая позволяет различать нормальные и аномальные ткани кишечника посредством улучшенной контрастности поверхностных структур слизистой оболочки, в том числе мелких кровеносных сосудов. Ранее было показано, что NBI-эндоскопия применяется для определения глубины инвазии новообразования толстой кишки путем оценки микрососудистой архитектуры и подходит для прогнозирования гистологического диагноза [13]. Новые поколения узкоспектральных эндоскопических аппаратов обеспечивают более широкий фокус с увеличением до 90 раз, что позволяет получить яркие изображения с высокой частотой кадров. Отличительной способностью новых моделей является совместимость с другими увеличительными приборами, а также с устройствами автоматического обнаружения колоректальных новообразований, в том числе на основе ИИ [14].
Для повышения эффективности оптической диагностики колоректальных полипов предлагается дополнять эндоскопию с узкополосной визуализацией увеличительной хромоэндоскопией, в особенности для участков с низкой степенью достоверности или для участков с глубокой инвазией [15]. Разработан алгоритм, объединяющий информацию, полученную путем узкополосной (NBI) и аутофлуоресцентной визуализации (AFI). Сообщается, что сочетание данных методов позволяет увеличить точность эндоскопической дифференциации аденом и неопластических полипов толстой кишки как опытным, так и начинающим эндоскопистам [16].
Другая методика расширения возможностей эндоскопической диагностики – система гибкой спектральной визуализации с улучшением цветопередачи (FICE) – также применяется в диагностике колоректальных новообразований путем распознавания и увеличения типов рисунка микрососудов. Недостатком технологии по сравнению с NBI считается невозможность гистологического прогнозирования [17].
Продолжается изучение диагностической точности молекулярной визуализации – метода, при котором для получения визуальной информации о состоянии слизистой оболочки в режиме реального времени используются флуоресцентно меченные антитела. Антитела позволяют визуализировать биохимические процессы в тканях, выделяя аномальные ткани и повышая диагностическую ценность эндоскопии при обнаружении полипов толстой кишки. Технология яркой флуоресценции новообразований толстой кишки отличается высокой стоимостью; распространению методики препятствуют длительный период полураспада антител и опасения относительно возможного иммунного ответа на их введение [18]. Однако в недавнем экспериментальном исследовании, в котором показана эффективность биоразлагаемых флуоресцентных наночастиц диоксида кремния при колоноскопии для выявления аденом толстой кишки, отмечается, что частицы являются биоразлагаемыми, хорошо переносятся и позволяют обнаружить аденомы размером до 0,5 мм2 [19]. Помимо этого, изучается применение наночастиц на основе полимера с инкапсулированным флуоресцентным ингибитором ЦОГ-2 – флуорококсибом для улучшения эффективности флуоресцентной эндоскопии [20].
Активное развитие эндоскопической диагностики, вероятно, приведет к значительному улучшению выявления КРР путем повсеместного применения оборудования высокой четкости и разрешения; сочетания колоноскопии с другими прорывными методиками за счет использования возможностей ИИ или 3D-визуализации.
Компьютерная томография-колонография
Компьютерная томография-колонография также рассматривается в качестве сопоставимой альтернативы оптической колоноскопии, в том числе для скрининга колоректального рака. Данный неинвазивный визуализирующий тест толстой кишки не требует тщательной подготовки и позволяет оценить внекишечные структуры. Компьютерная томографическая колонография также предлагается в качестве чувствительного и точного инструмента наблюдения за пациентами, перенесшими оперативное вмешательство по поводу КРР [21]. Помимо этого, было показано, что при обнаружении полипов диаметром ≥10 мм КТ-диагностика превосходит колоноскопию; а также отличается большей безопасностью [22].
Потенциальное клиническое применение КТ-колонографии в скрининговых программах ограничено из-за ее недостаточной эффективности при выявлении отдельных очагов размером менее 5 мм или плоских очагов, которые также имеют риск ма-лигнизации [23]. Отмечается, что чувствительность КТ-колонографии можно повысить путем диетической подготовки, применения слабительных препаратов и маркировки кишечного содержимого (прием водного контрастного препарата с йодом накануне исследования) [24]. Обследование рекомендуется дополнять применением контрастных веществ или эндоскопией, в том числе во избежание гипердиагностики колоректального рака, вызванной регистрацией внекишечных аномалий [22].
Данные об экономической эффективности скрининга посредством КТ-колонографии в научном дискурсе отличаются неоднородностью, т.к. исследования используют различные параметры оценки [25]. К примеру, КТ-колонография считается более рентабельной для скрининговых стратегий, предусматривающих более частые обследования; а колоноскопия была более экономически эффективной для проведения 1–2 скрининговых обследований [26]. J. Sha et al. отмечают, что КТ-колонография стоила дешевле, чем колоноскопия; а также пациенты психологически более склонны перенести КТ, чем эндоскопическую диагностику [22].
Новые возможности в леченииколоректального рака
На протяжении нескольких десятилетий традиционное лечение новообразований толстой кишки основывалось на хирургических вмешательствах, лучевой или химиотерапии. Новые подходы направлены на снижение рецидивов заболевания и смертности после лечения и включают таргетную терапию, иммунотерапию и достижения в области наномедицины. В качестве основного конкурента традиционных методов лечения выступает иммунотерапия (ИТ), которая нацелена на иммунные клетки, она повышает их способность выявлять и уничтожать опухоль; либо непосредственно на опухолевые клетки, которые подавляют иммунную систему. К примеру, ингибиторы контрольных точек иммунитета блокируют пути, которые используются клетками опухоли, чтобы избежать распознавания иммунной системой. Метод является эффективным при лечении КРР, который прогрессирует после предыдущих терапевтических подходов; ИТ часто используется в комбинации с химиотерапией и таргетной терапией [27].
Все большее распространение в клинической практике получает CAR-T-клеточная терапия, которая подразумевает генетическую модификацию иммунных клеток больного. Культивированные in vitro лимфоциты, полученные из опухоли, вводятся обратно пациенту с целью нацеливания и уничтожения злокачественных клеток [28]. Другой многообещающий метод – онколитическая виро-терапия (вирусное лечение). Применение вирусов позволяет использовать как врожденные, так и опухолеспецифические иммунные реакции для целенаправленного уничтожения опухоли. Метод также рассматривается для синергетического использования с цитокинами для усиления иммунотерапии при лечении КРР [29]. Для снижения частоты побочных эффектов системной химиотерапии разрабатываются платформы наноносителей для целенаправленной доставки препаратов. Наноносители стабильны в гипертермических условиях, в кислой среде, усиливают цитотоксический эффект препарата; а также способны длительно концентрироваться в органе-мишени [30].
Существующие препятствияв раннем выявлении КРР
Известно, что проведение скрининговых мероприятий по раннему выявлению колоректального рака сопровождается своевременной постановкой диагноза, что значительно экономит ресурсы здравоохранения. Затраты на проведение скрининговых исследований являются экономически оправданным мероприятием по сравнению с высокими затратами на диагностику и лечение запущенных случаев колоректального рака [31]. Несмотря на глобальную доступность скрининговых методик, страны с низким и средним уровнем развития, а также малообразованная часть населения развитых стран демонстрируют недостаточные показатели скрининга, соответственно, в этих группах наблюдается высокая частота рака толстой кишки [32].
Колоноскопия остается «золотым стандартом» обследования для выявления поражения толстой кишки. В России эндоскопические мероприятия по своевременной диагностике новообразований толстой кишки успешно реализуются в амбулаторных медицинских учреждениях как по системе ОМС, так и ДМС [31]. Определенно, качество обследования зависит как от опыта врача-эндоскописта, так и от оснащения эндоскопического подразделения. Отмечается, что эндоскопическими системами экспертного класса в стране оснащено лишь ограниченное количество учреждений; остальные проводят диагностическую оценку состояния толстой кишки с использованием эндоскопического оборудования «среднего» класса. Рутинное использование оборудования экспертного класса позволяет больше доверять результатам визуальной диагностики и существенно ограничить применение щипцовой биопсии [33]. Анализ отечественной литературы показывает, что скрининговые программы различаются технологией проведения и экономическими ресурсами. Нередко региональное здравоохранение пытается дополнять скрининговые программы проведением колоноскопии, при этом сдерживая нагрузку на эндоскопическую службу [34, 35]. Таким образом, успех стратегий по раннему выявлению КРР зависит не только от качества подобранных диагностических методик, но и от достаточной осведомленности населения в сочетании с адекватным ресурсным обеспечением [32].
В данном сообщении мы представляем результаты пятилетнего наблюдения и оценки состояния пациента с диагнозом: Карцинома in situ ректосигмоидного соединения толстой кишки.
Клинический случай
При видеоэндоскопии на расстоянии 28 см от анального сфинктера обнаружено полиповидное образование. При этом установлены морфологические признаки аденамотозного полипа толстой кишки с признаками очаговой интраэпителиальной неоплазии низкой степени. В плановом порядке в ноябре 2019 г. в условиях стационара выполнена эндоскопическая полипэктомия. Перед операцией пациент получил двухэтапную подготовку с применением слабительного и ветрогонного средств (Фортранс, Эспумизан). Просвет кишки равномерный, в просвете содержалось большое количество мутной жидкости с хлопьями; слизистая оболочка розовая, блестящая, с гладкой поверхностью и четким сосудистым рисунком. Складки по форме соответствовали отделам, обычной высоты и ширины, с нормальным расстоянием между ними; петли подвижны и смещаемы; кишка имела нормальный тонус. Полиповидное образование на ножке (диаметр головки до 1,5 см, длина ножки до 0,8 см, ширина ножки до 0,5 см) удалено с помощью электрохирургической системы, после предварительной инфильтрации полипа 5 мл физиологического раствора и накидывания поли-пэктомической петли на ножку. Ложе удаленного новообразования без особенностей, кровотечение отсутствовало. Операционный материал помещен в 10 % раствор нейтрального формалина и отправлен на патологоанатомическое исследование (ПГИ). Осложнений после эндоскопической полипэктомии не отмечено.
При микроскопическом исследовании операционного материала установлена морфологическая картина, соответствующая тубулярной аденоме толстой кишки, с признаками тяжелой дисплазии в единичных участках с трансформацией в высокодифференцированный рак in situ. Материал имел фрагменты тубулярной аденомы толстой кишки; железы различной величины и формы; ядра железистого эпителия умеренно полиморфны, крупные, гиперхромные, с конденсированным хроматином, с нарушенным ядерно-цитоплазматическим соотношением в пользу ядра, с нарушенной полярностью относительно базальной мембраны, в отдельных участках железы сливаются между собой с формированием криброзных структур. Образование резецировано в пределах здоровых тканей, инвазивного компонента не определяется, pTis ICD-0.
На основании полученных данных выставлен диагноз: Карцинома in situ ректосигмоидного соединения толстой кишки, TisN0М0 Стадия 0. Гистологический тип клеток – не плоскоклеточный. Пациент отказался от радикального лечения (резекция пораженного участка кишечника); выписан под наблюдение онколога и терапевта. Разработанный план наблюдения включал ежегодный прием онколога с оценкой состояния больного, физикальным обследованием; а также проведение фиброколоноскопии, УЗИ органов брюшной полости и периферических лимфатических узлов, рентгенографии органов грудной клетки, эзофагогастродуоденоскопии, клинического и биохимического анализов крови.
По результатам ежегодных консультаций – в течение 5 лет состояние пациента удовлетворительное. Антропометрические показатели в стабильных пределах – рост 176 см, вес – 79–81 кг (ИМТ – 25,5–26,1). Периферические лимфоузлы не увеличены; по данным инструментального и лабораторного исследования – без признаков онкологической патологии. Пациент продолжает вести активную трудовую деятельность.
Обсуждение
Представленный случай демонстрирует несоответствие результатов морфологического исследования биоптата, полученного при щипцовой биопсии, и операционного материала после эндоскопического удаления полипа. В некоторых клинических ситуациях малигнизация полипа очевидна (рис. 1); в других, как в приведенном клиническом случае, ключевой фигурой, определяющей дальнейшую тактику, является врач-морфолог.
Эндоскопия на протяжении длительного времени используется для проведения диагностических и лечебных манипуляций при новообразованиях толстой кишки. Эндоскопическое вмешательство позволяет принимать решение о тактике ведения больного, исходя из результатов морфологического исследования биопсийного материала или изучения удаленного образования [36]. При этом расхождение между результатами морфологической оценки при щипцовой биопсии и патогистологическом исследовании может быть значительным [37].
Ряд авторов отмечают, что в 28 из 535 удаленных новообразований путем эндоскопической полипэктомии при гистологическом исследовании выявлена малигнизация. При этом полипэктомию при диагностической колоноскопии проводили только при отсутствии визуальных признаков ма-лигнизации; а при наличии изъязвления с обиль-
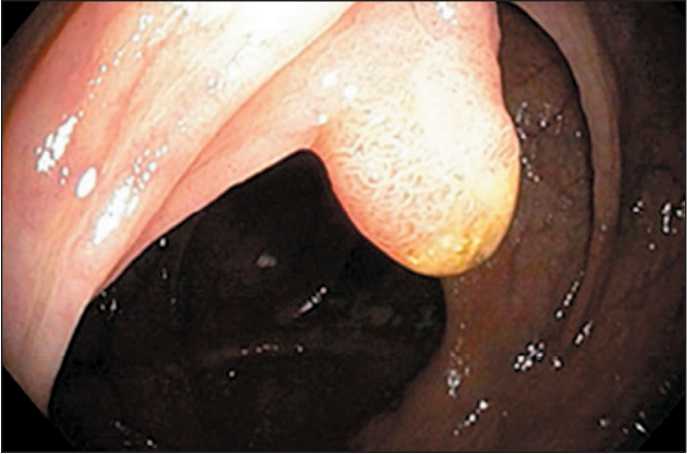
Рис. 1. Рак in situ в полипе толстой кишки. Примечание: рисунок выполнен авторами Fig. 1. Carcinoma in situ in a colon polyp. Note: created by the authors ным покрытием фибрином и некротическими массами, выраженной кровоточивости проводили щипцовую или петлевую биопсию для определения дальнейшей тактики, исходя из результатов гистологического заключения [38].
В другом исследовании [39] изучили информативность морфологического исследования биопсийного материала и удаленных колоректальных полипов. В ходе работы выполнялись предварительная прицельная биопсия из колоректальных полипов и последующая эндоскопическая полипэктомия. В 10,4 % случаев выявлены малигнизированные полипы; при этом из 494 полипов в 19 малигнизация установлена с помощью прицельной биопсии, а ПГИ после полипэктомии позволило выявить 52 случая малигнизации (чувствительность прицельной биопсии в диагностике малиг-низации – 36,5 %). Ранее другой коллектив заявил о необходимости пересмотра тактики рутинной биопсийной диагностики, особенно в случае заведомо неинвазивных образований толстой кишки. Заявление основано на крайне низкой чувствительности и негативной прогностической ценности метода в выявлении малигнизации полипов толстой кишки (16,6 %), а также в верификации зубчатых аденом. При анализе данных морфологического исследования 101 биоптата и операционного материала в 26 случаях малигнизация образования была распознана только после исследования удаленного образования [40].
В недавних рекомендациях по диагностике и лечению новообразований толстой кишки упоминается возможность не выполнять щипцовую биопсию новообразования толстой кишки размерами менее 20 мм при наличии признаков доброкачественности образования, установленных с помощью эндоскопической системы с функцией HD и цифрового/оптического контрастирования. В качестве дополнительного условия отмечаются соответствующий опыт врача в применении методик контрастирования и сопровождение эндоскопического обследования фото-/видеофик-сацией изображения. При выявлении признаков доброкачественности рекомендуется одноэтапное эндоскопическое удаление новообразования в условиях профильного регионального или федерального центра [37].
В целом, развитие эндоскопии с возможностью получения усиленного изображения несколько изменило подход к гистологической характеристике колоректальных полипов и прогнозированию глубины инвазии колоректального рака. Медицинские учреждения, располагающие современным эндоскопическим оборудованием, стали отказываться от иссечения или удаления образований при всех скрининговых колоноскопиях, которые ранее рассматривались в качестве предшественников колоректального рака. В качестве дополнительных преимуществ оптической дифференциации подтипов полипов отмечаются сокращение времени, которое затрачивается на биопсию, а также частота ошибочных диагнозов по результатам оценки при щипцовой биопсии [17]. Однако существует мнение, что 10 % ошибок при морфологической оценке биоптатов допускается по причине несоблюдения эталонного стандарта при взятии образцов и при обнаружении полипов в рутинной клинической практике, эндоскопическая оптическая диагностика и морфологическая оценка с помощью биопсии могут иметь одинаковую точность [17, 41].
Заключение
Разработка эффективных, высокочувствительных и высокоспецифичных подходов к диагностике раннего опухолевого поражения является единственно верной стратегией в снижении заболеваемости и смертности населения от КРР. Своевременная диагностика является основой для применения различного рода малоинвазивных вмешательств, способных эффективно разрешить клиническую задачу с сохранением приемлемого качества жизни пациента. Раннее выявление и лечение опухолей толстой кишки остается задачей специалистов первичного звена, а также региональных онкологических центров. В современных публикациях, направленных на изучение методик раннего выявления новообразований толстой кишки, лидирующая роль отводится новым эндоскопическим методам. В качестве наиболее перспективного подхода представляется точная оптическая диагностика, с возможностью информативного эндоскопического прогнозирования гистологии полипов в режиме реального времени, в том числе с высокой чувствительностью к выявлению новообразований малых размеров. Необходимо отметить, что большая часть исследований, направленных на разработку комплексных диагностических программ, опубликована зарубежными авторами и акцентирует внимание на достаточной точности прогнозирования морфологической структуры новообразования толстой кишки с помощью визуальной диагностики, в частности, посредством методик цифрового контрастирования. Учитывая, что кадровый, диагностический и терапевтический потенциал в различных регионах России значительно различается, отечественным исследователям необходимо формировать собственный опыт в проведении комплексных диагностических мероприятий, устранении экономических препятствий для эффективного выявления КРР; а также разрабатывать рациональные пути улучшения лечения новообразований толстой кишки, исходя из возможностей регионального здравоохранения.


