Радиочастотная денервация или консервативное лечение: что эффективнее для купирования боли при гонартрозе?
Автор: Абакиров М.Д., Абдрахманов Р.Р., Дамаж А.С., Ткешелашвили Т.Т., Егамов М.М., Карпович Н.И.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 2 (52), 2023 года.
Бесплатный доступ
Обоснование. Хроническая боль в коленном суставе при гонартрозе является важной клинической проблемой. Относительно новый метод радиочастотной денервации коленного сустава при гонартрозе пока исследован недостаточно.Цель исследования. Сравнение эффективности применения радиочастотной абляции геникулярных нервов и консервативного лечения пациентов с гонартрозом.Материалы и методы. Проспективное контролируемое исследование, включающее 65 пациентов с симптоматическим гонартрозом и болями в коленном суставе. У 31 пациента применяли радиочастотную денервацию (РЧД) геникулярных нервов в термическом режиме под контролем электронно-оптического преобразователя (группа РЧД); у 34 пациентов проводили комплексное амбулаторное консервативное лечение (группа КЛ). Сравнивали интенсивность боли по ВАШ, состояние коленного сустава по WOMAC, субъективное восприятие эффективности лечения, осложнения в сроки 1, 3, 6 месяцев.Результаты. Через 6 месяцев после лечения интенсивность боли была значимо меньше в группе РЧД, по сравнению с группой КЛ: 3 [2; 4] против 5 [5; 6] (p
Радиочастотная денервация, рчд, геникулярные нервы, гонартроз, остеоартроз коленного сустава
Короткий адрес: https://sciup.org/142238950
IDR: 142238950 | УДК: 617.3 | DOI: 10.17238/2226-2016-2023-2-7-15
Radiofrequency denervation or nonoperative treatment for osteoarthritic knee pain: what is more effective?
Background. Knee arthritis and associated chronic pain is a very common problem. Radiofrequency ablation (RFA) of genicular nerves in knee arthritis managament was introduced recently but rigorous studies are lacking.Objective. To compare the effi acy of RFA of genicular nerves and nonoperative treatment in patients with symptomatic knee arthritis.Methods. Th s prospective controlled study included 65 patients with symptomatic knee arthritis and associated knee pain. Thermal RFA of genicular nerves was used in 31 patients under the fluoroscopy guidance (RFA group); complex outpatient conservative treatment was performed in 34 patients (CT group). We compared Visual Analog Scale (VAS) score, functional state of knee joint according to WOMAC scale, Global Perceived Effect of treatment, complications throughout 6 months.Results. 6 months after treatment, the pain intensity was signifi antly lower in the RFA group compared to the CT group: 3 [2; 4] vs. 5 [5; 6], respectively (p
Текст научной статьи Радиочастотная денервация или консервативное лечение: что эффективнее для купирования боли при гонартрозе?
Боли в коленном суставе и нарушение ходьбы при гонартрозе являются ведущими инвалидизирующими симптомами этого хронического заболевания, которое приводит к ограничению физической активности и значительному снижению качества жизни [1]. Эндопротезирование коленного сустава – радикальный метод хирургического лечения, который показал высокую эффективность на поздних стадиях артроза, но сопряжен с риском осложнений, летальности и послеоперационной боли [2; 3]. Неоперативное лечение пациентов, которым тотальное эндопротезирование не выполнимо в связи с тяжелым соматическим статусом или не показано на ранних стадиях, ограничено лекарственной терапией, внутрисуставными инъекциями глюкокортикостероидов и гиалуроновой кислоты [1]. У некоторых лекарственных средств наблюдаются серьезные побочные реакции, а в части случаев терапия неэффективна [4].
Радиочастотная денервация (РЧД) суставов - перспективный метод интервенционного лечения боли, который является альтернативой консервативному и оперативному лечению. Изначально метод РЧД нашел применение при деструкции медиальных ветвей корешков спинно-мозговых нервов, иннервирующих фасетчатые суставы [5; 6], крестцово-подвздошные суставы [7; 8] и при дискогенных болях в вертебрологии [9]. Достигнут обезболивающий эффект после радиочастотной деструкции ветвей n.obturatorius и n.femoralis при артрозе тазобедренного сустава [10; 11]. При гонартрозе радиочастотное термическое воздействие направлено на верхний латеральный, верхний медиальный и нижний медиальный геникулярные нервы, которые являются проводниками восходящих болевых сигналов [4].
В иностранной литературе денервации коленного сустава при гонартрозе посвящены несколько исследований с небольшими группами пациентов и сроками наблюдения от 3 до 12 месяцев, их результаты, в основном, положительные [2; 6; 12; 13]. В России метод РЧД при артрозе коленного сустава исследован недостаточно. В отечественной научной библиотеке eLibrary при запросах «радиочастотная денервация» и «гонар-троз», «РЧД» и «коленный сустав», «радиочастотная абляция» и «артроз коленного сустава» и подобных выводится скудное число публикаций. В электронных базах диссертаций DisLib и Dissercat исследовательских работ по данной теме не найдено. Накопление клинического и научного опыта применения РЧД при гонартрозе, публикация на русском языке представляется важной задачей исследования.
Целью данного проспективного контролируемого исследования было сравнение результатов лечения пациентов с болями в коленном суставе на фоне гонартроза с применением радиочастотной денервации коленного сустава и консервативного лечения.
Материалы и методы
Протокол исследовательской работы прошел одобрение на заседании локального этического комитета медицинского ин- ститута Российского университета дружбы народов (РУДН). Все участники исследования были ознакомлены с сутью и содержанием планируемого исследования и подписали добровольное информированное согласие. Клиническую часть работы проводили на базах кафедры травматологии и ортопедии РУДН в Москве – ФГБУ ЦКБ РАН, отделение вертебрологии и алгологии, ГБУЗ ГКБ № 17 ДЗМ, отделение травматологии и ортопедии, а также ГБУЗ ГП № 220 и № 175 ДЗМ в период с 2018 по 2020 годы. В исследование включали участников, которые соответствовали следующим критериям: 1) с рентгенологически подтвержденным артрозом коленного сустава 2, 3, 4 стадии по Келлгрен-Лоуренсу; 2) с болями в коленном суставе на фоне гонартроза в течение более 3 месяцев; 3) возрастом старше 50 лет. Критериями исключения признавались: 1) острая боль в коленном суставе длительностью менее 3 месяцев; 2) системные воспалительные заболевания с вовлечением коленных суставов; 3) боли в коленном суставе на фоне травмы, неврологических заболеваний. Из исследования исключались пациенты с когнитивными и психическими нарушениями, декомпенсацией сопутствующих заболеваний, нарушением свертывающей системы крови. Не включались пациенты, если после артроскопических операций, внутрисуставных инъекций прошло менее 6 месяцев.
Дизайн исследования. В сравнительном контролируемом исследовании изучали результаты пункционного и неоперативного лечения пациентов с гонартрозом и хронической болью в коленном суставе. Применяли радиочастотную деструкцию геникуляр-ных нервов под флуороскопическим контролем в термическом режиме у 31 пациента (группа РЧД). В контрольной группе из 34 пациентов применяли комплексное консервативное лечение (КЛ). Изучали половозрастной состав пациентов, индекс массы тела, жалобы, анамнез заболевания и методы предшествующего лечения, оценивали функциональное состояние сустава и выраженность боли по визуальной аналоговой шкале (ВАШ). При оценке исходов лечения первичными конечными точками были: 1) среднее уменьшение интенсивности боли по ВАШ в срок 6 месяцев после лечения; 2) доля пациентов с уменьшением уровня боли ≥50% от изначального. Вторичными конечными точками были: динамика функционального состояния по шкале Western Ontario and McMaster Universities Index (WOMAC), удовлетворенность проведенным лечением по 7-балльной шкале Lykert (Таблица 1).
Контрольные визиты или телефонные опросы происходили через 1, 3, 6 месяцев после проведенного лечения. Регистрировали осложнения малоинвазивного лечения (инфекции, неврологические нарушения, гематомы) и побочные эффекты консервативного лечения (обострение боли, НПВС-ассоциированная гастропатия, подъем АД и др.).
Методы лечения пациентов
В группе РЧД проводили малоинвазивное оперативное лечение. Радиочастотную денервацию коленного сустава выполняли в асептических условиях операционной под контролем электрон- но-оптического преобразователя. 100-мм канюли с электродами вводили в области медиального и латерального надмыщелков бедренной кости и внутреннего мыщелка большеберцовой кости. Применяли радиочастотный генератор Cosman G4 (Boston Scientific, США). Проводили тестовую стимуляцию с напряжением 0,5V и частотой 50Hz – положительным ответом считали появление типичных болевых ощущений в коленном суставе. Отсутствие мышечных сокращений при моторной стимуляции (2,0V, 2 Hz) считали признаком безопасного расположения электродов и продолжали операцию, в противном случае переустанавливали канюли. Перед началом термической деструкции через канюли вводили 1,0 мл лидокаина 2%, денервацию выполняли в термическом режиме с температурой 80 градусов в течение 90 секунд.
Таблица 1
7-балльная шкала субъективного восприятия эффективности проведенного лечения (Global Perceived Effect)
|
Баллы |
Общее восприятие улучшения/ ухудшения |
% изменений |
|
7 |
Очень сильно улучшилось |
≥ 75% улучшения |
|
6 |
Сильно улучшилось |
≥ 50% улучшения |
|
5 |
Минимальное улучшение |
≥25% улучшения |
|
4 |
Без изменений, не лучше и не хуже |
0% улучшения или ухудшения |
|
3 |
Минимальное ухудшение |
≥25% ухудшения |
|
2 |
Сильно ухудшилось |
≥50% ухудшения |
|
1 |
Очень сильно ухудшилось |
≥75% ухудшения |
Пациентам контрольной группы проводили курс комплексного амбулаторного консервативного лечения, которое включало медикаментозную терапию, физиотерапию, лечебную физкультуру. Назначали курс нестероидных противовоспалительных препаратов (Эторикоксиб, Целекоксиб, Ибупрофен, Мелокси-кам и т.п.) в течение 10-14 дней с учетом противопоказаний и сопутствующих заболеваний. Среди хондропротекторов применяли препараты глюкозамин сульфата не менее 1500 мг в сутки (Дона, Терафлекс, Артра) на срок 3 месяца. Пациенты проходили курсы магнитотерапии, фонофореза с гидрокортизоном, вольтареном в течение 3 недель. Под контролем инструктора ЛФК пациенты с гонартрозом проходили групповые и индивидуальные занятия гимнастикой, направленной на укрепление мышц-стабилизаторов коленного сустава.
Статистический анализ. Анализ данных провели с помощью статистического приложения Jamovi. Оценку характера распределения производили с помощью W-теста Шапиро-Уилка: при значении p>0,05 считали, что переменные распределены нормально. Для количественных переменных с нормальным распределением описательная статистика представлена в виде средней и среднеквадратичного отклонения (m±SD). Межгрупповые различия оценивали по t-критерию Стьюдента для независимых выборок и по парному t-критерию для зависимых. При распределении, отличном от нормального, переменные представлены в виде медианы и межквартильного размаха Мe [P25; P75]. Для оценки различий использовали непараметрический U-критерий Манна-Уитни для независимых выборок. В связанных выборках, тесты по типу «до-после» проводили при помощи критерия Уилкоксона. Номинальные переменные в группах сравнивали при помощи теста Хи-квадрат или точного критерия Фишера согласно размеру выборки. При уровне значимости p<0,05 различия признавались статистически достоверными.
Результаты
Всего привлечено к исследованию 78 пациентов с гонар-трозом, которые распределены в 2 группы наблюдения. В 1 группе выполнена термическая радиочастотная деструкция геникулярных нервов (группа РЧД), во 2 группе включенным пациентам проводилось комплексное консервативное лечение (группа КЛ). У 13 пациентов выявлены критерии исключения: 6 пациентам в предыдущие 6 месяцев выполнялись внутрисуставные инъекции, у 4 пациентов произошла декомпенсация соматических заболеваний в первые полгода после начала исследования (сахарный диабет, ишемическая болезнь сердца, гипертоническая болезнь), 3 пациента отказались от контрольных наблюдений. Окончательный анализ данных и межгрупповые сравнения провели у 65 пациентов в двух группах (Таблица 2).
Клинические данные пациентов
Таблица 2
|
Группа РЧД (n=31) |
Группа КЛ (n=34) |
P |
|
|
Возраст, лет |
71,8±13,1 |
69,3±8,42 |
0,362* |
|
Мужчины, n (%) Женщины, n (%) |
13 (41,9) 18 (58,1) |
14 (41,2) 20 (58,8) |
0,951** |
|
Интенсивность боли по ВАШ, баллы |
7 [6; 8] |
7 [6; 8] |
0,524*** |
|
ИМТ, кг/м2 |
29,4±3,6 |
28,9±3,8 |
0,653* |
|
Длительность боли, мес |
24 [18; 42] |
24 [18; 36] |
0,785*** |
|
Степень гонартроза, n (%) 2 3 4 |
10 (32,3) 16 (51,6) 5 (16,1) |
13 (38,2) 16 (47,1) 5 (14,7) |
0,458** |
|
Сторона поражения, n (%) Левая Правая |
12 (38,7) 19 (61,3) |
18 (52,9) 16 (47,1) |
0,250** |
*t-тест Стьюдента; **Хи-квадрат; ***U-тест Манна-Уитни
Большинство пациентов – женщины, продолжительность боли в коленном суставе у пациентов составила от 8 до 72 месяцев, у большей части пациентов наблюдалась 3 стадия гонартроза. Межгрупповых различий по демографическим данным, интенсивности боли, индексу массы тела, длительности заболевания, степени артроза не выявлено.
Среди консервативных методов лечения в период, предшествующий проводимому исследованию, 80% пациентов применяли курсы НПВП, около 45% занимались лечебной физкультурой, более 52% проходили физиотерапию. Среди внутрисуставных вмешательств в анамнезе - инъекции глюкокортикостероидов и гиалуроновой кислоты у 19 (29,2%) пациентов, артроскопической санации коленного сустава – у 13 (20,0%). Выявлены не значимые межгрупповые различия в частоте использования различных методов лечения гонартроза в анамнезе (Таблица 3).
Таблица 3
Предшествующее лечение пациентов с гонартрозом
|
Группа РЧД (n=31) |
Группа КЛ (n=34) |
P* |
|
|
Физиотерапия, n (%) |
16 (51,6) |
18 (52,9) |
0,915 |
|
Лечебная физкультура, n (%) |
14 (45,2) |
15 (44,1) |
0,933 |
|
Нестероидные противовоспалительные препараты, n (%) |
25 (80,6) |
27 (79,4) |
0,901 |
|
Внутрисуставные инъекции, n (%) |
9 (29,0) |
10 (29,4) |
0,973 |
|
Артроскопическая санация, n (%) |
6 (19,4) |
7 (20,6) |
0,901 |
*Хи-квадрат
Результаты применения РЧД или консервативного лечения оценивали и сравнивали по интенсивности боли, доле пациентов, успешно ответивших на лечение, динамике функционального статуса, удовлетворенности от проведенного лечения. Интенсивность боли по визуальной аналоговой шкале (ВАШ) оценивали до операции, и в контрольные сроки через 1, 3, 6 месяцев после лечения (Рисунок 1).
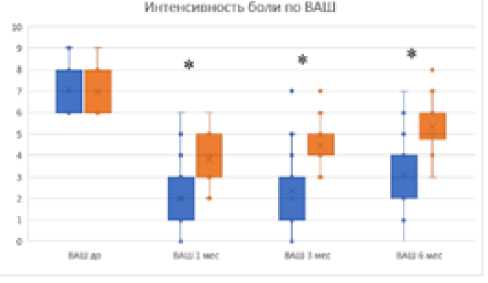
* для ВАШ 1, ВАШ 3, ВАШ 6
*-различия значимы, p<0,01 по U-критерию Манна-Уитни ■ - группа РЧД (n=31); ■ - группа КЛ (n=34)
Рис. 1. Интенсивность боли по ВАШ до лечения, через 1, 3, 6 месяцев после лечения
Медиана изначальной интенсивности боли по ВАШ составила 7 баллов (от 5 до 9 баллов), без значимых различий между испытуемыми в обеих группах. Назначенное лечение было эффективно: на всех этапах наблюдения в обеих группах отмечено значимое уменьшение интенсивности боли по сравнению с базовым уровнем (p<0,001, W-критерий Уилкоксона). Через 1, 3, 6 месяцев интенсивность боли у пациентов снизилась в среднем на 4,23, 3,72 и 2,85 баллов (Таблица 4).
Таблица 4
Интенсивность боли по ВАШ в обеих группах
|
Группа РЧД (n=31) |
Группа КЛ (n=34) |
||
|
ВАШ |
Ме [Q25; Q75] |
Me [Q25; Q75] |
P* |
|
До лечения |
7 [6; 8] |
7 [6; 8] |
0,524 |
|
1 месяц после лечения |
2 [1; 3] |
4 [3; 4,75] |
0,001 |
|
3 месяца после лечения |
2 [1; 3] |
4 [4; 5] |
0,001 |
|
6 месяцев после лечения |
3 [2; 4] |
5 [5; 6] |
0,001 |
|
Р** |
0,001** |
0,001** |
Ме [Q25; Q75] – медиана и межквартильный размах
Р* - межгрупповые различия для независимых выборок по U-критерию Манна-Уитни
Р** - различия измерений для зависимых выборок «до лечения-6 месяцев после лечения» по методу Уилкоксона
Межгрупповое сравнение интенсивности боли и степени снижения интенсивности боли говорит о лучших результатах в группе РЧД. Интенсивность боли была значимо меньше в группе РЧД, по сравнению с группой КЛ: через 1 месяц – 2 [1; 3] против 4 [3; 4,75] (p<0,001); через 3 месяца – 2 [1; 3] против 4 [4; 5] (p<0,001); через 6 месяцев – 3 [2; 4] против 5 [5; 6] (p<0,001). Среднее снижение уровня боли относительно изначального уровня было больше в группе РЧД, по сравнению с группой КЛ на всех этапах наблюдения: через 1 месяц -5,06±1,57 против -3,47±1,24 (p<0,001); через 3 месяца -4,71±1,66 против -2,82±1,17 (p<0,001); через 6 месяцев -3,97±1,87 против -1,82±1,40 (p<0,001)
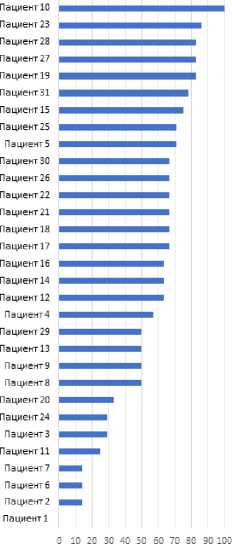
У 74,2% пациентов (23/31) из группы РЧД и у 11,8% (4/34) пациентов из группы КЛ достигнута первичная конечная точка исследования – купирование интенсивности боли на -50% и более от изначального уровня к 6 месяцу наблюдения (p<0,001, Хи-квадрат=26,0) (Рисунок 2). 8 из 31 (25,8%) и 30 из 34 (82,2%) пациентов из соответствующих групп не ответили на лечение (уровень боли уменьшился менее, чем наполовину, или сохранился прежним). В группе РЧД не наблюдалось пациентов, которые испытывали усиление боли через 6 месяцев после проведенного лечения, в то время как в группе КЛ таких пациентов было двое – 5,9% (p=0,170, Хи-квадрат=1,88).
?ЧДп=31
Консервативное лечение п=34
Пациент 63 ^^^^^—^^^^^—
Пациент 53 ^^^^^^^^^^^^"
Пациент47 ^^^^^^^^^^^
Пациент 43 ^^^^^^^^^^^^"
Пациент 62 ^^^^^^^^^^"
П а цие нт 5 7 ^^^^—^^^^—
Пациент 45 ^^^^^^^^—
Пациент 34 ^^^^—^^^^—
П а ци е нт 48 ^^^^^^^^^
П а ци е нт 45 ^^^—^^^—
Пациент41 | |
Пациент 61 ^^^^^^^™
Пациент 60 ^^^^^^^
П а ци е нт 54 ^^^^^^^™
Пациент 52 ^^^^^^^—
П а ци е нт 49 ^^—^-^
Пациент 33 ^^^^^^"
Пациент 42 ^^^^^^"
Пациент 39 ^^^^^^
Пациент 37 ^^^^^^"
Пациент 65 ^^^^^—
П а ци е нт 44 ^^^^—
Пациент 64 ^^^™
Пациент 50 ^^~
Пациент 55 ^^™
Пациент 38 ^^*
Пациент 40 ^^™
Пациент 58
Пациент 55
Пациент51
Пациент 35
Пациент 35
Пациеме*^
Пациент 83 ,
-30 -20 -10 0 10 20 30 40 50 60 70 80 90 100
■ - группа РЧД (n=31); ■ - группа КЛ (n=34)
Рис. 2. Степень изменения интенсивности боли в коленном суставе через 6 месяцев после лечения выражена в % от изначального уровня.
Уровень функциональной активности по шкале WOMAC перед началом исследования в обеих группах был сравнимым (Таблица 5). Отмечалось статистически значимое снижение средних показателей относительно изначального уровня в сроки 1, 3 и 6 месяцев в обеих группах наблюдения (p<0,001, по W критерию Уилкоксона). Значение по шкале WOMAC было значимо выше в группе КЛ в сроки 1, 3, 6 месяцев после проведенного лечения. Наблюдалась тенденция постепенного ухудшения функционального статуса коленного сустава в течение 6 месяцев после проведенного лечения и увеличения значения по шкале WOMAC. Лечебный эффект сохранился в обеих группах – различия по шкале WOMAC были значимыми при сравнении до-после через 6 месяцев после лечения, но более выраженными в группе РЧД.
По 7-балльной шкале Ликерта оценивали субъективное восприятие улучшения/ухудшения после проведенного лечения (Global Perceived Effect – общее восприятие эффективности лечения). Пациенты на контрольных осмотрах через 1, 3, 6 месяцев после окончания лечения отвечали на вопрос «Насколько изменилось ваше состояние после проведенного лечения?» - отмечали один из пунктов шкалы Ликерт. Через 1 месяц после лечения результаты опроса оказались сравнимыми в группах РЧД и КЛ: медианы и межквартильный размах составили 6 [5; 7] и 5 [5; 6] соответственно (p=0,135 по Манну-Уитни). Через 3 и 6 месяцев результаты опроса оказались значимо лучше в группе РЧД (p<0,001). Через 6 месяцев после выполнения РЧД 21/31 (67,7%) пациентов отмечали улучшение состояния – минимальное (5 баллов) или очень выраженное (7 баллов). В группе КЛ улучшение от 5 до 6 баллов отметили только 8 из 34 пациентов (23,5%). Различия значимые при сравнении по методу таблиц сопряженности, Хи-квадрат = 12,8, p<0,001. (рисунок 3).
Таблица 5
Динамика изменения функционального статуса коленного сустава по WOMAC
|
Группа РЧД (n=31) |
Группа КЛ (n=34) |
Межгрупповые различия, Р* |
|
|
WOMAC |
m ± SD |
m ± SD |
|
|
До лечения |
52,8±5,9 |
51,2±5,9 |
0,262 |
|
1 месяц после лечения |
30,2±4,7 |
36,9±5,3 |
<0,001 |
|
3 месяца после лечения |
31,0±5,3 |
39,7±5,9 |
<0,001 |
|
6 месяцев после лечения |
32,2±5,8 |
45,0±7,8 |
<0,001 |
|
P**(сравнение «до-6 месяцев после») |
<0,001 |
<0,001 |
Р* - межгрупповые различия для независимых выборок по парному t-критерию Стьюдента
Р** - различия измерений для зависимых выборок «до лечения-6 месяцев после лечения» по методу Уилкоксона m ± SD – средняя ± стандартное отклонение
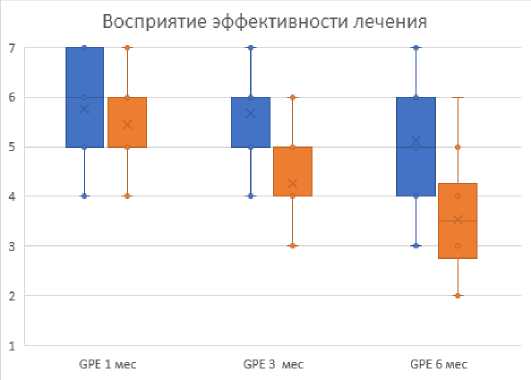
* для GPE 3 мес и GPE 6 мес
*-различия значимы, p<0.001 по критерию Манна-Уитни ■ - группа РЧД (n=31); - группа КЛ (n=34)
Рисунок 3 – GPE – Global Perceived Effect – общее восприятие эффективности лечения по шкале Ликерт от 1 до 7 баллов.
Не выявлено нежелательных явлений, связанных с проведенной РЧД: гипестезии, парестезий, парезов мышц, гематом, инфекционных осложнений в области вмешательства. Часть пациентов указывали на незначительные боли в точках введения электрода в области надкостницы, которые усиливались при пальпации. Это были временные жалобы, которые не требовали дополнительной анальгетической терапии. Схема приема НПВП и парацетамола, которые пациенты получали до начала лечения, не менялась, протокол исследования не препятствовал приему обезболивающих препаратов в послеоперационном периоде. Критерием исключения из исследования были внутрисуставные инъекции в срок менее 6 месяцев после начала лечения.
Обсуждение
Исследование показало, что радиочастотная денервация геникулярных нервов может превосходить по эффективности стандартное консервативное лечение при гонартрозе. В работе показана противоболевая эффективность обоих методов лечения, однако результаты значимо выше в группе РЧД, чем в группе КЛ: интенсивность боли по шкале ВАШ через 6 месяцев после начала лечения 3 [2; 4] против 5 [5; 6] баллов соответственно (p<0,001). Среднее уменьшение интенсивности боли в группе РЧД и КЛ составило через 6 месяцев -3,97±1,87 баллов против -1,82±1,40 баллов соответственно (p<0,001).
Статистически значимое долговременное снижение уровня боли при гонартрозе в течение 6 месяцев после радиочастотной денервации показано в работе Iannaccone [14]. Менее продолжительный срок обезболивания после манипуляции – 3 месяца –достигнут в исследовании Kim, в котором авторы сравнивали эффективность УЗИ и рентгеновской навигации [15]. Применение РЧД в вертебрологии показало значимое уменьшение интенсивности боли при симптоматическом спондилоартрозе у 67 из 72 (93,1%) пациентов [5], при дисфункции крестцовоподвздошных суставов – у 46% [7]. Радиочастотная денервация ветвей бедренного и запирательного нервов эффективна при хронической суставной боли на фоне коксартроза [10; 16]. Достигнуто значимое долговременное обезболивание и улучшение функционального состояния тазобедренного сустава по шкале Harris при артрозе 1, 2, 3 степени в исследовании 121 пациента [11].
Стойкое снижение интенсивности боли ≥50% от базисного уровня через 6 месяцев после проведенного лечения было одной из конечных точек исследования и признавалось положительным ответом на лечение. В исследовании доля пациентов, ответивших на курс лечения, в группах РЧД и КЛ составила 74,2% и 11,8% соответственно (p<0,001, Хи-квадрат=26,0). В протоколе исследования не исключалось применение анальгетиков, НПВС или физиотерапии в первые 6 месяцев после РЧД или первичного курса консервативного лечения, из исследования исключались пациенты, которым выполнялись внутрисуставные инъекции в пределах этого срока. Возможно, на положительный исход лечения в основной группе могли оказать влияние дополнительные методы консервативной терапии больных гонартрозом.
В рандомизированном контролируемом исследовании Choi, посвященном радиочастотной абляции при гонартрозе, доля пациентов, ответивших на лечение через 3 месяца после процедуры, составила 59% [12]. Доля пациентов с купированием боли наполовину и более от исходного уровня через 3 месяца после РЧД в разных работах колеблется от 40% [15] до 52% [14]. В исследовании Davis применение РЧД с охлаждаемыми электродами позволило уменьшить интенсивность боли на 50% и больше по шкале ВАШ у 74% пациентов через 6 месяцев [17]. Santanа показали уменьшение интенсивности болевого синдрома ≥50% через 6 месяцев у 64% пациентов, а через 12 месяцев – у 32% [2].
Для деструкции геникулярных нервов мы применяли термическую абляцию (80 °C, 90 секунд). Сравнить наши результаты с данными исследований других авторов не всегда возможно: в исследованиях применяются различные режимы деструкции, нагревания электродов, длительности воздействия. В большинстве исследований применялась термическая денервация: в работе El-Hakeim [6] электроды нагревались до 80 °C в течение 270 секунд (3 раза по 90), в исследовании Iannaccone [14] – до 60°C и 120 секунд, в статье Choi [12] – до 70°C и 90 секунд. В рандомизированном контролируемом исследовании [17] использовали охлаждаемые электроды (до 60°C, 150 секунд). Активно применяется процедура пульсовой РЧД, во время которой за счет коротких циклов нагревания температура электрода достигает 42°C в течение 120 секунд [3; 18]. Пульсовой режим радиочастотной денервации в меньшей степени повреждает окружающие мягкие ткани, при этом сильнее воздействует на чувствительные волокна, чем на двигательные, что снижает частоту нейропатии, артропатии Шарко и других осложнений [19; 20]. Сравнение эффективности пульсовой или термической РЧД, или РЧД с охлаждаемыми электродами не было целью данного исследования, однако в систематическом обзоре Gupta показана противоболевая эффективность обеих методик РЧД, которая достигает 1 года при минимальных осложнениях [21].
В работе показана значимая положительная динамика в функциональном статусе пациентов по сравнению с изначальным уровнем в обеих группах. Через 6 месяцев после проведенного лечения показатели по шкале WOMAC в группе РЧД и КЛ составили 32,2±5,8 и 45,0±7,8 соответственно (р<0,001). Таким образом, применение РЧД было ассоциировано c улучшением состояния коленного сустава согласно субшкалам опросника WOMAC (боль, скованность, физическая функция). В контролируемом исследовании El-Hakeim изучали результаты лечения 60 пациентов с остеоартрозом в двух группах: РЧД и неоперативное лечение [6]. Авторам удалось достичь значимого снижения интенсивности боли по ВАШ через 6 месяцев после начала исследования в обеих группах пациентов, но в группе РЧД в большей степени, чем в группе консервативного лечения (соответственно 3.13±0.3 против 5,73±0.26, p<0,001). Также сумма баллов по опроснику WOMAC была значимо ниже в группе РЧД через 6 месяцев: 33.13±4.1 против 43.5±2, соответственно, p<0,001 [6]. Подобное уменьшение интенсивности боли и улучшение функции коленного сустава по шкале WOMAC выявлено в работе Kim [15] через 3 месяца после выполнения РЧД и в работе Iannaccone [14] – через 6 месяцев наблюдения. В исследовании Davis состояние коленного сустава изучали по данным опросника Oxford Knee Score (OKS) в группах пациентов, которым выполняли либо РЧД с охлаждаемыми электродами, либо внутривенные инъекции кортикостероидов [17]. 95% доверительный интервал различий в сумме баллов по шкале OKS через 6 месяцев наблюдения составил 10,28 – 16,4 баллов (р<0,0001) в пользу РЧД.
В нашей работе не наблюдалось нежелательных явлений, ассоциированных с выполнением РЧД (инфекционных или неврологических). Подобные результаты получены в других работах, которые также показывают отсутствие осложнений [6; 12; 15], отсутствие серьезных осложнений [17], единичный случай кратковременной гипестезии [14]. В систематическом обзоре, посвященном различным модальностям радиочастотной денервации, Gupta и соавт. указывают на дефицит информации о осложнениях РЧД [21]. В 4 из 6 работах по термической денервации анализ осложнений не проводился, в 1 статье осложнения отсутствовали, а в исследовании Ikeuchi (n=35 пациентов) в 67% случаев отмечались жалобы на кровоподтеки в месте установки канюли, а в 78% – на длительную гипестезию [13; 21]. В 4 работах, посвященных РЧД с охлаждаемыми электродами, и в 6 статьях, посвященных пульсовой РЧД, осложнения не выявлены [21]. Для более тщательного изучения безопасности процедуры в перспективе планируется более скрупулезный учет осложнений, с разделением их на малые и серьезные нежелательные явления, в соответствии с методологией Good Clinical Practice.
Отсутствие стандартизации консервативного лечения несколько ограничивает воспроизводимость проведенного исследования: всем пациентам в группе КЛ проводилось комплексное амбулаторное лечение без выделения в подгруппы по применяемым НПВС, физиотерапевтическим процедурам, видам ЛФК. С одной стороны, это отражает практический подход к консервативному лечению пациентов с гонартрозом, принятый в различных лечебных учреждениях и описанный в рекомендациях. С другой стороны, это усложняет прямое сравнение методов: необходимость выделения подгрупп в зависимости от вида консервативного лечения приводит к многократному увеличению числа подгрупп, сокращению числа испытуемых в подгруппах и усложнению статистического анализа. Для более тщательного и показательного сравнения отдельных методов возможно проведение нескольких контролируемых исследований: для сравнения эффективности РЧД с различ- ными консервативными методами лечения, с включением и внутрисуставных инъекций.
Также ограничением исследования является применение консервативных методов лечения в группе РЧД в послеоперационный период, что могло способствовать лучшим результатам в группе. Планируется применение более строгого протокола исследования в будущем.
Заключение
Проспективное контролируемое исследование показало, что радиочастотная термическая деструкция геникулярных нервов под флуороскопическим контролем, с температурой электродов 80°C в течение 90 секунд, у пациентов с симптоматическим гонартрозом является более эффективным методом купирования боли в коленном суставе и улучшения его функции, чем консервативное лечение.
Список литературы Радиочастотная денервация или консервативное лечение: что эффективнее для купирования боли при гонартрозе?
- Hunter C, Davis T, Loudermilk E, Kapural L, DePalma M. Cooled Radiofrequency Ablation Treatment of the Genicular Nerves in the Treatment of Osteoarthritic Knee Pain: 18- and 24-Month Results // Pain Pract. 2020 Mar; 20(3): 238-246. DOI: 10.1111/papr.12844.
- Santana Pineda MM, Vanlinthout LE, Moreno Martín A et al. Analgesic effect and functional improvement caused by radiofrequency treatment of genicular nerves in patients with advanced osteoarthritis of the knee until 1 year following treatment // Reg Anesth Pain Med. 2017; 42: 62-68. DOI: 10.1097/AAP.0000000000000510
- Erdem Y, Sir E. The Efficacy of Ultrasound-Guided Pulsed Radiofrequency of Genicular Nerves in the Treatment of Chronic Knee Pain Due to Severe Degenerative Disease or Previous Total Knee Arthroplasty // Med Sci Monit. 2019; 25: 1857-1863. DOI: 10.12659/MSM.915359
- Conger A, Gililland J, Anderson L et al. Genicular Nerve Radiofrequency Ablation for the Treatment of Painful Knee Osteoarthritis: Current Evidence and Future Directions // Pain Medicine. 2021; 22 (Supp 1): 20-23. DOI: 10.1093/pm/pnab129
- Городнина А. В., Иваненко А. В., Орлов А. Ю. и др. Пункционные малоинвазивные методы при лечении хронической боли в спине // Российский нейрохирургический журнал им. профессора А.Л. Поленова. 2022. T.14, №2. С. 56-59. [Gorodnina A.V., Ivanenko A.V., Orlov A.Yu. et al. Puncture minimally invasive methods in the treatment of chronic back pain // Russian neurosurgical journal named after prof.A.L.Polenov. 2022. V.14, №2: 56-59. (in Russian)]
- El-Hakeim EH, Elawamy A, Kamel EZ et al. Fluoroscopic Guided Radiofrequency of Genicular Nerves for Pain Alleviation in Chronic Knee Osteoarthritis: A Single-Blind Randomized Controlled Trial // Pain Physician. 2018. 21: 169-177. PMID: 29565947
- Кавелина А.В., Исайкин А.И., Иванова М.А. Лечение неспецифической люмбалгии, обусловленной дисфункцией крестцово-подвздошного сочленения, методами интервенционной медицины // Неврология, нейропсихиатрия, психосоматика. 2018. Т.10, № 2. С. 33-37. [Kavelina A.V., Isajkin A.I., Ivanova M.A. Interventional medicine techniques in the treatment of nonspecific low back pain caused by sacroiliac joint dysfunction // Neurology, neuropsychiatry, psychosomatics. 2018. 10 (2): 33-37. (in Russian)] DOI: 10.14412/2074-2711-2018-2-33-37
- Sam J, Pastrak M, Duda L et al. Clinical Radiofrequency Ablation Outcomes of Combined Sensory Nerve Branch and Dorsal Entry Root Zone Complex Lesions for Sacroiliac Joint Complex Pain // Adv Ther. 2022. 39(8):3539-3546. DOI: 10.1007/s12325-022-02183-5
- Марцынишина К. Ю., Булыщенко Г. Г., Гайворонский А. И. и др. Пункционная радиочастотная абляция в лечении вертеброгенных болевых синдромов // Вестник Российской Военно-медицинской академии. 2019. № 4(68). С. 22-27. [Marcynishina K. Yu., Bulyshchenko G. G., Gajvoronskij A. I. et al. Puncture radiofrequency ablation for treatment of vertebral pain syndrome // Bulletin of the Russian Military Medical Academy. 2019. 4(68): 22-27. (in Russian)]
- Загородний Н.В., Кузьмин В.И., Горохов М.А. и др. Мониторинг боли в оценке эффективности лечения пациентов с коксартрозом методом радиочастотной денервации // Кафедра травматологии и ортопедии. 2018. №2 (32). С.20-24. [Zagorodnij N.V., Kuz’min V.I., Gorohov M.A. et al. Pain monitoring in patients with hip osteoarthrosis for assessment of radiofrequency denervation effectiveness // Department of traumatology and orthopedics. 2018. 2(32): 20-24 (in Russian)] DOI: 10.17238/issn2226-2016.2018.2.20-24
- Горохов М.А., Загородний Н.В., Черкашов А.М. и др. Биомеханика ходьбы до и после до и после радиочастотной денервации при дегенеративных заболеваниях тазобедренного сустава // Кафедра травматологии и ортопедии. 2019. №2(36). C. 37-41. [Gorohov M.A., Zagorodnij N.V., Cherkashov A.M. et al. Walking biomechanics before and after radiofrequency denervation during degenerative diseases of the hip joint // Department of traumatology and orthopedics. 2019. 2(36):37-41 (in Russian)] DOI: 10.17238/issn2226-2016.2019.2.37-41
- Choi WJ, Hwang SJ, Song JG et al. Radiofrequency treatment relieves chronic knee osteoarthritis pain: A double-blind randomized controlled trial // PAIN. 2011. 152: 481-487. DOI: 10.1016/j.pain.2010.09.029.
- Ikeuchi M, Ushida T, Izumi M, Tani T. Percutaneous radiofrequency treatment for refractory anteromedial pain of osteoarthritic knees // Pain Med. 2011. 12:546-551. DOI: 10.1111/j.1526-4637.2011.01086.x.
- Iannaccone F, Dixon S, Kaufman A.A Review of Long-Term Pain Relief after Genicular Nerve Radiofrequency Ablation in Chronic Knee Osteoarthritis // Pain Physician. 2017. 20: 437-444. PMID: 28339444
- Kim D-H, Lee M-S, Lee S et al. A Prospective Randomized Comparison of the Efficacy of Ultrasound- vs Fluoroscopy Guided Genicular Nerve Block for Chronic Knee Osteoarthritis // Pain Physician. 2019. 22: 139-146. PMID: 30921977
- Назаренко Г.И., Черкашов А. М., Кузьмин В.И. и др. Исследование эффективности радиочастотной денервации для купирования боли при дегенеративных заболеваниях тазобедренного сустава // Травматология и ортопедия России. 2014. № 2(72). С. 30-36. [Nazarenko G.I., Cherkashov A. M., Kuz’min V.I. et al. Effectiveness of radiofrequency denervation for pain relief in hip degenerative diseases. Traumatology and orthopedics of Russia. 2014. 2(72): 30-36. (in Russian)]
- Davis T, Loudermilk E, DePalma M et al. Prospective, Multicenter, Randomized, Crossover Clinical Trial Comparing the Safety and Effectiveness of Cooled Radiofrequency Ablation With Corticosteroid Injection in the Management of Knee Pain From Osteoarthritis // Reg Anesth Pain Med. 2018. 43(1): 84-91. DOI: 10.1097/AAP.0000000000000690.
- Kesikburun S, Yaşar E, Uran A et al. Ultrasound-Guided Genicular Nerve Pulsed Radiofrequency Treatment For Painful Knee Osteoarthritis: A Preliminary Report // Pain Physician. 2016. 19(5): 751-759. PMID: 27389118
- Abd-Elsayed A, Anis A, Kaye AD. Radio frequency ablation and pulsed radiofrequency for treating peripheral neuralgias // Curr Pain Headache Rep. 2018. 22(1): 5. DOI: 10.1007/s11916-018-0657-9
- Karaman H, Tüfek A, Kavak GÖ et al. Intra-articularly applied pulsed radiofrequency can reduce chronic knee pain in patients with osteoarthritis // J Chin Med Assoc. 2011. 74 (8): 336-340. DOI: 10.1016/j.jcma.2011.06.004.
- Gupta A, Huettner DP, Dukewich M. Effectiveness Review of Cooled Versus Pulsed Radiofrequency Ablation // Pain Physician. 2017. 20(3): 155-171. PMID: 28339430


