Радиомодифицирующие свойства бутилгидрокситолуола на примере Drosophila melanogaster
Автор: Е.А. Юшкова
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Статья в выпуске: 7 (83), 2025 года.
Бесплатный доступ
В экспериментах на Drosophila melanogaster проведена оценка радиомодифицирующего действия бутилгидрокситолуола (БГТ) путем исследования уровня повреждений ДНК и выживаемости у линии дикого типа Canton-S и мутантов по sod-генам. Установлено, что введение в диету дрозофил БГТ может вызвать снижение чувствительности к хроническому γ-излучению разной интенсивности (0,42 и 40,3 мГр/ч). У особей с нормальным функционированием генов (Canton-S), развивающихся в условиях хронического облучения, БГТ в концентрациях выше 1 мкМ благоприятно влияет на цитогенетический показатель (снижая его уровень при мощностях дозы 0,42 и 40,3 мГр/ч) и продолжительность жизни (увеличивая ее параметры при мощности дозы 0,42 мГр/ч). Обнаружено специфическое влияние БГТ на генотипы с низкой активностью цитоплазматической (sod[n1]/+) и митохондриальной (sod[delta02]/+) супероксиддисмутазы. По показателям “повреждения ДНК” и “выживаемость” наиболее выраженный радиопротекторный эффект БГТ был отмечен у животных линии sod[n1]/+. Этот эффект зафиксирован при концентрациях вещества, превышающих 10 мкМ, и всех мощностях облучения. У особей линии sod[delta02]/+ противолучевое действие БГТ выявлено в концентрациях 10-20 мкМ (на уровень повреждений ДНК) и 100 мкМ (на продолжительность жизни). Комбинация БГТ и хронического облучения имеет преимущественно антагонистический (у всех генотипов), реже синергический/аддитивный (у sod-мутантов) характер. Данный препарат в зависимости от концентрации способен уменьшать повреждения ДНК и увеличивать продолжительность жизни у особей определенного генотипа, что указывает на его способность замедлять процессы старения. Таким образом, экспериментальные данные указывают на то, что введение БГТ в диету дрозофил может оказывать радиопротекторное действие, адаптируя организм к хроническому γ-излучению, и влияние этого эффекта зависит от генетического фона животных, особенно уровня активности соответствующих sod-генов.
Дрозофила, γ-излучение, бутилгидрокситолуол, ДНК-разрывы, продолжительность жизни, антиоксидантная система, мутации в sod-генах
Короткий адрес: https://sciup.org/149149444
IDR: 149149444 | УДК: 575.167:57.04/57.017.3 | DOI: 10.19110/1994-5655-2025-7-25-34
Radiomodifying properties of butylhydroxytoluene using Drosophila melanogaster as an example
In experiments on Drosophila melanogaster, the radiomodifying effect of butylhydroxytoluene (BHT) was assessed by studying the level of DNA damage and lifespan in the wildtype Canton-S strain and sod-gene mutants. It was found that the introduction of BHT into the diet of Drosophila can lead to a decrease in sensitivity to chronic γ-radiation of different intensities (0.42 and 40.3 mGy/h). In individuals with normal gene functioning (Canton-S), which develop under conditions of chronic irradiation, BHT in concentrations above 1 μM has a beneficial effect on the cytogenetic index (reducing its level at dose rates of 0.42 and 40.3 mGy/h) and lifespan (increasing its parameters at dose rate of 0.42 mGy/h). A specific effect of BHT on genotypes with low activity of cytoplasmic (sod[n1]/+) and mitochondrial (sod[delta02]/+) superoxide dismutase was found. According to the "DNA damage" and "survival" parameters, the most pronounced radioprotective effect of BHT was noted in animals of the sod[n1]/+ strain. This effect was recorded at concentrations of the substance exceeding 10 μM and at all irradiation rates. In individuals of the sod[delta02]/+ strain, the antiradiation effect of BHT was revealed at concentrations of 10-20 μM (on the level of DNA damage) and 100 μM (on lifespan). The combination of BHT and chronic irradiation has a predominantly antagonistic (in all genotypes), less often synergistic/additive (in sod-mutants) character. This preparation, depending on the concentration, is able to reduce DNA damage and increase the lifespan of individuals of a certain genotype, which indicates its ability to slow down the aging process. Thus, the experimental data indicate that the introduction of BHT into the diet of Drosophila can have a radioprotective effect, adapting the organism to chronic γ-radiation. The efficiency of this effect depends on the genetic background of animals, especially on the activity level of the corresponding sod-genes.
Текст научной статьи Радиомодифицирующие свойства бутилгидрокситолуола на примере Drosophila melanogaster
Большое число популяций организмов, а также человек испытывают постоянное повышенное радиационное воздействие благодаря естественному и техногенному (вследствие развития ядерной энергетики, испытания ядерного оружия, аварий на объектах радиационной промышленности, растущего количества радиоактивных отходов) радиационному фону. Для человека риск радиационного поражения возрастает при применении ионизирующих излучений в лучевой диагностике и радиотерапии злокачественных опухолей. Накоплено много данных, свидетельствующих о том, что облучение индуцирует нестабильность генома, на фоне которого возникают различные типы повреждений ДНК, мутации, хромосомные аберрации и др. [1]. На сегодняшний день отсутствуют универсальные противолучевые средства, способные уменьшить поражающее действие облучения во всех диапазонах доз. Данный факт связан с различными биохимическими и молекулярно-генетическими механизмами, которые участвуют в формировании последствий воздействия ионизирующей радиации на организм [2, 3]. Важную роль в радиозащите клеток играет активация антиоксидантной системы, направленная на подавление свободных радикалов и последующего окислительного стресса [3].
Известно, что синтетические соединения обладают ра-диопротекторными свойствами по отношению к влиянию ионизирующего излучения в сублетальных и летальных дозах. В то время как вещества природного происхождения оказывают противолучевой эффект при низкоинтенсивном облучении [там же]. Поиск химических средств, повышающих радиорезистентность организма в условиях хронического облучения в малых дозах, в настоящее время становится все более актуальным в связи с широким использованием радиационных источников в клинической практике и повседневной деятельности человека. С этой целью активно ведутся разработка и апробация новых полусинтетических и синтетических антиоксидантов с низкой токсичностью, потенциально обладающих радиозащитным действием.
Бутилгидрокситолуол (БГТ, Butylhydroxytoluene (BHT)), одобренный FDA (Food and Drug Administration, США) широко используется в качестве консерванта в пищевой промышленности [4]. Это синтетическое вещество хорошо известно в клинических и биологических исследованиях как сильный антиоксидант, агент с противоканцерогенными, антинекротическими, противовирусными и антимикробными свойствами [5-7]. Данные свойства БГТ проявляются только при его воздействии на организм в небольших концентрациях [8]. Бутилгидрокситолуол в высоких концентрациях может вызвать выраженный цитотоксический эффект, нарушения эндокринной системы, гемолиз, репродуктивную токсичность и рак [5, 7]. Есть сведения, демонстрирующие его радиопротекторный потенциал у разных модельных животных, подвергшихся острому облучению [9, 10]. Роль БГТ в модификации эффектов хронического облучения разной интенсивности не изучена. Кроме того, неясно, способен ли БГТ компенсировать дефицит есте- ственных антиоксидантов организма в заданных условиях облучения.
Цель работы – оценить радиомодифицирующие свойства бутилгидрокситолуола путем исследования интегральных показателей выживаемости хронически облученных особей Drosophila melanogaster с низким уровнем ферментов антиоксидантной системы.
Материалы и методы
Линии Drosophila melanogaster . В качестве экспериментального материала были использованы линия дикого типа Canton-S и линии, характеризующиеся низким уровнем синтеза цитоплазматической Cu/Zn - (#4015, sod[n1]/+ , генотип: Sod[n1]red[1]/TM3,Sb[1]Ser[1]) и митохондриальной Mn- ( #27643, sod[delta02]/+ , генотип: y[1]w[*];Sod2[Delta02]/ CyO ) супероксиддисмутазы [11]. Данные линии получены из крупного зарубежного коллекционного центра (Блумингтон, США).
Методы. Биологическая эффективность бутилгидрокситолуола (2,6-ди-трет-бутил-4-метилфенол, ООО «БиоМир», Россия) была оценена критериями, определяющими продолжительность жизни и уровень повреждений ДНК (методом «ДНК-комет» в нейтральной версии рН). Анализ средней, медианной и максимальной продолжительности жизни был проведен на имаго самцов (не более 20 особей на пробирку, 300 особей на вариант), отобранных в течение суток после вылета и помещенных на обедненную сахароагаровую среду [12]. Самцы были пересажены на свежий корм дважды в неделю. Подсчет числа умерших особей был произведен ежедневно (кроме субботы и воскресенья). Полученные результаты были оформлены в виде кривых выживания и статистически обработаны с помощью лог-рангового теста. Значимость различий в средней, медианной и максимальной продолжительности жизни была рассчитана с использованием тестов Флеминга-Харингтона и Ванга-Аллисона с поправкой Бонферрони в онлайн-приложении OASIS 2 (https://sbi. [13].
Уровень повреждений ДНК был исследован в клетках нервных ганглиев (нейробластах) личинок третьего возраста [14]. Получение препаратов с нуклеоидами и их визуальная обработка подробно описаны в работе [15]. Статистическая значимость различий в значениях ОТМ (Olive tail moment – момент «хвоста кометы» по П. Л. Оливе) была определена по t-критерию Стьюдента.
Обработка БГТ. Бутилгидрокситолуол, растворенный в 96%-ном этаноле, в разных концентрациях (1, 10, 20 и 100 мкМ) был добавлен (по 30 мкл) на питательную (дрожжевую, сахарно-манковую) среду. В каждую пробирку со средой с БГТ и без (контроль, включающий только 96%-ный этанол) были помещены родительские формы исследуемых линий дрозофилы для получения кладок с эмбрионами. Обработка БГТ была проведена на чувствительных к различным воздействиям стадиях предимагинального развития дрозофил, когда происходит интенсивная пролиферация и дифференциация клеток организма. Для оценки цитогенетического показателя время экспозиции БГТ для всех концентраций составило 5 сут (стадии «эмбрион» – «личинка третьего возраста»), для анализа выживаемости – 12 сут (стадии «эмбрион» – «имаго»). Все экспериментальные культуры дрозофилы содержали в стандартных условиях: при температуре +23° С ± 0,1 и 12-часовом режиме освещения.
Условия облучения. Особи на предимагинальных стадиях были подвергнуты хроническому облучению в разных мощностях экспозиционной дозы (0,42 и 40,3 мГр/ч). Накопленные дозы составили 0,05, 0,12 и 4,8 Гр. Источником γ -излучения служил 226Ra (56 мГр/ч).
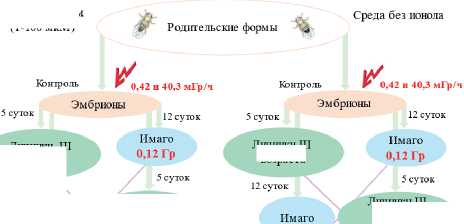
Дизайн эксперимента, включающий подробное описание особенностей обработки БГТ и условий облучения с указанием исследуемых стадий животных и показателей, представлен на рис. 1. Эксперимент был проведен в трех независимых биологических повторностях.
Среда с ионолом (1-100 мкМ)
возраста
Личинки 111
возраста
12 суток
Личинки III
Личинки 111
Имаго
Выживаемость
Выживаемость возраста 0,05 и 4,8 Гр возраста 0,05 и 4,8 Гр
Повреждения ДНК
Повреждения ДНК
Рисунок 1. Дизайн эксперимента, включающий подробное описание особенностей обработки БГТ и условий облучения с указанием исследуемых стадий животных и показателей.
Figure 1. Experimental design including a detailed description of BHT treatment and irradiation conditions, indicating the development stages of animals and parameters studied.
Личинки Ш
Коэффициенты взаимодействия БГТ и облучения. Оценка реакций животных на совместное действие ионизирующего излучения и БГТ в разных концентрациях была проведена с использованием коэффициентов взаимодействия (Kw), которые были рассчитаны по формуле: Kw = ДА(Х; У)/ Д Л(0; У) + А(Х;0), где ДЛ(Х;У) = Л(Х;У)-Л(0;0) – превышение совместного влияния факторов X (препарат) и Y (облучение) по сравнению с контролем; ДЛ(0;У) + А(Х;0) – сумма превышения эффектов при раздельном воздействии исследуемых факторов [16].
Результаты и их обсуждение
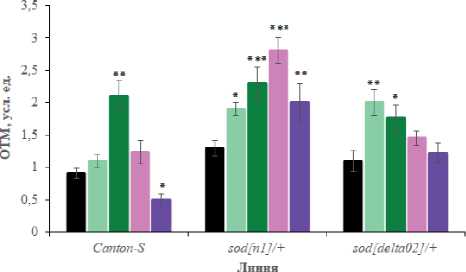
Оценка уровня повреждений ДНК. Показано, что раствор БГТ без облучения оказывает генотоксическое действие в концентрациях 1-10 мкМ (у линии sod[delta02]/+ ), 10 мкМ (у линии Canton-S ) и 1-100 мкМ (у линии sod[n1]/+ ) (рис. 2). У линий Canton-S и sod[delta02]/+ препарат в более высоких концентрациях (выше 20 мкМ) либо не влиял на цитогенетический параметр, либо значимо (р<0,05) снижал его уровень (у особей Canton-S ). Это свидетельствует о положительной эффективности БГТ в концентрациях, превышающих 20 мкМ при фоновых значениях радиации.
В отсутствии влияния БГТ хроническое облучение мощностью 40,3 мГр/ч приводит к увеличению (р<0,05)
повреждений ДНК у особей с дисфункцией sod -генов (рис. 3). У линии дикого типа Canton-S не обнаружено цитогенетического эффекта облучения, но при включении в диету БГТ характер реакции особей в ответ на облучение зависел от концентрации внесенного вещества и накопленной дозы γ -излучения (в единственном случае). У данного генотипа БГТ проявил радиопротекторные свойства при концентрациях 10-20 мкМ (р<0,01), снижая количество клеток с поврежденной ДНК. В то время как при концентрации 100 мкМ препарат усиливал (р<0,01) только действие хронического облучения мощностью 40,3 мГр/ч. Значимость наблюдаемых эффектов была получена при сравнении средних значений ОТМ между облученными особями, в чью диету входил БГТ, и особями, развивающимися в условиях раздельного действия изучаемых факторов («Контроль+облучение» или «Концентрация»). У линии sod[n1]/+ с низким синтезом цитоплазматической супероксиддисмутазы БГТ повлиял на формирование ра-диорезистентных признаков у облученных животных при воздействии всех концентраций вещества и накопленных доз γ-излучения (р<0,05-0,001). Так, уровень повреждений ДНК в клетках нервных ганглиев особей, испытывающих одновременное действие БГТ и облучения, оказался ниже уровня разрывов ДНК в нейробластах личинок, подвергавшихся либо действию БГТ, либо ионизирующему излучению. Напротив, у особей линии sod[delta02]/+ противолучевой эффект (р<0,05 и р<0,001) БГТ был обнаружен в концентрациях 1-20 мкМ и при хроническом низкоинтенсивном облучении (0,42 мГр/ч). У этого же генотипа БГТ в концентрациях 20-100 мкМ способен повышать (р<0,05) радиочувствительность особей, содержащихся при воздействии хронического облучения более высокой интенсивности (40,3 мГр/ч).
Оценка влияния БГТ на радиационно-индуцированные генетические нарушения у дрозофилы была изучена в работе [9], в которой описаны и проанализированы противоречивые результаты воздействия БГТ на половые клетки дрозофил мужского пола, подвергшиеся острому облучению. Показано, что радиозащитные эффекты БГТ наблюдались только на уровне рецессивных сцепленных
■Контроль И1мкМ ВЮмкМ ЯЗОмкМ ЦООмШ
Рисунок 2. Влияние БГТ в разной концентрации на уровень повреждений ДНК в клетках нервных ганглиев D. melanogaster .
Условные обозначения. *р<0,05; **р<0,01; ***р<0,001 – по сравнению с контролем.
Figure 2. Effect of BHT in different concentrations on the level of DNA damage in D. melanogaster nerve ganglion cells.
Keys. *p<0.05; **p<0.01; ***p<0.001 – compared to the control.
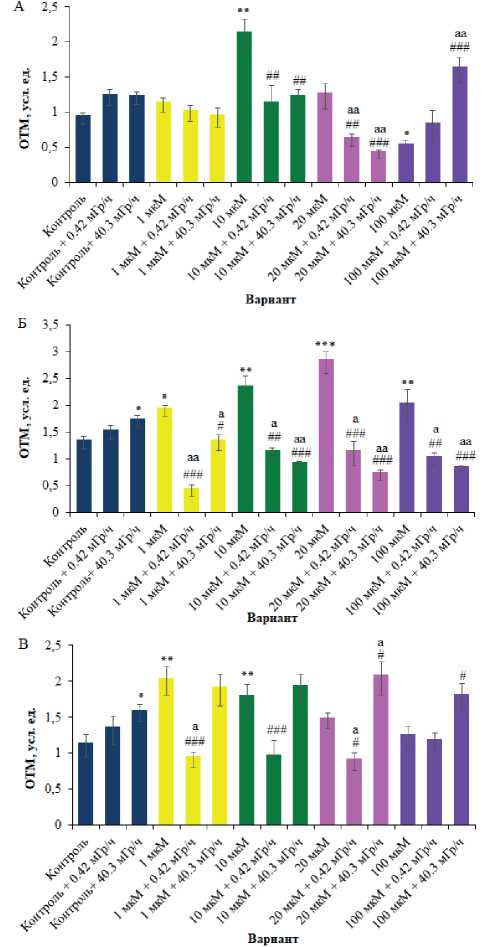
Рисунок 3. Уровень повреждений ДНК в клетках нервных ганглиев линий Canton-S (А), sod[n1]/+ (Б) и sod[delta02]/+ (В) после лечения БГТ и хронического облучения.
Условные обозначения. *р<0,05; **р<0,01; ***р<0,001 – по сравнению с контролем; #р<0,05; ##р<0,01; ###р<0,001 – между необлученными и облученными вариантами в соответствующих концентрации и мощности облучения; а р<0,05; аа р<0,01 – между облученным вариантом без БГТ («Контроль+0,42 мГр/ч» или «Контроль+40,3 мГр/ч») и облученным вариантом в соответствующей концентрации и мощности облучения.
Figure 3. The level of DNA damage in the nerve ganglion cells of the Canton-S (A), sod[n1]/+ (Б) and sod[delta02]/+ (В) strains after treatment with BHT and chronic irradiation.
Keys. *p<0.05; **p<0.01; ***p<0.001 – compared with the control; #p<0.05; ##p<0.01; ###p<0.001 – between non-irradiated and irradiated variants at the corresponding concentration and irradiation power; a p<0.05; aa p<0.01 – between the irradiated variant without BHT ("Control+0.42 mGy/h" or "Control+40.3 mGy/h") and the irradiated variant at the corresponding concentration and irradiation power.
с полом мутаций и транслокаций. По другим нарушениям генетического материала, включающим доминантные летальные мутации, аутосомно-рецессивные летали и потерю Х-хромосомы, препарат оказывал радиосенсибилизирующее действие. Настоящее исследование рассматривает цитогенетические эффекты БГТ на уровне соматического генома, что позволило более целостно оценить влияние препарата и интерпретировать полученные сведения относительно организма в целом. В большинстве случаев данные продемонстрировали снижение частоты повреждений ДНК в соматических клетках облученных животных, коррелирующее с повышенной их выживаемостью.
Оценка продолжительности жизни. У Canton-S по сравнению с контролем БГТ либо снижает параметры выживаемости, либо не влияет на них (рис. 4 А). Сравнение
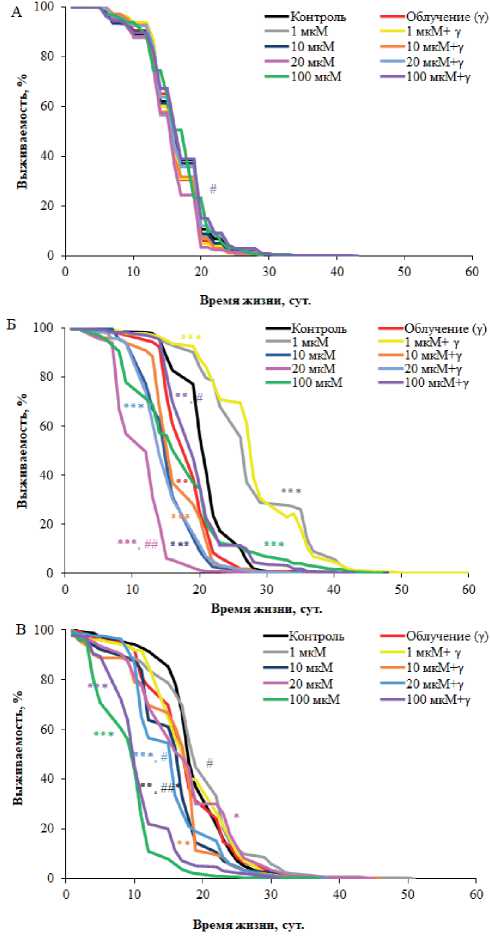
Рисунок 4. Кривые выживания самцов линий Canton-S (А), sod[n1] /+ (Б) и sod[delta02]/+ (В) после лечения БГТ и хронического низкоинтенсивного облучения (0,42 мГр/ч).
Условные обозначения. *р<0,05; **р<0,01; ***р<0,001 – по сравнению с контролем; #р<0,05; ##р<0,01 – между необлученными и облученными вариантами в соответствующей концентрации.
Figure 4. Survival curves of males of the Canton-S (A), sod[n1]/+ (Б) and sod[delta02]/+ (В) strains after treatment with BHT and chronic low-intensity irradiation (0.42 mGy/h).
Keys. *p<0.05; **p<0.01; ***p<0.001 – compared with the control; #p<0.05;
##p<0.01 – between non-irradiated and irradiated variants at the corresponding concentration.
Таблица 1
Продолжительность жизни самцов D. melanogaster после воздействия БГТ и хронического облучения мощностью 0,42 мГр/ч
Table 1
Lifespan of D. melanogaster males after exposure to BHT and chronic irradiation at a rate of 0.42 mGy/h
|
Линия |
УЭ |
Параметры продолжительности жизни |
|||||
|
М±SE |
∆М |
50 % |
∆50 % |
90 % |
∆90 % |
||
|
Контроль |
16,6 ± 0,3 |
Н |
16 |
Н |
22 |
Н |
|
|
Облучение (γ) |
16,2 ± 0,2 |
-2,4 |
16 |
0 |
21 |
-4,5 |
|
|
1 мкМ |
16,4 ± 0,2 |
-1,2 |
16 |
0 |
21 |
-4,5 |
|
|
1 мкМ + γ |
16,3 ± 0,2 |
-1,8 |
16 |
0 |
21 |
-4,5 |
|
|
Canton-S |
10 мкМ 10 мкМ + γ |
16,5 ± 0,3 16,2 ± 0,2 |
-0,6 -2,4 |
17 16 |
+6,2 0 |
21 21 |
-4,5 -4,5 |
|
20 мкМ |
15,7 ± 0,3 |
-5,4 |
16 |
0 |
20 |
-9,1* |
|
|
20 мкМ + γ |
16,8 ± 0,2 |
+1,2 |
16 |
0 |
22# |
0 |
|
|
100 мкМ |
17,1 ± 0,3 |
+3,0 |
19 |
+18,7* |
21 |
-4,5 |
|
|
100 мкМ + γ |
17,0 ± 0,3 |
+2,4 |
17# |
-6,2 |
22 |
0 |
|
|
Контроль |
22,8 ± 0,4 |
Н |
25 |
Н |
31 |
Н |
|
|
Облучение (γ) |
20,2 ± 0,4 |
-11,4* |
22 |
-12,0 |
25 |
-24,0* |
|
|
1 мкМ |
20.9 ± 0,7 |
-8,3 |
30 |
+20,0* |
36 |
+16,1* |
|
|
1 мкМ + γ |
27,6 ± 0,5# |
+20,0* |
21# |
-16,0* |
31# |
0 |
|
|
sod[n1]/+ |
10 мкМ |
19,3 ± 0,4 |
-15,3* |
17 |
-32,0* |
30 |
-3,2 |
|
10 мкМ + γ |
18,9 ± 0,5 |
-17,1* |
18 |
-28,0* |
30 |
-3,2 |
|
|
20 мкМ |
16,4 ± 0,2 |
-28,1* |
16 |
-36,0* |
21 |
-32,2* |
|
|
20 мкМ + γ |
18,9 ± 0,5# |
-17,1* |
17 |
-32,0* |
30# |
-3,2 |
|
|
100 мкМ |
21,6 ± 0,5 |
-5,2 |
21 |
-16,0* |
31 |
0 |
|
|
100 мкМ + γ |
23,8 ± 0,5 |
+4,4 |
25# |
0 |
35 |
+12,9 |
|
|
Контроль |
24,5 ± 0,3 |
Н |
25 |
Н |
31 |
Н |
|
|
Облучение (γ) |
23,8 ± 0,4 |
-2,8 |
24 |
-4,0 |
31 |
0 |
|
|
1 мкМ |
24,2 ± 0,4 |
-1,2 |
25 |
0 |
30 |
-3,2 |
|
|
1 мкМ + γ |
23,4 ± 0,4 |
-4,5 |
25 |
0 |
30 |
-3,2 |
|
|
sod[delta02]/+ |
10 мкМ 10 мкМ + γ |
21,2 ± 0,4 22,9 ± 0,3 |
-13,4 -6,5 |
24 24 |
-4,0 -4,0 |
30 30 |
-3,2 -3,2 |
|
20 мкМ |
22,4 ± 0,4 |
-8,6 |
23 |
-8,0 |
30 |
-3,2 |
|
|
20 мкМ + γ |
20,8 ± 0,3 |
-15,1* |
23 |
-8,0* |
30 |
-3,2 |
|
|
100 мкМ |
18,3 ± 0,5 |
-25,3* |
18 |
-28,0* |
29 |
-6,4 |
|
|
100 мкМ + γ |
20,5 ± 0,3# |
-16,3* |
23# |
-8,0* |
29 |
-6,4 |
|
Условные обозначения. УЭ – условия эксперимента; М ± SE – средняя продолжительность жизни (дни) ± стандартная ошибка (SE); 50 % – медианная продолжительность жизни; 90 % – возраст 90 % смертности (дни); ∆М и ∆50 % – различия в средней и медианной продолжительности жизни по сравнению с контролем; ∆90 % – различия в возрасте наступления 90 % смертности по сравнению с контролем; *р<0,05–0,0001 – по сравнению с контролем; #р<0,05–0,0001 – между необлученными и облученными вариантами в соответствующей концентрации; Н – не применимо.
Keys. УЭ – experimental conditions; M ± SE – mean lifespan (days) ± standard error (SE); 50 % – median lifespan; 90 % – age at 90 % mortality (days); ∆M and ∆50 % – differences in mean and median lifespan compared to the control; ∆90 % – differences in age at 90 % mortality compared to the control; *p<0.05–0.0001 – compared to the control; #p<0.05–0.0001 – between non-irradiated and irradiated variants at the corresponding concentration; H – not applicable.
симальной ПЖ на 6,2 и 42,8 % (при 20 мкМ), 19 и 12,9 (при 100 мкМ) % соответственно. У sod[delta02]/ + БГТ снижает ПЖ по сравнению с контролем (р<0,05–0,0001). При облучении БГТ способен повысить среднюю и медианную ПЖ особей этого генотипа на 12 и 27,8 % (р<0,05–0,0001).
Следует отметить, что БГТ способен увеличивать продолжительность жизни у линий Canton-S и sod[n1]/ + на 18,7 % (медианная, в концентрации 100 мкМ) и 16,1 % (максимальная, в концентрации 1 мкМ) соответственно. Это указывает на его потенциальные геропротекторные свойства, что согласуется с некоторыми данными исследований, демонстрирующими увеличение продолжительности жизни мышей и дрозофил [17, 18].
На сегодняшний день известны противоречивые факты действия БГТ относительно острого облучения. С одной стороны, БГТ оказывает радиосенсибилизирующее действие, вызывая высокую смертность мышей, подвергшихся воздействию рентгеновских лучей в острой дозе 7,25 Гр [19]. С другой – действует как радиопротектор у дрожжей при γ-излуче-нии в повреждающих дозах 100 и 400 Гр [10]. Как показали представленные в этой статье результаты, БГТ способен влиять на формирование радиорезистентных признаков у хронически облученных дрозофил, но данное его свойство сильно зависит от концентрации вещества и исходного уровня ферментов антиоксидантной системы восстановления в организме. Предположительно, такое радиопротекторное действие БГТ является следствием его способности к детоксикации свободных радикалов, особенно в случаях, когда наблюдается дефицит естественных ферментных систем необлученных и облученных вариантов этого генотипа после обработки БГТ в концентрации 20 мкМ показало увеличение средней и максимальной ПЖ на 10 и 7 % соответственно (р<0,05-0,0001). Обратная реакция наблюдается при концентрации 100 мкМ, при которой БГТ снижает медианную ПЖ на 10,5 % (р<0,01). У sod[n1]/+ БГТ вызвал в основном отрицательный эффект на выживаемость по сравнению с контролем (р<0,05–0,0001) (табл. 1, рис. 4). Исключение составляет его действие при концентрации 1 мкМ, увеличивающее медианную и максимальную ПЖ на 20 и 16 % соответственно (р<0,001). Хроническое низкоинтенсивное облучение (0,42 мГр/ч) негативно повлияло на ПЖ самцов, снижая их ПЖ на 11,4 (средняя), 12 (медианная) и 24 (максимальная) %. В условиях облучения БГТ проявил себя как радиопротектор, увеличивая параметры средней ПЖ на 32 (при 1 мкМ), 15,2 (при 20 мкМ) и 10,2 (при 100 мкМ) % (р<0,05–0,0001), параметры медианной и мак- антиоксидантной защиты. В пользу данного утверждения имеются сведения литературы, указывающие на то, что БГТ выступает в роли поглотителя свободных радикалов и может выполнять защитные функции, предотвращая химически индуцированные повреждения печени и замедляя процессы старения у животных. Однако БГТ может вызвать токсичность, обусловленную окислительным стрессом, возникающим вследствие селективной потери антиоксидантов, таких как глутатион-S-трансфераза (GSTP1), пероксиредоксин-2 (PRDX2), супероксиддисмута-за1 (Sod1), карбонилредуктаза (NADPH) и бутилированный гидрокситолуолхинонметид (BHT-QM) [7].
Считают, что основной механизм действия БГТ – это предотвращение свободнорадикального окисления [7]. Но есть и другое предположение, в основе которого БГТ рассматривается как ингибитор некоторых форм цитохрома P-450, связываясь с его феррихромом P-450 и вызывая связывание типа I [20]. Существует также мнение, что наблюдаемые эффекты связаны не столько с самим БГТ, сколько с продуктами его метаболизма [9]. Например, после приема БГТ у крыс формируются метаболиты в виде кислоты БГТ, образующейся при окислении кольцевой метильной группы, которая выделяется как в свободном виде, так и в составе, связанном с глюкуроновой кислотой, и производного меркаптуровой кислоты (S-(3,5-ди-трет-бу-тил-4-гидроксибензил)-N-ацетилцистеин) [21]. У человека БГТ метабилизируется в 5-кар-бокси-7-(1-карбокси-1-метилэтил)-3,3-ди-метил-2-гидрокси-2,3-дигидробензофуран и второстепенный компонент 3,5-ди-[1-13C]ме-тил-1-метилэтил-4-гидроксибензойную кислоту [21, 22]. Метаболическая судьба БГТ у дрозофилы неизвестна. Поэтому нельзя исключать, что эффекты, наблюдаемые в настоящем исследовании, обусловлены продуктами метаболизма БГТ и не только его исходной неизмененной структурой.
Таким образом, можно предположить механизмы действия БГТ при действии облучения и без него. Радио- и геропротекторный эффекты БГТ, скорее всего, происходят посредством его влияния (или метаболитов) на поддер жание антиоксидантного статуса животных (Kw>1). (в условиях окислительного стресса или сниженного уровня естественных антиоксидантов) и подавления цитохрома Р-450. Возможно, эффект БГТ обусловлен не только его прямым антиоксидантным действием, но и модуляцией сигналов о регуляции экспрессии антиоксидантных генов, что требует дополнительного изучения. Степень защиты БГТ при облучении зависит от множества факторов, включая дозу облучения, тип и режим облучения (рентгеновское или γ-излучение, кратковременное или хроническое), концентрации вещества и состояния антиоксидантной системы организма. Особенности таких динамических процессов требуют дальнейших детальных исследований, чтобы полностью понять, каким образом взаимодействуют эти факторы и как можно оптимально использовать потенциальные защитные свойства БГТ при различных формах окислительного стресса.
Оценка коэффициентов взаимодействия БГТ и облучения. При тестировании химических веществ в комбинации с другими факторами (физическими или биологическими) необходимо учитывать характер их взаимодействия (антагонизм, синергизм, аддитивность). Совместное их действие обуславливает принципиально различные типы ответной реакции организма [23]. Особенно это важно при поиске новых радиомодифицирующих средств [24, 25].
Биологический эффект совместного действия БГТ и облучения, оцениваемый на основании расчетов коэффициента взаимодействия (Kw), носит преимущественно антагонистический характер (табл. 2), когда сочетанный эффект двух исследуемых факторов меньше, чем раздельное действие каждого из них, или один фактор ос-
Таблица 2
Значения коэффициентов взаимодействия (Kw) при совместном действии БГТ и облучения
Table 2
Values of interaction coefficients (Kw) under the combined action of BHT and irradiation
|
Линия |
КБГТ, мкМ |
Показатель/накопленная доза облучения |
||||
|
Повреждения ДНК |
СрПЖ |
МедПЖ |
МаксПЖ |
|||
|
0,42 мГр/ч |
40,3 мГр/ч |
0,42 мГр/ч |
||||
|
Canton-S |
1 10 20 100 |
-0,64 0,21 -15,5 0,15 |
-0,10 0,32 -17,0 -0,98 |
-1,50 -1,33 -0,40 0,44 |
0 0 0 0,33 |
0 0 0 0 |
|
sod[n1]/+ |
1 10 20 100 |
-2,25 -0,25 -0,15 -0,60 |
0 -0,70 -0,54 -1,67 |
6,86 4,33 1,02 0,71 |
-0,50 1,40 1,33 0 |
0 -0,20 0,25 0,66 |
|
sod[delta02]/+ |
1 10 20 100 |
-0,28 -0,36 -1,69 -0,50 |
1,77 4,05 -8,54 -2,00 |
-2,75 0,61 2,64 0,73 |
0 0 2,00 0,33 |
1 1 1 1 |
Условные обозначения. КБГТ – концентрация БГТ (мкМ), СрПЖ – средняя продолжительность жизни, МедПЖ – медианная продолжительность жизни, МаксПЖ – максимальная продолжительность жизни.
Примечание. Значения Kw рассчитаны относительно контрольных значений. Типы взаимодействия исследуемых факторов (БГТ и облучения): антагонистическое (Kw<1), аддитивное (Kw=1) и синергическое (Kw>1).
Keys. КБГТ – BHT concentration (μM); СрПЖ – average lifespan; МедПЖ – median lifespan;
МаксПЖ – maximum lifespan.
Note. Kw values are calculated relatively to control values. The interaction types of the studied factors (BHT and irradiation): antagonistic (Kw<1), additive (Kw=1) and synergistic
лабляет влияние другого. У линии дикого типа Canton-S БГТ и облучение (независимо от времени экспозиции) в бóльшей мере проявляют антагонистическое действие на биологические показатели. У особей линии sod[n1]/+ также наблюдается антагонистический характер воздействия изучаемых агентов на уровень повреждений ДНК и выживаемость. Однако влияние их комбинации на среднюю и медианную продолжительность жизни (но не на максимальную ПЖ) может быть синергическим при концентрациях ниже 100 мкМ. У особей линии sod[delta02]/+, помимо антагонистических эффектов, встречаются случаи синергизма, когда комбинация воздействующих факторов выше, чем их раздельное действие. По показателю «повреждения ДНК» синергический эффект выявлен при концентрации вещества 1-10 мкМ и облучении мощностью 40,3 мГр/ч. В то время как влияние компонентов на среднюю и медианную продолжительность жизни является синергическим при концентрации БГТ 20 мкМ и хроническом облучении мощностью 0,42 мГр/ч. Для максимальной продолжительности жизни характерно аддитивное действие БГТ во всех концентрациях и ионизирующего излучения (0,42 мГр/ч), поскольку коэффициент взаимодействия равен единице. Это означает, что эффект совместно действующих факторов такой же, как и эффект суммарного действия каждого из них. Из вышеизложенного можно заключить, что характер взаимодействия двух факторов зависит от концентрации одного из них и генетических особенностей организма, где наличие нарушений в системе антиоксидантной защиты может смещать баланс в сторону усиления эффекта воздействия.
Заключение
Исходя из представленных данных, БГТ можно отнести к препаратам, способным в зависимости от концентрации модифицировать эффекты хронического облучения разной интенсивности (0,42 и 40,3 мГр/ч). Бутилгидрокситолуол как эффективный антиоксидант проявляет радио-протекторное действие не только на уровне повреждений ДНК, но и на организменном уровне (по показателю выживаемости). У облученных особей с нормальным генотипом Canton-S БГТ в концентрациях, превышающих 1 мкМ, благоприятно влияет на цитогенетический показатель (снижая его уровень при мощностях дозы 0,42 и 40,3 мГр/ч) и продолжительность жизни (увеличивая ее параметры при мощности дозы 0,42 мГр/ч). Бутилгидрокситолуол обладает более выраженным протекторным действием по отношению к облучению и бóльшей эффективностью (в концентрациях вещества выше 1 мкМ и во всех накопленных дозах облучения) у животных с дисфункцией гена sod[n1] , отвечающего за синтез цитоплазматической Cu/Zn-супероксиддисмутазы. В то время как у особей линии sod[delta02]/+ , отличающихся низким уровнем активности митохондриальной Mn-супероксиддисмутазы, противолучевая защита наблюдается при концентрациях 10-20 (по цитогенетическому показателю) и 100 (по продолжительности жизни) мкМ и только в условиях хронического облучения мощностью 0,42 мГр/ч. Это указывает на специфичность действия БГТ у генотипов с нарушенной активностью супероксиддисмутазы в разных структурах клетки. Анализ коэффициентов взаимодействия демонстрирует, что совместный вклад БГТ и хронического облучения в изменения биологических показателей вызывает в основном антагонистический эффект у всех генотипов. Однако есть случаи синергического и аддитивного действия комбинации БГТ (в концентрациях ниже 100 мкМ) и радиационного фактора на продолжительность жизни (реже на уровень ДНК-разрывов) у особей с нарушенной антиоксидантной системой защиты. Предполагается, что генетические особенности, связанные с антиоксидантной защитой, играют важную роль в определении конечного результата воздействия комбинации факторов. Более того, обнаружен геропротекторный потенциал действия БГТ, заключающийся в его способности снижать уровень повреждений ДНК и повышать продолжительность жизни в зависимости от концентрации препарата и генотипического статуса животных. В целом, экспериментальные данные демонстрируют, что БГТ является препаратом, обладающим концентрационно-зависимой эффективностью, специфичной для различных генотипов, что позволяет говорить о его потенциале в геропротекции и защите от хронического облучения.
Автор заявляет об отсутствии конфликта интересов.


