Radionuclide sorbents based on industrial wastes: physical and chemical properties and application potential
Author: Kotova O.B., Maskalchuk L.N., Shushkov D.A., Leontieva T.G., Baklai A.A.
Journal: Вестник геонаук @vestnik-geo
Section: Научные статьи
Article in issue: 4 (268), 2017.
Free access
The actual task is to unite the efforts of scientists from different countries to find efficient sorbing materials and develop technologies for their production for purification of water systems, technogenic structures from radionuclides, heavy metals and other contaminants. The objects of the research are red mud (RM) from Ural aluminum plant and clay-salt slimes (CSS) from the 3rd mining factory of JSC «Belaruskali», which were studied by modern analytical methods. We estimated the application potential of the industrial wastes of bauxite processing (Russia) and sylvinite ore (Belarus) accumulated at enterprises of mining industry of these countries, in the technologies of rehabilitation of disturbed agroecosystem and purification of water environments and ecosystems from radionuclides.
Red mud, clay-salt slimes, physical and chemical properties, sorption, radioactive contamination, uranium, radium, thorium, radiocesium
Short address: https://sciup.org/149129249
IDR: 149129249 | UDC: 549.08:622.7 | DOI: 10.19110/2221-1381-2017-4-29-36
Сорбенты радионуклидов на основе промышленных отходов: физико-химические свойства и перспективы использования
Актуальной задачей представляется объединение усилий ученых разных стран для поиска эффективных сорбирующих материалов и разработка технологий их получения для очистки водных систем, техногенных образований от радионуклидов, тяжелых металлов и других загрязнений. В качестве объектов исследования выбраны красные шламы Уральского алюминиевого завода и глинисто-солевые шламы 3-го рудоуправления ОАО «Беларуськалий», которые исследованы современными аналитическими методами. Дана оценка перспективности использования промышленных отходов переработки бокситов (Россия) и сильвинитовой руды (Беларусь), накопившихся на предприятиях горно-добывающей отрасли данных стран, в технологиях реабилитации нарушенных природных агроэкосистем и очистки водных сред и экосистем от радионуклидов.
Text of the scientific article Radionuclide sorbents based on industrial wastes: physical and chemical properties and application potential
Утилизация накопившихся промышленных отходов является одной из приоритетных проблем современности. В настоящее время остро стоят вопросы загрязнения атмосферы и гидросферы, восстановления и поддержания экологического баланса регионов, особенно после природных и техногенных аварий и катастроф. Считается, что вторичное использование отходов — наиболее ресурсосберегающий путь. Вопросам утилизации промышленных отходов посвящено множество работ [22, 25—27]. Так, в Российской Федерации существует проблема реабилитации водоемов, загрязненных радионуклидами (общий объем водной массы составляет около 3 ■ 108 м3) [1,11]. В результате аварии на Чернобыльской АЭС (ЧАЭС) значительному радиоактивному загрязнению подвергся целый ряд водных объектов и экосистем: пруд-охладитель ЧАЭС, водные экосистемы реки Днепр и каскад днепровских водохранилищ, ряд озер Брянской области (Россия) и Гомельской области (Беларусь), скандинавских стран (Швеция и др.) [6]. Наибольшую радиоэкологическую опасность представляет долгоживущий и биологически подвижный радионуклид 137Cs. Особенностью радиоактивного загрязнения является тот факт, что его невозможно ликвидировать химическим путем. Единственным определяющим фактором, позволяющим снизить уровень загрязнения, является физический распад данного радионуклида (для 137Cs — 30.2 лет). В работе [15] показано, что период полуочищения непроточных водоемов и озер средней полосы России от 137Cs составляет 10—20 лет. В этой связи для снижения радиационного воздействия на население необходимо проведение мероприятий по очистке данных водоемов от 137Cs путем его иммобилизации твердой фазой сорбента для обеспечения безопасной изоляции данного радионуклида.
К числу известных и успешно применяемых методов очистки водных сред от 137Cs относится сорбционный метод с использованием органических и неорганических материалов [16]. Эффективность очистки водных сред и различных природных экосистем от 137Cs зависит от селективности сорбентов и присутствия органических и неорганических компонентов в водных средах. К числу перспективных неорганических сорбентов относятся природные тонкоди- 29
сперсные алюмосиликатные сорбенты — клиноптилолит и глауконит [2, 12]. Авторами [2, 13] показана эффективность поглощения 137Cs сорбентами на основе природного минерального сырья, модифицированного кремнийсодержащими соединениями (торговая марка «Экозоль»), клиноптилолитом и глауконитом, модифицированными смешанными ферроцианидами никеля-калия (Россия).
Результатами ранее проведенных исследований установлена перспективность использования крупнотоннажных отходов калийного производства ОАО «Беларуськалий» (глинисто-солевых шламов) в качестве сорбентов 137Cs и 90Sr для решения проблемы реабилитации загрязненных радионуклидами почв Беларуси [10].
Целью работы является оценка перспективности использования красных шламов Уральского алюминиевого завода (г. Екатеринбург, Российская Федерация) и глинисто-солевых шламов ОАО «Беларуськалий» (г. Солигорск, Республика Беларусь) для реабилитации природных экосистем и очистки водных сред и экосистем от радионуклидов.
Материалы и методы
Красный шлам (КШ) — промышленные отходы от переработки бокситов. Химический состав КШ определяли с помощью силикатного анализа. Фазовую диагностику осуществляли методом рентгеновской дифракции (Shimadzu XRD-6000, излучение CuK a ). Удельную площадь поверхности определяли методом БЭТ (кривая адсорбции азота) с помощью анализатора площади поверхности и размера пор NOVA 1200e, Quantachrome. Плотность измеряли пикнометрическим методом.
Сорбцию радионуклидов проводили в статических условиях при комнатной температуре и соот ношении твердой и жидкой фаз 1 : 10 (3 г сорбента и 30 мл раствора) из водных растворов нитрата уранила, хлорида радия и хлорида тория, в которых радионуклиды представлены природной смесью изотопов [Титаева, 1992]. Время контакта фаз составляло от 0.5 до 24 ч; рН раствора 6. Кислотность жидкой фазы доводили до необходимого уровня путем подщелачивания концентрированным (13 моль/л) раствором гидроксида аммония. После сорбции сорбенты отделяли от жидкой фазы фильтрованием. В фильтрате определяли содержание радионуклидов, по убыли которых рассчитывали степень извлечения урана, радия и тория.
Определение естественных радионуклидов в фильтратах проводилось по общепринятым методикам. Содержание урана определяли люминесцентным методом (чувствительность 2.0 - 10-8 г/г, ошибка измерений 20 %) по свечению перлов с NaF, интенсивность свечения измеряли на фотометре ЛЮФ-57 [4]. Торий определяли фотоколориметрически с арсеназо III, с отделением примесей на катионите КУ-2 (чувствительность метода 1.0 - 10-8 г/г, ошибка измерений 20 %) [7]. Радий определяли эманационным методом на приборе «Альфа-1» (чувствительность — 2.0 - 10-12 г/г, ошибка измерений 15 %) [17].
Прочность поглощения (десорбцию) оценивали по содержанию радионуклидов в вытяжках, полученных последовательной обработкой обогащенного радионуклидами сорбента 30 мл дистистилли-рованной воды, 1М-растворами ацетата аммония (CH3COONH4) и соляной кислоты (HCl). Время контакта на каждой из стадий десорбции — 24 ч.
Глинисто-солевые шламы (ГСШ) — промышленные отходы от переработки сильвинитовой руды, представляющие собой взвешенный осадок глины в насыщенном растворе солей (KCl и NaCl) и относящиеся к 4-му классу опасности [Классификатор...,
Таблица 1
Химический состав красного шлама, мае. %
Table 1
Chemical composition of red mud, wt. %
|
Компонент / Component |
Содержание, % / Content, % |
Компонент / Component |
Содержание, % / Content, % |
|
SiO 2 |
7.87 |
KO |
0.13 |
|
TiO 2 |
3.27 |
Na2O |
2.68 |
|
Al 2 O 3 |
12.17 |
P 2 O 5 |
0.81 |
|
Fe 2, O 3 |
34.18 |
п.п.п. |
12.77 |
|
FeO |
5.40 |
SO 3 |
2.53 |
|
MnO |
0.41 |
H 2 O- |
1.96 |
|
CaO |
15.27 |
CO 2 |
6.00 |
|
MgO |
1.40 |
общ |
1.66 |
Таблица 2
Содержание радиоактивных элементов в красном шламе и бокситах
Table 2
Composition of radioactive elements in red mud and bauxites
|
Образец / Sample |
Уран, г/т Uranium g/t |
Радий, г/т Radium, g/t |
Торий, г/т Cesium, g/t |
|
Красный шлам / Red mud |
0.54 |
4.78 - 10-6 |
31 . 67 |
|
Бокситы (Вежаю-Ворыквинское месторождение, среднее содержание) [14] Bauxites (Vezhayu-Vorykva deposit, average content) |
7.5 |
8.5 |
35 |
2016]. Исследование образца ГСШ-1, отобранного из шламохранилища 3-го рудоуправления ОАО «Беларуськалий», проводили в соответствии с фундаментальным принципом физико-химического анализа материалов, который определяет взаимосвязь: состав — морфология (структура) — свойства. Образец ГСШ-2 получали в лабораторных условиях пятикратной промывкой н.о. образца ГСШ-1 дистиллированной водой с последующей сушкой до постоянной массы при 50 °С в течение 6 ч. Образец ГСШ-3 получали из образца ГСШ-2 путем разрушения карбонатов 0.1М-раствором соляной кислоты, промывкой дистиллированной водой и сушкой до постоянной массы при 50 °С в течение 6 ч.
Исследования физико-химических свойств образцов ГСШ осуществляли с использованием стандартизированных методик. Гранулометрический анализ образцов ГСШ-2 и ГСШ-3 осуществляли на лазерном анализаторе размеров частиц Analysette 22 (Fritsch, Германия). Диапазон измерения прибора 0.1—602.5 мкм. Морфологию и размер частиц образца ГСШ-3 изучали методом СЭМ на сканирующем электронном микроскопе JSM-5610LV (JEOL, Япония). Кратность увеличения варьировалась в диапазоне от х 500 до х 11000. Свободную удельную поверхность образца ГСШ-1 определяли методом БЭТ по адсорбции паров азота при температуре -195 °С на приборе ASAP-2010, Micromeritics.
Исследование сорбционных свойств образца ГСШ-1 по отношению к радиоцезию проводили в соответствии с методикой [23].
Результаты и обсуждение
Красные шламы. Основными компонентами химического состава КШ являются Fe 2 O 3 + FeO, CaO, AI 2 O 3 (табл. 1), потери при прокаливании составили 12.77 %. Рентгенофазовым анализом диагностированы гематит, кальцит, лепидокрокит, нозеан, пирит, гранаты, рентгеноаморфные соединения железа. Удельная площадь поверхности составила 18.7 м2/г, плотность 2.84—2.94 г/см3.
Как видно из данных, приведенных в табл. 2, содержание тория в красном шламе по сравнению с бокситами примерно одинаковое, урана — ниже в 14 раз, радия — в 10-6 раза.
КШ характеризуется высокой сорбционной активностью в отношении естественных долгоживущих радионуклидов — урана, радия, тория (U238, Ra226, Th223). Кинетика сорбции радионуклидов КШ (табл. 3) показала, что в течение 30 мин взаимодействия из раствора извлекается более 95 и 97 % урана и радия соответственно. Через 2 ч более 98.8 % радия (содержание в растворе ниже предела обнаружения) сорбируется КШ. Коэффициент распределения по радию составил более 4040 мл/г. Извлечение урана с увеличением времени реакции незначительно возрастает и достигает 96.63 %. Сорбция тория протекает хуже: через 1 ч извлекается около 20 %, через 24 ч — более 60 %.
Десорбция радионуклидов при последовательной обработке насыщенного радионуклидами КШ дистиллированной водой, ацетатом аммония и соляной кислотой представлена на рис. 1. Изучение характери-
Таблица 3
Показатели сорбции урана, радия, тория красным шламом
Table 3
Sorption of uranium, radium, thorium by red mud
|
Время контакта, ч Contact time, h |
Концентрация радионуклида в растворе после сорбции, г/мл Concentration of radionuclide in solution after sorption, g/ml |
Степень извлечения, % Degree of concentration, % |
Коэффициент распределения, мл/г Distribution coefficient, ml/g |
|
Уран, п х 10-6 г/мл (исходная концентрация урана в растворе 2.0657 х 10-6 г/мл) Uranium n x 10-6 g/ml (Initial сoncentration of uranium in solution 2.0657 х 10-6 g/ml) |
|||
|
0.5 |
0.0868 |
95.80 |
228.04 |
|
1 |
0.0778 |
96.23 |
246.95 |
|
2 |
0.0778 |
96.23 |
246.95 |
|
4 |
0.0696 |
96.63 |
258.03 |
|
24 |
0.0696 |
96.63 |
258.03 |
|
Радий, п х 10-10 г/мл (исходная концентрация радия в растворе 0.289 х 10-10 г/мл) Radium n x 10-10g/ml (Initial сoncentration of radium in solution 0.289 x 10-10g/ml) |
|||
|
30 |
0.007 |
97.7 |
420.5 |
|
2 |
<0.001 * |
99.8 |
4040 |
|
4 |
0.002 |
99.5 |
1698.0 |
|
24 |
0.004 |
98.6 |
601.5 |
|
Торий , п х 10-6 г/мл (исходная концентрация тория в растворе 0.58 х 10-6 г/мл) Thorium п х 10-6 g/ml (Initial сoncentration of thorium in solution 0.58 х 10-6 g/ml) |
|||
|
0.5 |
0.58 |
0 |
— |
|
1 |
0.45 |
21.7 |
2.7 |
|
4 |
0.23 |
61.2 |
14.2 |
|
24 |
0.24 |
58.3 |
11.7 |
Примечание. * — концентрация радия ниже предела обнаружения.
стик десорбции показало, что сорбенты обладают высокой прочностью поглощения (или низкой суммарной десорбцией). При взаимодействии с водой и ацетатом аммония десорбция радионуклидов составила менее 1 %, при кислотной обработке наиболее прочно удерживаются радий и уран (десорбция составила 6.3 и 11.6 % соответственно), наименее прочно — радий (до 48.4 % десорбируется в раствор).
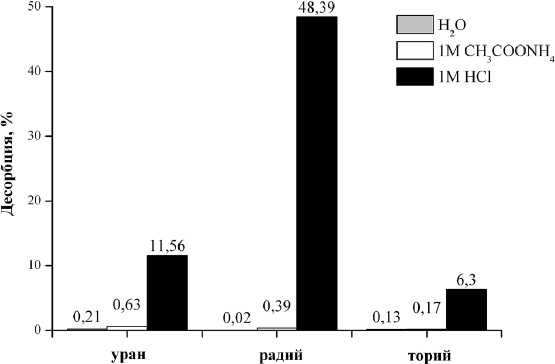
Рис. 1. Десорбция радионуклидов красным шламом
Fig. 1. Desorption of radionuclides by red mud
Глинисто-солевые шламы. В результате исследования физико-химических свойств образца ГСШ-1 установлено, что данный образец имеет щелочную реакцию среды (рНв равен 7.7), общее содержание водорастворимых солей составляет 55.5 г/л, потери при прокаливании — 24.6 %.
Результаты исследований химического состава образца ГСШ-1 приведены в таблице 4.
Согласно данным [8, 9], нерастворимый остаток (н.о.) образца ГСШ-1 содержит в своем составе доломит, кальцит, кварц, калиевый полевой шпат и иллит в количестве (8.1 ± 0.8), (5.2 ± 1.1), (24 ± 1.8), (27.7 ± 2.1), (34.9 ± 2.2) мас. % соответственно.
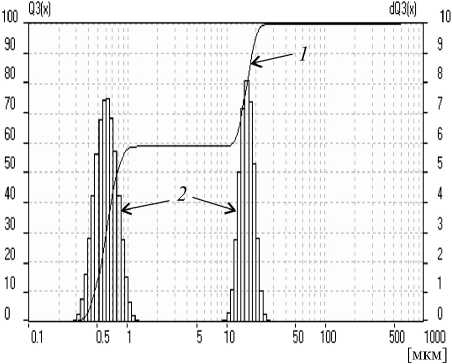
Распределение частиц по размерам для образцов ГСШ-2 и ГСШ-3 представлено на рис. 2 в виде интегральных и дифференциальных кривых.
Присутствие частиц различного размера в образцах ГСШ-2 и ГСШ-3 является следствием их многокомпонентного состава. Как видно из полученных данных (рис. 2), размер частиц в образцах ГСШ варьирует от 0.25 до 25 мкм. Для образца ГСШ-2 содержание основной фракции размером 0.25—1.5 мкм составляет 59 мас. %, а для образца ГСШ-3 при вариации размеров частиц от 0.25 до 4.5 мкм — 97 мас. %.
а)
б)
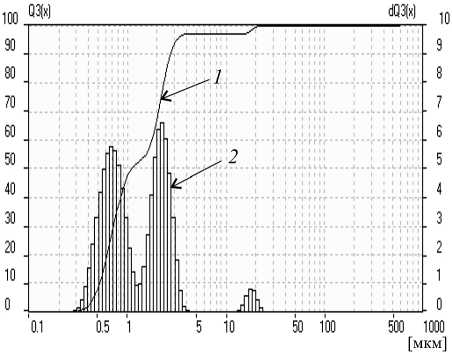
Рис. 2. Интегральная (1) и дифференциальная (2) дисперсные кривые для образцов ГСШ-2 (а) и ГСШ-3 (б)
Fig. 2. Integral (1) and differential (2) dispersed curves for samples ГСШ-2 (a) and ГСШ-3 (б)
Разрушение карбонатов в н. о. образца ГСШ-1 является одним из способов модификации, позволяющим повысить его дисперсность в 1.6 раза. По размеру частиц к глинам принадлежат материалы, состоящие более чем на 50 мас. % из частиц размером до 10 мкм [3]. Полученные результаты свидетельствуют о том, что образцы ГСШ-2 и ГСШ-3 можно отнести к глинистым материалам.
Известно, что водорастворимые соли значительно изменяют структурное состояние глинистых минералов. В работе [19] показано, что для NaCl-смектита характерно образование микроагрегатов из плотно-упакованных пластинчатых элементов. Согласно результатам электронно-микроскопического анализа, дисперсный состав образца ГСШ-3 (рис. 3) представлен как крупными агломератами, так и более мелкими частицами округлой формы. Размер частиц ГСШ-3 колеблется в пределах от 0.25 до 25 мкм. Структура ча-
Химический состав образца ГСШ-1, мас. %
Таблица4
Table 4
Chemical composition of sample ГСШ-1, wt. %
|
Компонент / Component |
Содержание, % Composition, % |
|
SiO2 |
27.35 |
|
TiO 2 |
1.07 |
|
Al 2 O 3 |
7.53 |
|
FeO |
9.72 |
|
Компонент / Component |
Содержание, % Composition, % |
|
CaO |
19.85 |
|
MgO |
5.26 |
|
K2O |
13.21 |
|
Na2O |
2.86 |
стиц слоистая и состоит из плотноупакованных пластинчатых элементов, что хорошо согласуется с данными [23].
Удельная поверхность ГСШ-1, определенная по тепловой десорбции азота, составляет (42.8 ± 4.7) м2/г. Значительная степень дефектности кристаллической структуры и высокое значение удельной поверхности образца ГСШ-1 обусловливают его высокую сорбционную способность.

Рис. 3. Микроструктура образца ГСШ-3
Fig. 3. Microstructure of sample ГСШ -3
Неорганические сорбционные материалы обладают высокой химической и радиационной устойчивостью и проявляют селективность по отношению к некоторым радионуклидам [12]. Также известно, что селективные свойства сорбционных материалов в значительной мере определяются природой матрицы сорбента и его функциональных групп [12]. Помимо высокой селективности сорбционные материалы должны обладать высокой скоростью извлечения радионуклидов, что определяется природой сорбционного материала и возможной формой их использования (мелкодисперсной, волокнистой, гранулированной). В работе [23] показано, что перспективными природными материалами для селективной сорбции ионов цезия из растворов являются глинистые минералы группы иллита.
Для оценки возможности использования ГСШ-1 в качестве сорбционного материала для очистки водных сред и экосистем от 137Cs проведены сорбционные эксперименты, согласно которым сорбция 137Cs на образце ГСШ-1 из водопроводной воды заканчивается в течение первых 60 мин контакта, и далее значение количества сорбированного 137Cs не изменяется. Степень сорбции 137Cs образцом ГСШ-1 при этом составляет (96.4 ± 2.1)%. Водопроводную воду использовали в качестве аналога водной среды с низким со-лесодержанием. По результатам эксперимента рассчитывали равновесную концентрацию 137Cs в растворе [ C p] и его концентрацию в твердой фазе ГСШ-1 [ C г]. Полученные результаты представлены на рис. 4.
Изотерма сорбции цезия на образце ГСШ-1 получена в широком диапазоне концентраций и имеет сложный вид (рис. 4), что свидетельствует о возможном присутствии в его структуре нескольких типов сорбционных центров, которые характеризуют- lg[CTL мг/г
2Т
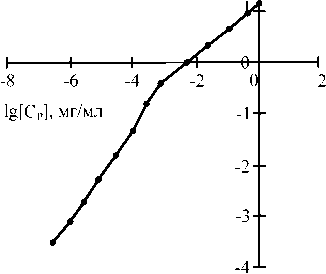
Рис. 4. Изотерма сорбции цезия на ГСШ-1из водопроводной воды, рН = 7.8, ионная сила раствора I = 0.1M NaClO4
Fig. 4. Isotherm of cesium sorption in ГСШ-1 from tap water, pH = 7.8, Ionic strength of the solution I = 0.1M NaClO4
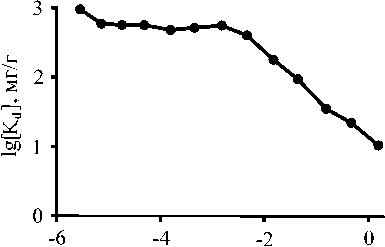
ся различными коэффициентами распределения ( Kd ). Зависимость Kd от концентрации цезия в водопроводной воде [ C p] приведена на рис. 4. Анализируя полученные данные, можно сделать вывод о том, что при концентрациях цезия в диапазоне 10-6—10-3 г/л для данной системы выполняется закон Генри и ион Cs + является микрокомпонентом, а Kd характеризуется постоянством (рис. 5). В этом диапазоне концентра-
lg[C0], мг/мл
Рис. 5. Зависимость Kd от исходной концентрации 137Cs в системе «ГСШ-1 — водопроводная вода»
Fig. 5. Dependence of Kd on the initial concentration of 137Cs in the system ГСШ-1 — tap water ций ГСШ-1 обладает высокой селективностью по отношению к Cs+, что обусловлено наличием в нем активных компонент — иллита и калиевого полевого шпата. При концентрациях Cs+ менее 10-3 г/л наблюдается линейный участок изотермы:
lg [ Ct ] = 2,63 + 0,95 lg [ Cp ]. (1)
Полученное из выражения (1) значение Kd составляет 426.6 л/кг при концентрации K+, равной 15.2 мэкв/л.
Авторы [23] на основании изучения сорбции иона Cs+ на иллите все многообразие сорбционных мест в порядке возрастания селективности разделили на три основных типа:
-
— RES (Regular Exchange Sites) — неселективные центры обменной сорбции, расположенные на плоских внешних гранях кристаллов минералов;
-
— FES (Frayed Edge Sites) — селективные центры сорбции, расположенные на ребрах и в краевой (клиновидной) зоне кристаллической решетки минералов со слоистой структурой;
-
— HAS (High Affinity Sites) — высокоселективные участки межпакетного пространства слоистых алюмосиликатов.
В работе [23] получено выражение для системы «сорбент — раствор», которое связывает емкость селективной сорбции [FES] и коэффициент селективности Cs+ по отношению к К+ ( Kc (Cs+/K+)), коэффициент распределения 137Cs( Kd ) и концентрацию К+ в растворе [ C к ]:
Kc (Cs+/K+)[FES] = Kd [ C к ]. (2)
Величина Kc (Cs+/K+)[FES] или Kd [ C к] постоянна в широком интервале концентраций К+ в растворе при условии, что доля К+ на [FES] при следовых количествах Cs+ стремится к единице. Выражение (3) определяет такой показатель, как потенциал связывания радиоцезия (Radiocaesium Interception Potential — RIP), характеризующий способность сорбционных материалов в условиях, контролируемых селективной сорбцией, удерживать катионы 137Cs+ в присутствии конкурирующего катиона К+:
-
R IP(K) = Kc (Cs+/K+)[FES] = Kd [ C k]. (3)
Значение RIP(K) используется для сравнения способности различных материалов сорбировать 137Cs из растворов [24].
Заключение
В результате исследований установлена высокая сорбционная способность КШ Уральского алюминиевого завода в отношении естественных радионуклидов (урана, радия, тория). Показано, что в течение 30 мин взаимодействия из раствора извлекается более 95 и 97 % урана и радия соответственно. Коэффициент распределения по радию составил более 4040 мл/г. Сорбция тория протекает медленнее: через 1 ч извлекается около 20 %, через 24 ч — более 60 %.
Изучение характеристик десорбции показало, что КШ обладает высокой прочностью поглощения (или низкой суммарной десорбцией). При взаимодействии с водой и ацетатом аммония десорбция радионуклидов составила менее 1 %, при кислотной обработке наиболее прочно удерживаются радий и уран (десорбция составила 6.3 и 11.6 % соответственно), наименее прочно — радий (до 48.4 % десорбируется в раствор).
Сочетание высокой сорбционной активности со способностью прочно удерживать загрязняющие вещества является важной характеристикой сорбционного материала с точки зрения его практического использования, поскольку позволяет избежать вторичного (обратного) загрязнения рабочей среды радионуклидами.
В отношении глинисто-солевых шламов ОАО «Беларуськалий» установлено, что размер частиц в 34
н.о. образца ГСШ-1 варьирует в пределах от 0.25 до 25 мкм, а содержание основной фракции размером 0.25—1.5 мкм составляет 59 мас. %. Показано, что разрушение карбонатов в н.о. ГСШ-1 является одним из возможных способов его модификации, позволяющим повысить дисперсность данного образца в 1.6 раза. Методом СЭМ установлено, что структура частиц слоистая и состоит из плотноупакованных пластинчатых элементов, что определяет высокую сорбционную способность ГСШ-1 по отношению к 137Cs. Удельная поверхность ГСШ-1 составляет (42.8 ± 4.7) м2/г. Установлено, что степень сорбции 137Cs образцом ГСШ-1 из водопроводной воды при концентрации К+ 15.2 мэкв/л достигает (96.4 ± 2.1) % в течение 1 ч. Значение Kd 137Cs для ГСШ-2 составляет 6.6 - 104 л/кг. Образец ГСШ-1 обладает высокой селективностью по отношению к Cs+ при его концентрации в водопроводной воде от 10-6 до 10-3 г/л.
Учитывая наличие в Российской Федерации больших запасов красных шламов (более 200 млн т [21]) и глинисто-солевых шламов в Республике Беларусь (более 110.5 млн т [20]), хорошие сорбционные показатели данных промышленных отходов в отношении ряда радионуклидов, возможность и сравнительную простоту технологического процесса их переработки, данные материалы можно рассматривать в качестве вторичного минерального ресурса для получения сорбентов радионуклидов различного состава и назначения.
Работа выполнена при частичной поддержке программы Уральского отделения РАН (проект «Развитие инновационных технологий эффективного и комплексного использования минерального сырья и получение новых материалов на минеральной основе», № 15-11-5-33).
Авторы благодарят к. б. н. И. И. Шуктомову и к. б. н. Г. Н. Рачкову за помощь в аналитических исследованиях радионуклидов.
References Radionuclide sorbents based on industrial wastes: physical and chemical properties and application potential
- Баранов С. В., Баторшин Г. Ш., Мокров Ю. Г., Глинский М. Г., Дрожко Е. Г., Линге И. И., Уткин С. С. Теченский каскад водоемов ФГУП «ПО "Маяк"»: текущее состояние и перспективы//Вопросы радиационной безопасности. 2011. № 2. С. 5-14.
- Блинова М. О., Воронина А. В., Семенищев В. С. Разработка метода реабилитации радиоактивно загрязненных почв//Актуальные проблемы радиохимии и радиоэкологии: Материалы II Междунар. науч.-технич. конф. Екатеринбург. 2014. С. 194-199.
- Глины. Минеральные ресурсы//Горная энциклопедия. URL: http://www.mining-enc.ru/g/gliny/(дата обращения: 09.02.2016).
- Добролюбская Т. С. Люминесцентный метод//Аналитическая химия урана. М., 1962. С. 143-165.
- Классификатор отходов, образующихся в Республике Беларусь: утвержден постановлением Министерства природных ресурсов и охраны окружающей среды Респ. Беларусь от 8 ноября 2007 г. № 85 URL: http://www.minpriroda.gov.by/uploads/folderForLinks/000116_964480.docx (дата обращения: 10.02.2016).


