Рак коры надпочечника
Автор: Горбунова В.А., Бельцевич Д.Г., Бохян В.Ю., Жуликов Я.А., Коломейцева А.А., Мельниченко Г.А., Феденко А.А.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Практические рекомендации
Статья в выпуске: 3S2-1 т.14, 2024 года.
Бесплатный доступ
Рак коры надпочечника, кортизол, митотан
Короткий адрес: https://sciup.org/140307400
IDR: 140307400 | DOI: 10.18027/2224-5057-2024-14-3s2-1.1-22
Текст статьи Рак коры надпочечника
Рак коры надпочечника — редкая агрессивная злокачественная опухоль, исходящая из коркового слоя надпочечника. Заболеваемость составляет 1–2 случая на 1 миллион населения, смертность не превышает 0,2% смертей от всех злокачественных новообразований. Около 60% опухолей — гормонально активные и продуцируют кортизол, половые гормоны, альдостерон. Рак коры надпочечника в Российской Федерации входит в перечень орфанных заболеваний. Лечение проводится только в специализированных медицинских учреждениях.
1. КЛАССИФИКАЦИЯ И ОПРЕДЕЛЕНИЕ СТАДИИ
Стадирование рака коры надпочечника должно проводиться по системе TNM/UICC (8-е издание, 2017 г., табл. 1 и 2).
Таблица 1. Стадирование рака коры надпочечника по TNM
|
Т — первичная опухоль |
|
|
Тх |
Первичная опухоль не может быть оценена |
|
Т0 |
Отсутствуют данные о первичной опухоли |
|
Т1 |
Опухоль не более 5 см в наибольшем измерении без инвазии за пределы надпочечника |
|
Т2 |
Опухоль более 5 см без инвазии за пределы надпочечника |
|
Т3 |
Опухоль любого размера с очаговой инвазией, но без прорастания в прилежащие органы |
|
Т4 |
Опухоль любого размера с инвазией в смежные органы (почка, печень, диафрагма, поджелудочная железа, крупные сосуды); опухолевый тромбоз почечной вены или НПВ |
|
N — регионарные лимфоузлы |
|
|
Nx |
Регионарные лимфоузлы не могут быть оценены |
|
N0 |
Регионарные лимфоузлы не поражены |
|
N1 |
Метастазы в регионарных лимфоузлах |
|
M — отдаленные метастазы |
|
|
M0 |
Отдаленных метастазов нет |
|
M1 |
Есть отдаленные метастазы |
Таблица 2. Группировка по стадиям рака коры надпочечника согласно классификации UICC
|
Стадия UICC |
T |
N |
M |
|
I |
T1 |
N0 |
M0 |
|
II |
T2 |
N0 |
M0 |
|
III |
T1–2 T3–4 |
N1 N0–1 |
M0 M0 |
|
IV |
T1–4 |
N0–1 |
M1 |
Прогностически более достоверной считается классификация по ENSAT (табл. 3).
Таблица 3. Соотношение стадий рака коры надпочечника в классификациях TNM и ENSAT
|
ENSAT |
TNM |
Определение |
|
I |
T1N0M0 |
Размер < 5 см |
|
II |
T2N0M0 |
Размер > 5 см |
|
III |
T1–2N1M0 T3–4N0–1M0 |
Метастазы в лимфоузлах, опухолевая инфильтрация соседних органов и почки и/или тромбоз нижней полой вены |
|
IV |
T1–4N1–2M1 |
Отдаленные метастазы |
2. ДИАГНОСТИКА
Диагноз рака коры надпочечника основывается на данных осмотра, результатах инструментальных методов обследования и патоморфологическом заключении. Диагностика производится в рамках дифференциального диагноза с другими опухолями надпочечников, наиболее часто выявляемыми случайно. В случае обнаружения опухоли надпочечника размером более 1 см в первую очередь рекомендовано определить гормональную активность данного образования.
Дооперационная морфологическая диагностика при подозрении на первичную злокачественную опухоль надпочечника проводится редко. Пункционная биопсия целесообразна лишь при подозрении на метастатическое поражение надпочечников, при котором чувствительность цитологического исследования составляет 80–86%. При других вариантах опухолей надпочечников диагностическая ценность предоперационной пункционной биопсии низкая и связана с риском таких осложнений как разрыв капсулы опухоли с перитонеальной диссеминацией, развитием гипертонического криза у пациентов с феохромоцитомой. Перед пункционной биопсией необходимо исключить гиперпродукцию катехоламинов опухолью путем оценки их концентрации в крови и суточной моче.
Первичное обследование должно быть проведено до всех видов лечебных воздействий и включает в себя:
сбор анамнеза и физикальный осмотр;
подавляющий тест с 1 мг дексаметазона (в 23:00) и последующим определением кортизола в сыворотке крови в утренние часы;
определение АКТГ в сыворотке крови в утренние часы;
определение экскреции свободного кортизола в суточной моче;
определение стероидных гормонов сыворотки крови (дегидроэпиандростеронсульфат, 17-оксипрогестерон, андростендион, тестостерон, 17-β-эстрадиол у мужчин и женщин в менопаузе);
определение соотношения между уровнем альдостерона и активностью ренина плазмы (у пациентов с АГ и/или гипокалиемией);
развернутый клинический и биохимический анализы крови, расширенную коагулограмму;
УЗИ органов брюшной полости, КТ органов брюшной полости с в/в контрастированием;
R-графию органов грудной клетки, КТ органов грудной клетки;
сцинтиграфию костей скелета (при подозрении на метастатическое поражение костей скелета);
МРТ/КТ головного мозга с в/в контрастированием (при подозрении на метастатическое поражение головного мозга);
ПЭТ с 18ФДГ/ПЭТ-КТ;
прямую ангиографию (для оценки инвазии крупных сосудов, опухолевого тромбоза почечной вены и НПВ);
определение уровня MSI в опухоли (ПЦР, ИГХ) при местнораспространенном или метастатическом раке коры надпочечника.
Рекомендуемый алгоритм лечебно-диагностических мероприятий при раке коры надпочечника представлен на рис. 1.
3. ЛЕЧЕНИЕ 3.1. Лечение локализованных стадий ракакоры надпочечника
Хирургическое удаление опухоли единым блоком без повреждения капсулы опухоли при локализованных стадиях болезни (I–III ст.) — единственный метод, позволяющий излечить больного раком коры надпочечника. При низком риске рецидива заболевания после выполнения радикальной резекции (R0) и при Ki-67 ≤ 10%, I–II стадии рекомендовано динамическое наблюдение.
При высоком риске рецидива (микроскопическая инвазия в сосуды, капсулу опухоли, Ki-67 > 10%, повреждение капсулы опухоли во время операции, III стадия, резекция R1) рекомендована адъювантная терапия. В качестве адъювантной лекарственной терапии применяется ингибитор стероидогенеза митотан, который проявляет адренолитическую активность, действуя на пучковую и частично сетчатую зону, и приводит к клеточной дегенерации коры надпочечника, не затрагивая клубочковую зону. Наряду с противоопухолевым воздействием, митотан повреждает внутриклеточные ферменты, участвующие в синтезе стероидов, таким образом, снижает интенсивность надпочечникового стероидогенеза. Продолжительность приема митотана в качестве адъювантной терапии составляет 2 года, но не должна превышать 5 лет.
Назначение адъювантной ХТ при раке коры надпочечника остается предметом дискуссий. Адъювантная ХТ может быть рекомендована в отдельных случаях при очень высоком риске рецидива (Ki 67 ≥ 20%, обширная сосудистая инвазия, наличие опухолевого тромба в НПВ, IV стадия или резекция R1). В качестве адъювантной терапии в сочетании с митотаном может быть использована комбинация противоопухолевых препаратов этопозида и цисплатина/карбоплатина в количестве от 4 до 6 курсов.
Адъювантная ЛТ может быть рекомендована при высоком риске локального рецидива, например, при резекции R1 или Rx или III ст. Паллиативная ЛТ является методом выбора при метастазах в костях и головном мозге (30–40 Гр).
-
3.2. Лечение распространенного рака коры надпочечника
Пациенты с неоперабельным раком коры надпочечника, наличием распространённого метастатического процесса после резекции первичной опухоли, быстрым прогрессированием заболевания должны получать цитотоксическую терапию в комбинации с мито-таном. Пациенты с медленной прогрессией, олигометастатической болезнью в качестве первичного лечения могут получать монотерапию митотаном, возможно в комбинации с циторедуктивными операциями. Наиболее эффективной схемой ХТ при распространенном раке коры надпочечника является комбинация этопозида, доксорубицина и цисплатина на фоне постоянного приема митотана (EDP-M). При наличии противопоказаний к назначению антрациклинов рекомендуется проводить цитотоксическую терапию по схеме «этопозид + цисплатин/карбоплатин» на фоне постоянного приема митотана (табл. 4).
Таблица 4. Рекомендуемый режим химиотерапии I линии распространенного рака коры надпочечника
|
EDP-M1 |
Этопозид 100 мг/м 2 в/в во 2–4-й дни + доксорубицин 40 мг/м 2 в/в в 1-й день + цисплатин 40 мг/м 2 в/в в 3-й и 4-й дни, 1 раз в 28 дней, 6–8 курсов + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно |
|
EP-M1 |
Этопозид 100 мг/м 2 в/в в 1–3-й дни + цисплатин 75 мг/м 2 в/в в 1-й день каждые 21 день + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно |
|
EC–M1 |
Этопозид 100 мг/м 2 в/в в 1–3-й дни + карбоплатин AUC5 в/в в 1-й день каждые 21 день + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно |
1 В данный режим (кроме митотана) входят препараты, не зарегистрированные по показанию адренокортикальный рак.
Следует рассмотреть добавление локальных методов контроля (хирургическое лечение, стереотаксическая лучевая терапия/хирургия, интервенционные вмешательства) у пациентов с олигометастатическим заболеванием при длительности контроля заболевания на фоне системной терапии не менее 6 мес.
Пациентам с прогрессированием в сроки ≥ 6 мес. после завершения платиносодержащей ХТ по поводу метастатического рака коры надпочечника следует рассмотреть проведение реиндукции платиносодержащей ХТ на фоне продолжающегося приема митотана.
Во II линии лечения рака коры надопочечника может применяться комбинация гемцитабина и капецитабина на фоне постоянного приема митотана (табл. 5). В качестве III линии терапии возможно назначение темозоломида в монорежиме или в комбинации с митотаном.
Таблица 5. Рекомендуемые режимы химиотерапии, применяемые во II–III линиях лечения распространенного рака коры надпочечника
Гемцитабин1 800 мг/м 2 в/в в 1-й и 8-й дни каждые 21 день + капецитабин 1650–2000 мг/м 2 внутрь 1–14-й дни каждые 21 день + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
Гемцитабин1 800 мг/м 2 в/в в 1-й и 8-й дни каждые 21 день + капецитабин 1500 мг/сут. внутрь ежедневно до прогрессирования заболевания или неприемлемой токсичности + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
Темозоломид1 150–200 мг/м 2 внутрь в 1–5-й дни цикла каждые 28 дней ± митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
-
3.3. Рекомендации по лечению митотаном
Терапию митотаном начинают с дозы 0,5–1 г/ сут. с последующим повышением на 1 г каждые 4–7 дней до 4–6 г/сут. ежедневно. Препарат принимается 2–3 раза в сутки во время еды. Повышение дозы регулируется:
-
• достигнутой терапевтической концентрацией (14–20 мг/ л);
-
• переносимостью препарата.
Проверять уровень митотана в крови необходимо:
-
• каждые 6–8 нед. до достижения целевой концентрации;
-
• при сохранении концентрации митотана в пределах терапевтического диапазона в течение ≥ 6 мес. в дальнейшем возможен контроль концентрации митотана каждые 3 мес.
-
3.4. Рекомендации по заместительной терапии при лечении митотаном
Определение уровня митотана в крови необходимо при возникновении побочных эффектов.
В связи с возможностью блокирования синтеза кортизола и опасностью развития острой надпочечниковой недостаточности больные, получающие митотан, должны также получать заместительную терапию ГКС, она начинается с первого дня терапии митота-ном и продолжается после завершения его приема. Исключения составляют пациенты с метастатическим раком коры надпочечника с выраженным гиперкортицизмом, которым терапия митотаном может быть начата без заместительной терапии ГКС. Рекомендуемые дозы ГКС, используемые для заместительной терапии:
• гидрокортизон 50–75 мг/сут. или
• кортизона ацетат 75–100 мг / сут. или
• преднизолон 10–20 мг/сут.
4. НАБЛЮДЕНИЕ
Оценка эффективности заместительной терапии производится по клиническим критериям. Оценивать минералокортикоидную недостаточность необходимо по уровню электролитов с последующей коррекцией флудрокортизоном. Гипогонадизм у мужчин оценивается по клиническим проявлениям (эректильная дисфункция, гинекомастия) и подтверждается гормональной оценкой с последующим назначением заместительной терапии. Вторичный гипотиреоз (ТТГ — норма, свободный Т4 снижен) также требует заместительной терапии.
Наблюдение рекомендуется проводить, ориентируясь на общие онкологические принципы наблюдения за пациентами после хирургических вмешательств и/или ХТ. Периодичность визитов составляет 1 раз в 3 мес. в течение 1-го года, 1 раз в 6 мес. — в течение 2-го года, в дальнейшем пожизненно 1 раз в год.
Опухоль резектабельна
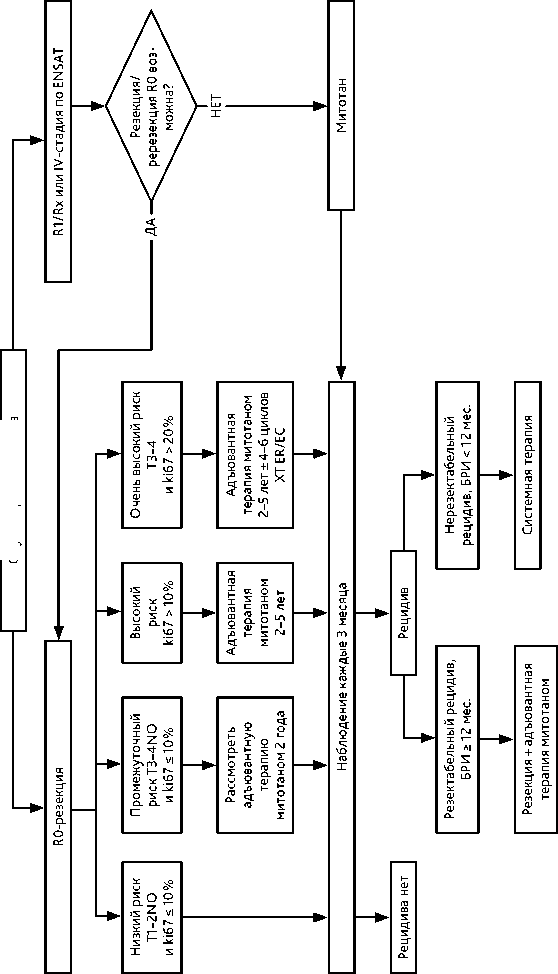
Рисунок 1. Алгоритм лечения адренокортикального рака
том /vol. 14(3s2) 2024
ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ
Malignant Tumors


