Рак коры надпочечника
Автор: Горбунова В.А., Бельцевич Д.Г., Бохян В.Ю., Жуликов Я.A., Коломейцева А.А., Мельниченко Г.А., Феденко А.А.
Журнал: Злокачественные опухоли @malignanttumors
Статья в выпуске: 3S2-1.1 т.15, 2025 года.
Бесплатный доступ
В данном разделе указаны критерии оценки клинической значимости применения дорогостоящей противоопухолевой лекарственной терапии в соответствии со шкалой, разработанной экспертной группой (см. стр. 7). В тексте они обозначены, как магнитуда клинической значимости (МКЗ).
Рак коры надпочечника, кортизол, митотан
Короткий адрес: https://sciup.org/140312948
IDR: 140312948 | DOI: 10.18027/2224-5057-2025-15-3s2-1.1-22
Текст научной статьи Рак коры надпочечника
Рак коры надпочечника — редкая злокачественная опухоль, исходящая из коркового слоя надпочечника. Заболеваемость составляет 1–2 случая на 1 миллион населения, смертность не превышает 0,2% смертей от всех злокачественных новообразований. Частота гормонально активных опухолей колеблется по различным данным от 30 до 60%, включая также так называемую субклиническую активность. В преобладающем большинстве случаев гормональная активность проявляется гиперкортицизмом (продукция глюкокортикостериодов). Рак коры надпочечника в Российской Федерации входит в перечень орфанных заболеваний. Лечение проводится только в специализированных медицинских учреждениях.
1. КЛАССИФИКАЦИЯ И ОПРЕДЕЛЕНИЕ СТАДИИ
Стадирование рака коры надпочечника должно проводиться по системе TNM/UICC (8-е издание, 2017 г., табл. 1 и 2).
Таблица 1. Стадирование рака коры надпочечника по TNM
Т — первичная опухоль
Тх Первичная опухоль не может быть оценена
Т0 Отсутствуют данные о первичной опухоли
Т1 Опухоль не более 5 см в наибольшем измерении
Т2 Опухоль более 5 см в наибольшем измерении
Т3 Опухоль любого размера с выходом за пределы капсулы, но без прорастания в прилежащие органы
Т4 Опухоль любого размера с инвазией в смежные органы (почка, печень, диафрагма, поджелудочная железа, крупные сосуды); опухолевый тромбоз почечной вены или НПВ
N — регионарные лимфоузлы
Nx Регионарные лимфоузлы не могут быть оценены
N0 Регионарные лимфоузлы не поражены
N1 Метастазы в регионарных лимфоузлах (аортокавальные/паранефральные)
M — отдаленные метастазы
M0 Отдаленных метастазов нет
M1 Есть отдаленные метастазы
Таблица 2. Группировка по стадиям рака коры надпочечника согласно классификации UICC
|
Стадия UICC |
T |
N |
M |
|
I |
T1 |
N0 |
M0 |
|
II |
T2 |
N0 |
M0 |
|
III |
T1–2 |
N1 |
M0 |
|
T3–4 |
N0–1 |
M0 |
|
|
IV |
T1–4 |
N0–1 |
M1 |
Прогностически более достоверной считается классификация по ENSAT (табл. 3).
Таблица 3. Соотношение стадий рака коры надпочечника в классификациях TNM и ENSAT
|
ENSAT |
TNM |
Определение |
|
I |
T1N0M0 |
Размер < 5 см |
|
II |
T2N0M0 |
Размер > 5 см |
|
III |
T1–2N1M0 T3–4N0–1M0 |
Метастазы в лимфоузлах, опухолевая инфильтрация соседних органов и почки и/или тромбоз нижней полой вены |
|
IV |
T1–4N1–2M1 |
Отдаленные метастазы |
2. ДИАГНОСТИКА
Диагноз рака коры надпочечника основывается на данных осмотра, результатах инструментальных методов обследования и патоморфологическом заключении. Диагностика производится в рамках дифференциального диагноза с другими опухолями надпочечников, наиболее часто выявляемыми случайно. В случае обнаружения опухоли надпочечника размером более 1 см в первую очередь рекомендовано определить гормональную активность данного образования.
Диагностика адренокортикального рака основывается на лучевых методах диагностики, в первую очередь на КТ с динамическим внутривенным контрастированием и оценкой злокачественного потенциала опухоли на основании изучения плотностных характеристик опухоли на разных фазах контрастирования.
Дооперационная морфологическая диагностика при подозрении на первичную злокачественную опухоль надпочечника проводится редко. Пункционная биопсия целесообразна лишь при подозрении на метастатическое поражение надпочечников. При других вариантах опухолей надпочечников диагностическая ценность предоперационной пункционной биопсии низкая и связана с риском таких осложнений как разрыв капсулы опухоли с перитонеальной диссеминацией, развитием гипертонического криза у пациентов с феохромоцитомой. Перед пункционной биопсией необходимо исключить гиперпродукцию катехоламинов опухолью путем оценки их концентрации в крови и суточной моче.
Первичное обследование должно быть проведено до всех видов лечебных воздействий и включает в себя:
• сбор анамнеза и физикальный осмотр;
• подавляющий тест с 1 мг дексаметазона (в 23:00) и последующим определением кортизола в сыворотке крови в утренние часы;
• определение АКТГ в сыворотке крови в утренние часы;
• определение стероидных гормонов сыворотки крови (дегидроэпиандростеронсульфат, андростендион, тестостерон, 17-β-эстрадиол у мужчин и женщин в менопаузе);
• определение соотношения между уровнем альдостерона и активностью ренина плазмы (у пациентов с АГ и/или гипокалиемией);
• развернутый клинический и биохимический анализы крови, расширенную коагулограмму;
• КТ органов брюшной полости с в / в контрастированием;
• КТ органов грудной клетки;
• МРТ брюшной полости при противопоказаниях к проведению КТ с внутривенным контрастированием;
• сцинтиграфию костей скелета (при подозрении на метастатическое поражение костей скелета);
• МРТ /КТ головного мозга с в/в контрастированием (при подозрении на метастатическое поражение головного мозга);
• ПЭТ с 18ФДГ/ ПЭТ-КТ при неоднозначных данных КТ;
• определение уровня MSI в опухоли (ПЦР, ИГХ) при местнораспространенном или метастатическом раке коры надпочечника.
3. ЛЕЧЕНИЕ
3.1. Лечение локализованных стадий рака коры надпочечника3.2. Лечение распространенного рака коры надпочечника
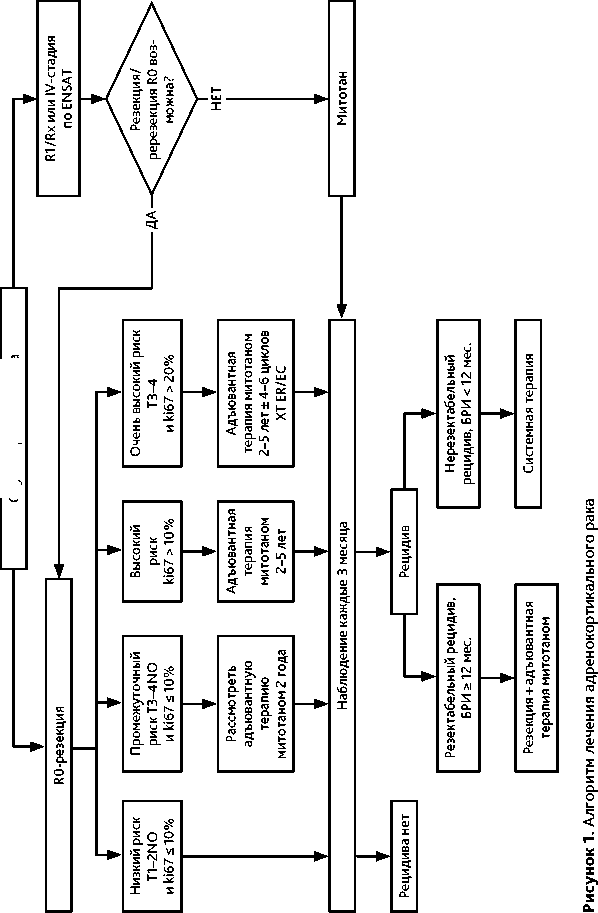
Рекомендуемый алгоритм лечебно-диагностических мероприятий при раке коры надпочечника представлен на рис. 1.
Хирургическое радикальное удаление опухоли единым блоком без повреждения капсулы опухоли при локализованных стадиях болезни (I–III ст.) — единственный метод, позволяющий излечить больного раком коры надпочечника. Адреналэктомию при раке коры надпочечника следует выполнить лапаротомным доступом. При низком риске рецидива заболевания после выполнения радикальной резекции (R0) и при Ki-67 ≤ 10%, I–II стадии рекомендовано динамическое наблюдение.
При высоком риске рецидива (микроскопическая инвазия в сосуды, капсулу опухоли, Ki-67 > 10%, повреждение капсулы опухоли во время операции, III стадия, резекция R1) рекомендована адъювантная терапия митотаном. Продолжительность приема митотана в качестве адъювантной терапии составляет от 2 до 5 лет. Длительность определяется индивидуально, исходя из переносимости и рисков прогрессирования.
Назначение адъювантной ХТ при раке коры надпочечника остается предметом дискуссий. Адъювантная ХТ может быть рекомендована в отдельных случаях при очень высоком риске рецидива (Ki 67 ≥ 20% и Т3/4 или N1). В качестве адъювантной терапии в сочетании с митотаном может быть назначена химиотерапия по схеме EP/EC или EDP в количестве от 4 до 6 курсов.
Адъювантная ЛТ может быть рекомендована при высоком риске локального рецидива, например, при резекции R1 или Rx, или III ст.
У больных с метастатическим АКР и опухолевым тромбозом нижней полой вены на первом этапе необходимо рассмотреть возможность хирургического вмешательства с тромбэктомией.
Пациентам с медленным прогрессированием, олигометастатической болезнью в качестве первичного лечения может быть назначена терапия митотаном в монорежиме, возможно в комбинации с циторедуктивными операциями.
Пациенты с неоперабельным раком коры надпочечника, наличием распространённого метастатического процесса после резекции первичной опухоли, быстрым прогрессированием заболевания должны получать цитотоксическую терапию в комбинации с митотаном. Наиболее эффективной схемой ХТ при распространенном раке коры надпочечника является комбинация этопозида, доксорубицина и цисплатина на фоне постоянного приема митотана (EDP-M). При наличии противопоказаний к назначению антрациклинов рекомендуется проводить цитотоксическую терапию по схеме этопозид + цисплатин/карбоплатин на фоне постоянного приема митотана (табл. 4).
Паллиативная ЛТ является методом выбора при метастазах в костях и головном мозге (30–40 Гр).
|
Таблица 4. Рекомендуемые режимы химиотерапии I линии распространенного рака коры надпочечника |
||
|
Режим |
Класс клинической значимости |
|
|
EDP-M1 |
Этопозид 100 мг/м 2 в/в во 2–4-й дни + доксорубицин 40 мг/м 2 в/в в 1-й день + цисплатин 40 мг/м 2 в/в в 3-й и 4-й дни, 1 раз в 28 дней, 6–8 курсов + мито-тан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно |
IIB |
|
EP-M1 |
Этопозид 100 мг/м 2 в/в в 1–3-й дни + цисплатин 75 мг/м 2 в/в в 1-й день каждые 21 день + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно |
IIB |
|
EC-M1 |
Этопозид 100 мг/м 2 в/в в 1–3-й дни + карбоплатин AUC5 в/в в 1-й день каждые 21 день + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно |
IIB |
1 В данный режим (кроме митотана) входят препараты, не зарегистрированные по показанию адренокортикальный рак.
Следует рассмотреть добавление локальных методов контроля (хирургическое лечение, стереотаксическая лучевая терапия/хирургия, интервенционные вмешательства) у пациентов с олигометастатическим заболеванием при длительности контроля заболевания на фоне системной терапии не менее 6 мес.
Пациентам с прогрессированием в сроки ≥ 6 мес. после завершения платиносодержащей ХТ по поводу метастатического рака коры надпочечника следует рассмотреть проведение реиндукции платиносодержащей ХТ на фоне продолжающегося приема митотана.
. Рекомендуется сохранять терапию митотаном как минимум в течение двух линий лечения. В третьей и последующих линиях терапии у пациентов с бесплатиновым интервалом < 6 мес. при отсутствии признаков гиперкортицизма и плохой переносимости митотана, возможна его отмена, при этом заместительная терапия гидрокортизоном продолжается.
В качестве 2-й и последующих линий лечения рака коры надопочечника могут применяться: комбинация гемцитабина и капецитабина, темозоломид, пембролизумаб и кабозантиниб (табл. 5).
В качестве II и последующих линий может быть рекомендован пембролизумаб (табл. 5). Лечение пембролизумабом может быть эффективным при прогрессирующем на предшествующих режимах ХТ распространенном раке коры надпочечников независимо от уровня MSI. В исследованиях II фазы частота объективного ответа на терапию пембро-лизумабом варьирует от 14 до 23%, а контроль болезни наблюдается примерно у 50% больных. Препарат может быть назначен по решению врачебной комиссии.
Кабозантиниб продемонстрировал свою эффективность в качестве второй и последующих линий терапии АКР в одном ретроспективном и одном проспективном исследовании
II фазы, ЧОО 11%, частота контроля болезни ≥ 4 мес. — 72%, медиана выживаемости без прогрессирования 6 мес. Назначение кабозантиниба требует отмены митотана, поскольку митотан является индуктором экспрессии CYP3A4, что приводит к быстрому метаболизму и снижению концентрации кабозантиниба. При этом заместительная терапия гидрокортизоном продолжается. В клиническом исследовании кабозантиниб назначался только пациентам с концентрацией митотана в плазме крови < 2 мкг/мл. Поскольку продолжение митотана в комбинации с химиотерапией во второй линии лечения повышает эффективность терапии, кабозантиниб может быть назначен в качестве третьей и последующих линий терапии по решению врачебной комиссии.
Рекомендуемый алгоритм лечения распространенного рака коры надпочечника представлен на рис. 1
Таблица 5. Рекомендуемые режимы химиотерапии, применяемые во II–III линиях лечения распространенного рака коры надпочечника
Уровень клинической
Режим значимости
Гемцитабин1 800 мг/м 2 в/в в 1-й и 8-й дни каждые 21 день + капецитабин 1650–2000 мг/м 2 IID внутрь 1–14-й дни каждые 21 день + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
Гемцитабин1 800 мг/м2 в/в в 1-й и 8-й дни каждые 21 день + капецитабин 1500 мг/сут. IID внутрь ежедневно до прогрессирования заболевания или неприемлемой токсич ности + митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
Темозоломид1 150–200 мг/м2 внутрь в 1–5-й дни цикла каждые 28 дней ± митотан IID ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
Пембролизумаб1 200 мг в/в кап. 1 раз в 3 нед. или 400 мг 1 раз в 6 нед. до прогресси- IID рования или неприемлемой токсичности, но не более 2 лет ± митотан ежедневно в дозе, обеспечивающей его содержание в сыворотке крови на уровне 14–20 мкг/мл, непрерывно
Кабозантиниб1,2,3 60 мг внутрь 1 раз в сутки ежедневно до прогрессирования заболевания IID или неприемлемой токсичности
-
3.3. Рекомендации по лечению митотаном
Терапию митотаном начинают с дозы 1–2 г/сут. с последующим повышением на 1 г каждые 4–7 дней до 4–6 г/сут. ежедневно. Препарат принимается 2–3 раза в сутки во время еды. Повышение дозы регулируется:
-
• достигнутой терапевтической концентрацией (14–20 мг/л);
-
• переносимостью препарата.
Проверять уровень митотана в крови необходимо:
-
• через 4 недели от момента выхода на дозу 4 или 6 г /сут;
-
• каждые 6–8 нед. до достижения целевой концентрации;
-
• при сохранении концентрации митотана в пределах терапевтического диапазона в течение ≥ 6 мес. в дальнейшем возможен контроль концентрации митотана каждые 3 мес.
-
3.4. Рекомендации по заместительной терапии при лечении митотаном
Определение уровня митотана в крови необходимо при возникновении побочных эффектов.
В связи с возможностью блокирования надпочечникового стероидогенеза и опасностью развития острой надпочечниковой недостаточности все пациенты без гиперкортицизма, получающие митотан, должны также получать заместительную терапию ГКС, она начинается с первого дня терапии митотаном и продолжается после завершения его приема. У пациентов с гиперкортицизмом заместительная терапия должна быть назначена при появлении клинических или лабораторных признаков надпочечниковой недостаточности. В небольшом наблюдательном исследовании было показано, что у 78,3% больных гипоталамо-гипофизарно-надпочечниковая система полностью восстанавливается после отмены митотана, а медиана времени до ее восстановления — 2,5 года. Таким образом заместительная терапия ГКС продолжается даже после завершения адъювантной терапии митотаном. Решение вопроса о снижении суточной дозы или отмене ГКС возможно только после лабораторного обследования под контролем эндокринолога. Рекомендуемые дозы ГКС, используемые для заместительной терапии:
• гидрокортизон 50–75 мг / сут. или
• кортизона ацетат 75–100 мг /сут. или
• преднизолон 12.5–25 мг/сут.
4. НАБЛЮДЕНИЕ
При присоединении интеркуррентных заболеваний, стрессе (психологические или тяжелые физические нагрузки) необходимо увеличивать дозу ГКС в 1.5–3 раза на время острой фазы заболевания или момент воздействия стресса. В дальнейшем целесообразен возврат к обычной заместительной дозе, которую пациент принимал до болезни.
В случае невозможности перорального приема ГКС по любым причинам, возникновения любых острых состояний необходим переход на парентеральный путь введения ГКС.
Оценка эффективности заместительной терапии производится по клиническим критериям. Оценивать минералокортикоидную недостаточность необходимо с учетом параметров гемодинамики по уровню электролитов и ренина с последующей коррекцией флудрокортизоном. Гипогонадизм у мужчин оценивается по клиническим проявлениям (эректильная дисфункция, гинекомастия) и подтверждается гормональной оценкой с последующим назначением заместительной терапии. Вторичный гипотиреоз (ТТГ — норма или снижен, свободный Т4 снижен, свободный Т3 снижен) также требует заместительной терапии.
Наблюдение рекомендуется проводить, ориентируясь на общие онкологические принципы наблюдения за пациентами после хирургических вмешательств и/или ХТ. Периодичность визитов составляет 1 раз в 3 мес. в течение 1-го года, 1 раз в 6 мес. — в течение 2-го года, в дальнейшем пожизненно 1 раз в год. В объем обследований входит КТ. ПЭТ-КТ рекомендуется проводить только при подозрении на метастатический процесс по данным КТ.
Опухоль резектабельна
| том/vol. 15(3s2)2025
ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ
Malignant Tumors


