Рак молочной железы у молодых женщин: современные данные об эпидемиологии, клинических особенностях и персонализированных подходах к лечению и профилактике
Автор: Блинова К.А., Кострыгин А.К., Малеева А.М., Алексеев В.В., Фролова Д.Е., Золкина М.А., Блинова А.А., Копышева Е.Н., Гудухин А.А., Мишина И.Е.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Обзоры
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Цель исследования – провести систематический анализ современных данных об эпидемиологии и факторах риска рака молочной железы (РМЖ), разработать стратегию профилактики для групп высокого риска, составить клинический профиль молодых пациенток с РМЖ и описать особенности их лечения и реабилитации. Материал и методы. Поиск проводился в базах данных Web of Science, PubMed, Scopus, Google Scholar. В обзоре использовано 60 источников (систематические обзоры, метаанализы, рандомизированные клинические исследования), оцениваемое вмешательство представляло сравнительный анализ факторов риска, клинической картины, диагностики, лечения и реабилитации РМЖ у молодых пациенток и пациенток старшего возраста. Результаты. Рак молочной железы является серьезной проблемой для женщин в возрасте до 40 лет, являясь второй по значимости причиной смертности от рака в этой возрастной группе во всем мире. При этом наблюдается тревожная тенденция к увеличению заболеваемости РМЖ у молодых женщин. Отсутствие программ скрининга, ориентированных на молодых женщин, приводит к диагностике РМЖ на более поздних стадиях, что негативно сказывается на клинических исходах и увеличивает риск осложнений лечения по сравнению с пациентками старшего возраста. Патоморфология опухолей, выявленных у молодых женщин, характеризуется низкой дифференцировкой клеток, повышенной экспрессией Ki67, наличием генных мутаций и преобладанием HER2-позитивных и трижды негативных иммуногистохимических подтипов. Несмотря на очевидные различия, исследований РМЖ у молодых женщин недостаточно, что создает пробелы в понимании его факторов риска, диагностики, прогноза и лечения. Отсутствие репрезентативных клинических данных с возрастной стратификацией и доказательной базы делает невозможным экстраполяцию стандартных протоколов лечения, валидированных для пациенток старшего возраста, на популяцию молодых женщин. Заключение. Необходимы дальнейшие исследования для сбора возрастных клинических данных и разработки новых методов лечения рака молочной железы у молодых женщин, что позволит улучшить результаты лечения и определить перспективные направления исследований в этой области.
Рак молочной железы, рак у молодых, возрастные особенности рака, генетические факторы риска, BRCA1/2, HER2-позитивный рак, тройной негативный рак, мультидисциплинарная команда
Короткий адрес: https://sciup.org/140314352
IDR: 140314352 | УДК: 618.19-006.6-053.84-08:616-084 | DOI: 10.21294/1814-4861-2026-25-1-107-122
Breast cancer in young women: current data on epidemiology, clinical features and personalised approaches to treatment and prevention
Objectives: to conduct a systematic review of current data on breast cancer epidemiology and risk factors; to develop a clinical profle of young breast cancer patients and describe approaches to their treatment and rehabilitation; to develop a prevention strategy for high-risk groups. Material and Methods. A search was conducted in the Web of Science, PubMed, Scopus, and Google Scholar databases. The review incorporated 60 sources (systematic reviews, meta-analyses, randomized clinical trials). A comparative analysis of risk factors, clinical presentation, diagnosis, treatment, and rehabilitation of young breast cancer patients compared to elderly patients was conducted. Results. Breast cancer poses a signifcant health challenge for women aged under 40 years, representing the second leading cause of cancer-related mortality in this age group worldwide. A trend towards an increase in breast cancer incidence is observed among young women. The lack of tailored breast cancer screening for young women causes signifcant diagnostic delays, leading to late-stage cancer at detection, negatively impacting clinical outcomes and increasing the risk of treatmentrelated complications compared to elderly patients. Pathomorphology of tumors detected in young women is characterized by poorly differentiated cells, increased Ki67 expression, the presence of gene mutations, and a predominance of HER2-positive and triple-negative immunohistochemical subtypes. Despite these evident differences, research on breast cancer in young women remains insuffcient, creating gaps in understanding its risk factors, diagnosis, prognosis, and treatment. A lack of age-specifc clinical data and outcomes hinders the adaptation of standard treatment approaches, developed for elderly patients, to the needs of young women. Conclusion. Further research is needed to collect age-specifc clinical data and develop novel treatment strategies for breast cancer in young women, ultimately improving treatment outcomes and identifying promising research directions in this area.
Текст научной статьи Рак молочной железы у молодых женщин: современные данные об эпидемиологии, клинических особенностях и персонализированных подходах к лечению и профилактике
В последнее время рак молочной железы (РМЖ) у молодых женщин стал объектом пристального внимания исследователей. Согласно данным Global Cancer Observatory (GLOBOCAN) и Global Burden of Disease, в 2022 г. частота РМЖ у женщин в мире составила 2,3 млн случаев, занимая вторую позицию среди самых распространенных онкологических заболеваний (23,4 % от всех случаев рака) и четвертое место среди причин смертности от всех видов рака (666 000 смертей в год, 6,9 %) [1]. В Российской Федерации, по данным 2023 г., РМЖ является самым распространенным злокачественным новообразованием (22,5 %) и причиной смерти у 15,9 % женщин. В структуре заболеваемости у пациенток молодого возраста РМЖ имеет наибольший удельный вес (30–59 лет – 29,2 %), являясь причиной смерти каждой пятой женщины (30–39 лет – 23,1 %; 40–49 лет – 23,3 %; 50– 59 лет – 20,3 %) [2].
В контексте РМЖ не существует общепринятого определения «молодая женщина». Предыдущие работы использовали различные критерии возраста, включая порог в 35 лет [3], разделение на группы до и после 40 лет [4], а также учет менопаузального статуса [5]. На данный момент консенсусные руководящие принципы Европейской школы онкологии и Европейского общества медицинской онкологии (ESMO) считают «молодой женщиной» пациентку моложе 40 лет на момент постановки диагноза РМЖ [6].
В отличие от пациенток старшего возраста, РМЖ у молодых женщин имеет свои особенности, включающие характеристику опухоли, прогноз заболевания и показатели выживаемости, выбор диагностических и терапевтических стратегий, влияние на репродуктивную функцию. Совокупность таких факторов, как низкая дифференцировка опухолевых клеток, наличие патогенных мутаций в генах и повышенная экспрессия Ki67, обусловливает более агрессивное течение РМЖ у молодых женщин и, как следствие, менее благоприятный прогноз [7]. Дополнительно неблагоприятный прогноз усугубляется тем, что молодые женщины, как правило, не охвачены программами скрининга РМЖ, что приводит к более поздней диагностике заболевания [8]. Терапия РМЖ может негативно влиять на репродуктивную функцию молодых женщин, повышая риск преждевременной овариальной недостаточности. При выборе лечения необходимо учитывать потенциальное воздействие на овариальный резерв и проводить с пациенткой совместное обсуждение тактики [9].
РМЖ у молодых женщин остается недостаточно изученным. Отсутствуют специфические клинические данные и данные о результатах лечения для этой возрастной группы. Большинство стандартных методов лечения, применяемых у молодых женщин, первоначально разрабатывались и тестировались на пациентках старшего возраста.
Цель исследования – провести систематический анализ современных данных об эпидемиологии и факторах риска РМЖ. Разработать стратегию профилактики для групп высокого риска. Составить клинический профиль молодых пациенток с РМЖ и описать особенности их лечения и реабилитации.
Поиск проводился в базе данных Web of Science, PubMed, Scopus, Google Scholar по ключевым словам «рак молочной железы у молодых», «возрастные особенности рака груди». Всего на апрель 2025 г. отобрано 60 источников, из которых 17 (28,3 %) – систематические обзоры и метаанализы, 28 (46,7 %) – данные рандомизированных клинических исследований. Статьи были опубликованы в последние 15 лет, оцениваемое вмешательство представляло сравнительный анализ факторов риска, клинической картины, диагностики, лечения и реабилитации РМЖ у мо- лодых пациенток и пациенток старшего возраста. Выборка должна была включать пациенток с РМЖ моложе 40 лет, находящихся на диагностическом этапе или проходящих специализированное лечение. Результат вмешательства оценивался по частоте рецидивов, показателям выживаемости и смертности. Последний поиск осуществлялся 10 апреля 2025 г.
Географическая распространенностьРМЖ у молодых женщин
Несмотря на значимость проблемы, различия заболеваемости и смертности от РМЖ у молодых женщин в разных странах остаются недостаточно изученными по сравнению с данными по общей популяции. Показатели заболеваемости РМЖ у молодых пациенток во Франции, Австралии/Новой Зеландии, Северной Америке и Северной Европе в 4 раза превышают аналогичные показатели Южной и Центральной Азии и Средней Африки [1]. Различия в заболеваемости РМЖ, вероятно, связаны с более высокой распространенностью многочисленных факторов риска в развитых странах. К этим факторам относятся особенности репродуктивного здоровья, такие как поздние первые роды, меньшее количество родов и более короткий период грудного вскармливания. Кроме того, значительную роль играют факторы риска, связанные с образом жизни, включая использование заместительной гормональной терапии и оральных контрацептивов, употребление алкоголя, избыточный вес и недостаточную физическую активность [10]. Несмотря на то, что заболеваемость РМЖ может быть сопоставимой в разных регионах, смертность от данного заболевания значительно варьирует. Например, в Западной Африке и Северной Америке показатели заболеваемости составили 9,8 и 11,3 случая на 100 000 женщин соответственно, однако смертность в Западной Африке (6,4 случая на 100 000 женщин) существенно превышала аналогичный показатель в Северной Америке (1,8 случая на 100 000 женщин) [11]. Аналогичная тенденция наблюдается при сравнении Канады и Нигерии, где распространенность раннего РМЖ была схожей (0,61 и 0,64 % соответственно), но смертность в Нигерии более чем в 6 раз превышала канадские показатели (0,25 vs 0,04 %). В 2018 г. средний показатель риска летального исхода от РМЖ к 40 годам составил 0,08 %, однако в Африке этот показатель оказался значительно выше (0,18 %), что свидетельствует о существенных различиях в исходах заболевания в зависимости от региона [12].
Поскольку в возрастной группе до 40 лет скрининг РМЖ обычно не проводится, различия в смертности от этого заболевания между регионами (1,1–6,4 на 100 000 населения) связаны с другими факторами. Предполагается, что эти показатели обусловлены осведомленностью о симптомах, доступностью лечения и используемыми терапев- тическими подходами. В развитых странах более высокая выживаемость связана с эффективным лечением и своевременной диагностикой, тогда как в странах с низким и средним уровнем дохода смертность повышена из-за недостаточной информированности и ограниченного доступа к медицинской помощи [13].
Факторы риска развития РМЖ у молодых женщин
Факторы риска, связанные с образом жизни.
Имеющиеся данные показывают, что физическая активность и уменьшение индекса массы тела значимо снижают риск раннего начала РМЖ. Метаанализ 48 исследований, проведенный P.J. Hardefeldt et al. [14], включавший почти 4 млн человек, показал, что физическая активность значительно снижает риск развития РМЖ. В метаанализе S.Y. Cohen et al. [15] обнаружили, что у женщин, ведущих активный образ жизни, риск развития РМЖ был на 23 % ниже, чем у пациенток с низким уровнем физической активности. Физическая активность действует как защитный фактор против РМЖ в основном за счет влияния на гормональный фон, снижая концентрацию гормонов яичников. В репродуктивном возрасте интенсивная физическая активность снижает уровень эстрогенов, уменьшает частоту менструаций и объем жировой ткани, участвующей в синтезе эстрогенов. Также важное значение в прогнозировании выживаемости среди молодых женщин, у которых недавно диагностировали РМЖ, имеет соотношение площади скелетных мышц и жировой ткани. A.D. de Lima Bezerra et al. [16] продемонстрировали, что низкая мышечная масса, измеряемая как индекс скелетных мышц при компьютерной томографии, является значимым предиктором повышенной смертности (9 % на каждое снижение индекса на 1 см2/м2).
Связанные с профессией длительные ночные смены в молодом возрасте могут быть еще одним фактором, способствующим повышению риска развития РМЖ. Считается, что работа в ночную смену нарушает циркадный ритм, поскольку ночное освещение подавляет выработку эпифизом мелатонина. Мелатонин способен подавлять рост опухоли, снижая выработку эстрогенов [17]. Исследования показали, что у женщин, когда-либо работавших в ночную смену, вероятность развития РМЖ до наступления менопаузы на 26 % выше, чем у тех, кто не работал в таких условиях. При этом риск возрастает с увеличением частоты и продолжительности работы ночью [18]. Анализ крупного исследования здоровья медсестер, длившегося 24 года и охватившего более 116 тыс. женщин в возрасте 25–42 лет, показал, что у пациенток, работающих в ночные смены более 20 лет, риск развития РМЖ на 40 % выше, чем у тех, кто никогда не работал ночью [19].
Генетические факторы риска
Наследственная природа РМЖ может быть заподозрена при отягощенном семейном анамнезе по РМЖ, наличии нескольких локализаций рака у одного человека (рак яичников, рак поджелудочной железы), поражении обеих молочных желез или мультифокальности заболевания. Выявление генетических мутаций на ранних стадиях и обследование членов семьи крайне важны для профилактики и лечения. Для более детального изучения генетических изменений, связанных с наследственным РМЖ, используются секвенирование нового поколения (NGS) и анализ генетических маркеров с использованием ДНК-микрочипов.
Генетические мутации можно разделить на группы в зависимости от степени риска развития рака: мутации с высоким риском (более чем в 5 раз), умеренным риском (в 1,5–5 раз) и низким риском (менее чем в 1,5 раза). Наследственные факторы составляют примерно 5–10 % всех случаев РМЖ и вызваны мутациями в генах с высокой или средней пенетрантностью [20].
Гены с высокой пенетрантностью включают BRCA1, BRCA2, TP53, PTEN, STK11, CDH1 и PALB2 [20]. Мутации в генах BRCA1 и BRCA2 являются наиболее распространенными генетическими предикторами наследственного РМЖ, обусловливая до 40 % случаев. Данные метаанализов и результаты исследований, включая CARRIERS и анализ Консорциума Ассоциации по борьбе с РМЖ, демонстрируют, что наличие мутаций в этих генах ассоциировано с существенным повышением риска развития РМЖ в молодом возрасте, достигая 9,4–12 % к 40 годам [21, 22]. Важно отметить, что мутации в гене BRCA1 демонстрируют более сильную ассоциацию с повышенным риском, превосходя по данному показателю BRCA2 .
Гены семейства RAD51 (RAD51B, RAD51C, RAD51D, XRCC2 и XRCC3 ), участвующие в ответе на повреждения ДНК и гомологичной рекомбинации, также связаны с риском РМЖ. Анализ данных более 113 тыс. женщин выявил ассоциацию между мутациями в генах RAD51C и RAD51D и повышенным риском РМЖ к 40 годам [22]. Исследование генетических данных 7 216 семей показало, что мутации в RAD51C сильнее повышают риск РМЖ у женщин 20–49 лет, чем у женщин старше 50 лет, в то время как мутации в RAD51D увеличивают риск примерно одинаково в обеих возрастных группах [28].
Репродуктивные факторы риска
Гормональные и репродуктивные факторы, в частности, использование гормональных контрацептивов, заместительной гормональной терапии, а также беременность и грудное вскармливание, могут оказывать влияние на риск развития РМЖ у молодых женщин. В странах с высоким уровнем дохода отмечается увеличение использования гормональных препаратов, таких как комбинированные оральные контрацептивы (КОК) и менопаузальная гормональная терапия (МГТ), а также тенденция к снижению рождаемости и поздним первым родам. Использование гормональных контрацептивов (КОК) может оказывать влияние на риск развития РМЖ. Данные свидетельствуют о том, что у женщин с высоким риском РМЖ влияние КОК может быть аналогичным общей популяции [29]. Крупное проспективное когортное исследование L.S. Mørch et al. [31], включавшее 1,8 млн датских женщин, показало, что текущее или недавнее использование КОК ассоциировано с повышенным риском РМЖ, причем увеличение продолжительности использования КОК коррелирует с увеличением риска [30]. Систематический обзор и метаанализ также выявили связь между использованием левоноргестрел-содержащих вну-триматочных систем и повышенным риском РМЖ у женщин моложе 50 лет.
Преждевременная менопауза, определяемая как наступление менопаузы в возрасте до 40 лет, является редким явлением, затрагивающим около 1 % женщин. Для облегчения климактерических симптомов и профилактики остеопороза используют МГТ, включающую эстрогены или их комбинацию с прогестинами. Крупный метаанализ 2019 г. (Collaborative Group on Hormonal Factors in Breast Cancer) не выявил значимого увеличения риска РМЖ при использовании МГТ, начатой в возрасте 30–39 лет, в течение 5–15 лет [32]. Согласно современным рекомендациям, МГТ может быть рекомендована женщинам со средним риском и преждевременной менопаузой до достижения возраста естественной менопаузы. При наличии матки предпочтительна комбинированная МГТ (эстроген и прогестин), при гистерэктомии – монотерапия эстрогенами. Важно использовать минимально эффективные дозы и ограничивать продолжительность терапии. Женщинам с высоким риском РМЖ требуется консультация специалиста для индивидуального подбора МГТ [33].
Возраст наступления беременности оказывает модулирующее влияние на риск РМЖ. В развитых странах около 13 % случаев РМЖ диагностируется в репродуктивном возрасте, 2 % – у женщин до 35 лет. Возраст первых родов влияет дифференцированно: ранние роды (до 20 лет) значительно снижают долгосрочный риск (на 50 %), поздние роды (после 35 лет) умеренно повышают его [34]. После родов наблюдается двухфазное изменение риска. В течение первых 10 лет наблюдается временное повышение риска, достигающее пика примерно через 5 лет, что, вероятно, связано с процессами инволюции молочной железы. В долгосрочной перспективе, через 34 года, риск падает до уровня ниже, чем у нерожавших женщин, что обусловлено уменьшением популяции эстроген-зависимых клеток в ткани молочной железы [35].
Грудное вскармливание ассоциируется со снижением риска РМЖ, хотя точный механизм остается не полностью изученным [36]. Наблюдается относительное снижение риска на 4 % за каждые 12 мес грудного вскармливания, при этом защитный эффект более выражен при пременопаузальном ТНГ РМЖ (5,1 %). [37]. Всемирная организация здравоохранения рекомендует поддерживать грудное вскармливание молодых матерей не менее 6 мес до отлучения от груди, чтобы воспользоваться его защитным эффектом.
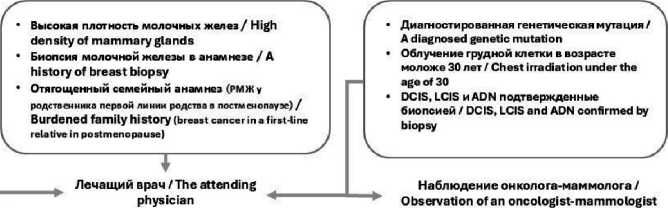
Основные факторы риска развития РМЖ у молодых женщин представлены в таблице. В целях эффективной профилактики РМЖ у молодых женщин с повышенным риском необходимо обеспечить тесное взаимодействие между лечащим врачом, генетиком и онкологом (рис. 1).
Клинико-патологическаяхарактеристика РМЖ у молодых женщин
Рак молочной железы у молодых женщин характеризуется более агрессивными клиникопатологическими характеристиками [37], что проявляется в высокой степени злокачественности, частом поражении регионарных лимфоузлов, а также повышенной лимфоваскулярной инвазии и лимфоцитарной инфильтрации [37, 38]. Исследования указывают на частое выявление опухоли большего размера и низкой степени дифференцировки [38]. Важно отметить, что диагностика РМЖ на поздних стадиях также чаще встречается у женщин моложе 40 лет [39], что может быть связано с поздней обращаемостью или особенностями скрининга в этой возрастной группе.
Геномный анализ позволяет более детально изучить биологические особенности РМЖ у молодых женщин. Анализ данных ДНК-микрочипов
Факторы высокого риска у молодых женщин / High-risk factors in young women
Отягощенный семейный анамнез (ранний РМЖ; рак яичников; РМЖу мужчин; синдромы, ассоциированные с РМЖ) / Burdened family history (early breast cancer; ovarian cancer; breast cancer in men; breast cancer-associated syndromes)
Диагностированный тройной негативный РМЖ у родственников / Diagnosed triple negative breast cancer in relatives
Этническая принадлежность/Ethnicity
Консультация генетика/
Consultation of a geneticist

Рис. 1. Комплексная стратегия превентивных мероприятий у молодых пациенток с высоким риском развития РМЖ. Примечание: рисунок выполнен авторами
Fig. 1. Comprehensive strategy of preventive measures in young patients with a high risk of developing breast cancer.
Note: created by the authors
Таблица/table
Факторы риска развития РМЖ у молодых женщинRisk factors for breast cancer in young women
|
Категория |
Меры профилактики/ |
|
факторов/ Фактор риска/ Category Risk factor of factors |
Описание/механизм/ Степень доказанности/ снижения риска/ Description/mechanism Level of evidence Prevention/risk reduction measures |
|
Низкая физическая активность/ Low physical activity |
Снижение воздействия Снижение риска развития Регулярная физическая циркулирующих гормонов РМЖ на 23 % при активность (не менее яичников, уменьшение активном образе жизни/ 30 мин, 3 раза в нед)/ жировой ткани/ Reducing the risk of devel- Regular physical activity Reducing the effects of cir- oping breast cancer by 23% (at least 30 minutes, 3 times culating ovarian hormones, with an active lifestyle [15] a week) reducing adipose tissue |
|
Высокий индекс массы тела Образ жизни/ (ИМТ)/ esye High Body Mass Index (BMI) |
Избыточная жировая ткань Поддержание способствует выработке здорового веса/ эстрогенов/ Maintaining Excess adipose tissue a healthy weight promotes the production of estrogens |
|
Работа в ночную смену/ Night shift work |
Нарушение циркадного Вероятность развития Минимизация работы ритма, подавление выра- РМЖ до менопаузы выше в ночную смену/ ботки мелатонина/ на 26 %/ Minimizing night Circadian rhythm disorder, The probability of developing shift work suppression of melatonin breast cancer before meno- production pause is higher 26% [18] |
Окончание Таблицы/end of table
|
Мутации в генах BRCA1/2 / Mutations in the BRCA1/2 genes |
Нарушение репарации ДНК, повышение риска развития РМЖ и рака яичников/ Violation of DNA repair, increased risk of developing breast cancer and ovarian cancer |
К 40 годам риск 9,4–12 %/ By age 40, the risk is 9.4–12 % [21] |
Генетическое консультирование, скрининг, профилактическая мастэктомия/ Genetic counseling, screening, preventive mastectomy |
|
|
Генетические/ Genetic |
Мутации в других генах с высокой/ средней пенетрантностью/ Mutations in other genes with high/ medium penetrance ( TP53, PTEN, STK11, CDH1, PALB2, RAD51C, RAD51D ) |
Нарушение различных клеточных процессов (регуляция клеточного цикла, апоптоз, репарация ДНК), повышение риска развития РМЖ/ Disruption of various cellular processes (cell cycle regulation, apoptosis, DNA repair), increased risk of developing breast cancer |
Риск варьирует в зависимости от конкретного гена/ The risk varies depending on the specific gene |
Генетическое консультирование, усиленный скрининг/ Genetic counseling, enhanced screening |
|
Использование КОК/ The use of hormonal contraceptives |
Повышение уровня эстрогенов/ Increased estrogen levels |
Использование КОК в текущий момент или в недавнем прошлом/ Current or recent use of hormonal contraceptives [30] |
Обсуждение рисков и преимуществ с врачом, выбор альтернативных методов контрацепции (в отдельных случаях)/ Discussing the risks and benefits with a doctor, choosing alternative methods of contraception (in some cases) |
|
|
Репродуктивные/ Reproductive |
Использование левоноргестрелсодержащих ВМС/ The use of levonorgestrel-containing IUDs |
Механизм влияния до конца не изучен/ The mechanism of influence is not fully understood. |
У женщин моложе 50 лет/ For women under 50 years of age [31] |
Обсуждение рисков и преимуществ с врачом, выбор альтернативных методов контрацепции (в отдельных случаях)/ Discussing the risks and benefits with a doctor, choosing alternative methods of contraception (in some cases) |
|
Поздние первые роды (после 35 лет)/ Late first birth (after 35 years) |
Механизм до конца не изучен, возможно, связан с более длительным воздействием эстрогенов на ткани молочной железы/ The mechanism is not fully understood, possibly related to the longer-term effects of estrogens on breast tissue |
Поздние роды умеренно повышают риск/ Late delivery increases the risk moderately [34] |
||
|
Отсутствие или короткий период грудного вскармливания/ No breastfeeding or a short period of breastfeeding |
Грудное вскармливание снижает уровень эстрогенов и способствует дифференцировке клеток молочной железы/ Breastfeeding reduces estrogen levels and promotes breast cell differentiation |
Относительное снижение риска на 4 % за каждые 12 мес грудного вскармливания/ Relative risk reduction of 4% for every 12 months of breastfeeding [37] |
Поддержка грудного вскармливания (не менее 6 мес)/ Breastfeeding support (at least 6 months) |
Примечание: таблица составлена авторами.
Note: created by the authors.
РМЖ ранней стадии выявил, что в опухолях женщин моложе 45 лет отмечается значительное снижение экспрессии мРНК рецепторов эстрогена альфа и бета, а также рецепторов прогестерона, в то время как уровни мРНК HER2 и рецептора эпидермального фактора роста (EGFR) были повышены [40]. Анализ обогащения генных наборов (GSEA) также позволил идентифицировать 367 генов, уникальных для опухолей молодых женщин, которые участвуют в иммунных реакциях, ответе на гипоксию, функциях гена BRCA1 , апоптозе и активации про-онкогенных сигнальных путей mTOR, Myc, E2F и Ras [39]. Важно отметить, что активность генов в здоровой ткани молочной железы может модулироваться в зависимости от фазы менструального цикла у женщин в пременопаузе. Исследование B.P. Kundaktepe et al. [41], использовавшее NGS, выявило, что в лютеиновой фазе по сравнению с фолликулярной фазой наблюдается повышение активности 221 гена и снижение активности 34 генов.
Таким образом, современные исследования демонстрируют, что РМЖ у молодых женщин характеризуется уникальным профилем геномных изменений, что может объяснить более агрессивное течение заболевания.
Риск местного рецидива и метастазирования Согласно современным данным, молодой возраст является фактором риска местного рецидива РМЖ, при этом риск возрастает примерно на 7 % с каждым годом уменьшения возраста [42]. При этом влияние выбора хирургического метода на риск местного рецидива остается противоречивым. Краткосрочные результаты (5 лет) исследования M.L. Quan et al. [43] не выявили различий в частоте местных рецидивов после органосохраняющих операций или мастэктомии у пациенток до 35 лет. Однако более длительное (11 лет) наблюдение [44] указало на увеличение частоты локорегионарных рецидивов после органосохраняющей операции. Также установлено, что частота рецидива не зависит от степени злокачественности и размера первичной опухоли. Независимым фактором, ассоциированным с повышенной 10-летней кумулятивной частотой местных рецидивов у женщин до 35 лет, является наличие нелюминального HER2-позитивного подтипа РМЖ [45].
У молодых женщин наблюдается более высокая частота метастатического поражения при РМЖ. При пятилетнем наблюдении метастазы были обнаружены у 24 % женщин моложе 40 лет, в то время как у женщин старше 40 лет этот показатель составил всего 9 % (p<0,0001) [46]. Данный факт подтверждается результатами объединенного анализа G.H. De Bock et al. [47], охватившего 36 000 женщин, где возраст моложе 40 лет был определен как независимый прогностический фактор, ассоциированный с увеличением относительного риска отдаленного метастазирования на 79 %.
Индивидуальный подходк ведению РМЖ у молодых женщин
Диагностика РМЖ
Современные методы диагностики РМЖ у молодых женщин не имеют четко определенных, научно обоснованных отличий, что обусловлено недостатком исследований, проведенных на этой возрастной группе. Диагностический поиск при подозрении на РМЖ у молодых женщин должен учитывать особенности структуры молочной железы и повышенную распространенность генетических мутаций. В этой связи оправдано применение адаптированных протоколов, включающих более активное использование УЗИ в дополнение к маммографии, применение МРТ молочных желез у носительниц мутаций BRCA1/2 , а также использование цифровой маммографии с томосинтезом (3D-маммографии) для повышения чувствительности и специфичности диагностики [48]. Данные методы позволяют улучшить раннюю диагностику РМЖ, что особенно важно для женщин с высокой плотностью ткани молочной железы, которая может затруднять визуализацию опухолей при стандартной маммографии.
Учитывая существующие сложности в ранней диагностике РМЖ у молодых женщин, жидкостная биопсия представляет собой перспективный подход для выявления заболевания на ранних стадиях. Жидкостная биопсия является минимально инвазивной процедурой, потенциально позволяющей получать информацию об опухоли в режиме реального времени. Данная особенность очень важна для молодых пациенток, нуждающихся в продолжительном мониторинге и терапии. Несмотря на многообещающие перспективы применения технологий жидкостной биопсии, объем научных данных пока остается ограниченным. Авторами оценивалась клиническая значимость анализа Videssa Breast для исключения диагноза РМЖ у женщин в возрасте до 50 лет, которые имели высокую плотность молочной железы (BI-RADS 3 или 4). В этой популяции тест продемонстрировал чувствительность 87,5 % и специфичность 83,8 % [49]. Тест Syantra DX™ Breast Cancer Test, также применяемый в качестве метода жидкостной биопсии, был оценен на предмет клинической эффективности у женщин моложе 50 лет. Результаты показали лучшие характеристики по сравнению с другими методами: клиническая чувствительность составила 91,7 %, специфичность – 99,0 % [49]. Несмотря на перспективность жидкостной биопсии в контексте ранней диагностики РМЖ у молодых женщин, необходимы дальнейшие, более масштабные и репрезентативные исследования для подтверждения ее клинической ценности и обеспечения надежной доказательной базы [50].
Для оптимизации существующих методов визуализации и разработки новых диагностических подходов онкологических заболеваний использует- ся интенсивное внедрение технологий искусственного интеллекта (ИИ). Интегративный подход, объединяющий жидкостную биопсию, методы визуализации и ИИ, открывает перспективы для комплексной оценки опухолевого процесса и разработки персонализированных стратегий лечения. Жидкостная биопсия играет критическую роль на ранних этапах диагностики, позволяет осуществлять мониторинг эволюции опухоли, отслеживая динамику мутационного профиля раковых клеток и оценивая эффективность проводимой терапии. В свою очередь, методы визуализации обеспечивают возможность выявления и локализации новообразований, а также количественной оценки их характеристик, таких как размер, степень дифференцировки и наличие метастатического поражения. Интеграция алгоритмов ИИ в процесс анализа результатов обследования повышает точность и воспроизводимость интерпретации данных, снижая субъективность оценок. Таким образом, комплексный подход, объединяющий раннее выявление с помощью жидкостной биопсии, пространственно-функциональную оценку с помощью визуализации и прогнозирование рисков и исходов с помощью ИИ, обладает значительным потенциалом для улучшения диагностики и оптимизации лечения РМЖ. Несмотря на то, что совместное использование этих технологий находится на начальной стадии, данное направление представляется чрезвычайно перспективным [49, 51].
Лечение РМЖ у молодых пациенток
Подходы к лечению как ранних, так и распространенных стадий заболевания у молодых женщин должны базироваться на тех же клиникопатологических факторах, что и при лечении женщин старшего возраста, однако при этом необходимо учитывать уникальные биологические, гормональные и генетические особенности, характерные для этой группы. Хирургические подходы к лечению РМЖ у молодых женщин аналогичны применяемым у пациенток старшего возраста и включают: органосохраняющую терапию, состоящую из радикальной резекции молочной железы с последующей лучевой терапией, и радикальную мастэктомию. Изучение влияния типа хирургического лечения на выживаемость молодых женщин с РМЖ дает неоднозначные результаты. В краткосрочной перспективе до 5 лет исследование M.L. Quan et al. [43] не выявило значимых различий в выживаемости у пациенток до 35 лет. Несмотря на то, что в исследовании [44] с периодом наблюдения в 11 лет были зафиксированы некоторые различия в эффективности локорегионарного контроля, авторы пришли к выводу, что эти различия не оказали значимого влияния на общую выживаемость. Важно отметить, что, согласно ретроспективному анализу данных пациенток до 40 лет [45], даже при развитии нежелательных событий, 10-летняя безметастатическая выживаемость остается высокой, достигая 84,7 %. Современные исследования подтверждают онкологическую безопасность немедленной и отсроченной реконструкции молочной железы, а также процедур, направленных на сохранение соска. Более того, не выявлено преимуществ в показателях выживаемости при выполнении контралатеральной профилактической мастэктомии [44, 45, 52].
В адъювантном лечении РМЖ лучевая терапия после радикальной резекции имеет особое значение для молодых пациенток. Повышенный риск местного рецидива у молодых пациенток позволяет обоснованно ожидать более выраженный клинический эффект от данного вида лечения. Кроме того, адъювантная лучевая терапия рекомендована молодым пациенткам после мастэктомии при местнораспространенном РМЖ. Клинические испытания демонстрируют, что этот метод способствует улучшению локорегионарного контроля и показателей выживаемости у женщин как в пре-, так и в постменопаузе, при наличии крупных первичных опухолей (более 5 см), поражении кожи или грудной стенки, а также поражении лимфатических узлов [45, 52]. Однако при лучевой терапии необходимо соблюдать меры предосторожности, направленные на минимизацию дозы облучения, получаемой окружающими здоровыми тканями. Это обусловлено необходимостью снижения риска развития отсроченных побочных эффектов и вторичных злокачественных новообразований, учитывая молодой возраст и, как следствие, длительный период потенциальной выживаемости [52].
В 60–75 % случаев у молодых пациенток с РМЖ выявляется положительный статус гормональных рецепторов. Однако применение ингибиторов ароматазы ограничено в этой группе из-за их низкой эффективности в пременопаузе. В последние годы ряд клинических исследований (ABCSG-12, SOFT и TEXT) были посвящены изучению оптимальных режимов адъювантной гормональной терапии у молодых пациенток с HR+/HER2- РМЖ, особое внимание уделялось медикаментозной менопаузе (ММ). Несмотря на отсутствие различий в эффективности монотерапии анастрозолом и тамоксифеном, выявленных в исследовании ABCSG-12, консолидированный анализ данных SOFT и TEXT продемонстрировал, что адъювантное применение экземестана в сочетании с ММ обеспечивает значимое улучшение 8-летней безрецидивной выживаемости по сравнению с комбинацией тамоксифена и ММ. Кроме того, подгрупповой анализ исследования SOFT выявил, что добавление ММ к тамоксифену после адъювантной химиотерапии ассоциировано с увеличением 5-летней выживаемости при РМЖ у женщин в возрасте до 35 лет, что подчеркивает потенциальную пользу данного подхода в этой возрастной группе. Наконец, метаа- нализ, объединивший данные ABCSG XII, SOFT, TEXT и HOBOE, подтвердил, что комбинированная терапия, включающая ингибиторы ароматазы и ММ, значительно снижает риск рецидива по сравнению с монотерапией тамоксифеном, что свидетельствует о целесообразности комбинированных режимов в данной популяции [53].
В отличие от оптимизации гормональной терапии, где активно изучаются индивидуализированные подходы, подходы к химиотерапии у молодых пациенток с РМЖ высокого риска остаются унифицированными. В связи с ограниченностью клинических данных, позволяющих оптимизировать режимы химиотерапии для этой возрастной группы, применяются стандартные комбинированные схемы, включающие антраци-клины и таксаны, аналогичные используемым у пациенток старшего возраста. Однако несмотря на то, что выбор химиотерапевтической стратегии в основном определяется стадией заболевания и молекулярно-биологическими характеристиками опухоли, имеются данные, указывающие на то, что неоадъювантная химиотерапия (НАХТ) может быть особенно эффективной у молодых пациенток. Так, исследование GeparTrio выявило более высокий показатель патоморфологического полного ответа (pCR) после НАХТ у женщин моложе 40 лет с трижды негативным раком (ТНР) молочной железы или опухолями высокой степени злокачественности по сравнению с пациентками старше 40 лет. Метаанализ EBCTCG показал, что антрациклины ассоциированы с более выраженным снижением смертности от РМЖ у молодых женщин (<50 лет) по сравнению с женщинами старшего возраста, независимо от других факторов. Добавление так-санов к антрациклинам обеспечивает улучшение безрецидивной и общей выживаемости в обеих возрастных группах, а отказ от химиотерапии у молодых женщин ассоциирован со значительным повышением частоты летального исхода [54].
Применение ингибиторов иммунных контрольных точек в составе НАХТ у молодых пациенток с ТНР РМЖ демонстрирует противоречивые результаты. В то время как исследование KEYNOTE выявило значимое увеличение частоты pCR при добавлении пембролизумаба к НАХТ вне зависимости от уровня экспрессии PD-L1, исследование GeparNuevo показало лишь скромное увеличение pCR, сопровождавшееся значительным улучшением выживаемости без прогрессирования. Напротив, исследование NeoTRIPaPDL1 не выявило значимого влияния атезолизумаба на частоту pCR. Таким образом, необходимы дополнительные исследования для оптимизации стратегий иммунотерапии у этих пациенток [55].
Сохранение репродуктивной функции является важным аспектом лечения РМЖ у молодых женщин. Противоопухолевая терапия может вызвать повреждение яичников, преждевременную менопаузу и снижение овариального резерва. Важно информировать пациенток о возможных рисках и предлагать варианты сохранения фертильности до начала лечения. К методам сохранения фертильности относятся криоконсервация ооцитов, эмбрионов или ткани яичника, а также применение агонистов гонадотропин-рилизинг гормона. Необходимо также обсуждать с пациентками возможности восстановления фертильности после завершения лечения РМЖ, включая экстракорпоральное оплодотворение с использованием замороженных ооцитов или эмбрионов, а также донорство ооцитов. Всем молодым женщинам, планирующим деторождение в будущем, рекомендуется консультация репродуктолога до начала лечения РМЖ. Важно также учитывать время, необходимое для проведения процедур сохранения фертильности, и согласовывать их с онкологическим лечением [9].
Особенности реабилитации молодых пациенток с РМЖ
Принимая во внимание, что у молодых женщин с РМЖ чаще встречаются более агрессивные типы опухолей, требующие проведения интенсивной лучевой, химио- и таргетной терапии, актуальным вопросом становится профилактика побочных эффектов. В настоящее время физические упражнения все чаще рассматриваются как эффективный способ борьбы с негативными последствиями противоопухолевого лечения [56]. При назначении физических тренировок увеличивается аэробная выносливость (VO2peak), которая является признанным мощным и независимым предиктором общей смертности и сердечно-сосудистых осложнений [57]. Контролируемые и разнообразные физические упражнения могут улучшить качество жизни и снизить риск полинейропатии у онкологических пациентов, получающих химиотерапию [58]. Лучшие результаты наблюдались, когда пациенты начинали заниматься физическими упражнениями вскоре после начала лечения, при этом рекомендовалась продолжительность занятий не менее 30 мин, не реже 3 раз в неделю, в течение 8–12 нед [59].
Учитывая более высокую цифровую грамотность молодых пациентов, становится возможным применение телереабилитации, особенно для пациентов, проживающих в отдаленных районах, а также носимых устройств, которые способны предоставлять важную информацию для отслеживания эффективности лечения, прогнозирования его результатов и проведения реабилитационных мероприятий [59].
Молодым женщинам, перенесшим РМЖ, особенно необходима психологическая поддержка. Страх, тревога и депрессия, прежде всего, связаны с наличием заболевания, дефектом груди и изменением образа тела, проблемами с фертиль- ностью, неуверенностью в поддержке семьи. Для психологической реабилитации молодых женщин, переживших РМЖ, могут быть эффективны проведение тренингов когнитивно-поведенческой терапии, онлайн-программы для пар, основанные на принципах осознанности, включающие психообразование и практические упражнения; терапия принятия и ответственности, а также проведение косметических процедур для онкологических пациентов и другие подходы [60].
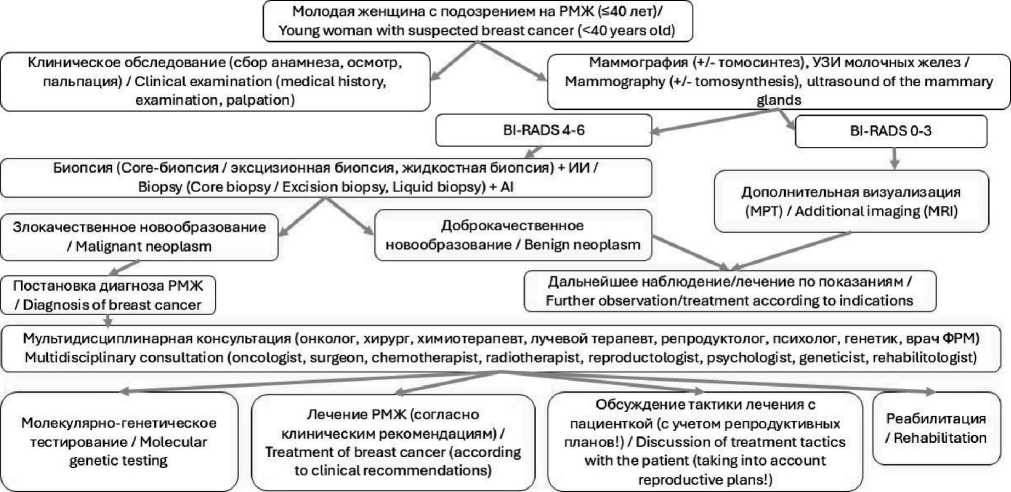
На рис. 2 представлена схема, описывающая последовательность действий при ведении молодых женщин с РМЖ и направленная на оптимизацию диагностики, лечения и реабилитации.
Заключение
Представленные данные подтверждают, что РМЖ у женщин моложе 40 лет следует рассматривать как отдельную нозологическую единицу, требующую специализированного подхода к диагностике, лечению и профилактике. Эти особенности характеризуются агрессивным течением, высокой долей эстроген-отрицательных, ТНГ и HER2-положительных подтипов, худшим прогнозом, высоким уровнем местного рецидива, регионарного и отдаленного метастазирования, а также более частым обнаружением мутаций, в особенности BRCA1/2. Наличие специфических клинических и биологических характеристик РМЖ у молодых пациенток обусловливает необходимость дифференцированного подхода к диагностике и терапии. Несмотря на наличие исследований, по- священных РМЖ у молодых женщин (например, исследования группы POSH, анализ баз данных SEER), они не позволяют сформировать доказательную базу уровня Level 1 evidence. Важную роль в преодолении этой проблемы играют регистры молодых пациенток, такие как Young Women’s Breast Cancer Study, которые способствуют сбору и анализу специфических клинических данных, необходимых для более глубокого понимания этой группы заболеваний.
Анализ представленных данных позволяет выделить ряд ключевых положений, определяющих подходы к ведению молодых пациенток с РМЖ. Следует учитывать, что у этой возрастной группы отмечается повышенная частота агрессивных подтипов, а также генетических мутаций, особенно в генах BRCA1/2 . В связи с этим возникает необходимость в ранней диагностике, достигаемой путем адаптации существующих скрининговых программ, внедрения МРТ молочных желез для носительниц мутаций BRCA, что позволяет выявлять опухоли на ранних стадиях, когда лечение наиболее эффективно. Для обеспечения оптимального ведения молодых пациенток с РМЖ необходим мультидисциплинарный подход, включающий не только хирургическое и лекарственное лечение, но и психологическую поддержку и реабилитацию, учитывающие уникальные потребности этой возрастной группы. Исходя из этого, представляется целесообразным выделить следующие рекомендации для клинической практики. Всем молодым пациенткам с РМЖ, особенно при наличии отяго-
Долгосрочное наблюдение/ Long-term monitoring
Рекомендации по здоровому образу жизни / Recommendations for a healthy lifestyle
Психологическая поддержка и адаптация кжизни после РМЖ/ Psychological support and adaptation to life after breast cancer
Рис. 2. Персонализированный подход к ведению РМЖ у молодых женщин. Примечание: рисунок выполнен авторами Fig. 2. Personalized approach to breast cancer management in young women. Note: created by the authors
щенного семейного анамнеза или специфических подтипов опухоли, важно проводить генетическое тестирование. Параллельно необходимы разработка и внедрение адаптированных программ скрининга, учитывающих повышенный риск РМЖ у молодых женщин, с акцентом на использование МРТ молочных желез для женщин с высоким генетическим риском. Кроме того, следует обеспечить комплексное ведение молодых пациенток с РМЖ посредством мультидисциплинарного подхода, объединяющего специалистов различного профиля, и разработать стандартизированные протоколы для своевременного направления к соответствующим специалистам и координации их усилий. Целесообразно предлагать всем молодым женщинам с РМЖ консультацию репродуктолога до начала лечения и обсуждать возможности сохранения фертильности. Наконец, крайне важна интеграция психологической поддержки и реабилитации в стандартный уход за молодыми пациентками с РМЖ, начиная с момента постановки диагноза и на протяжении всего периода лечения и наблюдения.
Для дальнейшего улучшения результатов лечения и понимания особенностей РМЖ у молодых женщин необходимо сосредоточиться на будущих исследованиях. Важно расширить изучение РМЖ у молодых женщин с целью понимания молекулярных механизмов, драйверов опухолевого роста и факторов, определяющих прогноз. Следует проводить углубленный геномный и протеомный анализ, а также анализ микроокружения опухоли, принимая во внимание менструальный цикл и репродуктивный статус. Крайне важны клинические исследования, специально разработанные для молодых женщин с РМЖ, для оценки эффектив- ности различных терапевтических стратегий с учетом уникальных биологических особенностей опухолей и долгосрочных последствий лечения. Необходимо расширять и поддерживать регистры молодых пациенток с РМЖ для сбора и анализа данных о клинических характеристиках, лечении и исходах заболевания. Наконец, для повышения эффективности раннего выявления РМЖ у молодых женщин важно оценить возможности комплексного использования инновационных методов диагностики, включая жидкостную биопсию, современные методы визуализации и алгоритмы искусственного интеллекта.


