Рак щитовидной железы: уроки Чернобыля и их применение к ситуации в Фукусиме
Автор: Иванов В.К., Кащеев В.В., Чекин С.Ю., Максютов М.А., Туманов К.А., Меняйло А.Н., Власов О.К., Кочергина Е.В., Кащеева П.В., Щукина Н.В., Галкин В.Н., Каприн А.Д., Саенко В.А., Ямасита С.
Рубрика: Научные статьи
Статья в выпуске: 2 т.25, 2016 года.
Бесплатный доступ
В статье рассматривается вопрос оценки радиационных рисков и эффекта скрининга рака щитовидной железы (РЩЖ). В качестве внешнего контроля использовалась спонтанная заболеваемость РЩЖ населения России в целом. В исследование были включены 327 тыс. жителей наиболее загрязнённых территорий Брянской, Орловской, Тульской и Калужской областей, подвергшихся радиационному воздействию в результате аварии на Чернобыльской АЭС в 1986 г. Для учёта латентного периода в индукции солидных злокачественных новообразований включён 5-летний временной лаг, т.е. период наблюдения выбран с 1.01.1991 по 31.12.2013 гг. Используя имеющуюся информацию о месте жительства и возрасте членов исследуемой когорты в 1986 г., были получены индивидуализированные оценки доз облучения щитовидной железы от инкорпорированных радионуклидов йода. Показано, что доза облучения щитовидной железы в группе детей и подростков до 18 лет снижается с возрастом при облучении. В то же время доза облучения щитовидной железы для взрослых старше 18 лет от возраста при облучении не зависит. Средняя доза облучения щитовидной железы для детей и подростков в когорте составляет 174 мГр и 36 мГр для взрослых. Максимальные дозы равны 4,48 Гр и 0,66 Гр соответственно. В период наблюдения установлен ярко выраженный скрининговый эффект в процессе регистрации заболеваний РЩЖ (6,74 для детей и подростков 0-17 лет на момент аварии и 1,5 для группы 18 лет и старше). Оценка коэффициента скрининга по периодам наблюдения выявила значимое (p
Чернобыльская аэс, фукусима, когортное исследование, загрязнённая радионуклидами территория, рак щитовидной железы, население, заболеваемость, избыточный относительный риск, чувствительность, специфичность, эффект скрининга
Короткий адрес: https://sciup.org/170170251
IDR: 170170251
Thyroid cancer: lessons of Chernobyl and projections for Fukushima
Estimating radiation risks of thyroid cancer in the range of middle an low doses and prediction of the incidence with account of screening effect is a complex problem. The present article considers the problem of radiation risks estimation and screening effect on detection of thyroid cancer. Development of methodology and risk assessment were based on radiation-epidemiological information accumulated for 30 years at the National Radiation Epidemiological Registry (NRER). In order to research into screening effect and relationship between radiation dose and thyroid cancer the cohort method was used. National statistical data on thyroid cancer incidence among Russian population were used as referent. In the present study residents of the most contaminated territories of Bryansk, Orel, Tula and Kaluga oblasts exposed to radiation as a consequence of the Chernobyl accident in 1986 composed the cohort. Taking into account the 5-year latent period the study was carried out from 1.01.1991 to 31.12.2013. Such information as place of residence in 1986, and the age available for all members of the cohort was used for estimation of thyroid dose from incorporated radioiodine. The total number of the cohort members was 327 thousand. Previously published data demonstrated dependence of thyroid dose on age of children and adolescents, younger than 18 years at exposure, the dose exponentially reduced with age. At the same time thyroid dose of adults, older than 18 years at exposure, did not depend on age. Average thyroid dose to children and adolescents was 174 mGy, and it was 36 mGy to adults, the highest doses were 4.48 Gy and 0.66 Gy respectively. All cohort members underwent yearly comprehensive medical examination. It is possible to suggest that recorded increase in thyroid cancer incidence, as compared with national statistical data, is a result of the examinations. This increase can be defined as screening effect. During the follow-up period (1991 through 2013) screening effect was 6.74 in the group younger than 18 years at exposure and 1.5 in the group older than 18 years at exposure. From 1996 the effect reduced twofold as compared with the first 5-year period (1991-1995). Obtained methodology was used for estimation of expected pediatric thyroid cancer incidence in Japan after the accident at the Fukushima-Daichi NPP. It is necessary to stress that actual data on thyroid cancer incidence are in good agreement with predicted data.
Текст научной статьи Рак щитовидной железы: уроки Чернобыля и их применение к ситуации в Фукусиме
Неблагоприятное влияние радиационного фактора риска на возможное повышение частоты онкологических заболеваний при высоких дозах облучения было доказано в результате проведения крупномасштабных эпидемиологических исследований среди жителей японских городов Хиросима и Нагасаки, подвергшихся в 1945 г. атомной бомбардировке. Результаты этих исследований положены в основу международных принципов радиационной безопасности
Иванов В.К. - Председатель РНКРЗ, зам. директора по научн. работе, чл.-корр. РАН; Кащеев В.В.* - зав. лаб., к.б.н.; Чекин С.Ю. - зав. лаб.; Максютов М.А. – зав. лаб., к.т.н.; Туманов К.А. – зав. лаб., к.б.н.; Меняйло А.Н. – ст. научн. сотр,, к.б.н.; Власов О.К. – зав. лаб., д.т.н.; Кочергина Е.В. – зав. лаб., к.м.н.; Кащеева П.В. – ст. научн. сотр,, к.б.н.; Щукина Н.В. – ст. научн. сотр.; Галкин В.Н. – директор, д.м.н., проф. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИРЦ» Минздрава России. Каприн А.Д. – ген. директор, чл.-корр. РАН, д.м.н., проф. ФГБУ «НМИРЦ» Минздрава России. Саенко В.А. – ассоциированный профессор, к.б.н.; Ямасита С. – проректор, зав. отд., д.м.н. Университет Нагасаки, Япония.
Научным комитетом ООН по действию атомной радиации (НКДАР ООН), Международной комиссией по радиологической защите (МКРЗ) и МАГАТЭ.
Вместе с тем, крупные радиационные катастрофы последних лет (Три-Майл Айленд, Чернобыль, Фукусима), приведшие к облучению значительных контингентов населения и персонала, ставят в качестве основного приоритета проблему оценки возможных радиационных рисков индукции онкологических заболеваний при средних и малых дозах облучения. Объективное и научно обоснованное решение указанной проблемы в значительной степени влияет на стратегию формирования групп повышенного риска для оказания необходимой и своевременной медицинской помощи органами практического здравоохранения, позволяет широко использовать – при минимизации отдалённых радиологических последствий – современные дорогостоящие медицинские технологии.
После аварии на Чернобыльской АЭС прошло 30 лет, однако результаты постчернобыльских эпидемиологических исследований стали особенно актуальны в последнее время. Это в первую очередь связано с важностью и необходимостью использования накопленных знаний и опыта для уменьшения возможных радиологических последствий аварии на АЭС «Фукусима-1» в Японии. Проблема оценки возможных радиологических последствий для населения этой префектуры островного государства остаётся крайне актуальной.
«Опыт Чернобыля» показал, что особое место в оценке радиологических последствий отводится изучению заболеваемости раком щитовидной железы (РЩЖ) населения наиболее загрязнённых радионуклидами территорий. Многочисленные исследования выявили рост заболеваемости РЩЖ среди лиц из населения загрязнённых территорий в сравнении со спонтанными национальными показателями в Белоруссии, России и Украине [1-7]. Также было показано, что дети (на момент облучения) могут быть отнесены к группе повышенного радиационного риска по РЩЖ [5, 8-12].
Вместе с тем, оценка радиационных рисков раковой патологии щитовидной железы в диапазоне малых и средних доз облучения, а также прогноз радиационно-индуцированной заболеваемости РЩЖ в последующие годы в условиях выраженных скрининговых эффектов остаётся непростой задачей.
Современные Рекомендации МКРЗ 2007 г. [13] содержат прогнозные модели радиационного риска РЩЖ, идентифицированные в когортах, подвергшихся внешнему облучению. Эти модели основаны на оценках комбинированного исследования E. Ron et al. (1995) [14], а также, в основном, на 40-летнем исследовании японской когорты лиц, переживших атомные бомбардировки [15]. Хотя исследованные когорты имели большую статистическую мощность, их условия облучения являются нехарактерными для населения, проживавшего или проживающего на загрязнённых радионуклидами территориях и подвергшегося внутреннему облучению щитовидной железы. В связи с этим, МКРЗ предупреждает об опасности некорректного переноса моделей риска на другие популяции в целях прогноза.
Не менее важной проблемой в прогнозе заболеваемости РЩЖ является вопрос корректной оценки эффекта скрининга в процессе регистрации редких патологий (таких как РЩЖ) в когортах наблюдения. В этом случае эффект скрининга возникает за счёт дополнительной «углублённой» диспансеризации с использованием современных диагностических средств (как в случае ежегодной диспансеризации жителей наиболее загрязнённых территорий) и может приводить к значительному приросту числа выявляемых спонтанных радиационно-необусловленных случаев РЩЖ в сравнении с национальной статистикой [16].
Оценка радиационных рисков и эффекта скрининга рака щитовидной железы в когорте населения РФ, облучённого в результате аварии на Чернобыльской АЭС
Данный раздел настоящего исследования ставит целью оценку эффекта скрининга РЩЖ среди населения РФ, подвергшегося внутреннему облучению щитовидной железы от инкорпорированных радионуклидов йода. Полученные оценки позволят адекватно взглянуть на результаты проводимого в настоящее время ультразвукового обследования щитовидной железы у детей в префектуре Фукусима [17].
Ранее вопрос оценки радиационных рисков и эффекта скрининга РЩЖ уже рассматривался авторами настоящего исследования на примере детского и взрослого населения Брянской и Орловской областей. Отмечалось, что специфической проблемой для постчернобыльских когорт наблюдения является влияние методов диагностики РЩЖ на оценки радиационных рисков этого заболевания [16]. Масштабное применение ультразвукового скрининга заболеваний щитовидной железы на облучённых вследствие чернобыльской катастрофы когортах резко повысило выявляемость заболеваний, по сравнению со средним состоянием по всему населению России, что необходимо учитывать при оценке радиационных рисков.
Другой важной особенностью исследований заболеваемости РЩЖ в постчернобыльских когортах является необходимость учитывать, что не только фоновая заболеваемость зависит от достигнутого возраста, но и доза внутреннего облучения от радиоизотопов йода, поглощённая в щитовидной железе, нелинейно связана с возрастом при облучении [16]. Поэтому зависимость фоновой заболеваемости РЩЖ от достигнутого возраста и радиационный риск РЩЖ нельзя получить методом внутреннего сравнения только по данным наблюдения за исследуемой когортой. Для оценки фоновой заболеваемости требуется привлечение внешних данных, например, полученных в системе общего здравоохранения [18].
Разработка методов и оценка радиационного риска РЩЖ среди населения наиболее загрязнённых территорий Российской Федерации с учётом эффекта скрининга проведены с использованием радиационно-эпидемиологических данных, накопленных за 30 лет после аварии на ЧАЭС на базе Национального радиационно-эпидемиологического регистра [19].
В настоящее исследование были включены люди, подвергшиеся радиационному воздействию в результате аварии на Чернобыльской АЭС в 1986 г. и проживающие на наиболее загрязнённых территориях Брянской, Орловской, Тульской и Калужской областей. Для учёта латентного периода в индукции солидных злокачественных новообразований использовался 5-летний временной лаг, т.е. период наблюдения был выбран с 1.01.1991 по 31.12.2013 гг. Поскольку для членов этой когорты имеется индивидуальная информация об их месте жительства в 1986 г. и возрасте, были получены индивидуализированные оценки доз облучения щитовидной железы от инкорпорированных радионуклидов йода [12]. Общее число людей, включённых в настоящее исследование, составило 327 тыс. человек.
Как было показано в недавнем исследовании [16], доза облучения щитовидной железы в группе детей и подростков до 18 лет сильно зависит от возраста на момент облучения. Зависимость имеет экспоненциальный вид, и доза облучения щитовидной железы снижается с возрастом при облучении. В то же время доза облучения щитовидной железы для взрослых старше 18 лет не зависит от возраста при облучении. Средняя доза облучения щитовидной железы для детей и подростков в когорте составляет 174 мГр и 36 мГр для взрослых. Максимальные дозы равны 4,48 Гр и 0,66 Гр соответственно.
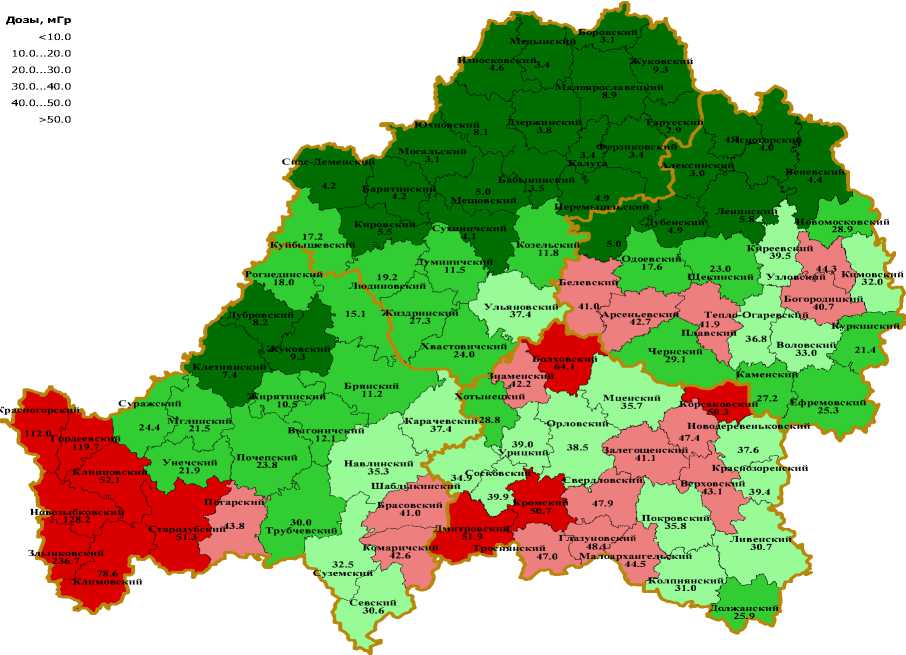
На рис. 1 приведена карта среднерайонных доз облучения щитовидной железы детей и подростков 4-х рассматриваемых областей. Как видно из рисунка, наибольшему облучению подверглись дети и подростки юго-западных районов Брянской области.
На рис. 2 показано дозовое распределение среди детей и подростков по 7 юго-западным районам Брянской области, где средняя доза превышает 50 мГр.
Дозы, мГр
<10.0
>50.0
Киро
39.5
23.0
Рогнединск
32.0
Дубро
39.0
38.5
37.6
41.1
23.8
39.9
47.9
41.0
5.8
тародубс
78.6
31.0
Севский
30.6
30.0...40.0
40.0...50.0
20.0...30.0
10.0...20.0
Навлинский
35.3
Богородиц
40.7
17.2 Куйбышев
Чернский 29.1
32.5 Суземск
Должанский 25.9
30.0 Трубчевский й 48.1
47.0 Малоарханге
44.5
Карачевский28.8
37.4
Рис. 1. Карта среднерайонных доз облучения щитовидной железы для детей и подростков (0-17 лет) на момент аварии, проживающих в Брянской, Орловской, Тульской и Калужской областях.
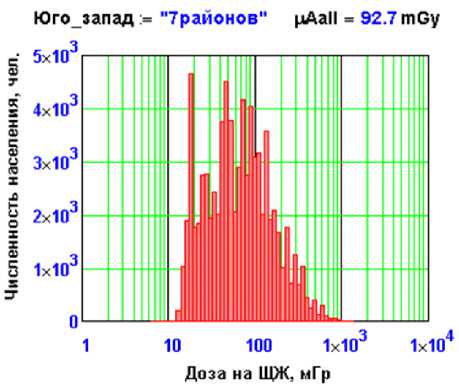
Рис. 2. Дозовое распределение среди детей и подростков юго-западных районов Брянской области, где средняя доза выше 50 мГр.
Все жители наиболее загрязнённых территорий 4-х областей, включённые в исследование, проходят ежегодные медицинские осмотры. За период наблюдения с 1991 по 2013 гг. в рассматриваемых когортах был выявлен 1241 случай РЩЖ (из них 316 случаев среди детей и подростков в возрасте 0-17 лет на момент аварии и 925 случаев среди взрослых 18 лет и старше на момент аварии). Не более 8,5% диагнозов РЩЖ среди детей и подростков и 10,5% среди взрослых на момент аварии определены только клиническими методами. Остальные случаи выявлены на основе радиоизотопных, ультразвуковых и других методов; диагнозы подтверждены морфологически у 89% детей и подростков и у 79% взрослых.
Согласно национальной статистике [18], в общей структуре заболеваемости злокачественными новообразованиями населения России РЩЖ занимает менее 3% и, следовательно, его можно считать достаточно редкой патологией. Дополнительная «углублённая» диспансеризация с использованием современных диагностических средств (как в случае ежегодной диспансеризации жителей наиболее загрязнённых территорий Брянской, Орловской, Тульской и Калужской областей, включённых в исследование) может приводить к значительному приросту числа выявляемых редких патологий, в т.ч. и РЩЖ, в сравнении с национальной статистикой. Данный процесс может быть охарактеризован «эффектом скрининга».
Метод оценки случай-контроль не даёт возможности оценить фоновую заболеваемость, не связанную с радиацией, что в свою очередь исключает возможность оценки эффекта скрининга РЩЖ на загрязнённых территориях. Таким образом, для исследования эффекта скрининга и зависимости заболеваемости РЩЖ от дозы облучения был использован современный метод когортных исследований [16]. При этом использовались индивидуальные данные о населении представленных когорт (дети и подростки младше 18 лет и взрослые), которые были стратифицированы по полу, достигнутому возрасту – пятилетние интервалы и календарному времени – годовые интервалы. Стратификация по полу, возрасту и календарному времени проводилась с целью описания фоновой (не связанной с облучением) заболеваемости РЩЖ в когорте при помощи внешней контрольной группы. Подобная методика позволяет оценить эффект скрининга. В качестве внешнего контроля использовалась спонтанная заболеваемость РЩЖ населения России в целом [18]. Время нахождения каждого человека под риском заболеть РЩЖ вычисляется как разница дат Т1 и Т0 , где Т0 – время облучения и Т1 – дата диагноза РЩЖ, последнего медицинского осмотра, дата смерти или выбытия из-под наблюдения в силу неизвестных причин.
Оценка зависимости заболеваемости РЩЖ от дозы инкорпорированного облучения щитовидной железы радионуклидами йода проводилась с использованием Пуассоновской регрессии. Использовалась модель избыточного относительного риска (Excess Relative Risk – ERR) следующего вида:
X = X sp . [ 1 + p (d) ] , (1)
где X sp - фоновая заболеваемость РЩЖ в когорте, не зависящая от облучения; p (d) - функция, характеризующая зависимость заболеваемости от дозы инкорпорированного облучения щитовидной железы.
Фоновая заболеваемость определялась с использованием внешней контрольной группы:
X sp = exp ( в ) 'X rus (s,a,t) , (2)
где X ruS(s,a,t) - годовые половозрастные показатели заболеваемости РЩЖ населения России [18]; exp( р) = ES - эффект скрининга (коэффициент, учитывающий различие спонтанных заболеваемостей в изучаемой и российской популяции в рассматриваемый период времени), β – неизвестная константа.
Как для детей и подростков на момент аварии, так и для взрослого населения, рассматривались линейные модели зависимости заболеваемости РЩЖ от дозы инкорпорированного облучения щитовидной железы [16]:
для детей: ρ (d ) = ERR ⋅ d ⋅ exp[ υ ⋅ e + ω ⋅ ln( a / 20 )] , (3)
для взрослых: ρ (d ) = ERR ⋅ d ⋅ exp[ υ ⋅ (e - 45 ) + ω ⋅ ln( a / 60 )] , (4)
где ERR 1Гр – избыточный относительный риск на единицу дозы 1 Гр; d – индивидуализированная доза инкорпорированного облучения щитовидной железы радионуклидами йода в Гр, e – возраст при облучении, a – достигнутый возраст, υ и ω – неизвестные константы.
Подбор неизвестных констант ERR 1Гр , β , ω и υ осуществлялся с помощью максимизации функции правдоподобия. Так же оценивалась статистическая значимость ( p- value) исследуемых параметров. Статистическим тестом для этих целей служит тест отношения правдоподобий. Подбор неизвестных констант, оценки значимости и 95% доверительные интервалы (95% ДИ) проводились с помощью программного пакета R [20]. На рис. 3 графически отражена используемая методология оценки эффекта скрининга и линейной зависимости увеличения частоты РЩЖ от дозы облучения.
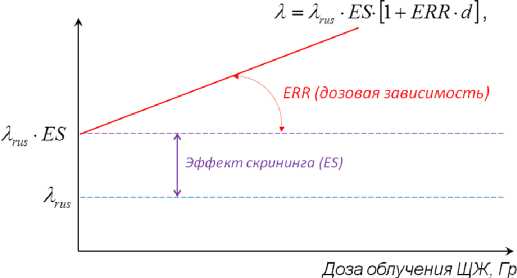
Рис. 3. Модель оценки эффекта скрининга и линейной зависимости увеличения частоты РЩЖ от дозы облучения [16].
На основании когортных регрессионных моделей (с учётом чувствительности и специфичности) были оценены величины эффекта скрининга и радиационных рисков РЩЖ для рассматриваемых когорт. Полученные результаты представлены ниже. Так, в табл. 1 показаны величины избыточных относительных рисков на единицу дозы облучения щитовидной железы 1 Гр (ERR/Гр) и коэффициентов скрининга ( ES ) для детей и подростков на момент аварии, а также для взрослых. Как видно из табл. 1, значимый радиационный риск индукции РЩЖ установлен только для детей и подростков (0-17 лет) на момент аварии. Высокое значение оцениваемой в модели величины ES за весь период наблюдения (6,74 для детей и подростков 0-17 лет на момент аварии и 1,5 для группы 18 лет и старше) подтверждает выраженный скрининговый эффект в процессе регистрации заболеваний РЩЖ. Как и следовало ожидать, выявленный эффект скрининга выше для молодых возрастов, в сравнении с взрослыми. Установлено, что для детей и подростков на момент аварии радиационный риск РЩЖ значимо зависит от возраста на момент облучения и достигнутого возраста. Оценка коэффициента скрининга ES по 4 периодам наблюдения позволила выявить значимое (p<0,001) 2-кратное снижение эффекта скрининга, начиная с 1996 г., в сравнении с первым периодом (1991-1995 гг.).
Таблица 1
Значения избыточного относительного риска (ERR) и эффекта скрининга (ES) для заболеваний РЩЖ в когорте лиц из Брянской, Орловской, Тульской и Калужской областей, за период с 1991 по 2013 гг.
|
Период наблюдения: 1991-2013 гг. |
Дети и подростки на момент аварии (0-17 лет) |
Взрослые на момент аварии (18+ лет) |
|
Всего человек Число случаев Средняя доза для когорты, мГр Средняя доза среди случаев, мГр Эффект скрининга ES , (95% ДИ), p-value ES1 : 1991 – 1995 ES2 : 1996 – 2000 ES3 : 2001 – 2005 E S4: 2006 – 2013 ES средний за период: 1991 – 2013 ERR/Гр , (95 % ДИ), p-value ω, (95% ДИ), p-value υ, (95% ДИ), p-value |
108166 316 174 190 Модель (3) 12,8 (8,6; 17,9); p<0,001 6,6 (4,8; 8,9); p<0,001 5,8 (4,4; 7,4); p<0,001 6,8 (5,4; 8,1); p<0,001 6,74 (5,6; 7,9); p<0,001 4,73 (2,54; 7,72); p<0,001
|
219544 925 35 36 Модель (4) 1,3 (0,9; 1,9); p=0,11 1,2 (1,0; 1,4); p=0,04 1,9 (1,5; 2,1); p<0,001 1,6 (1,2; 2,3); p<0,001 1,5 (1,2; 1,6); p<0,001 -0,60 (-2,93; 1,53); p=0,38 -0,12 (-1,17; 1,94); p>0,5 -0,04 (-0,26; 0,23); p>0,5 |
20,0
ш 18,0
Ё 16,0
Z 14,0 | 12,0
о 10,0 ф 8,0
I 68,,00 t 4,0
8 2,0
^ 0,0
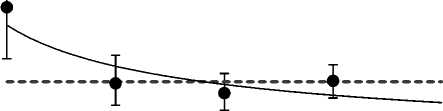
• ES - по периодам наблюдения ES - cреднее значение
1991-1995 1996-2000 2001-2005 2006-2013
Календарный период наблюдения
Рис. 4. Зависимость эффекта скрининга от календарного времени наблюдения за когортой детей и подростков (0-17 лет) на момент аварии.
На рис. 4 приведено графическое представление зависимости эффекта скрининга от календарного времени наблюдения за когортой детей и подростков на момент аварии. Следует еще раз подчеркнуть, что эффект скрининга (коэффициент ES ) в течение 1991-1995 гг. для детей и подростков составил 12,8.
Проведённый анализ показывает, что из выявленных 316 случаев заболеваний РЩЖ к радиационно-обусловленным следует отнести 71 случай (т.е. 22,5%). Однако в когорте детей 0-4 года на момент аварии из 86 выявленных случаев заболеваний РЩЖ за период наблюдения с 1991 по 2013 гг. к радиационно-обусловленным следует отнести 52 случая, что составляет 60,5% от всех выявленных случаев (табл. 2).
Таблица 2
Доля радиационно-обусловленных раков щитовидной железы среди детей в зависимости от возраста в 1986 г.
|
Возраст в 1986 г. (лет) |
0-4 |
5-9 |
10-17 |
|
Средняя доза (мГр) |
326 |
149 |
88 |
|
Число выявленных случаев РЩЖ |
86 |
78 |
152 |
|
Число радиационно-обусловленных РЩЖ |
52 |
23 |
4 |
|
Доля радиационно-обусловленных РЩЖ (%) |
60,5 |
30,0 |
2,6 |
Регистрация рака щитовидной железы среди детского населения Японии после аварии на АЭС «Фукусима-1»
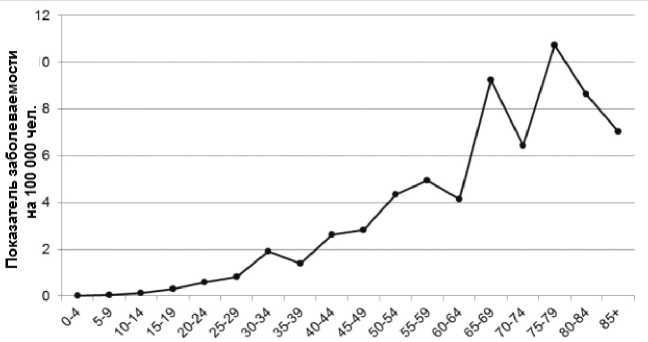
В 2015 г. МАГАТЭ опубликовало итоговый отчёт о последствиях аварии на АЭС «Фукусима-1» [21]. Четвёртый том этого отчёта посвящён прогнозу возможных радиологических последствий аварии для населения префектуры Фукусима. Активное участие в оценке ожидаемых для японского населения отдалённых эффектов радиационного воздействия принимали авторы настоящей статьи с использованием 30-летнего опыта ведения в России Национального радиационно-эпидемиологического регистра после аварии на Чернобыльской АЭС. Было в частности установлено с использованием моделей, разработанных МКРЗ и ВОЗ, а также фактических чернобыльских данных, что риск возможной индукции радиационно-обусловленных раков щитовидной железы составляет 0,1% для взрослого населения и 1,4% для детского населения от спонтанного уровня заболеваемости этой патологией в Японии. Частота спонтанной заболеваемости раком щитовидной железы в Японии показана на рис. 5 [21]. На основании этих данных был сделан основной вывод о крайне низкой вероятности регистрации повышения частоты заболеваемости раком щитовидной железы в Японии, обусловленной радиационным воздействием.
Возрастная группа
Рис. 5. Частота заболеваемости раком щитовидной железы на 100 000 чел. в зависимости от возраста в Японии (мужчины) в 2004 г.
В 2011 г. в Японии было инициировано крупномасштабное скрининговое ультразвуковое исследование патологии щитовидной железы среди детей и подростков префектуры Фукусима. В течение первого раунда диагностики в период с 2011 по 2013 гг. включительно ультразвуковое исследование прошли 298577 человек. Было диагностировано 110 случаев заболеваний раком щитовидной железы [17].
Фактические данные Национального регистра о заболеваемости РЩЖ населения Брянской, Тульской, Калужской и Орловской областей позволили спрогнозировать число нерадиационных случаев РЩЖ в рассматриваемой когорте детей и подростков префектуры Фукусима с учётом эффекта скрининга.
Так, по данным официальной национальной статистики в Японии [22], усреднённый показатель заболеваемости РЩЖ среди детей и подростков (0-19 лет) в Японии составляет 2.2 случая на 1 млн в год соответствующего населения. При известной численности в когорте наблюдения, ожидаемое число фоновых онкологических заболеваний с учётом эффекта скрининга может быть вычислено по следующей формуле:
СASES = ∑ PYR i ⋅λ i(Japan ) ⋅ ES , (5)
где PYR i – число человеко-лет под наблюдением в i -ой группе достигнутого возраста (0-4, 5-9, 10-14 и 15-19 лет), рассчитываемое как произведение численности исследуемой группы на средней возраст в группе, λ i(Japan) – показатель спонтанной заболеваемости РЩЖ в Японии среди детей и подростков в i -ой возрастной группе, ES – эффект скрининга в первый период наблюдения за когортой детей и подростков 4-х загрязнённых областей РФ после аварии на ЧАЭС ( ES =12,8; 95% ДИ: 8,6; 17,9).
Используя данные о численности возрастных групп из приложения 2 «Промежуточного доклада ультразвукового исследования щитовидной железы (первичный скрининг)» от 12 февраля 2015 г. [17] и значения усреднённых за период с 2000 по 2010 гг. показателей заболеваемости РЩЖ для детей и подростков в Японии (рис. 6) были рассчитаны человеко-годы под наблюдением для всей когорты. При расчёте человеко-лет под наблюдением в группе лиц проходивших обследование в 2012-2013 гг., учитывалось смещение в дате начала скрининга от 2011 г. Общее число человеко-лет под наблюдением составило 3 018 073.
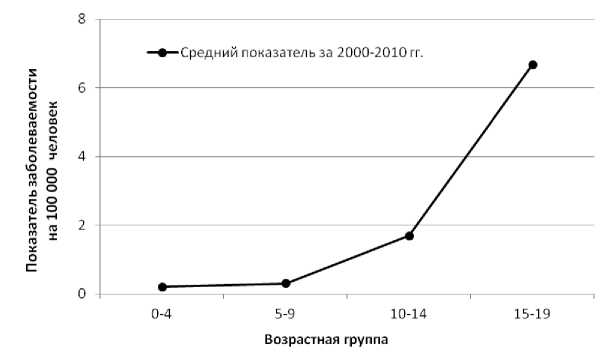
Рис. 6. Усреднённый за период с 2000 по 2010 гг. показатель заболеваемости раком щитовидной железы на 100 000 чел. в зависимости от возраста в Японии (оба пола) [22].
В табл. 3 приведены результаты прогноза числа нерадиационных случаев РЩЖ в рассматриваемой когорте детей и подростков префектуры Фукусима с учётом эффекта скрининга. В таблице также отражено число выявленных случаев РЩЖ по результатам первичного ультразвукового скрининга, проведённого в период с 9 октября 2011 г. по 31 марта 2014 г. [17]. Как видно из табл. 3, прогнозные и фактические данные о выявленных случаях заболеваний РЩЖ находятся в хорошем согласии.
Таблица 3
Прогноз числа нерадиационных случаев РЩЖ в рассматриваемой когорте детей и подростков префектуры Фукусима с учётом эффекта скрининга и среднего значения показателя заболеваемости РЩЖ в Японии (за 2000-2010 гг.)
|
Год скрининга |
Число детей и подростков, прошедших исследование |
Число выявленных случаев РЩЖ |
Прогнозируемое число случаев с учётом эффекта скрининга, 95% ДИ |
|
2011 |
41810 |
15 |
13,5 (9,0; 18,8) |
|
2012 |
139339 |
56 |
41,0 (27,6; 57,4) |
|
2013 |
117428 |
39 |
28,7 (19,3; 40,1) |
|
Всего |
298577 |
110 |
83,2 (55,9; 116,3) |
Заключение
Полученные результаты позволяют сделать следующие основные выводы:
-
1. На территориях Брянской, Тульской, Калужской и Орловской областей, в наибольшей степени подвергшихся радиационному загрязнению вследствие аварии на Чернобыльской АЭС, выявлено значительное увеличение частоты заболеваемости РЩЖ среди населения.
-
2. Значимый радиационный риск индукции РЩЖ установлен только для детей и подростков (0-17 лет) на момент аварии. Установлено, что для детей и подростков на момент аварии радиационный риск РЩЖ зависит от возраста на момент облучения и достигнутого возраста.
-
3. Для населения наиболее загрязнённых территорий Брянской, Тульской, Калужской и Орловской областей установлен выраженный скрининговый эффект в процессе регистрации заболеваний РЩЖ (6,74 для детей и подростков 0-17 лет на момент аварии и 1,5 для группы 18 лет и старше). Оценка коэффициента скрининга по периодам наблюдения выявила значимое (p<0,001) 2-кратное снижение эффекта скрининга, начиная с 1996 г., в сравнении с первым периодом (1991-1995 гг.).
-
4. Полученные данные Национального радиационно-эпидемиологического регистра оценки радиационных рисков заболеваний РЩЖ среди детей и подростков после аварии на Чернобыльской АЭС и о скрининговом эффекте были использованы для прогноза возможной регистрации РЩЖ в Японии после аварии на АЭС «Фукусима-1». Прогнозные и фактические данные о выявленных случаях заболеваний РЩЖ после аварии на АЭС «Фукусима-1» находятся в хорошем согласии.
Список литературы Рак щитовидной железы: уроки Чернобыля и их применение к ситуации в Фукусиме
- Ilyin L.A., Balonov M.I., Buldakov L.A., Bur'yak V.N., Gordeev K.I., Dement'ev S.I., Zhakov I.G., Zubovsky G.A., Kondrusev A.I., Konstantinov Y.O., Linge I.I., Likhtarev I.A., Lyaginskaya A.M., Matyuhin V.A., Pavlovsky O.A., Potapov A.I., Prysyazhnyuk A.E., Ramsaev P.V., Romanenko A.E., Savkin M.N., Starkova N.T., Tron'ko N.D., Tsyb A.F. Radiocontamination patterns and possible health consequences of the accident at the Chernobyl nuclear power station//J. Radiol. Prot. 1990. V. 10, N 1. P. 3-29.
- Kazakov V.S., Demidchik E.P., Astakhova L.N. Thyroid cancer after Chernobyl//Nature. 1992. V. 359. P. 1.
- Tronko M.D., Howe G.R., Bogdanova T.I., Bouville A.C., Epstein O.V., Brill A.B., Likhtarev I.A., Fink D.J., Markov V.V., Greenebaum E., Olijnyk V.A., Masnyk I.J., Shpak V.M., McConnell R.J., Tereshchenko V.P., Robbins J., Zvinchuk O.V., Zablotska L.B., Hatch M., Luckyanov N.K., Ron E., Thomas T.L., Voilleque P.G., Beebe G.W. A cohort study of thyroid cancer and other thyroid diseases after the Chernobyl accident: thyroid cancer in Ukraine detected during first screening//J. Natl. Cancer Inst. 2006. V. 98, N 13. P. 897-903.
- Average doses of exposure of a thyroid gland of inhabitants of the different age living in 1986 in settlements of Bryansk, Tula, Oryol and Kaluga areas contaminated by radionuclides after the Chernobyl accident: Directory, the Edition Official. Eds. Balonov M.I., Zvonova I.A. Moscow: Ministry of Health of Russia, 2002.
- Likhtarov I., Kovgan L., Vavilov S., Chepurny M., Ron E., Lubin J., Bouville A., Tronko N., Bogdanova T., Gulak L., Zablotska L., Howe G. Post-Chernobyl thyroid cancers in Ukraine. Report 2: risk analysis//Radiat. Res. 2006. V. 166, N 2. P. 375-386.
- Jacob P., Bogdanova T.I., Buglova E., Chepurniy M., Demidchik Y., Gavrilin Y., Kenigsberg J., Meckbach R., Schotola C., Shinkarev S., Tronko M.D., Ulanovsky A., Vavilov S., Walsh L. Thyroid cancer risk in areas of Ukraine and Belarus affected by the Chernobyl accident//Radiat. Res. 2006. V. 165, N 1. P. 1-8.
- Cardis E., Kesminiene A., Ivanov V., Malakhova I., Shibata Y., Khrouch V., Drozdovitch V., Maceika E., Zvonova I., Vlasov O., Bouville A., Goulko G., Hoshi M., Abrosimov A., Anoshko J., Astakhova L., Chekin S., Demidchik E., Galanti R., Ito M., Korobova E., Lushnikov E., Maksioutov M., Masyakin V., Nerovnia A., Parshin V., Parshkov E., Piliptsevich N., Pinchera A., Polyakov S., Shabeka N., Suonio E., Tenet V., Tsyb A., Yamashita S., Williams D. Risk of thyroid cancer after exposure to 131I in childhood//J. Natl. Cancer Inst. 2005. V. 97, N 10. P. 724-732.
- Brenner A.V., Tronko M.D., Hatch M., Bogdanova T.I., Oliynik V.A., Lubin J.H., Zablotska L.B., Tereschenko V.P., McConnell R.J., Zamotaeva G.A., O'Kane P., Bouville A.C., Chaykovskaya L.V., Greenebaum E., Paster I.P., Shpak V.M., Ron E. I-131 dose response for incident thyroid cancers in Ukraine related to the Chernobyl accident//Environ. Health Perspect. 2011. V. 119, N 7. P. 933-939.
- Zablotska L.B., Ron E., Rozhko A.V., Hatch M., Polyanskaya O.N., Brenner A.V., Lubin J., Romanov G.N., McConnell R.J., O'Kane P., Evseenko V.V., Drozdovitch V.V., Luckyanov N., Minenko V.F., Bouville A., Masyakin V.B. Thyroid cancer risk in Belarus among children and adolescents exposed to radioiodine after the Chernobyl accident//Br. J. Cancer. 2011. V. 104, N 1. P. 181-187.
- Jacob P., Bogdanova T.I., Buglova E., Chepurniy M., Demidchik Y., Gavrilin Y., Kenigsberg J., Kruk J., Schotola C., Shinkarev S., Tronko M.D., Vavilov S. Thyroid cancer among Ukrainians and Belarusians who were children or adolescents at the time of the Chernobyl accident//J. Radiol. Prot. 2006. V. 26, N 1. P. 51-67.
- Walsh L., Jacob P., Kaiser J.C. Radiation risk modeling of thyroid cancer with special emphasis on the Chernobyl epidemiological data//Radiat. Res. 2009. V. 172, N 4. P. 509-518.
- Ivanov V.K., Kashcheev V.V., Chekin S.Yu., Maksioutov M.A., Tumanov K.A., Vlasov O.K., Shchukina N.V., Tsyb A.F. Radiation-epidemiological studies of thyroid cancer incidence in Russia after the Chernobyl accident (estimation of radiation risks, 1991-2008 follow-up period)//Radiat. Prot. Dosimetry. 2012. V. 151, N 3. P. 489-499; DOI: 10.1093/rpd/ncs019
- Публикация МКРЗ/Под ред. М.Ф. Киселёва и др. М.: ПКФ «Алана», 2009. 311 с.
- Ron E., Lubin J.H., Shore R.E., Mabuchi K., Modan B., Pottern L.M., Schneider A.B., Tucker M.A., Boice J.D.Jr. Thyroid cancer after exposure to external radiation: a pooled analysis of seven studies//Radiat Res. 1995. V. 141, N 3. P. 259-277.
- Preston D.L., Ron E., Tokuoka S., Funamoto S., Nishi N., Soda M., Mabuchi K., Kodama K. Solid cancer incidence in atomic bomb survivors: 1958-1998//Radiat. Res. 2007. V. 168, N 1. P. 1-64.
- Кащеев В.В., Чекин С.Ю., Максютов М.А., Туманов К.А., Корело А.М., Кочергина Е.В., Власов О.К., Щукина Н.В., Иванов В.К. Оценка радиационных рисков и эффекта скрининга рака щитовидной железы среди населения Брянской и Орловской областей Российской Федерации//Радиация и риск. 2015. Т. 24, № 1. С. 8-22.
- Overview of the Fukushima Health Management Survey. Available at: http://fmu-global.jp/fukushima-health-management-survey (accessed 19.05.2016).
- Злокачественные новообразования в России в 2012 гг. (заболеваемость и смертность): справочник/Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М., 2014.
- Медицинские радиологические последствия Чернобыля: прогноз и фактические данные спустя 30 лет/Под общей ред. чл.-корр. РАН В.К. Иванова, чл.-корр. РАН А.Д. Каприна. М.: ГЕОС, 2015. 450 с.
- Dalgaard P. Introductory Statistics with R. Springer, 2nd edition, 2008. ISBN 978-0-387-79053-4.
- The Fukushima Daiichi Accident. Technical Volume 4/5. Radiological Consequences. Vienna: IAEA, 2015. 250 p.
- Cancer Statistics in Japan. Available at: http://www.ncc.go.jp/en/index.html (accessed 19.05.2016).


