Ранние исходы аутологичной трансплантации гемопоэтических стволовых клеток у пациентов с ремиттирующим типом течения рассеянного склероза
Автор: Николаев И.С., Шамтиева К.В., Пугачев А.Ю., Мельниченко В.Я., Федоренко Д.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4-2 т.17, 2022 года.
Бесплатный доступ
Обоснование исследования: В течение более 20 лет в мире успешно применяется высокодозная иммуносупрессивная терапия (ВИСТ) с аутологичной трансплантацией гемопоэтических стволовых клеток (аутоТГСК) для остановки прогрессирования рассеянного склероза (РС). Эффективность такой терапии доказана во многих многоцентровых рандомизированных исследованиях. Однако, данных о исходах такого лечения в раннем посттрансплантационном периоде (до трех месяцев) в мировой литературе недостаточно. Цель: оценить ранние неврологические исходы ВИСТ с последующей аутоТГСК у пациентов с ремиттирующим типом течения рассеянного склероза (РРС). Методы: в исследование включено 20 пациентов с достоверным РРС (McDonald 2017). Среди них 6 мужчин и 14 женщин в возрасте от 19 до 51 года (медиана 34,2±9,6 года), перенесших ВИСТ (R-Cph 200) с последующей аутоТГСК. Период наблюдения составил от 31 до 34 дней (медиана 31,45 дня). В обеих точках исследования оценен неврологический статус по Scripps neurologic rating scale (SNRS), балл по расширенной шкале нарушения жизнедеятельности Куртцке (EDSS), МРТ головного и спинного мозга с контрастированием, наличие спастичности в паретичных конечностях по модифицированной шкале Ашворта (MAS). Результаты. После проведения лечения были получены значимые различия как для EDSS (p = 0,0001), так и SNRS (p = 0,00004). Улучшение по шкале EDSS в среднем составило 0,5 баллов [0; 1] у 13 пациентов (65%). По шкале SNRS — 5 баллов [3; 9] у 19 пациентов (95%). Исчезновение накопления контраста отмечено у трёх пациентов (30%), однако, у одного (10%) выявлено накопление контрастного препарата, которого ранее не наблюдалось. Наличия отрицательной динамики по шкалам EDSS и SNRS у этого пациента не отмечено. У 6 (75%) пациентов выявлено уменьшение выраженности повышения пирамидного тонуса по MAS не менее чем на 1 балл. Заключение. ВИСТ с аутоТГСК способно улучшить показатели шкалы неврологического рейтинга и расширенной шкалы инвалидизации даже в раннем посттрансплантационном периоде. Для более точной оценки эффективности лечения предпочтительнее оценка динамики по шкале SNRS за счет ее комплексности и полноты используемых показателей. Отсутствие накопления контрастного вещества при МРТ в ранние сроки после лечения выявлено в 30% случаев. У 75% пациентов отмечено уменьшение спастичности на 1 балл по шкале MAS через 2 недели после ВИСТ с аутоТГСК.
Ремиттирующий рассеянный склероз, ВИСТ+аутоТГСК, аутологичная трансплантация стволовых кроветворных клеток. Autologous hematopoietic stem cell transplantation, HSCT
Короткий адрес: https://sciup.org/140300769
IDR: 140300769 | DOI: 10.25881/20728255_2022_17_4_2_81
Early outcomes of autologous hematopoietic stem cell transplantation in patients with relapsing-remitting type of multiple sclerosis
Background of the study: for more than 20 years, high-dose immunosuppressive therapy (HIST) with autologous hematopoietic stem cell transplantation (autoHSCT) has been successfully used in the world to stop the progression of multiple sclerosis (MS). The effectiveness of this therapy has been proven in many multicenter randomized trials. However, data on the outcomes of such treatment in the early post-transplant period (up to three months) in the world literature is not enough. Objective: to evaluate the early neurological outcomes of HIST followed by autoHSCT in patients with relapsing-remitting multiple sclerosis (RRMS). Methods: the study included 20 patients with significant RMS (McDonald 2017). Among them, 6 men and 14 women aged 19 to 51 years (median 34.2±9.6 years) who underwent VIST (R-Cph 200) followed by autoHSCT. The follow-up period ranged from 31 to 34 days (median 31.45 days). At both points of the study, the neurological status was assessed according to the Scripps neurologic rating scale (SNRS), the score on the extended Kurtzke disability scale (EDSS), MRI of the brain and spinal cord with contrast, the presence of spasticity in the paretic limbs according to the modified Ashworth scale (MAS). Results. After treatment, significant differences were obtained for both EDSS (p = 0.0001) and SNRS (p=0.00004). Improvement on the EDSS scale averaged 0.5 points [0; 1] in 13 patients (65%). According to the SNRS scale — 5 points [3; 9] in 19 patients (95%). The disappearance of contrast accumulation was noted in three patients (30%), however, in one (10%), an accumulation of a contrast agent was detected, which was not previously observed. The presence of negative dynamics according to the EDSS and SNRS scales was not observed in this patient. In 6 (75%) patients, a decrease in the severity of the increase in pyramidal tone according to MAS was revealed by at least 1 point. Conclusion. HIST with autoHSCT can improve the performance of the neurological rating scale and the extended disability scale even in the early post-transplant period. For a more accurate assessment of the effectiveness of treatment, it is preferable to evaluate the dynamics on the SNRS scale due to its complexity and completeness of the indicators used. Absence of accumulation of a contrast agent during MRI in the early stages after treatment was detected in 30% of cases. In 75% of patients, a decrease in spasticity by 1 point on the MAS scale was noted 2 weeks after VIST with autoHSCT.
Текст научной статьи Ранние исходы аутологичной трансплантации гемопоэтических стволовых клеток у пациентов с ремиттирующим типом течения рассеянного склероза
фузному поражению центральной нервной системы, ведущее к инвалидизации и значительному снижению качества жизни [1]. Причины возникновения РС в настоящее время остаются неизвестными. Средний возраст начала РС в различных исследованиях ко-

леблется от 28 до 31 года. Чаще всего клиническая картина дебютирует в возрасте от 15 до 45 лет [2]. Ремиттирующий тип РС (РРС) имеет более раннее начало и в течение 15 лет с вероятностью в 60% может привести к вторичному прогрессированию [3]. По данным многоцентровых клинических исследований препараты, изменяющие течение рассеянного склероза (ПИТРС) безопасны и способны снижать частоту обострений до 68% по сравнению с плацебо, а риск прогрессирования заболевания до 42% в течение 2 лет в зависимости от типа течения РС [4]. Однако, ведущей в определении эффективности терапии является клиническая картина. Традиционные методы патогенетической терапии более чем в 30% случаев [5] не позволяют добиться стойкого контроля над заболеванием, кроме того, обладают рядом побочных эффектов. Первые данные об эффективности высокодозной иммуносупрессивной терапии (ВИСТ) с аутологичной трансплантацией гемопоэтических стволовых клеток (аутоТГСК) при РС представлены Fassas et al. в 1997 году. Длительные неврологические улучшения были обнаружены как при оценке по расширенной шкале ивалидизации Курцке (EDSS), так и Scripps neurologic rating scale (SNRS) [6]. Исследование навело на мысль, что использование ВИСТ+аутоТГСК представляется возможной у больных РС и дает положительный клинический эффект.
В России первая трансплантация кроветворных клеток при РС проведена в 1999 году на базе клиники гематологии и клинической иммунологии Военномедицинской академии под руководством Ю.Л. Шевченко, А.А. Новика, РАН М.М. Одинака [7; 8].
Учитывая ряд удачных клинических исследований за последние 5–7 лет, аутоТГСК все чаще рассматривается в качестве альтернативного метода лечения РС при отказе пациентов от стандартной терапии или ее неэффективности [8–10].
По данным зарубежных авторов, у пациентов с РРС лимфаблативный протокол приводил к более позднему прогрессированию заболевания, улучшению неврологических показателей и уменьшению количества новых очагов по данным МРТ. Данные показатели оценивались в течение 5 лет [11–13]. Литературных данных в настоящее время о раннем эффекте ВИСТ+аутоТГСК недостаточно, что и послужило поводом для данного исследования.
Цель исследования — оценить ранние неврологические исходы ВИСТ с аутоТГСК у пациентов с РРС.
Материалы и методы
В исследование включено 20 пациентов (34,2±9,6 лет, 6 мужчин и 14 женщин) с достоверным РРС, установленный согласно критериям Макдональда от 2017 г. (средняя длительность заболевания — 4,7±2,5 года), перенесших ВИСТ по немиелоаблативному протоколу (R-Cph 200) с последующей аутоТГСК. Критериями включения в исследование были: подтвержденный диагноз ремиттирующего РС, возраст старше 18 лет, отсутствие абсолютных противопоказаний к лечению (наличие тяжелой соматической патологии, инфекционные заболевания, иммунодефицит, аномальные показатели тромбоцитов или лейкоцитов до лечения). Критерии исключения — отказ пациента от участия в исследовании, дальнейшего лечения, возраст младше 18 лет, наличие ВИЧ-инфекции, первичный или вторичный прогрессирующий рассеянный склероз, наследственные неврологические заболевания, беременность, легочная, сердечная, почечная или печеночная недостаточность, аномальные показатели тромбоцитов или лейкоцитов до лечения, активная инфекция, предшествующее лечение алемтузумабом или митоксантро-ном в течение 1 года до ВИСТ с аутоТГСК.
Период наблюдения составил от 31 до 34 суток (медиана 31,45 суток). Первичный осмотр проводился при поступлении в клинику. Инфузия гемопоэтических стволовых клеток (ГСК) проводилась на 7–19 сутки после первичного осмотра (медиана 14,6 суток). Повторный осмотр проводился на 11–20 сутки (медиана 13,1 суток) после даты трансплантации. В обеих точках наблюдения у пациента был оценен неврологический статус по шкале SNRS [14] и EDSS [15], выполнена МРТ головного и спинного мозга с контрастированием. МРТ-исследование головного мозга проводилось на магнитно-резонансном томографе Siemens MAGN-ETOM Verio с величиной магнитной индукции 3 Тл с использованием 12-канальной головной катушки (Siemens AG, Erlangen, Германия), контрастное усиление (КУ) «Ультравист» 0,2 мл/кг массы тела. Оценивались аксиальные, коронарные и сагиттальные срезы. Активными считали очаги патологического накопления контрастного вещества в белом веществе [16; 17]. При оценке учитывались наличие/отсутствие активности в очагах демиелинизации. Также, при первичном обращении фиксировались эффект от предшествующей терапии ПИТРС и динамика показателей EDSS в течение 12 месяцев. У всех пациентов отмечалось прогрессирование заболевания на проводимой терапии ПИТРС. Проведена оценка мышечного тонуса с целью выявления спастичности в паретичных конечностях. Данный параметр оценивался по модифицированной шкале Ашворта (MAS) [18] до и после лечения.
Характеристика программы трансплантации
20 пациентов были подвержены мобилизации стволовых кроветворных клеток с помощью гранулоцитарного колониестимулирующего фактора (G-CSF) в дозе 10 мкг/кг/сутки в течение 4-х суток. На 5-е сутки проведен лейкоцитаферез с забором CD34+-клеток в количестве 2-4 х 10 6 /кг массы тела больного. Полученный материал подвергался криоконсервации с помощью диметилсульфаксида 10% и жидкого азота температурой -180 °С, где хранился до использования.

Николаев И.С., Шамтиева К.В., Пугачев А.Ю. и др.
РАННИЕ ИСХОДЫ АУТОЛОГИЧНОЙ ТРАНСПЛАНТАЦИИ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК У ПАЦИЕНТОВ С РЕМИТТИРУЮЩИМ ТИПОМ ТЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА
Высокодозную иммуносупрессию проводили с использованием Циклофосфамида со 2 по 5 сутки в дозе 200 мг/кг, и Ритуксимаба 500 мг/м2 при нормализации показателей гемограммы, однократно. По окончанию химиотерапии производилось размораживание и инфузия ГСК. Оттаивание замороженного трансплантата осуществлялось на водняной бане при температуре 37 °С непосредственно перед инфузией. Введение ГСК осуществлялось внутривенно через центральный катетер на фоне проведения инфузионно-корригирующей терапии и премедикации.
Статистическая обработка данных
Статистический анализ проводился с помощью программного обеспечения SPSS Statistics 23.0 (IBM). Основной описательной статистикой для категориальных и порядковых переменных были частота и процентная доля, для количественных переменных — среднее и стандартное отклонение или медиана и квартили. Во всех случаях использовали двусторонние варианты статистических критериев. Нулевую гипотезу отвергали при p<0,05. Учитывая объем выборки менее 30, в спорных случаях предпочтение отдавалось анализу непараметрическими методами.
Для оценки состояния пациентов до и после лечения по исследуемым шкалам использовался t-критерия Стьюдента для связанных выборок, т.к. показатели подсчета являлись количественными. Для одновременного уточнения связи многих признаков использовался метод многофакторного статистического анализа — линейный регрессионный анализ. Для оценки предсказательной способности отдельных показателей в развитии ожидаемых исходов использовали бинарную логистическую регрессию.
Результаты
Все пациенты вошедшие в группу исследования имели ремиттирующий характер течения РС и длительность заболевания не более 10 лет (таблица 1).
Табл. 1. Общая характеристика группы
|
Показатель |
Пациенты с РРС n = 20 |
|
Средний возраст (mean ± SD) |
34,2±9,6, min. 18, max 51 |
|
Соотношение мужчин / женщин (n, %) |
6 (30%) / 14 (70%) |
|
Длительность заболевания (Me [Q25%; Q75%]) |
4,7±2,5, min. 1, max 10 |
|
EDSS за 12 месяцев до начала лечения (Me [Q25%; Q75%]) |
3 [1,5; 4,5] |
|
EDSS за 6 месяцев до начала лечения (Me [Q25%; Q75%]) |
3,5 [3,0; 4,0] |
|
EDSS при начале лечения (Me [Q25%; Q75%]) |
4,5 [3,5; 4,5] |
|
SNRS при начале лечения (Me [Q25%; Q75%]) |
83 [76; 92] |
|
МРТ головного и спинного мозга с контрастированием (КУ «Ультравист» 0,2 мл/кг м тела) |
20 (100%) |
|
-Gd+ |
10 (50%) |
|
-Gd- |
10 (50%) |
|
Спастический парез (тип) |
8 (40%) |
|
-Гемипарез |
3 (37,5%) |
|
-Парапарез |
5 (62,5%) |
|
-Трипарез |
0 |
|
-Монопарез |
0 |
|
Спастичность (MAS) -0 |
8 (40%) |
|
-1 |
2 (25%) |
|
-1+ |
3 (37,5%) |
|
-2 |
2 (25%) |
|
-3 |
1 (12,5%) |
|
-4 |
0 |
После проведения лечения были получены значимые различия как для EDSS (p = 0,0001), так и SNRS (p = 0,00004) (Рис. 1).
Пациенты удовлетворительно перенесли процедуру. Жизнеугрожающих осложнений и летальных исходов не было.
Улучшение по шкале EDSS составило 0,5 баллов [0; 1], улучшение функциональной активности при использовании оценки данной шкалой лечения на-
SNRS
EDSS р = 0,0001
p = 0,00004
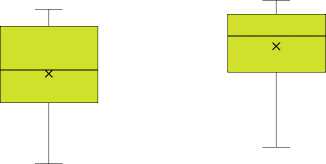
до лечения после лечения
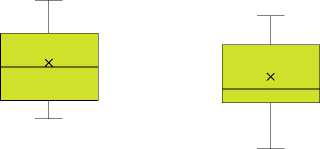
до лечения после лечения
Рис. 1. Сопоставление шкал EDSS и SNRS до и после лечения.

блюдалось у 13 пациентов (65%). В то время как при использовании SNRS улучшение составило 5 баллов [3; 9] и было в той или иной степени показано у 19 пациентов (95%).
При использовании множественной линейной регрессии показано, что балл по шкале EDSS через 2 недели после лечения зависел только от исходного показателя непосредственно перед лечением. Не было выявлено зависимости степени улучшения пациентов после проведения терапии от исходного балла EDSS за 12 месяцев и 6 месяцев, длительности заболевания и возраста пациентов. SNRS через 2 недели после лечения также зависел только от исходного показателя непосредственно перед лечением, но не от длительности заболевания и возраста пациентов.
При включении в исследование у 10 пациентов было выявлено накопление контраста очагами демиелинизации. После лечения отсутствие накопления контраста отмечено у трёх пациентов (30%). Однако, у одного (10%) выявлено накопление контрастного препарата, которого ранее не наблюдалось. Наличия отрицательной динамики по шкалам EDSS и SNRS у этого пациента не отмечено.
Из 20 пациентов, включенных в исследование, 8 (40%) имели спастичность. У 5 пациентов выявлено изменение мышечного тонуса в нижних конечностях и у 3 по гемитипу. При повторном осмотре у 4 пациентов из группы спастического парапареза и у 2 пациентов из группы гемипареза отмечалось снижение мышечного тонуса на 1 балл по шкале MAS. Таким образом, у 6 (75%) пациентов выявлено уменьшение выраженности повышения пирамидного тонуса по шкале Ашворта не менее чем на 1 балл. Использование логистической регрессии не выявлено значимой связи данного феномена ни с длительностью заболевания, ни с возрастом, ни с показателями EDSS или SNRS до и после лечения.
Выводы
ВИСТ с аутоТГСК способно улучшить показатели шкалы неврологического рейтинга (SNRS) и расширенной шкалы инвалидизации Курцке (EDSS) даже в раннем посттрансплантационном периоде. Однако, в нашем исследовании отмечено, что для более точной оценки эффективности лечения предпочтительнее оценка динамики по шкале SNRS за счет ее комплексности и полноты используемых показателей.
Показатель EDSS и SNRS в динамике через 2 недели после лечения зависел только от исходного показателя непосредственно перед лечением. Зависимости от длительности заболевания, возраста и функционального состояния пациентов в течение предшествующего года не отмечено. Отсутствие связи эффективности лечения и длительности заболевания можно объяснить тем, что в данной выборке средняя длительность заболевания составляла менее 5 лет, что является благоприятным предиктором такого лечения [19].
Отсутствие накопления контрастного вещества при МРТ в ранние сроки после лечения отмечена в 30% случаев, что не является показательной на данном этапе оценки эффективности такого лечения. У 1 пациента отмечена фиксация парамегнетика после лечения, хотя ранее МР-активности зафиксировано не было. Однако, МР-картина не коррелировала с отрицательной динамикой по шкале SNRS и EDSS.
Ценностью данного исследования является оценка динамики спастичности в ранние сроки после ВИСТ с аутоТГСК при РРС, что в настоящее время в литературе не освещено. В открытом неконтролируемом клиническом исследовании отмечена положительная динамика регресса спастичности при церебральном параличе у детей от 2–15 лет после аутологичной трансплантации мононуклеарных клеток костного мозга, но результаты представлены на 3–6 мес наблюдений [20]. В нашем исследовании показано уменьшение спастичности на 1 балл по шкале MAS в 75% случаев у пациентов с РРС через 2 недели после ВИСТ с аутоТГСК.
Ограничением исследования является небольшая выборка пациентов, однако уже на ней получены доказательства влияния ВИСТ с аутоТГСК на неврологический дефицит, спастичность и степень ивалиди-зации.
Таким образом, оценка ранних исходов ВИСТ с аутоТГСК у больных РРС позволяет сделать предварительные выводы об эффективности и безопасности данной процедуры, однако, необходимы дальнейшие исследования данной программы терапии.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
РАННИЕ ИСХОДЫ АУТОЛОГИЧНОЙ ТРАНСПЛАНТАЦИИ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК У ПАЦИЕНТОВ С РЕМИТТИРУЮЩИМ ТИПОМ ТЕЧЕНИЯ РАССЕЯННОГО СКЛЕРОЗА
Список литературы Ранние исходы аутологичной трансплантации гемопоэтических стволовых клеток у пациентов с ремиттирующим типом течения рассеянного склероза
- Гусев Е.И., Гехт А.Б. Клинические рекомендации по рассеянному склерозу, 2018.
- Goodin DS. The epidemiology of multiple sclerosis: insights to disease pathogenesis. Handb Clin Neurol. 2014; 122: 231.
- Гусев Е.И. Рассеянный склероз и другие демиелинизирующие заболевания. — М. : Миклош, 2004. — С.162.
- Вотинцева М.В., Петров А.М., Столяров И.Д. Препараты на основе моноклональных антител: настоящее и будущее в лечении рассеянного склероза (по материалам 32-го Конгресса Европейского комитета по лечению и исследованию рассеянного склероза-ECTRIMS) // Анналы клинической и экспериментальной неврологии. — 2017. — Т.11. — №2. doi 10.18454/ACEN.2017.2.12. — EDN YZFQLX.
- Котов С.В., Якушина Т.И., Лиждвой В.Ю. Длительное сравнительное исследование эффективности препаратов, изменяющих течение рассеянного склероза // Альманах клинической медицины. — 2011. — №25.
- Fassas A, et al. Peripheral blood stem cell transplantation in the treatment of progressive multiple sclerosis: first results of a pilot study. Bone marrow transplantation. 1997; 20(8): 631-638.
- Новик А.А., Богданов А.Н. Принципы трансплантации костного мозга и стволовых клеток периферической крови. — СПб.: ВМА, 2001.
- Shevchenko YL, Novik AA, Kuznetsov AN, et al. Autologous hematopoietic stem cell transplantation in multiple sclerosis. Cellular Therapy and Transplantation. doi 10.1007/s00277-015-2337-8.
- Atkins HL, Bowman M, Allan D, et al. Immunoablation and autologous haemopoietic stem-cell transplantation for aggressive multiple sclerosis: a multicentre single-group phase 2 trial. Lancet. 2016; 388: 576-85.
- Burt RK, Balabanov R, Burman J, et al. Effect of Nonmyeloablative Hematopoietic Stem Cell Transplantation vs Continued Disease-Modifying Therapy on Disease Progression in Patients With Relapsing-Remitting Multiple Sclerosis: A Randomized Clinical Trial. JAMA. 2019; 321(2): 165-174. doi:10.1001/jama.2018.18743.
- Mancardi GL, Sormani MP, Gualandi F, et al. Autologous hematopoietic stem cell transplantation in multiple sclerosis: a phase II trial. Neurology. 2015; 84: 981-8.
- Burt RK, Balabanov R, Han X, et al. Association of nonmyeloablative hematopoietic stem cell transplantation with neurological disability in patients with relapsing-remitting multiple sclerosis. JAMA. 2015; 313: 275-84.
- Nash RA, Hutton GJ, Racke MK, et al. High-dose immunosuppressive therapy and autologous HCT for relapsing-remitting MS. Neurology 2017; 88: 842-52.
- Koziol JA, et al. Responsiveness of the Scripps neurologic rating scale during a multiple sclerosis clinical trial. Canadian journal of neurological sciences. 1999; 26(4): 283-289.
- Kurtzke JF. Rating neurologic impairment in multiple sclerosis: an expanded disability status scale (EDSS). Neurology. 1983; 33: 1444-1452.
- Paty DW, et al. MRI in the diagnosis of MS: a prospective study with comparison of clinical evaluation, evoked potentials, oligoclonal banding, and CT. Neurology. 1988; 38(2): 180.
- Offenbacher H. et al. Assessment of MRI criteria for a diagnosis of MS. Neurology. 1993; 43(5): 905.
- Barnes MP, et al. Spasticity in multiple sclerosis. Neurorehabilitation and neural repair. 2003; 17(1): 66-70.
- Федоренко Д.А. Принципы оценки эффективности аутологичной трансплантации гемопоэтических стволовых клеток у больных лимфомами и рассеянным склерозом: Дис.… докт. мед. наук, 2015.
- Nguyen LT, et al. Outcomes of autologous bone marrow mononuclear cells for cerebral palsy: an open label uncontrolled clinical trial. BMC pediatrics. 2017; 17(1): 104.


