Ранняя послеоперационная реабилитация (fast track) при лапаро-торакоскопических резекциях проксимального отдела желудка и грудного отдела пищевода при кардиоэзофагеальном раке
Автор: Аллахвердян А.С., Овезов А.М., Анипченко Н.Н., Анипченко А.Н.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 4 (56), 2017 года.
Бесплатный доступ
Препятствием к использованию малоинвазивных видеоэндоскопических доступов при радикальных хирургических операциях по по- воду кардиоэзофагеального рака служит необходимость выполнения резекции и лимфаденэктомии в двух анатомических зонах. Решение проблемы травматизма хирургических доступов актуализирует проблему оптимального послеоперационного ведения данной категории больных.В 2015-16 гг. было выполнено 27 резекций проксимального отдела желудка и ниж-не-грудного отдела пищевода с одномоментной внутриплев- ральной эзофагогастропласти-кой комбинированным лапароскопическим и правосторонним торакоскопическим досту-пом. Преобладали больные в III стадии заболевания - 14 (51,9 %) больных. В 4 (14,8 %) случаях была выявлена IV стадия. Резекция R0 была выполнена 24 (88,9%) больным, R1 - 3 (11,1 %). При гистологическом исследовании в среднем исследовалось 42±3 лимфатиче-ских узла. Преимущества радикальных операций при кардиоэзофагеальном раке комби-нированным лапароскопическим и правосторонним торакоскопическим доступом: чет-кость визуализации, хо- роший контроль гемостаза, удобство мобилизации желудка и пи-щевода, ранняя активизация больных в послеоперационном периоде (на 4-е сутки), со-кращение сроков стационарного лечения (7,3 суток). Применение технологии ранней по-слеоперационной реабилитации (fast-track ) позволяет уменьшить сроки госпитализации, ускорить выздоровление и восстановление трудоспособности больных.
Кардиоэзофагеальный рак, лапаро-торакоскопический доступ, ранняя реабилитация
Короткий адрес: https://sciup.org/142212761
IDR: 142212761 | УДК: 616.33-073.75
Early postoperative rehabilitation (fast track) after laparo-thoracoscopic re-section of the proximal stomach and thoracic esophagus about cardioesophageal cancer
An obstacle to the use of minimally invasive video-endoscopic approaches for radical surgical operations for cardioesophageal cancer is the need of resection and lymphadenectomy in the two anatomical areas. The resolution of the problem of injuries surgical accesses actualizes the problem of optimal postoperative management of these patients. In 2015-16, we performed 27 resection of the proximal stomach and lower esophagus with one-stage intrapleural esophagogastroplasty a combined laparoscopic and right thoracoscopic access. Prevailed patients in III stage of disease - 9 14 (51,9 %) patients. In 4 cases ( 14,8%) cases were identified with stage IV. R0 resection was performed in 24 (88,9%) patients, R1 - 3 (11,1 %). Histological examination was studied on average 42±3 lymph node. The advantages of radical operations for cardioesophageal cancer a combined laparoscopic and right thoracoscopic approaches: the clarity of the visualization, good control of hemostasis, ease of mobilization of the stomach and esophagus, early activation of patients in the postoperative period (4 days), reduced length of hospital stay (7.3 days). The use of early rehabilitation after surgery technology (ERAS or “fast-track”) allows to reduce the duration of hospitalization, accelerate recovery and rehabilitation of patients.
Текст научной статьи Ранняя послеоперационная реабилитация (fast track) при лапаро-торакоскопических резекциях проксимального отдела желудка и грудного отдела пищевода при кардиоэзофагеальном раке
Внедрение эндоскопических методов лечения привело к уменьшению сроков госпитализации, скорейшему выздоровлению и восстановлению трудоспособности оперируемых пациентов. Однако использование малотравматичных доступов не уменьшает объем операции и предполагает решение комплекса задач, направленного на ускорение ранней реабилитации больных.
Уменьшение травматичности онкологических операций больших объемов ставит перед хирургами целый комплекс сложных задач. Это особенно значимо при лечении карди-оэзофагеального рака (КЭР), которое представляет трудности даже в «открытой» хирургии. Они обусловлены необходимостью выполнения резекции и лимфаденэктомии в двух анатомических зонах [1, 2, 3]. До сих пор остаются спорными вопросы целесообразных объемов резекции и выбора «открытого» хирургического доступа. Чаще всего используются трансторакальные (левосторонний торакоабдоминальный по Осаве-Гэрлоку, комбинированный ла-паротомный с правосторонней торакотомией по Льюису) и трансхиатальный абдоминоцервикальный доступы [1, 4, 5, 6, 7]. Бесспорна необходимость расширенной лимфодис-секции в средостении и брюшной полости при радикальном удалении опухоли с резекцией и желудка, и пищевода [2, 3,
4, 6]. Подобные вмешательства также сопровождаются реконструкцией пищеварительного тракта. Трансторакальные доступы, позволяющие достичь большего радикализма и выполнить реконструкцию оптимальным образом, наиболее травматичны и затрудняют последующую реабилитацию больных, осложняя тем самым проведение комбинированного лечения. Реже используемый абдоми-но-медиастинальный доступ позволяет достичь меньшего травматизма даже по сравнению со стандартным трансхиатальным абдоминоцервикальным [6]. В то же время он существенно ограничивает уровень резекции пищевода и объем медиастинальной лимфодиссекции, что определяет целесообразность его применения при распространении опухоли не выше наддиафрагмального сегмента пищевода.
Поиски, направленные на снижение травматизма доступов и выполнения малоинвазивных хирургических операций, неизбежно привели к использованию возможностей видеоэндоскопической хирургии. При этом хирурги также столкнулись с трудностями, обусловленными необходимостью выполнения массивных операций в двух анатомических зонах. По-прежнему ключевую роль играют доступ и способ реконструкции, включающий особенности формирования пищеводного анастомоза. Очевидно, что хирургический доступ, при малой травматичности, должен обеспечить возможность полноценного выполнения резек- ционного и реконструктивного этапов. В нашем арсенале лишь два малоинвазивных доступа, позволяющих решить поставленные задачи. Это лапароскопический и торакоскопический доступы в различных комбинациях.
Есть публикации, посвященные лапароскопическим операциям у данной категории больных [8, 9]. Однако, оценка радикальности подобных операций не внушает оптимизма. Ряд авторов выполняют лапароскопические трансхиатальные эзофагэктомии при КЭР 1 типа, когда нет необходимости обширной проксимальной резекции желудка, и существует возможность формирования желудочного трансплантата достаточной длины, формируя пищеводный анастомоз на шее [8, 10, 11]. В похожих случаях используется также комбинация лапароскопического и правостороннего торакоскопического доступов с формированием пищеводного анастомоза третьим, шейным, доступом [12]. При невозможности формирования пищеводного анастомоза на шее, выполнялась торакотомия. Авторы отмечают значительное снижение числа послеоперационных, в первую очередь легочных и сердечно-сосудистых, осложнений после малоинвазивных вмешательств.
Тем не менее, следует отметить, что малоинвазивная хирургия в этом разделе осуществляется путем использования комбинации малоинвазивных, видеоэндоскопических, и открытых доступов. И это, в первую очередь, связано с трудностями, которые представляет восстановление целостности пищеварительного тракта после резекции и пищевода и желудка. Длина формируемого желудочного стебля не всегда позволяет вывести анастомоз на шею, и в такой ситуации чаще всего возникает необходимость резекции пищевода на уровне среднегрудного его отдела. Кроме того, в случаях, когда одномоментная эзофагогастрэктомия не показана, механический пищеводно-желудочный анастомоз сформировать на указанном уровне технически невозможно. Формирование «ручного» пищеводно-желудочного анастомоза на уровне грудного отдела может решить проблему мало-инвазиных операций по поводу кардиоэзофагеального рака.
В результате поиска эффективных методов лечения хирургических больных с минимальным риском возникло новое понятие — fast track хирургия («быстрый путь в хирургии», «хирургия быстрого пути», ускорение различных этапов лечебного процесса), или ERAS (early rehabilitation after surgery — ранняя реабилитация после операции). Подбор методов анестезии, минимально инвазивных способов оперативного лечения, опти-мального контроля боли и активного послеоперационного восстановления (в том числе ранние пероральное питание и мобилизация) в fast track хирургии уменьшает стрессовые реакции и дисфункцию органов, значительно сокращая время, необходимое для полного восстановления. Принципам fast track хирургии полностью соответствует применение видеоэндоскопиче-ских технологий [13].
Цель работы
Уменьшение травматизма и ранняя реабилитация больных после хирургического лечения кардиоэзофагеального рака путем выполнения малоинвазивных видеоэндоскопи-ческих радикальных операций с использованием методики ранней реабилитации.
Материалы и методы
В Московском областном центре «Видеоэндоскопиче-ская и малоинвазивная хирургия», функционирующем на базе хирургического торакального отделения ГБУЗ МО МОНИКИ им. М.Ф. Владимирского, разработана методика резекций проксимального отдела желудка и нижнегрудного отдела пищевода с одномоментной внутриплевральной эзофагогастропластикой комбинированным лапароскопическим и правосторонним торакоскопическим доступом. В течение 2015-16 гг. по данной методике было выполнено 27 операций (М/Ж=21/6; средний возраст 64,4 года).
У трёх (11,1 %) больных была выявлена I стадия, у шестерых (22,2 %) - II стадия. Преобладали больные в III стадии заболевания – 14 (51,9 %) больных. В 4-х (14,8 %) наблюдениях была выявлена IV стадия. Чаще встречались опухоли II типа по J. Siewert – у 16 (59,3 %) больных. У 6 (22,2 %) больных была опухоль I типа. В 5-и (18,5 %) случаях – III типа. В 5 (18,5 %) случаях опухоль распространялась на абдоминальный отдел пищевода, в 7 (25,9 %) – на диафрагмальный. У 9 (33,3 %) больных проксимальный край опухоли определялся на уровне наддиафрагмального сегмента, у 6 (22,2 %) – на уровне ретроперикардиального.
Лапароскопический этап включал мобилизацию желудка и кардии (в 2-х случаях с резекцией ножек диафрагмы), удаление обоих сальников, абдоминальную лимфодиссекцию D2. После мобилизации абдоминального и нижнегрудного отделов пищевода в нижнем средостении выполняли лимфо-диссекцию. Завершался лапароскопический этап резекцией проксимального отдела желудка с формированием узкого желудочного трансплантата. Как правило, пищевод резецировали трансдиафрагмально непосредственно над опухолью в нижнегрудном отделе. Это позволяло удалялить препараты через силиконовый рукав, введенный через расширенный до 3 см лапаропорт. у четырёх больных таким способом удалили из брюшной полости только клетчатку с лимфатическими узлами и большой сальник, а основной гистопрепарат – через расширенное до 3 см отверстие для торакопорта в 8-м межреберье. Второй этап операции выполняли путем видеоторакоскопии справа в положении больного на левом боку. Выполняли мобилизацию грудного отдела пищевода и медиастинальную лимфодиссекцию, включающая лимфатические узлы пара-эзофагеальных, паратрахеальных и бифуркационных групп. После ререзекции пищевода на 6-8 см выше проксимального края опухоли формировали двухрядный пищеводно-желудочный анастомоз узловыми швами (Рисунок 1).
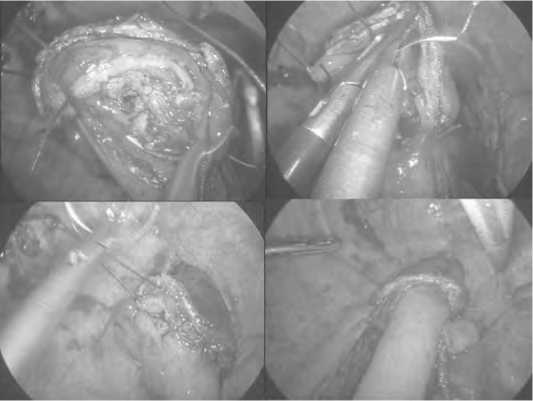
Рис. 1. Формирование «ручного» двухрядного пищеводно-желудочного анастомоза на торакоскопическом этапе операции
Нами использовались принципы ранней реабилитации больных («fast track»), которая охватывает все фазы периоперационной терапии: предоперационную, интраоперационную и послеоперационную.
Предоперационная стратегия
-
1. Обучение пациента – объяснение и реальная информация о предстоящих медицинских процедурах, операции, послеоперационном периоде, преимуществах программы fast track.
-
2. Отсутствие ограничения питания до операции. Учитывая, что удлинение периода голодания со снижением рН желудочного содержимого увеличивает риск аспирации, пациенту в течение ночи разрешают пить до 400 мл прозрачной жидкости, так как данный объём не увеличивает риск аспирационных осложнений во время интубации. С применением принципов доказательной медицины продемонстрировано, что дооперационное голодание существенно снижает резервы гликогена в печени и вызывает послеоперационную устойчивость к инсулину. Результатом этого является уменьшение восстановительных ресурсов организма. Вследствие этого обосновано применение 150 мл декстрозы (глюкозы) за 2 ч до операции, что также способствует уменьшению чувства голода, жажды, дискомфорта, утомления, а, следовательно, и стрессовой реакции. Уменьшение выраженности страха в результате выброса эндогенных опиоидов в свою очередь приводит к снижению интраоперационной потребности в анестетиках.
-
3. Согласно результатам рандомизированных исследований, необходимость механической подготовки кишечника к операции не считают обоснованной.
Интраоперационная стратегия
-
1. Анестезиологическое обеспечение с применением со-
- временных анестетиков (пропофол, десфлуран), миорелаксантов (рокурония бромид), сугаммадекса, протективной ИВЛ, мультимодального обезболивания (НПВС, парацетамол, 0,2 % раствор ропивакаина) позволяет экстубировать всех пациентов после резекций проксимального отдела желудка и нижнегрудного отдела пищевода с одномоментной внутриплевральной эзофагогастропластикой комбинированным лапароскопическим и правосторонним торакоскопическим доступом.
-
2. Использование минимально агрессивной видеоэндо-скопической хирургической методики уменьшает воспалительный компонент стрессового ответа, существенно не влияя на нейроэндокринный и метаболический ответ.
-
3. Оптимизированная инфузионная терапия (directed goal therapy) во время оперативного вмешательства предполагает предупреждение интраоперационной гиповолемии и чрезмерной инфузии кристаллоидов, которые могут привести к отёкам, ухудшению оксигенации тканей и замедлению заживления. Возможность же употребления жидкости ночью и отказ от подготовки кишечника приводит к отсутствию гиповолемии в начале операции и снижению интраоперационной инфузии. В связи с вышеизложенным, интраоперационно придерживались рестриктивной стратегии инфузионной терапии.
-
4. Обеспечение интраоперационной нормотермии. Развитие интраоперационной гипотермии влечёт за собой ухудшение гемостаза с увеличением внутри- и послеоперационной кровопотери, усиление послеоперационной дрожи с повышенным потреблением кислорода и повышение риска ишемии миокарда. Интраоперацинно нормотермию обеспечивали согреванием инфузионных сред и использованием подогревающего матраца.
Послеоперационная стратегия
-
1. Эффективное купирование боли. Послеоперационная боль – важнейший фактор, влияющий на длительность послеоперационного пребывания пациента в стационаре. Анальгезию обеспечивали введением НПВС, парацетамола и по показаниям трамадола.
-
2. Ранняя пероральная гидратация.
-
3. Раннее восстановление энтерального питания. При наличии тошноты и рвоты показана фармакологическая терапия (дексаметазон, ондансетрон).
-
4. Ранняя вертикализация (1-е сутки после операции) и мобилизация пациента.
Результаты
Резекция R0 была выполнена 24 (88,9%) больным, R1 – 3 (11,1 %). При гистологическом исследовании в среднем исследовалось 42±3 лимфатических узла.
Средняя продолжительность операции составила 6 ч 21 мин. В 100 % случаев перевод на самостоятельное дыхание осуществлялся непосредственно после операции, в опера- ционной. Средняя продолжительность нахождения больных в реанимации составила 17 часов. Мобилизация больного – в первые сутки после операции. Начало энтерального питания осуществлялось на 4-е сутки. Послеоперационные осложнения были отмечены всего у одного больного – левосторонняя плевропневмония. Он был выписан на 12-е сутки для долечивания в терапевтическом отделении по месту жительства.
Среднийпослеоперационныйкойко-деньсоставил7,3су-ток соответственно.
Заключение. Преимущества радикальных операций при кардиоэзофагеальном раке комбинированным лапароскопическим и правосторонним торакоскопическим досту-пом очевидны: четкость визуализации, хороший контроль гемостаза, удобство мобилизации желудка и пищевода, ранняя активизация больных в послеоперационном периоде, сокращение сроков стационарного лечения. Применение технологии ранней послеоперационной реабилитации (fast track) позволяет уменьшить сроки госпитализации, ускорить выздоровление и восстановление трудоспособности больных.
Список литературы Ранняя послеоперационная реабилитация (fast track) при лапаро-торакоскопических резекциях проксимального отдела желудка и грудного отдела пищевода при кардиоэзофагеальном раке
- Черноусов А.Ф., Черноусов Ф.А., Хоробрых Т.В., Вычужа-нин Д.В. Хирургиче-ское лечение больных кардиоэзофагеальным раком.//Вестник хирургической гастроэнтерологии. -2009 -№2 -С. 67-77
- Давыдов М.И., Туркин И.Н., Стилиди И.С. и др. Кардиоэзо-фагеальный рак: классификация, хирургическая тактика, основные факторы прогноза.//Вестник РОНЦ им. Н.Н. Блохина РАМН. -2003 -№1 -С. 82-89
- Siewert J.R., Feith M., Stein H.J. Biologic and clinical variations of adenocarcinoma at the esophago-gastric junction: relevance of a topo-graphic-anatomic subclassification. J Surg Oncol. 2005 Jun 1; 90(3): 139-46
- Orringer M.B., Marshall B., Chang A.C., et al. Two thousand tran-shiatal esophagectomies: changing trends, lessons learned. Ann Surg. -2007-V 246 -p. 363-372
- Sasako M., Sano T., Yamamoto S. et al. Left thoracoabdominal approach versus abdominal-transhiatal approach for gastric cancer of the cardia or subcardia: a randomized controlled trial.//Lancet Oncol. -2006-№7 -р. 644-651
- Стилиди И. С., Рябов А. Я., Бохян В. Ю. и др. Оптимизированный абдомино-медиастинальный доступ в хирургии рака желудка с переходом на пищевод.//Вестник РОНЦ им. Н.Н. Блохина РАМН. -2006 -т. 17, № 4 -С. 47-51
- ыхно Ю.А., Самотесов П.А., Батухтина Ю.В. Топографо-анатомическое обос-нование хирургического доступа при кардио-эзофагеальном раке в зависимости от типа телосложения//Сибирский онкологический журнал -2004-№4 (12) -С. 42-47
- Esquivel C.M., Ampudia C., Fridman A. et al. Technique and outcomes of laparoscopic-combined linear stapler and hand-sutured side-to-side esophagojejunostomy with Roux-en-Y reconstruction as a treatment modality in patients undergoing proximal gastrectomy for benign and malignant disease of the gastroesophageal junction.//Surg Laparosc Endosc Percutan Tech. -2014 -Feb; 24(1) -p. 89-93
- Израилов Р.Е., Васнев О.С., Кошкин М.А. с соавт. Возможности лапароскопиче-ской хирургии в лечении раков кардиоэзофагеального перехода.//«Альманах Института хирургии имени А.В. Вишневского». Тезисы докладов xVIII съезда Общества эндоскопических хирургов России. 17-19 февраля 2015г -г. Москва 2015 -№1-С. 494
- Montenovo M.I., Chambers K., Pellegrini C.A., Oelschlager B.K. Outcomes of lapa-roscopic-assisted transhiatal esophagectomy for adeno-carcinoma of the esophagus and esophago-gastric junction.//Dis Esophagus. -2011 -Aug;24(6) -р. 430-436
- Maas K.W., Biere S.S., Scheepers J.J. et al. Laparoscopic versus open transhiatal esophagectomy for distal and junction cancer.//Rev Esp Enferm Dig.-2012 -Apr;104(4)-p. 197-202
- Liu Hong, Yujie Zhang, Hongwei Zhang, Jianjun Yang, Qingch-uan Zhao The Short-Term Outcome of Three-Field Minimally Invasive Esophagectomy for Siewert Type I Esophagogastric Junctional Adenocarcinoma.//Ann Thorac Surg-2013 -V. 96 -p. 1826-1832
- Gemmill E.H., Humes D.J., Catton J.A. Systematic review of enhanced recovery after gastro-oesophageal cancer surgery.//Ann R Coll Surg Engl. -2015 -Apr;97(3)-p.173-179


