Расчет физико-химического взаимодействия титановых сплавов с материалами литейной формы
Автор: Ганеев Альмир Амирович, Деменок Анна Олеговна, Бакерин Сергей Васильевич, Кулаков Борис Алексеевич, Мухамадеев Ильшат Рифкатович, Гарипов Альберт Ринатович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Литейное производство
Статья в выпуске: 3 т.16, 2016 года.
Бесплатный доступ
Термохимическая инертность форм - одно из основных условий получения качественных отливок из титановых сплавов. Применяемые в литейном производстве огнеупорные формовочные и связующие материалы активно взаимодействуют с титаном. Поэтому термохимическая стойкость форм может быть повышена выбором наиболее инертных по отношению к титану исходных формовочных и связующих материалов и разработкой оптимального технологического процесса. Для оценки возможности взаимодействия титана при заливке в формы с формовочными материалами Al2O3, ZrO2, Y2O3 и связующими на основе SiO2 рассмотрены основные вероятные реакции и рассчитаны изменения изобарно-изотермического потенциала (энергия Гиббса). Рассматривалось протекание реакций при температуре 1700 °С (температура плавления 1668 °С), при условии, что титан находится в жидком состоянии. Исходя из расчетных значений ΔZ (ΔG) рассмотренных реакций показано, что реакция восстановления титаном оксида иттрия, циркония и алюминия термодинамически невозможна. В условиях России экономически неоправданно использование в качестве формовочных материалов окислов иттрия и циркония для получения оболочковых форм при литье титановых сплавов. Появление же альфированного слоя на отливках титановых сплавов при использовании связующего на основе SiO2 вызвано, как показали термодинамические расчеты, протеканием реакций с образованием алюмосиликатов, ухудшающих химическую стойкость формы и ее огнеупорность. Для получения качественных отливок из титановых сплавов экономически целесообразно использование оболочковых форм на основе электрокорунда с обязательной заменой связующих на основе SiO2 на алюмозоли.
Фасонные отливки, оболочковые формы, выплавляемые модели, химическая активность, инертные материалы, термохимическая инертность форм, формовочные материалы, связующие материалы, вероятность реакции, изобарно-изотермический потенциал
Короткий адрес: https://sciup.org/147157046
IDR: 147157046 | УДК: 621.742.4 | DOI: 10.14529/met160310
Calculation of physical-chemical interaction of titanium alloys with the materials of the mold
Thermochemical inertness of molds is one of the principal conditions for obtaining high-quality castings in titanium alloys. Refractory and binder materials used in foundry molding actively interact with titanium. Therefore, thermochemical resistance of molds can be improved by selecting molding and binder materials the most inert to titanium and by development of optimum technological process. To assess the possibility of interaction of titanium when poured into molds with molding materials of Al2O3, ZrO2, Y2O3, and a binder based on SiO2 the main possible reactions are discussed and the changes of isobaric-isothermal potential (Gibbs energy) are calculated. The course of reactions was considered at 1700 °C (melting point 1668 °C), with the condition that titanium is in liquid state. Based on the calculated values of ΔZ (ΔG) it is shown that the reaction of reduction of yttrium, zirconium and aluminum oxides by titanium is thermodynamically impossible. In Russian conditions it is not economic to use yttrium and zirconium oxides as molding materials to produce shell molds for casting titanium alloys. The appearance of α layer on titanium alloy castings when using a SiO2 based binder is caused, as shown by thermodynamic calculations, by reactions forming aluminum silicates that worsen chemical resistance and refractoriness of the mold. To obtain high-quality castings of titanium alloys it is economically feasible to use shell molds based on fused alumina with the mandatory replacement of SiO2 based binders with aluminia sols.
Текст научной статьи Расчет физико-химического взаимодействия титановых сплавов с материалами литейной формы
В настоящее время перед литейщиками поставлена задача разработки технологии литья тонкостенных крупногабаритных фасонных отливок из титановых сплавов. Благодаря уникальному сочетанию физических и механических свойств этих сплавов, а именно: высокой удельной прочности, малой плотности, жаростойкости, высоким антикоррозионным свойствам, хорошему сопротивлению усталостному разрушению и ползучести, они много лет сохраняют свои позиции в разряде перспективных для авиационной промышленности и двигателестроения.
Освоение такого вида отливок связано с рядом трудностей, обусловленных, во-первых, разработкой технологии плавки и литья, во-вторых, наличием специфического оборудования на стадии изготовления моделей, изготовления форм, плавки и заливки сплавов на основе титана.
Производство деталей из сплавов на основе титана отличается высокой трудоемкостью, энергоемкостью и стоимостью. Поэтому, с целью эко-
номии материалов и удешевления конечной продукции, заготовки из них должны быть максимально приближены по конфигурации и размерам к готовой детали. В то же время из-за усложнения конструкций и условий работы современных технических систем требования к качеству отливок постоянно возрастают. С этих позиций наиболее рациональным во многих случаях способом получения заготовок является литье в оболочковые формы по выплавляемым моделям. Однако получение высококачественных отливок осложняется высокими температурами заливки и высокой химической активностью титановых сплавов, что приводит к интенсивному взаимодействию металла с литейной формой и, как следствие, к снижению служебных свойств литых изделий.
Малая толщина стенки отливки предопределяет необходимость предварительного подогрева формы перед заливкой до 900…1000 °С, что в свою очередь резко повышает требования к инертности материала формы к жидкому титановому сплаву и в
предельной степени ограничивает возможный выбор материалов основы формы и связующего.
Термохимическая инертность форм – одно из основных условий получения качественных отливок из титановых сплавов. Применяемые в литейном производстве огнеупорные формовочные и связующие материалы активно взаимодействуют с титаном. Поэтому термохимическая стойкость форм может быть повышена выбором наиболее инертных по отношению к титану исходных формовочных и связующих материалов
и разработкой оптимального технологического процесса.
Для оценки возможности взаимодействия титана при заливке в формы с формовочными материалами Al 2 O 3 , ZrO 2 , Y 2 O 3 и связующими на основе SiO 2 рассмотрены основные вероятные реакции и рассчитаны изменения изобарно-изотермического потенциала (энергия Гиббса).
Рассмотрим протекание реакций при температуре 1700 °С (температура плавления 1668 °С), при условии, что Ti находится в жидком состоянии [1].
Реакция 1
SiO2 + 2Ti = 2TiO + Si
A H 298 = 2 - ( - 542 ) + 0 - ( - 910,7 ) - 2 ■ 0 = - 173,3 кДж/моль;
A S 2 0 98 = 2 ■ 34,79 + 18,81 - 41,46 - 2 ■ 30,72 =- 14,51 Дж/(моль ■ К);
A G 2 0 98 =- 173,3 - 10 3 - ( - 14,51 ) - 298 =- 1168,98 кДж/моль.
С помощью следующих формул (1.1) найдем энтальпию и энтропию реакций при различных температурах [2]:
T 2
А Н т 2 = A H ^ + J A C p dT ;
T 1
T 2 dT
-
AAT2 = ASt + J A Cp —;
-
T 1 T
A GT = A HT -A ST .
C p ( TiO ) = 44,22 + 15,06 ■ T ■ 10 - 3 + ( - 7,78 ) - T - 2 ■ 105 Дж/(моль ■ К);
C p ( Si ) = 24,02 + 2,58 ■ T ■ 10 - 3 + ( - 4,23 ) ■ T " 2 ■ 10 5 Дж/(моль ■ К);
C p ( SiO 2 ) = 46,94 + 34,31 * T ■ 10 - 3 + ( - 11,3 ) " T - 2 ■ 105 Дж/(моль ■ К);
C p ( Ti ) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
ACp = 2Cp (TiO) + Cp (Si) - Cp (SiO2)- 2Cp (Ti)
A C p = 2 ■ ( 44,22 + 15,06 ■ T ■ Io - 3 - 7,78 ■ T - 2 ■ Io5 ) + ( 24,02 + 02,58 ■ T ■ Io - 3 - 4,23 ■ T - 2 ■ Io5 ) -
-
- ( 46,94 + 34,31 " T ■Ю- 3 - 11,3 ■ T " 2 ■Ю 5 ) - 2 ■ ( 22,09 + 10,04 ■ Io - 3 ■ T ) =
= 21,34 - 21,69 ■ T ■Ю- 3 - 8,49 ■ T - 2 ■Ю 5 Дж/(моль ■ К).
A H 10973 =- 173,3 ■Ю 3 + J ( 21,34 - 21,69 ■ T ■ Io - 3 - 8,49 ■ T " 2 ■Ю 5 ) dT = 298
C T2 7’ 1 ^
= -173,3 ■Ю3 + 21,34 ■ T - 21,69 ■Ю-3---8,49 ■Ю5
( 2
= - 173,3 ■Ю3 + ( 42103,82 - 42 216,65 + 430,31 - 6359,32 + 963,08 - 2849 ) = - 181,23 кДж/моль. 1973
A S 0 973 =- 14,51 + J ( 21,34 - 21,69 ■ T ■ Io - 3 - 8,49 ■ T '4 0 5 ) — =
T -2 9
= (21,34■ lnT-21,69■io-3 ■ T-8,49■Ю5
-
-2 J
= - 14,51 + ( 161,91 - 42,79 + 0,11 - 121,58 + 6,46 - 4,78 ) =- 15,18 Дж/(моль ■ К);
A G 0 973 =- 181,23 ■Ю3 - 1973 ■ ( - 15,18) = - 151,28 кДж/моль.
Реакция 2
SiO2 + Ti = TiO 2 + Si
A H 298 = - 944 + 0 - ( - 910,7) - 2 ■ 0 = - 33,3 кДж/моль;
A S 2 0 98 = 50,62 + 18,81 - 41,46 - 30,72 = - 2,75 Дж/(моль ■ К);
A G 2 0 98 = - 33,3 ■ 10 3 - ( - 2,75) ■ 298 = - 32,48 кДж/моль.
C p (TiO2) = 71,71 + 4,1 ■ T ■Ю - 3 + ( - 14,64) ■ T " 2 ■ 105 Дж/(моль ■ К);
C p (Si) = 24,02 + 2,58 ■ T ■ 10 - 3 + ( - 4,23) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p (SiO2) = 46,94 + 34,31 ■ T ■ 10 - 3 + ( - 11,3) ■ T " 2 ■ 10 5 Дж/(моль ■ К);
C p (Ti) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
A C p = C p (TiO) + C p (Si) - C p (SiO 2 ) - C p (Ti)
A C p = ( 71,71 + 4,1 - T ■Ю - 3 - 14,64 ■ T - 2 ■Ю5 ) + ( 24,02 + 2,58 ■ T ■Ю - 3 - 4,23 ■ T " 2 ■Ю5 ) -
- ( 46,94 + 34,31 - T ■Ю - 3 - 11,3 ■ T " 2 ■Ю5 ) - ( 22,09 + 10,04 ■Ю- 3 ■ T ) =
= 26,7 - 37,67 ■ T ■Ю- 3 - 7,57 ■ T 2 ■Ю 5 Дж/(моль ■ К).
A H 10973 =- 33,3 ■Ю 3 + J ( 26,7 - 37,67 ■ T ■Ю- 3 - 7,57 ■ T - 2 ■ 105 ) dT = 298
f T 2 T - 1 ^
= -33,3 ■io3 + 26,7 ■ T - 37,67 ■Ю-3---7,57 ■Ю5--=
( 2 -1 J
= - 33,3 ■ io3 + ( 52 679,1 - 73 319,55 + 383,68 - 7956,6 + 1672,62 - 2540,27 ) = - 62,38 кДж/моль.
dT T
A 5 0,73 =- 2,75 + J ( 26,7 - 37,67 ■ T ■ Io - 3 - 7,57 ■ T - 2 ■ 105 298
f a < Г-2 )
= - 2,75 + 26,7 ■ In T - 37,67 ■Ю- 3 ■ T - 7,57 ■Ю 5-- =
I -2 I
= - 2,75 + ( 202,58 - 74,32 + 0,097 - 152,11 + 11,23 - 4,26 ) = - 19,53 Дж/(моль ■ К);
A G 1973 =- 62,38■Ю3 - 1973 ■ 65,56 =- 23,85 кДж/моль.
Реакция 3
Al2O3 + 3Ti = 3TiO + 2Al
A H 2 0 98 = 3 ■ ( - 542 ) + 2 ■ 0 - ( - 1675,7 ) - 3 ■ 0 = 49,7 кДж/моль;
A S 2 0 98 = 3 ■ 34,79 + 2 ■ 28,35 - 50,92 - 3 ■ 30,72 = 17,99 Дж/(моль ■ К);
A G 2 0 98 = 48,7 ■ 10 3 - 17,99 ■ 298 = 44,34 кДж/моль.
C p ( TiO ) = 44,22 + 15,06 ■ T ■ 10 - 3 + ( - 7,78 ) ■ T " 2 ■ 105 Дж/(моль ■ К);
C p ( Al ) = 20,67 + 12,39 ■ T ■ 10 - 3 Дж/(моль ■ К);
C p ( Al2O3 ) = 114,56 + 12,89 ■ T ■ 10 - 3 + ( - 34,31) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p ( Ti ) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
ACp = 3Cp (TiO) + 2Cp (Al) - Cp (A12O3) -3Cp (Ti)
A Cp = 3 ■ ( 44,22 + 15,06 ■ T ■Ю - 3 + ( - 7,78 ) - T " 2 ■Ю 5 ) + 2 ■ ( 20,67 + 12,39 ■ T ■Ю - 3 ) -- ( 114,56 + 12,89 ■ T ■Ю- 3 + ( - 34,31 ) - T " 2 ■Ю5 ) - 3 ■ ( 22,09 + 10,04 ■Ю- 3 ■ T ) = = - 6,83 + 26,95 ■ T ■Ю- 3 + 10,97 ■ T - 2 ■ 105 Дж/(моль ■ К).
A H 10973 = 49,7 . 10 3 + J ( - 6,83 + 26,95 . T . 10 - 3 + 10,97 . T - 2 . 10 5 ) dT = 298
f T2
= 49,7-103 + -6,83 ■ T + 26,95-10-3 --+10,97-105
( 2
= 49,7 . 103 + ( - 13 475,59 + 52 454,52 - 556 + 2035,34 - 1196,63 + 3 681,2 ) = 92,64 кДж/моль. 1973
A S 10973 = 17,99 + J ( - 6,83 + 26,95 . T Л0 - 3 + 10,97 . T '4 0 5) — =
(
I-
= 17,99 + ( - 51,82 + 53,17 - 0,14 + 38,91 - 8,03 + 6,18 ) = 56,26 Дж/(моль . К);
A G 1 0 973 = 92,64 . 10 3 - 1973 . 56,26 = - 18,36 кДж/моль.
Реакция 4
2Al2O3 + 3Ti = 3TiO2 + 4Al
A H 2 0 98 = 3 . ( - 944) + 4 . 0 - 2 . ( - 1675,7) - 3 . 0 = 519,4 кДж/моль;
A S 2 0 98 = 3 . 50,62 + 4 . 28,35 - 2 . 50,92 - 3 . 30,72 = 71,26 Дж/(моль . К);
A G 2 0 98 = 519,4 . 10 3 - 71,26 . 298 = 498,16 кДж/моль.
C p ( TiO 2 ) = 71,71 + 4,1 . T . 10 - 3 + ( - 14,64 ) . T - 2 . 10 5 Дж/(моль . К);
C p ( Al ) = 20,67 + 12,39 . T . 10 - 3 Дж/(моль . К);
C p ( Al2O3 ) = 114,56 + 12,89 . T . 10 - 3 + ( - 34,31 ) . T " 2 . 105 Дж/(моль . К);
C p ( Ti ) = 22,09 + 10,04 . 10 - 3 . T Дж/(моль . К).
A C p = 3 C p (TiO 2 ) + 4 C p (Al) - 2 C p (Al^) - 3 C p (Ti)
A C p = 3 . ( 71,71 + 4,1 . T . 10 - 3 + ( - 14,64 ) . T ~2 . 10 5 ) + 4 . ( 20,67 + 12,39 . T Л0 - 3 ) -
- 3 . ( 114,56 + 12,89 . T . 10 - 3 + ( - 34,31 ) . T " 2 . 10 5 ) - 3 . ( 22,09 + 10,04 Л0 - 3 . T ) =
= 2,42 + 5,96 . T . 10 - 3 + 24,7 . T 2 . 10 5 Дж/(моль . К).
A H 1 0 973 = 519,4 . 10 3 + J ( 2,42 + 5,96 . T Л0 - 3 + 24,7 . T - 2 . 105 ) dT = 298
f т 2 т - 1 ^
= 519,4.103 + 2,42. T + 5,96 Л0-3 --+ 24,7.105
| 2
= 519,4 . 10 3 + ( 4774,66 + 11 600,33 - 1251,9 - 721,16 - 264,64 + 8288,6 ) = 541,83 кДж/моль. 1973
A S j^ = 71,26 + J ( 2,42 + 5,96 . T Л0 - 3 + 24,7 . T 210 5 ) — =
f
I-
= 71,26 + ( 18,36 + 11,76 - 0,32 - 13,79 - 1,78 + 13,9 ) = 99,39 Дж/(моль . К);
A G 1 0 973 = 541,83 . 10 3 - 1973 . 99,39 = 345,73 кДж/моль.
Реакция 5
ZrO2 + 2Ti = 2TiO + Zr
A H 098 = 2 ■ ( - 542 ) + 0 - ( - 1100,3 ) - 2 ■ 0 = 16,3 кДж/моль;
A A 098 = 2 ■ 34,79 + 38,98 - 50,39 - 2 ■ 30,72 = - 3,27 Дж/(моль ■ К);
A G 0 98 = 16,3 ■ 103 - ( - 3,27 ) ■ 298 = 17,27 кДж/моль.
C p ( TiO ) = 44,22 + 15,06 ■ T ■ 10 - 3 + ( - 7,78 ) ■ T " 2 ■ 105 Дж/(моль ■ К);
C p ( Zr ) = 28,58 + 4,69 ■ T ■ 10 - 3 + ( - 3,81 ) ■ T " 2 ■ 105 Дж/(моль ■ К);
C p ( ZrO2 ) = 69,62 + 7,53 ■ T ■ 10 - 3 + ( - 14,06 ) ■ T " 2 ■ 10 5 Дж/(моль ■ К);
C p ( Ti ) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
A C p = 2 C p (TiO) + C p (Zr) - C p (ZrO 2 ) - 2 C p (Ti)
A C p = 2 ■ ( 44,22 + 15,06 ■ T ■Ю- 3 + ( - 7,78 ) - T - 2 00 5 ) + ( 28,58 + 4,69 ■ T ■Ю- 3 +
+ ( - 3,81 ) - T - 2 ■Ю 5 ) - ( 69,62 + 7,53 ■ T ■Ю- 3 + ( - 14,06 ) ' T " 2 ■Ю 5 ) -
- 2 ■ ( 22,09 + 10,04■Ю - 3 ■ T ) = 3,22 + 7,2 ■ T ■ 10 - 3 - 5,31 * T - 0 ■ 1O5 Дж/(моль ■ К).
A H 0 973 = 16,3 ■Ю 3 + J ( 3,22 + 7,2 ■ T ■Ю- 3 - 5,31 " T - 0 ■ 1O5 ) dT = 298
Л 7'2 T -1 ^
= 16,3 ■Ю3 + 3,22 ■ T - 7,2 ■10-3---5,31■105
( 2
= 16,3 ■Ю3 + ( 6353,06 + 14 013,82 + 269,13 - 959,56 - 319,69 - 1781,88 ) = 33,87 кДж/моль.
A A 0 973 =- 3,27 + J ( 3,22 + 7,2 ■ T ■ 10 - 3 - 5,31 ' T '405 ) — =
T - 2 ^
= -3,27 + 3,22■ InT + 7,2■10-3 ■ T-5,31■105
-
-2 J
= - 3,27 + ( 24,43 + 14,21 + 0,07 - 18,34 - 2,15 - 2,99 ) = 11,96 Дж/(моль ■ К);
A G 0973 = 33,87■Ю3 - 1973 ' 11,96 = 10,27 кДж/моль.
Реакция 6
ZrO2 + Ti = TiO2 + Zr
A H 098 = - 944 + 0 - ( - 1100,3) - 2 ■ 0 = 156,3 кДж/моль;
A A 0 98 = 50,62 + 38,98 - 50,39 - 30,72 = 8,49 Дж/(моль ■ К);
A G 058 = 156,3 ■Ю3- 8,49 ■ 298 = 153,77 кДж/моль.
C p ( TiO2 ) = 71,71 + 4,1 ■ T ■ 10 - 3 + ( - 14,64 ) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p ( Zr ) = 28,58 + 4,69 ■ T ■ 10 - 3 + ( - 3,81 ) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p ( ZrO2 ) = 69,62 + 7,53 ■ T ■ 10 - 3 + ( - 14,06 ) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p ( Ti ) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
ACp = Cp (TiO2) + Cp (Zr) - Cp (ZrO2) - Cp (Ti)
A Cp = ( 71,71 + 4,1 ' T ■ 10 - 3 + ( - 14,64 ) ' T " 2 00 5 ) + ( 28,58 + 4,69 ■ T ■ 10 - 3 +
+ ( - 3,81 ) ' T - 2 00 5 ) - ( 69,62 + 7,53 ■ T ■ 10 - 3 + ( - 14,06 ) ■ T - 2 00 5 )
-
- ( 22,09 + 10,04 ■ 10 - 3 ■ T ) = 8,58 - 8,78 ■ T ■ 10 - 3 - 4,39 ■ T - 0 ■ 1O5 Дж/(моль ■ К).
AH 10973 = 156,3 - 10 3 + J ( 8,58 - 8,78 ■ T - IO - 3 - 4,39 ■ T - 2 ■ 105 ) dT = 298
f T2 T — 1 A
= 156,3■Ю3 + 8,58 ■ T - 8,78 ■Ю- 3 ---4,39 ■Ю 5 -- =
( 2 - 1 J
= 156,3 - 103 + ( 16 928,34 - 17 089,08 + 222,5 - 2556,84 + 3 89,85 - 1473,15 ) = 152,72 кДж/моль.
dT T
A 5 10973 = 8,49 + J ( 8,58 - 8,78 ■ T ■Ю- 3 - 4,39 ■ T - 2 ■ 105 298
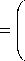
T - 2 A
8,58 ■ In T - 8,78 ■ 10 - 3 ■ T - 4,39■Ю5-- =
-
- 2 J
= 8,49 + ( 65,1 - 17,32 + 0,06 - 48,88 + 2,62 - 2,47 ) = 7,6 Дж/(моль ■ К);
A G 0 973 = 152,72 ■Ю3 - 1973 ■ 7,6 = 137,73 кДж/моль.
Реакция 7
Y2O3 + 3Ti = 3TiO + 2Y
A H 2 0 98 = 3 ■ ( - 542 ) + 2 ■ 0 - ( - 1905 ) - 3 ■ 0 = 279 кДж/моль;
A 5 2 0 98 = 3 ■ 34,79 + 2 ■ 44,43 - 99,16 - 3 ■ 30,72 = 1,91 Дж/(моль ■ К);
A G 2 0 98 = 279 ■Ю3 - 1,9b 298 = 44,34 кДж/моль.
C p ( TiO ) = 44,22 + 15,06 ■ T ■ 10 - 3 + ( - 7,78 ) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p ( Y ) = 25,52 Дж/(моль ■ К);
C p ( Y2O3 ) = 102,42 Дж/(моль ■ К);
C p ( Ti ) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
A C p = 3 C p ( TiO ) + 2 C p ( Y ) - C p ( Y 2 O 3 ) - 3 C p ( Ti )
A C p = 3 ■ ( 44,22 + 15,06 ■ T T0 - 3 + ( - 7,78 ) ■ T " 2 T05 ) + 2 ■ 25,52 - 102,42 -
-
- 3 ■ ( 22,09 + 10,04■Ю - 3 ■ T ) = 15,01 + 15,06 ■ T ■Ю - 3 - 23,34 ■ T - 2 ■ 105 Дж/(моль ■ К). 1973
A H 0 973 = 279 ■Ю 3 + J ( 15,01 + 15,06 ■ T T0 - 3 - 23,34 ■ T - 2 ■ 105 ) dT = 298 f yr2 rp - 1
= 279 ■Ю3 + 15,01 ■ T + 15,06 T0 - 3 ---23,34 ■Ю5--
( 2
= 279 ■Ю3 + ( 29 614,73 + 29 312,25 + 1182,97 - 44 729,8 - 668,69 - 7832,21 ) = 285,88 кДж/моль. 1973
A50973 = 1,91 + J (15,01 +15,06■ T■Ю-3 -23,34■ T-2■Ю5) — = 298
f
= 1,91 + 15,01*lnT +15,06■Ю-3 ■ T + 23,34■Ю5
-
3 3 3 3о
I-
= 1,91 + ( 113,89 + 29,71 + 0,3 - 85,51 - 4,49 - 13,14 ) = 42,67 Дж/(моль ■ К);
A G 0 973 = 285,88 ■Ю3 - 1973 ■ 42,67 = 201,69 кДж/моль.
Реакция 8
2Y 2 O 3 + 3Ti = 3TiO2 + 4Y
A H 098 = 3 ■ ( - 944 ) + 4 ■ 0 - 2 - ( - 1905 ) - 3 ■ 0 = 978 кДж/моль;
A S 2 0 98 = 3 ■ 50,62 + 4 ■ 44,43 - 2 ■ 99,16 - 3 ■ 30,72 = 39,1 Дж/(моль ■ К);
A G 0 98 = 978 ■ 10 3 - 39,1 " 298 = 966,35 кДж/моль.
C p ( TiO2 ) = 71,71 + 4,1 ■ T ■ io - 3 + ( - 14,64 ) ■ T - 2 ■ 105 Дж/(моль ■ К);
C p ( Y ) = 25,52 Дж/(моль ■ К);
C p ( Y2O3 ) = 102,42 Дж/(моль ■ К);
C p ( Ti ) = 22,09 + 10,04 ■ 10 - 3 ■ T Дж/(моль ■ К).
ACp = 3Cp (TiO2) + 4Cp (Y)- 2Cp (Y^) - 3Cp (Ti)
A C p = 3 ■ ( 71,71 + 4,1 ' T ■Ю- 3 + ( - 14,64) ■ T - 2 ■Ю 5 ) + 4 ■ 25,52 - 2 ' 102,42 -
-
- 3 ■ ( 22,09 + 10,04■Ю - 3 ■ T ) = 46,1 - 17,82 ■ T ■ Io - 3 - 43,92 ■ T - 2 ■ 105 Дж/(моль ■ К).
A H 0973 = 978 ■Ю 3 + J ( 46,1 - 17,82 ■ T ■ Io - 3 - 43,92 ■ T - 2 ■ 105 ) dT =
—
T - 1
43,92 ■Ю5--
- 1
I
= 978 ■io3 + 46,1' T -17,82 ■Io-3--
I
= 978 ■Ю3 + ( 90 955,3 - 34 684,22 + 2226,05 - 13 737,8 + 791,24 - 14 738,26 ) = 1008,81 кДж/моль. 1973
A S 10973 = 39,1 + J ( 46,1 - 17,82 ■ T TO - 3 - 43,92 ■ T '4 0 5) — =
I
= 39,1 + 46,1 ' ln T - 17,82 ■Ю- 3 ■ T - 43,92TO5--
I
= 39,1 + ( 349,78 - 35,16 + 0,56 - 262,64 + 5,31 - 24,73 ) = 72,22 Дж/(моль ■ К); A G 0973 = 1008,81 ■ 103 - 1973 ■ 72,22 = 866,32 кДж/моль.
Результаты вычислений
|
Реакция |
A H 1973 , Дж/моль |
0 A S 1973 , Дж/(моль ■ К) |
A G 1973 , кДж/моль |
|
SiO2 + 2Ti = 2TiO + Si |
–109,69 |
65,56 |
–151,28 |
|
SiO2 + Ti = TiO 2 + Si |
–62,38 |
–19,53 |
–23,85 |
|
Al2O3 + 3Ti = 3TiO + 2Al |
92,64 |
56,26 |
–18,36 |
|
2A1 2 O 3 + 3Ti = 3TiO2 + 4Al |
541,83 |
99,39 |
345,73 |
|
ZrO2 + 2Ti = 2TiO + Zr |
33,87 |
11,96 |
10,27 |
|
ZrO2 + Ti = TiO2 + Zr |
152,72 |
7,6 |
137,73 |
|
Y2O3 + 3Ti = 3TiO + 2Y |
285,88 |
42,67 |
201,69 |
|
2Y 2 O 3 + 3Ti = 3TiO2 + 4Y |
1008,81 |
72,22 |
866,32 |
Расчетные значения A Z ( A G ) рассмотренных реакций показали, что реакция восстановления титаном оксидов иттрия, циркония и алюминия термодинамически невозможна.
В условиях России экономически неоправданно использование в качестве формовочных материалов окислов иттрия и циркония для получения оболочковых форм при литье титановых сплавов.
Появление же альфированного слоя на отливках титановых сплавов при использовании связующего на основе SiO 2 вызвано, как показали термодинамические расчеты, протеканием следующих реакций с образованием алюмосиликатов:
A1 2 O 3 + SiO2 = Al 2 SiO 5 .
Расчетное значение изобарного потенциала при температуре T = 1600 K составляет
G = 43 224 МДж/моль .
В свою очередь алюмосиликаты вступают в реакцию
Al2SiO 5 + 2Ti = 2TiO + Al2O3 + Si.
Расчетные значения изобарного или G потенциала при T = 1073 К составляет
G = - 28 017 МДж/моль.
Поэтому при использовании в качестве формовочного материала электрокорунда для исключения альфированного слоя необходимо использовать алюмозоли.
Анализ результатов термодинамических расчетов позволяет прийти к выводу об отрицательном влиянии SiO 2 , содержащегося в связующем, при литье титановых сплавов в электрокорундо-
вых формах, ухудшая их вследствие возможного образования алюмосиликатов, менее огнеупорных и химически стойких.
Выводы
-
1. Рассмотрены возможные термодинамические реакции при литье титановых сплавов с использованием различных формовочных материалов и связующих на основе SiO2.
-
2. Рассчитаны изобарные потенциалы (энергия Гиббса) термодинамических реакций.
-
3. Показано, что формовочные материалы на основе оксидов иттрия, циркония и электрокорунда термодинамически устойчивы к титановым сплавам.
-
4. Методом термодинамических расчетов доказано, что при использовании SiO 2 в качестве связующих, в электрокорундовых формах образуются алюмосиликаты, ухудшающие химическую стойкость формы и огнеупорность.
-
5. Для получения качественных отливок из титановых сплавов экономически целесообразно использование оболочковых форм на основе электрокорунда с обязательной заменой связующих на основе SiO 2 на алюмозоли.
Список литературы Расчет физико-химического взаимодействия титановых сплавов с материалами литейной формы
- Краткий справочник физико-химических величин/под ред. А.А. Равделя и А.М. Пономаревой. -Изд. 8-е, перераб. -Л.: Химия, 1983. -232 с.
- Основы физической химии. Теория и задачи: учеб. пособие для вузов/В.В. Еремин, С.И. Каргов, И.А. Успенская и др. -М.: Изд-во «Экзамен», 2005. -480 с.


