Расчёт фармакокинетических и дозиметрических характеристик микросфер альбумина, меченных 188Re, при различных путях введения
Бесплатный доступ
Радиофармацевтические лекарственные препараты (РФЛП), меченные 188Re, находят широкое применение при метастазах в костной ткани, гепатоцеллюлярной карциноме и метастатическом поражении печени, при опухолях кожи, для лечения келоидных поражений, ревматоидных артритов и синовитов. В настоящее время разрабатываются новые терапевтические РФЛП с 188Re. Микросферы сывороточного альбумина человека (МСА) представляют собой уникальные носители для избирательной и контролируемой доставки радионуклидов в злокачественные опухоли. Цель работы – разработка камерной математической модели кинетики меченных 188Re МСА (188ReМСА) в организме лабораторных животных при различных путях введения и расчёт на её основе фармакокинетических и дозиметрических характеристик данного препарата. Исследования проводились на беспородных белых мышах и на инбредных мышах C57Bl/6 с перевитой аденокарциномой Льюиса при внутривенном, внутримышечном и внутриопухолевом путях введения. Объект исследования – 188ReМСА диаметром 1020 мкм. Идентификация кинетических параметров модели выполнялась с использованием экспериментальных данных о биораспределении 188ReМСА в органах и тканях мышей. Расчёт фармакокинетических и дозиметрических характеристик 188ReМСА в организме лабораторных животных осуществлялся на основе идентифицированных кинетических параметров. Результаты моделирования показали, что фармакокинетические и дозиметрические характеристики 188ReМСА в организме существенно зависят от пути его введения. Наиболее высоким было содержание 188ReМСА в органах и тканях при внутривенном введении с максимальным накоплением в лёгких. Содержание 188ReМСА в органах и тканях при внутримышечном или внутриопухолевом введении было существенно ниже, и его максимальная концентрация долго сохранялась в камере введения. Также выявлено повышенное накопление радиоактивности в щитовидной железе при всех путях введения. Максимальные значения поглощённых доз при внутривенном введении получены в камере лёгких, при внутримышечном – в камере мышцы бедра, при внутриопухолевом – в камере опухоли. Результаты моделирования и расчёта характеристик 188ReМСА могут быть использованы для оценки его потенциала для терапии опухолей при внутрисосудистом или внутриопухолевом введении.
Рений-188, радиофармпрепарат, фармакокинетика, камерное моделирование, ядерная медицина, поглощённая доза, сывороточный альбумин человека, радиобиология
Короткий адрес: https://sciup.org/170211677
IDR: 170211677 | УДК: 615.849.2:[547.962.3+546.719.02.188]-092.9 | DOI: 10.21870/0131-3878-2026-35-1-103-116
Calculation of pharmacokinetic and dosimetric characteristics of albumin microspheres labeled with 188Re for various routes of administration
Radiopharmaceutical drugs labeled with 188Re are widely used in bone metastases, hepatocellular carcinoma and metastatic liver damage, skin tumors, for the treatment of keloid lesions, rheumatoid arthritis and synovitis. New therapeutic radiopharmaceutical drugs with 188Re are also currently being developed. Human serum albumin microspheres (HSA) are unique carriers for the selective and controlled radionuclide delivery to malignant tumors. The aim of the work is to develop a chamber mathematical model of the kinetics of 188Re labeled HSA (188ReHSA) in laboratory animals with various routes of administration and calculate the pharmacokinetic and dosimetric characteristics of this drug based on it. The studies were carried out on outbred white mice and inbred C57BL/6 mice with transplanted Lewis adenocarcinoma after intravenous, intramuscular and intratumoral administration. The object of the study is 188ReHSA with a diameter of 1020 microns. The kinetic parameters of the model were identified using experimental data on the biodistribution of 188ReHSA in mouse organs and tissues. Calculations of the pharmacokinetic and dosimetric characteristics of 188ReHSA in laboratory animals were based on the identified kinetic parameters. The simulation results showed that the pharmacokinetic and dosimetric characteristics of 188ReHSA in the body significantly depend on the administration route. The highest concentration of 188ReHSA in organs and tissues with maximum accumulation in the lungs was observed after intravenous administration. After intramuscular or intratumoral administration the concentration of 188ReHSA in organs and tissues was significantly lower, and the maximum concentration remained in the injection chamber for a long time. An increased accumulation of 188ReHSA in the thyroid gland was also detected after all routes of administration. The maximum values of absorbed doses were obtained in the lung chamber after intravenous administration, in the thigh muscle chamber after intramuscular administration, and in the tumor chamber after intratumoral administration. The obtained results can be used to evaluate the 188ReHSA potential for tumor therapy after intravascular or intratumoral administration.
Текст научной статьи Расчёт фармакокинетических и дозиметрических характеристик микросфер альбумина, меченных 188Re, при различных путях введения
Микросферы на основе сывороточного альбумина крови человека (МСА) являются уникальным транспортом для селективной доставки разнообразных лекарств и радиоизотопов к очагам поражения органов и тканей. В отличие от микросфер, полученных из других материалов (ионообменные смолы, стекло, полимеры, желатин и др.), МСА обладают целым рядом преимуществ, таких как простота получения, биосовместимость, способность метаболизироваться в организме без образования токсических продуктов. Кроме того, МСА способны связывать радионуклиды с разными химическими свойствами за счёт пористой структуры и высвобождать их одновременно с протеолизом денатурированного белка [1].
Радиоактивные микросферы широко применяются в ядерной медицине для диагностики и терапии онкологических и неонкологических заболеваний. Оптимальными для этих целей явля-
ются β-излучающие радионуклиды: 90Y, 131I, 166Ho, 177Lu, 186Re, 188Re и др. [2]. Например, микросферы, меченные 90Y и 166Ho, в настоящее время успешно применяются для трансартериальной радиоэмболизации химиорезистентного и неоперабельного рака печени [3]. Сообщается также о возможности мечения 188Re микросфер из стекла [4], полимерных смол [5], природных и синтетических полимерных материалов [6]. Таким образом, микросферы являются перспективными носителями радиоактивной метки и характеризуются высокой степенью избирательного накопления в органах и тканях, что определяется не только их физико-химическими параметрами, но и способами введения в организм.
В качестве перспективного для радионуклидной терапии в нашей стране уже давно зарекомендовал себя препарат 188Re-МСА [7, 8]. В МРНЦ им. А.Ф. Цыба в 2021-2023 гг. были разработаны и проведены клинические исследования I-II фазы радиофармацевтических лекарственных препаратов (РФЛП) «Микросферы альбумина 5-10 мкм, 188Re» и «Микросферы альбумина 20-40 мкм, 188Re» – препаратов для радиосиновэктомии и радиоэмболизации соответственно, продемонстрировавших высокую эффективность и безопасность проводимой терапии [7-10].
Преимущества 188Re перед другими радиоизотопами состоят в том, что он является генераторным радионуклидом и может быть использован для получения РФЛП в клинике ex tempore [11]. Хороший терапевтический эффект 188Re обусловлен β-излучением высокой энергии (E β max=2,12 МэВ) и небольшим периодом полураспада (Т 1/2 =17,0 ч), а наличие в спектре γ-квантов с оптимальной энергией (E γ =155 кэВ) позволяет отслеживать распределение РФЛП в организме с помощью гамма-камеры [12].
В работе [13] получены экспериментальные данные фармакокинетики меченных 188Re МСА диаметром 10-20 мкм в организме лабораторных мышей при разных путях введения РФЛП (внутривенные, внутримышечные, внутриопухолевые инъекции). На основе экспериментальных результатов с помощью статистических методов было показано, что способ введения 188Re-МСА существенно влияет на его поведение в организме, а сами полученные экспериментальные данные могут быть использованы для оценки потенциала 188Re-МСА для радионуклидной терапии опухолей разных локализаций.
Для более детального изучения фармакокинетических и дозиметрических характеристик 188Re-МСА в организме лабораторных животных можно использовать метод камерного моделирования. Данный метод позволяет количественно описать течение процесса in vivo , математически рассчитывать скорости перехода РФЛП между органами и тканями (камерами модели), а также зависимые от них фармакокинетические и дозиметрические характеристики [14]. Кроме того, метод камерных моделей и построения экспоненциальных функций камерного накопления-выведения даёт естественную возможность строить индивидуальные модели кинетики РФЛП в критических органах и патологических очагах и тем самым обеспечить более адекватную оценку уровней их внутреннего радиационного облучения, чем применение стандартных методик из рекомендаций Международной комиссии по радиологической защите [15].
Таким образом, цель работы заключалась в разработке камерной математической модели кинетики меченных 188Re МСА в организме лабораторных животных при различных путях введения в соответствии с условиями эксперимента [13] и расчёте на её основе фармакокинетических и дозиметрических характеристик (накопленных к определённому моменту времени и полных поглощённых доз) данного РФЛП.
Материалы и методы
Объектом исследования являлся меченный 188Re препарат на основе МСА (188Re-Микро-сферы альбумина диаметром 10-20 мкм). Методика получения этого РФЛП описана в работе [13]. Изучение биораспределения 188Re-МСА при внутривенной и внутримышечной инъекциях препарата проводили на беспородных белых мышах и при внутриопухолевой инъекции – на инбредных мышах С57Bl/6. Методика получения солидного варианта аденокарциномы Льюиса также описана в работе [13]. Средняя масса лабораторных животных составляла 22±3 г. Всего было использовано 90 мышей. Введение РФЛП осуществлялось внутривенно (в хвостовую вену) – № 1, внутримышечно (в мышцу бедра) – № 2 и внутриопухолево (в центр опухоли) – № 3 по 185 кБк суспензии 188Re-МСА в 0,1% растворе Твина-80 в физиологическом растворе в объёме 0,1 мл.
Через определённые интервалы времени (5 мин, 1, 3, 24, 48 и 72 ч) по пять животных в каждый срок умерщвляли под наркозом декапитацией, выделяли пробы органов и тканей, помещали в пластиковые пробирки, взвешивали на электронных весах «Sartorius» (Германия) и проводили радиометрию с помощью автоматического гамма-счётчика «Wizard» версии 2480 фирмы «PerkinElmer/Wallac» (Финляндия). По данным радиометрии на каждый срок наблюдения рассчитывали количество радиоактивности на 1 г органа (ткани) в процентах от введённой активности. Статистически обработанные результаты радиометрии приведены в работе [13].
Камерная модель и идентификация её параметров
Для описания кинетики 188Re-МСА в организме мышей в соответствии с условиями эксперимента [13] мы разработали камерную модель, геометрическая схема которой представлена на рис. 1. Данная модель включает в себя центральную камеру крови (обозначена цифрой 0) и периферические камеры: почек (1), печени (2), других органов и тканей (обозначены буквой i). Внутривенная инъекция РФЛП соответствует способу введения № 1 на данной схеме. При внутримышечной и внутриопухолевой инъекциях (способ введения № 2) появляется ещё одна камера (обозначена буквой а).
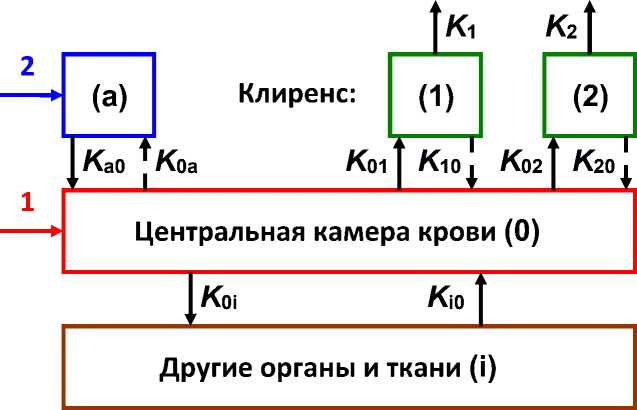
Рис. 1. Иллюстрация камерной модели.
Функции удержания активности 188Re-МСА в камерах (или функции накопления-выведения) будем обозначать как F с нижним индексом, соответствующим обозначению данной камеры. Транспортные константы (биологические константы скорости перехода РФЛП между камерами, на рис. 1 изображены стрелочками) имеют обозначения K с двумя нижними индексами, где первый индекс указывает на камеру, из которой выводится РФЛП, и второй индекс – на камеру, в которой он накапливается. Константы K i и K 2 (в сумме с K 10 и K 20 ) определяют скорости почечного и печёночного клиренса соответственно (на рис. 1 изображены выходящими стрелочками из камер почек и печени). Также в модели учтён радиоактивный распад изотопа 188Re, постоянная распада которого λ ≈0,041 ч-1. Образующийся дочерний нуклид 188Os является стабильным.
Математическая интерпретация данной камерной модели в рамках химической кинетики первого порядка [14] сводится к следующей системе линейных дифференциальных уравнений с постоянными коэффициентами:
f^ = K 0a F 0 -(K a0 +A)F a ,
"^Т = K a0 F а + K 10 F 1 + K 20 F 2 + K i0 F i - (K 0a + K 01 + K 0i + ^)F 0 ,
—^Koifzfo - (“1(2)0 + K1(2) + ^)F0, “£■ = K0iF0 - (Ki0 + %)Fi, где при внутривенном введении Fa=0, K0 a=0, Ka 0=0 (остаётся только три уравнения). Функции F удобно выражать в относительных единицах (на единицу введённой активности A 0) и, таким образом, они могут принимать значения от 0 до 1. Начальные условия для системы уравнений (1) принимают вид:
F 0(0) = 1, F i(2)(0) = Fi (0) = 0 - способ введения № 1,
Fa (0) = 1, F 0(0) = F 1(2)(0) = Fi (0) = 0 - способ введения № 2. (2)
Система (1) с условиями (2) представляет собой задачу Коши, решение которой может быть найдено аналитически или при помощи численных методов [16]. При аналитическом решении получаются очень громоздкие математические выражения, в которых фармакокинетические кривые F для всех камер представляются через линейную комбинацию экспоненциальных функций, т.е. являются полиэкспоненциальными со многими константами скорости накопления и выведения. Поскольку при доклинических исследованиях не требуется достижение повышенной точности расчётов фармакокинетических и дозиметрических характеристик РФЛП [17], фармакокинетические кривые достаточно выразить через комбинацию двух экспонент, одна из которых учитывает процесс накопления, а другая - процесс выведения РФЛП [18]. Таким образом, решение системы уравнений (1) можно представить в приближённом виде (при λ =0):
' Fa(t) = C a exp(-K a0 t)
F 0 (t) = € 0 ““° (exp(-K 0 t) - exp(-K a0 t)),
Ka0-K0
F 1(2) (t) = ^“^—“—^ - eXp(-K 01(2) t)),
(F i (t) = €
“ 0i (expt-Kat) - exp(-K 0i t)),
K0i -“ i0
где C a , C 0 , C 1(2) и Ci - максимальные значения соответствующих функций удержания активности. Учёт радиоактивного распада 188Re-МСА ( λ ≠0) приводит к появлению дополнительного множителя exp(-λt) в правой части всех уравнений (3).
Задача идентификации кинетических параметров модели (транспортных констант) решается с помощью функционала невязки Ф( К ) , который задаёт меру отклонения расчётной (модельной) характеристики (в нашем случае это функции F ) от её экспериментальных значений в заданные моменты времени tj . В качестве таких значений использовались результаты радиометрии органов и тканей мышей, приведённые в работе [13]. Тогда функционал невязки принимает вид:
Ф(К) = X^ i fF мод (t^ - F эксп (t j )} 2 , (4)
где К - вектор кинетических параметров модели (значения всех транспортных констант);
N – количество экспериментальных значений для каждой камеры модели.
Для определения истинных значений транспортных констант требуется решить вариационную задачу по нахождению минимума функционала (4), т.е.
8Ф(К)1К >° = ° , 82ф > ° , (5)
при условии положительных значений всех транспортных констант, которые в данном случае приобретают смысл вариационных параметров. Найденные таким образом значения транспортных констант далее подставляются в упрощённые решения (3) системы уравнений (1) для построения фармакокинетических кривых «Концентрация-время» (при λ =0) или «Активность-время» (при λ ≠0).
При условии быстрого накопления РФЛП в камере (когда значение константы скорости накопления много больше значения константы скорости выведения, например, K о i >> Ki 0 ) из решений (3) следует, что константа накопления может быть также определена через тангенс угла наклона касательной, проведённой к фармакокинетической кривой на начальном участке её подъёма, например для i -камеры:
KoJ^F ' i(t = 0) = tg(a) . (6)
Методика расчёта фармакокинетических и дозиметрических характеристик
Зная константы скорости выведения для каждой камеры, можно рассчитать биологические и эффективные периоды полувыведения 188Re-МСА по формулам:
Tbi0 - tmax + In 2/K , Teff = , (7)
" Tbio + Tl/2
где tmax – время достижения максимальной концентрации в камере; K – биологическая константа выведения 188Re-МСА для данной камеры. Также значения периодов полувыведения можно определить по построенным фармакокинетическим кривым F = F ( t ) «Концентрация-время» (биологический период полувыведения) и «Активность-время» (эффективный период полувыведения) как время, за которое количество 188Re-МСА уменьшается вдвое по сравнению с его максимальным значением в камере.
Другими важными фармакокинетическими характеристиками для оценки функциональной пригодности РФЛП являются клиренс крови Cl , кажущийся объём распределения Vd и средняя концентрация активности < CA > [14]:
Cl = A ° /AUC , Vd = Cl/(K + А) , < СА >= A ° /Vd , (8)
где AUC (area under curve) – площадь под кривой «Активность-время», физическим смыслом которой является число ядерных распадов РФЛП в камере.
К дозиметрическим характеристикам 188Re-МСА относятся накопленные к определённому моменту времени и полные поглощённые дозы в органах и тканях организма. Рассчитать их можно для всех камер модели с использованием фармакокинетических кривых «Активность-время». Причём достаточно учесть вклад только от β-частиц, т.к. именно они оказывают существенный терапевтический эффект, а вкладом от γ-излучения 188Re-МСА можно пренебречь [19].
Накопленная к моменту времени t поглощённая доза в j -органе определяется через площадь AUCj в соответствующей j - камере [20]:
D j (t) = kA0^AUC j (t) , AUC j (t) = ?0Р}(т)(1т , (9)
где < Eβ > – средняя энергия β-частиц распада радионуклида 188Re (< E β >=0,780 МэВ/распад [19]); mj - масса j - органа; k - коэффициент пропорциональности. Так как пробег в-частиц в органах и тканях не превышает нескольких мм [19], то органом-источником в этом случае является только сам орган-мишень, в котором и происходит облучение ( j - орган). Длина же пробега Y-квантов намного больше размера исследуемых камер, но их линейная передача энергии существенно ниже. Поэтому для расчёта формирования поглощённых доз в камерах достаточно учёта лишь β-распада. При t → ∞ из формул (9) получаются также полные поглощённые дозы во всех органах.
Результаты и обсуждение
Идентификация транспортных констант камерной модели проводилась с использованием численных методов (наименьших квадратов, Хука-Дживса) [16]. Для осуществления процедур минимизации (4), (5) и расчёта дозиметрических характеристик (9) нами была разработана и написана программа на языке программирования C++.
В табл. 1 представлены рассчитанные во всех камерах модели транспортные константы накопления и выведения и основные фармакокинетические характеристики 188Re-МСА в организме мышей при трёх путях введения РФЛП: внутривенный (первая строка чисел для каждого органа), внутримышечный (вторая строка), внутриопухолевый (третья строка). В скобках указаны приближённые значения констант накопления, определённые через тангенс угла наклона касательной по формуле (6). Периоды полувыведения рассчитывались по формулам (7).
Таблица 1
Фармакокинетические характеристики 188Re-МСА в организме мышей
|
Ткань, орган |
t max |
с тс , %/г |
с тах , %/г |
Биологические константы скорости, ч–1 |
Периоды полувыведения, ч |
||
|
накопления |
выведения |
биол. |
эффект. |
||||
|
– |
0,81±0,07 |
0,67 |
– |
0,028 |
24,8 |
10,1 |
|
|
Кровь |
3 ч |
0,22±0,01 |
0,21 |
1,54 (6,80) |
0,025 |
30,7 |
10,9 |
|
24 ч |
0,17±0,04 |
0,17 |
0,20 (4,96) |
0,009 |
101,0 |
14,6 |
|
|
3 ч |
74,3±22,4 |
65,3 |
1,54 (4,16) |
0,030 |
26,1 |
10,3 |
|
|
Щитовидная |
24 ч |
17,80±3,76 |
16,17 |
0,20 (0,79) |
0,018 |
62,5 |
13,4 |
|
железа |
3 ч |
27,0±4,28 |
23,0 |
1,54 (0,82) |
0,001 |
696,0 |
16,6 |
|
5 мин |
311,3±12,8 |
282,0 |
55,5 (12,0) |
0,010 |
69,4 |
13,7 |
|
|
Лёгкие |
24 ч |
0,10±0,01 |
0,11 |
0,20 (6,13) |
0,027 |
49,7 |
12,7 |
|
3 ч |
2,15±0,50 |
2,35 |
1,54 (1,69) |
0,040 |
20,3 |
9,3 |
|
|
5 мин |
3,00±0,14 |
2,60 |
55,5 (12,0) |
0,020 |
34,7 |
11,4 |
|
|
Почки |
24 ч |
0,46±0,02 |
0,46 |
0,20 (1,54) |
0,019 |
60,5 |
13,3 |
|
> 72 ч |
– |
– |
– |
– |
– |
– |
|
|
3 ч |
12,70±0,55 |
12,21 |
1,54 (11,0) |
0,008 |
89,6 |
14,3 |
|
|
Печень |
24 ч |
0,20±0,02 |
0,20 |
0,20 (2,60) |
0,011 |
87,0 |
14,2 |
|
3 ч |
1,89±0,28 |
1,64 |
1,54 (4,40) |
0,022 |
34,5 |
11,4 |
|
Продолжение таблицы 1
|
Ткань, орган |
t max |
С тс , %/г |
с то , %/г |
Биологические константы скорости, ч–1 |
Периоды полувыведения, ч |
||
|
накопления |
выведения |
биол. |
эффект. |
||||
|
3 ч |
10,10±0,95 |
10,6 |
1,54 (6,01) |
0,007 |
102,0 |
14,6 |
|
|
Селезёнка |
24 ч |
0,053±0,01 |
0,050 |
0,20 (3,37) |
0,005 |
162,6 |
15,4 |
|
24 ч |
0,29±0,04 |
0,39 |
0,20 (3,74) |
0,045 |
39,4 |
11,9 |
|
|
3 ч |
5,10±1,11 |
3,11 |
1,54 (4,07) |
0,044 |
18,8 |
8,9 |
|
|
Желудок |
3 ч |
0,93±0,10 |
1,17 |
1,54 (0,94) |
0,041 |
19,9 |
9,2 |
|
24 ч |
0,76±0,19 |
0,86 |
0,20 (2,94) |
0,016 |
67,3 |
13,6 |
|
|
Мышца бедра |
5 мин |
0,089±0,012 |
0,060 |
55,5 (12,0) |
0,025 |
27,7 |
10,5 |
|
24 ч |
0,055±0,007 |
0,057 |
0,20 (4,01) |
0,032 |
45,7 |
12,4 |
|
|
интактная |
3 ч |
0,046±0,012 |
0,046 |
1,54 (2,61) |
0,008 |
89,6 |
14,3 |
|
Мышца бедра с введ. МСА |
– |
191,6±14,3 |
183,6 |
– |
0,010 |
69,3 |
13,7 |
|
Опухоль с введ. МСА |
– |
22,9±2,42 |
19,94 |
– |
0,004 |
173,2 |
15,5 |
В табл. 2 представлены рассчитанные по формулам (8) значения эффективных фармакокинетических характеристик 188Re-МСА на 1 кБк вводимой активности РФЛП для камеры введения: крови при внутривенном, мышцы бедра при внутримышечном и опухоли при внутриопухоле-вом способе введения.
Таблица 2 Эффективные фармакокинетические характеристики 188Re-МСА для камеры введения
|
Способ введения |
Площадь под кривой «Активность-время», кБк·ч/мл |
Клиренс, мл/ч |
Кажущийся объём распределения, мл |
Средняя концентрация активности, кБк/мл |
|
В/вен. |
0,10 |
10,31 |
149,42 |
0,01 |
|
В/мыш. |
36,00 |
0,03 |
0,55 |
1,82 |
|
В/опух. |
4,43 |
0,22 |
5,00 |
0,20 |
Анализ результатов моделирования и расчёта характеристик, представленных в табл. 1 и 2, показал, что способ введения существенно влияет на поведение 188Re-МСА в организме лабораторных животных. Так, после внутривенной инъекции происходит максимально быстрая миграция РФЛП из крови в периферические камеры. Константы накопления 188Re-МСА во всех органах при этом пути введения достигают высоких значений 1,54≤ K ≤55,5 ч-1. Напротив, при внутримышечной и внутриопухолевой инъекциях скорости накопления 188Re-МСА в органах и тканях примерно в 10 раз меньше: 0,20≤ K ≤6,80 ч-1 - при внутримышечном введении и 0,20≤ K ≤4,96 ч-1 - при внутриопухолевом введении РФЛП. При внутривенном введении максимальная концентрация 188Re-МСА достигается уже через 5 мин в лёгких (282,0 %/г), тогда как при внутримышечной и внутриопухолевой инъекциях максимальные концентрации 188Re-МСА в течение нескольких часов сохраняются в камере введения (183,6 %/г - для мышцы бедра и 19,94 %/г - для опухоли). Кроме того, при внутривенном введении максимальные концентрации РФЛП во всех исследованных органах и тканях в различные моменты времени в несколько раз превышают аналогичные значения концентраций при внутримышечном и внутриопухолевом путях введения.
Критическим органом со значительным накоплением активности при всех путях введения является щитовидная железа. Например, при внутриопухолевом введении РФЛП максимальное значение активности, достигаемое в ней через 3 ч (23,0 %/г), даже превышает аналогичное значение для опухоли. Данный процесс может быть вызван дополнительным накоплением в щитовидной железе освободившегося 188Re в результате частичного распада депонированного в органах и тканях 188Re-МСА по мере рассасывания белковых микросфер.
Сравнение значений констант выведения из почек и печени при внутривенном и внутримышечном путях введения РФЛП позволяет сделать вывод о преимущественно почечном клиренсе 188Re-МСА из организма в целом. При внутриопухолевом введении РФЛП оценить почечный клиренс не удалось из-за отсутствия экспериментальных данных о биораспределении 188Re-МСА после 72 ч от момента его введения в опухоль ( tmax >72 ч).
Рассчитанные значения эффективных периодов полувыведения 188Re-МСА из всех органов лежат в пределах от 8,9 ч (желудок при внутривенном введении) до 16,6 ч (щитовидная железа при внутриопухолевом введении) и не превышают периода физического полураспада 188Re равного 17 ч (табл. 1). Как было показано ранее в нашей работе [18], значения эффективных периодов полувыведения совпадают со значениями периодов полунакопления полной поглощённой дозы в соответствующих органах и они могут быть использованы в качестве дозиметрической характеристики для оценки скорости накопления поглощённых доз в камерах.
Анализ результатов расчётов характеристик, представленных в табл. 2, позволяет извлечь дополнительную информацию о распределении 188Re-МСА в организме в целом, которая согласуется с уже сделанными выводами. Так, при внутривенном введении рассчитанное значение клиренса крови примерно в 50 и 350 раз превышает значение клиренса РФЛП из опухоли и мышцы при внутриопухолевом и внутримышечном путях введения соответственно. При этом значение клиренса из опухоли примерно в 7 раз больше, чем из мышцы. Следовательно, 188Re-МСА при внутриопухолевом введении в начале распределения выводится из опухоли быстрее, чем при внутримышечном введении из мышцы. Сравнение рассчитанных значений объёмов распределения показывает, что при внутривенной инъекции 188Re-МСА из системного кровотока практически весь депонируется в органах и тканях ( Vd >4 мл, для мышей). Напротив, при внутримышечной и внутриопухолевой инъекциях объём распределения сопоставим с объёмом органа и весь 188Re-МСА преимущественно находится в мышце и опухоли соответственно.
С использованием данных табл. 1 по формулам (9) рассчитывались накопленные к определённому моменту времени и полные поглощённые дозы в органах и тканях мышей от 188Re-МСА. В качестве примера на рис. 2 приведены накопленные поглощённые дозы в некоторых органах, рассчитанные при разных путях введения РФЛП: 1 – внутривенный, 2 – внутримышечный, 3 – внутриопухолевый. Органом-мишенью являются органы с максимальным депонированием 188Re-МСА: лёгкие, мышца бедра и опухоль соответственно.
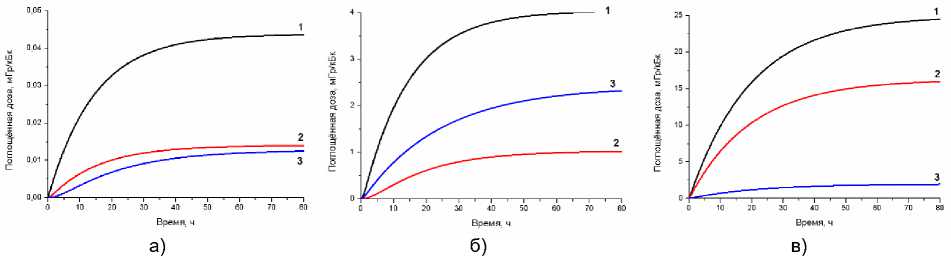
Рис. 2. Динамика накопления поглощённых доз от 188Re-МСА в а) крови, б) щитовидной железе, в) органе-мишени лабораторных мышей.
Как видно из рис. 2, значения поглощённых доз монотонно возрастают со временем, достигая своих предельных значений, равных полным поглощённым дозам, примерно к 80 ч от начала введения РФЛП при всех инъекциях. Причём «выпуклость» кривой поглощённой дозы зависит не только от предельного значения, но и от значения периода полунакопления полной поглощённой дозы, равного эффективному периоду полувыведения 188Re-МСА из соответствующего органа (о чём уже упоминалось ранее). Как показали наши расчёты, предельное значение поглощённой дозы в органе достигается за промежуток времени, равный или больший пяти эффективным периодам полувыведения, т.е. ≥5 Teff . Полученные в других органах зависимости накопленных поглощённых доз аналогичны, однако значения самих поглощённых доз в камерах при разных способах введения РФЛП существенно различаются.
В табл. 3 представлены значения полных поглощённых доз в органах и тканях мышей, рассчитанные при разных путях введения РФЛП. В скобках указаны значения поглощённых доз, определённые через константы накопления с применением формулы (6).
Таблица 3
Полные поглощённые дозы от 188Re-МСА, мГр/кБк
|
Способ введения |
Органы и ткани |
|||||||||
|
кровь |
лёгкие |
щитовидная железа |
почки |
печень |
селезёнка |
желудок |
мышца бедра инт. |
мышца бедра с вв. МСА |
опухоль с введ. МСА |
|
|
В/вен. |
0,044 |
24,922 (24,856) |
4,037 (4,104) |
0,192 (0,191) |
1,095 (1,120) |
0,971 (0,990) |
0,161 (0,163) |
0,004 (0,004) |
– |
– |
|
В/мыш. |
0,014 (0,014) |
0,006 (0,007) |
1,026 (1,175) |
0,029 (0,034) |
0,014 (0,017) |
0,004 (0,005) |
0,063 (0,062) |
0,003 (0,003) |
16,238 |
– |
|
В/опух. |
0,013 (0,015) |
0,127 (0,128) |
2,408 (2,355) |
– |
0,114 (0,116) |
0,017 (0,020) |
0,057 (0,067) |
0,004 (0,004) |
– |
2,000 |
Рассчитанные в рамках внутривенного способа введения значения полных поглощённых доз во всех камерах в несколько раз превышают аналогичные значения, полученные при внутримышечном и внутриопухолевом способах, что отражает факт депонирования 188Re-МСА в органах и тканях при внутривенном введении. При этом наибольшее значение поглощённой дозы достигается в лёгких. И оно в десятки раз превышает значения поглощённых доз в других органах, что отражает тропность 188Re-МСА к лёгочной ткани при внутривенной инъекции. Напротив, при внутримышечном и внутриопухолевом путях введения РФЛП наибольшие значения поглощённых доз получены в камерах введения (мышцы бедра и опухоли соответственно), которые также в десятки раз превышают значения поглощённых доз в других органах. Критическим органом при всех путях введения является щитовидная железа, рассчитанное значение полной поглощённой дозы в которой существенно больше аналогичных значений в других органах, а при внутриопухолевом введении оно даже превышает значение поглощённой дозы в опухоли! Наименьшее значение полной поглощённой дозы получено для мышцы бедра интактной при всех способах введения РФЛП.
Таким образом, динамика накопления поглощённых доз в органах и тканях от 188Re-МСА полностью соответствует его фармакокинетике (табл. 1, 2) при всех рассмотренных путях введения. А фармакокинетические и дозиметрические характеристики 188Re-МСА в организме лабораторных животных существенно зависят от способа его введения.
Заключение
Разработана камерная математическая модель кинетики 188Re-МСА в организме лабораторных животных при различных путях введения в соответствии с условиями эксперимента. С использованием экспериментальных данных радиометрии органов и тканей получены и проанализированы фармакокинетические кривые и кривые накопления поглощённых доз в камерах модели (органах и тканях), а также определены фармакокинетические и дозиметрические характеристики 188Re-МСА (транспортные константы накопления и выведения, биологические и эффективные периоды полувыведения, максимальные концентрации и времена их достижения, клиренс крови и кажущийся объём распределения, площадь под кривой и средняя концентрация активности, накопленные и полные поглощённые дозы внутреннего облучения и их периоды полунакопления).
Анализ рассчитанных фармакокинетических характеристик показал, что 188Re-МСА при внутривенном введении избирательно накапливается в лёгких, тогда как при внутримышечном и внут-риопухолевом введениях он остаётся в данной камере длительное время (мышца бедра и опухоль соответственно). Также выявлено повышенное накопление 188Re-МСА в щитовидной железе при всех путях введения, и в камерах печени и селезёнки при внутривенном введении, что может быть обусловлено частичным распадом депонированного 188Re-МСА в лёгких, мышце бедра и опухоли по мере рассасывания белковых микросфер. При этом сам 188Re-МСА выводится из организма преимущественно почками, а скорость и время выведения зависят от пути введения.
Из анализа рассчитанных дозиметрических характеристик следует, что значения накопленных поглощённых доз в органах и тканях при всех путях введения монотонно возрастают от момента введения 188Re-МСА, достигая своих предельных значений, равных полным поглощённым дозам примерно к 80 ч (этот промежуток времени примерно равен значению пяти эффективных периодов полувыведения). Максимальные значения полных поглощённых доз при внутривенном введении получены в камере лёгких, при внутримышечном – в камере мышцы бедра, при внут-риопухолевом – в камере опухоли. Также критическим органом для 188Re-МСА является щитовидная железа. В ней выявлены более высокие значения поглощённых доз по сравнению с остальными камерами модели при всех путях введения. Рассчитанные лучевые нагрузки на кровь при всех способах введения являются незначительными, однако при внутривенном введении они примерно в три раза больше, чем при других путях введения. При внутримышечном и внутриопухолевом введениях 188Re-МСА характеризуется более медленной динамикой накопления поглощённых доз во всех органах и тканях, чем при внутривенном введении.
Полученные результаты моделирования в совокупности позволяют рассматривать 188Re-МСА в качестве перспективного РФЛП для радионуклидной терапии опухолей разной локализации. При этом фармакокинетические и дозиметрические характеристики 188Re-МСА в организме существенно зависят от способа его введения.


