Расчёт оптической силы интраокулярной линзы при использовании разработанной технологии хирургического лечения катаракты, осложнённой выраженным спаечным процессом при неинфекционном увеите
Автор: Сафонова О.В., Шиловских О.В., Казайкин В.Н., Титаренко Е.М.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.20, 2025 года.
Бесплатный доступ
Обоснование: Современные технологии хирургии увеальной катаракты позволяют достигать высоких функциональных результатов. В последнее время повысились требования к рефракционным результатам лечения, проявилась проблема точного расчёта оптической силы интраокулярной линзы (ИОЛ), поскольку новые технологии предполагают её позиционирование, отличное от стандартного. Цель: определить величину поправки к формуле расчёта оптической силы ИОЛ при хирургии увеальной катаракты по разработанной технологии. Методы: Две группы пациентов были прооперированы по поводу увеальной катаракты, осложнённой выраженным спаечным процессом, по разработанной технологии, при которой положение ИОЛ сдвигалось на ?? мм к заднему полюсу (для профилактики рецидива воспаления и формирования спаек). У всех пациентов для оценки глубины передней камеры, положения ИОЛ и дистанции между радужкой и передней поверхностью ИОЛ в предоперационном периоде и через 3 месяца после операции проводилась оптическая когерентная томография переднего сегмента глаза. Расчёт оптической силы ИОЛ проводился по формуле Holladay II, при этом в основной группе применялась поправка к планируемому сфероэквиваленту -0,6 диоптрии (дптр) в миопическую сторону, в контрольной группе расчет проводился стандартно (поправка не учитывалась). Величина рефракционной ошибки оценивалась в сроки 3 месяца после операции. Результаты: В основной группе величина рефракционной ошибки оказалась отрицательной и составила -0,16±0,07 дптр. В 85% случаев (36 глаз) достигнутая рефракция находилась в пределах ±0,5 дптр от целевой, а в 97,5% случаев (39 глаз) – в пределах ±1,0 дптр. В контрольной группе наблюдался гиперметропический сдвиг рефракции цели по сравнению с планируемой, величина рефракционной ошибки составила 0,58±0,16 дптр, при этом в 27,5% случаев (11 глаз) послеоперационная рефракция отклонялась от целевой на ±0,5 дптр, а в 55% случаев (22 глаза) – на ±1,0 дптр. Различие статистически значимо и составило (p<0,001). Заключение: При хирургии увеальной катаракты, осложнённой выраженным спаечным процессом, по разработанной технологии при расчёте оптической силы ИОЛ по формуле Holladay II для улучшения рефракционных результатов требуется вносить поправку -0,6 дптр.
Увеальная катаракта, неинфекционный увеит, задний капсулорексис, расчёт ИОЛ
Короткий адрес: https://sciup.org/140312731
IDR: 140312731 | DOI: 10.25881/20728255_2025_20_4_S1_119
IOL power calculation using the developed technology for surgical treatment of cataracts complicated by a severe adhesive process in noninfectious uveitis
Backgraund: Modern uveal cataract surgery technologies allow for high functional results. Recently, refractive performance requirements have increased, and calculating the optical power of intraocular lenses (IOLs) is a pressing issue, as new technologies require different positioning. Aim: To determine the correction value for the IOL power calculation formula in uveal cataract surgery using the developed technology. Materials and methods: Two groups of patients underwent cataract surgery complicated by severe adhesions using the developed technique. All patients underwent anterior segment optical coherence tomography preoperatively and three months later to assess anterior chamber depth, iris-to-IOL distance, and IOL position. IOL power was calculated using the Holladay II formula. In the study group, a correction of -0.6 diopters (D) toward the myopic side was applied to the planned spherical equivalent. Anterior segment structures, IOL position, and refractive error were assessed three months after surgery. Results: In the study group, the refractive error was negative, amounting to -0.16+0.07 D. In 85% of cases (36 eyes), the achieved refraction was within ±0.5 D of the target, and in 97.5% of cases (39 eyes), it was within ±1.0 D. In the control group, the refractive error was 0.58+0.16 D, indicating a hyperopic shift in the target refraction compared to the planned one. In 27.5% of cases (11 eyes), the postoperative refraction deviated from the target by ±0.5 D, and in 55% of cases (22 eyes), it was within ±1.0 D. Conclusions: The use of a developed technology for cataract surgery complicated by severe adhesions in non-infectious uveitis allows for stable anatomical and topographic results and reduces the risk of recurrent adhesions in the anterior segment. Calculating IOL power using the Holladay II formula (with adjustments) in this group of patients significantly improves refractive outcomes.
Текст научной статьи Расчёт оптической силы интраокулярной линзы при использовании разработанной технологии хирургического лечения катаракты, осложнённой выраженным спаечным процессом при неинфекционном увеите
Обоснование
Хирургическое лечение увеальной катаракты (УК) связано с более высокой частотой осложнений, чем при обычных старческих катарактах [1]. Исход лечения УК зачастую непредсказуем вследствие многочисленных факторов, включая технические сложности самой операции и неопределённое влияние воспаления на ткани глаза в послеоперационном периоде.
Хирургия катаракты при увеите первое время (в 90е годы) выполнялась без имплантации ИОЛ, поскольку воспалительный процесс рецидивировал до 51,3% случаев (Foster et al., 1992-93) [2]. В настоящее время наиболее частым осложнением при хирургии УК по-прежнему остаётся послеоперационное воспаление, которое трудно контролировать, и которое часто приводит к нежелательным исходам: помутнению задней капсулы, образованию

иридокапсулярных сращений, зрачковых мембран, значимой преципитации на поверхности интраокулярных линз (ИОЛ), кистозному макулярному отёку, прогрессированию лентовидной кератопатии, послеоперационной гипотонии, транзиторному повышению внутриглазного давления (ВГД) или вторичной глаукоме. При рецидивах воспаления тяжесть спаечного процесса нарастает, зачастую сопровождается окклюзией или секклюзией зрачка и смещением ИОЛ с нарушением её правильной позиции [3].
В раннем послеоперационном периоде (в первые дни, недели) смещение ИОЛ встречается редко и преимущественно связано со слабостью волокон цинновой связки. В позднем периоде оно развивается в среднем в 1,9% случаев (до 4% при синдроме Фукса, до 8% при болезни Бехчета), что значительно выше в сравнении с неосложненными случаями – около 0,1–1% [4]. Значительно чаще при УК возникает децентрация ИОЛ – до 40% случаев, против 6,6% – при неосложненной катаракте [5; 6].
В настоящее время в ассортименте хирургов появились технологии, существенно снижающие частоту и степень перечисленных осложнений: рецидивов воспаления, даже при выраженном спаечном процессе – до 15%, повторного образования спаек – до 5% (в сравнении соответственно с 33% и 93% при традиционных технологиях) [7]. При таких результатах показатели максимально корригированной остроты зрения выросли с 0,2 до 0,7 (по таблице Сивцева) (p<0,001), и, естественно, повысились требования к точности послеоперационной рефракции. Поскольку некоторые новые технологии с целью снижения вероятности спаечного процесса после операции предполагают изменение позиционирования ИОЛ вдоль оптической оси глаза, актуализировался вопрос внесения поправочных данных в известные формулы расчёта оптической силы ИОЛ, используемые в ежедневной хирургической практике.
Прогнозирование рефракционной ошибки (PО) все чаще становится фокусом усилий по улучшению зрения пациентов с катарактой, осложнённой увеитом, однако на сегодняшний момент данные литературы весьма ограничены и встречаются только в единичных публикациях, в которых указанная средняя РО составила 0,56±0,67 диоптрий (дптр), а в 39,8% случаев отклонение от предполагаемого рефракционного результата оказалось не менее чем 0,5 дптр [8; 9].
Цель
На основании анатомо-топографического и клинико-функционального анализа результатов применения разработанной технологии хирургического лечения увеальной катаракты, осложненной выраженным спаечным процессом, определить величину поправки к формуле расчёта оптической силы ИОЛ Holladay II для трёхчастной ИОЛ с ангулированной гаптикой.
Методы
Ретроспективно-проспективное исследование проводилось на базе АО «Екатеринбургский Центр МНТК
«Микрохирургия глаза» (г. Екатеринбург) в период с 2016 по 2024 г. Исследование соответствовало требованиям Хельсинкской декларации (в редакции 2003 года), все участники подписывали информированное добровольное согласие на диагностическое обследование и хирургическое лечение.
Для анализа были сформированы две группы пациентов с хроническим неинфекционным увеитом, прооперированные по поводу осложнённой катаракты по разработанной технологии. У всех пациентов на предоперационном этапе наблюдался выраженный спаечный процесс в переднем сегменте глаза (более 2/3 протяженности окружности зрачка).
В 1 группе (основной), включившей 40 глаз 26 пациентов, применялась поправка к планируемому сферо-эквиваленту по формуле Holladay II – минус 0,6 дптр (в миопическую сторону).
Во 2 группе (контрольной), включившей 40 глаз 25 пациентов, расчёт ИОЛ проводился стандартно (без поправки), по формуле Holladay II.
В обеих группах оценивалась величина рефракционной ошибки через 3 месяца после операции, что связано со стабилизацией анатомо-топографических показателей переднего сегмента к указанному сроку [10].
Отбор пациентов в основную и контрольную группы осуществляли на основе разработанных критериев включения и исключения.
Критерии включения : верифицированный диагноз «неинфекционный увеит в стадии ремиссии» (в том числе, медикаментозной), катаракта с выраженным спаечным процессом в переднем сегменте глаза (протяженность задних синехий ≥2/3 окружности зрачка).
Критерии невключения : инфекционный увеит, обострение увеита, детский возраст (до 18 лет), другие внутриглазные вмешательства в анамнезе (кроме лазерной иридотомии по поводу бомбажа радужки), гипотония (ВГД менее 6 мм рт.ст.), глаза с ПЗО менее 20,0 и более 28 мм, фиброз/фимоз капсульного мешка, приводящий к нарушению положения ИОЛ, исходная и послеоперационная центральная толщина сетчатки (ЦТС) более 350 мкм.
Предоперационные биометрические измерения – ке-ратометрия, осевая длина (ПЗО), WTW, глубина передней камеры, толщина хрусталика были получены с помощью IOLMaster 700 (Carl Zeiss Meditec AG), была зафиксирована рефракция цели.
Послеоперационная рефракция была преобразована в сферический эквивалент (SE; в дптр) и рассчитана как сферическая составляющая плюс половина цилиндрической составляющей. Показатель рефракционной ошибки оценивался в сроки 3 месяца после хирургии и был рассчитан как разница фактического послеоперационного сфероэквивалента и рефракции цели. Положительная рефракционная ошибка отражала гиперметропический сдвиг в послеоперационном периоде (по сравнению с планируемой рефракцией), а отрицательная – миопический сдвиг.

Для уточнения состояния взаиморасположения структур переднего сегмента глаза в пред- и послеоперационном периоде всем пациентам дополнительно проводилась оптическая когерентная томография переднего сегмента глаза на приборе CASIA-2 («Tomey», Германия). С помощью данного метода в автоматическом или ручном режиме были получены величины следующих структур переднего сегмента глаза: ACD (Anterior Chamber Depth) – глубина передней камеры (расстояние от эндотелия в центре роговицы до переднего полюса хрусталика или ИОЛ), расстояние от задней поверхности радужки в области зрачка до передней поверхности ИОЛ (D) в носовом, височном, нижнем и верхнем секторах, угол наклона ИОЛ (TILT) – угол наклона ИОЛ относительно фронтальной плоскости, децентрация ИОЛ – смещение оптической части ИОЛ относительно зрительной оси глаза.
Все исследования выполнялись одним врачом.
Показатели состояния передней камеры регистрировались в стандартных условиях, показатели положения ИОЛ исследовались через 15 минут после 1-кратного закапывания глазных капель, содержащих фенилэфрин и тропикамид.
Статистическая обработка результатов исследования осуществлена с помощью пакетов программы Statistica v. 10.0 (StatSoft Inc., США). Для проверки формы распределения количественных данных использовали тест Колмагорова-Смирнова. Количественные переменные описаны через значение среднего (М) и стандартной ошибки среднего (SE) в виде М±SE. Сравнение показателей наблюдения проводилось с помощью t-критерия Стьюдента. Коррелятивный анализ проводился методом ранговой корреляции Спирмена. Результаты считались статистически значимыми при p <0,05.
Результаты
Группы были статистически сравнимы по предоперационным данным биометрии, клинико-функциональным и анатомо-топографическим показателям (p>0,05). Значимых различий, связанных с воспалительной реакцией и степенью выраженности спаечного процесса, а также различий по этиологическому признаку в исследуемых группах выявлено не было (р>0,05) (Таблица 1).
В основной группе время от начала увеита до хирургии катаракты составило 6,83±0,08 лет (от 8 месяцев до 27 лет), в контрольной группе – 7,23±0,81 лет (от 1 года до 14 лет).
В обеих группах первичный воспалительный процесс преимущественно локализовался в переднем сегменте, имел двусторонний рецидивирующий характер. Хирургическое лечение проводилось по разработанной технологии.
Применяемая авторская технология (Патент РФ на изобретение № 2336853/27.10.2008.), предполагала разделение синехий, факоэмульсификацию, проведение заднего капсулорексиса размером 3,5-4 мм, частичной витрэктомии в передних отделах витреальной полости
Табл. 1. Предоперационная характеристика исследуемых групп
|
Показатель |
Основная группа n = 40 |
Контрольная группа n = 40 |
|
Пол (мужчины/женщины) |
12 (46,1%)/ 14 (53,9%) |
11 (42,3%) 15 (57,7%) |
|
Возраст, лет |
44,47±3,11 |
43,89±2,59 |
|
Кератометрия, Дптр |
43,71±0,07 |
43,66±0,06 |
|
ПЗО, мм |
23,94±0,31 |
23,90±0,25 |
|
МКОЗ |
0,23±0,03 |
0,2±0,02 |
|
ВГД, мм рт.ст. |
16,45±1,33 |
15,96±1,41 |
|
Передние синехии |
5 (12,5%) |
4 (10%) |
|
Экссудативная зрачковая мембрана |
39 (97,5%) |
38 (95%) |
|
Бомбаж радужки |
13 (32,5%) |
14 (35%) |
|
ГПК, мм |
2,21±0,04 |
2,24±0,04 |
|
ЦТС, мкм |
327,25±20,17 |
319,24±19,35 |
|
Этиологический признак |
||
|
Ревматоидный артрит |
10 (25%) |
12 (30%) |
|
Анкилозирующий спондилоартрит |
7 (17,5%) |
6 (15%) |
|
Псориатический артрит |
8 (20%) |
8 (20%) |
|
Саркоидоз |
2 (5%) |
1 (2,5%) |
|
HLA B27- ассоциированный передний увеит |
6 (15%) |
8 (20%) |
|
Неясная этиология* |
7 (17,5%) |
5 (12,5%) |
Примечание : *– на момент хирургии отсутствовали убедительные данные за системное заболевание, инфекционные причины были исключены.
Табл. 2. Клинико-функциональные и анатомо-топографические показатели к 3 месяцам после операции
|
Показатели |
Основная группа |
Контрольная группа |
|
МКОЗ |
0,57±0,04 |
0,59±0,02 |
|
ВГД, мм рт.ст. |
14,38±0,70 |
13,87±1,29 |
|
Средняя дистанция от задней поверхности радужки до ИОЛ |
0,87±0,03 |
0,88±0,04 |
|
Глубина передней камеры, мм |
4,37±0,05 |
4,45±0,04 |
|
Тилт, град. |
5,23±0,23 |
5,31±0,21 |
|
Децентрация, мм |
0,36±0,02 |
0,34±0,03 |
|
Рецидивы воспаления |
3 (7,5%) |
2 (5%) |
|
Образование синехий* |
2 (5%) |
2 (5%) |
|
ЦТС, мкм |
295,13±15,36 |
301,72±21,46 |
Примечание : *– локальные синехии, не приводящие к бомбажу радужки.
роговичным доступом и погружение оптической части трёхчастной ИОЛ с ангулированной гаптикой за края заднего капсулорексиса. В результате достигалась увеличенная дистанция между радужкой и поверхностью ИОЛ, что значительно снижает вероятность формирования синехий в послеоперационном периоде.
Хирургическое лечение было выполнено одним хирургом, без интраоперационных осложнений.
Статистически значимых различий по частоте послеоперационных осложнений, по клинико-функциональным результатам и анатомо-топографическим показателям через 3 месяца после операции в исследуемых группах выявлено не было (р>0,05) (Таблица 2).
Анализ рефракционных результатов в контрольной группе показал, что величина рефракционной ошибки составила 0,58±0,16 дптр, то есть наблюдался гиперметропический сдвиг рефракции цели по сравнению с планируемой. В контрольной группе послеоперационная рефракция отклонялась от целевой на ±0,5 дптр в 27,5% случаев (11 глаз), а на ±1,0 дптр – в 55% случаев (22 глаза).
Благодаря внесению поправки к расчёту ИОЛ минус 0,6 дптр к 3 месяцам после операции в основной группе величина рефракционной ошибки была отрицательной и составила минус 0,16±0,07 дптр. Достигнутая рефракция находилась в пределах ±0,5 дптр от целевой в 85% случаев (36 глаз), в пределах ±1,0 дптр – в 97,5% случаев (39 глаз).
Распределение рефракционной ошибки в основной и контрольной группах к 3 месяцам после операции представлено на рисунке 1.
Статистически значимой корреляционной зависимости величины РО от величины ПЗО, ГПК, ЦТС, средней дистанции от радужки до ИОЛ выявлено не было (p>0,05).
Обсуждение
Новые технологии хирургического лечения катаракты, развившейся вследствие хронического увеита, и осложненной выраженным спаечным процессом, позволяют добиваться значительного снижения послеоперационных осложнений, включая рецидивирование спаечного процесса (до 5%, в сравнении с 93% при традиционных технологиях), и тем самым, обеспечивают существенный рост функциональных показателей, в-первую очередь, максимально корригированной остроты зрения [11]. Такие качественные изменения актуализировали тему точности расчёта оптической силы ИОЛ. Один требования к точности расчёта возникают при МКОЗ в послеоперационном периоде до 0,1 (по таблице Сивцева-Головина), и совсем иные – при МКОЗ 0,7.
При использовании разработанной в Екатеринбургском центре технологии хирургического лечения увеальной катаракты трёхчастная ИОЛ с ангулированной гаптикой позиционируется за задним капсулорексисом, т.е. смещается в сторону витреальной полости, и происходит очевидное увеличение расстояние между передней поверхностью оптической части ИОЛ и задней поверхностью радужки. Такое расположение ИОЛ значительно снижает риски рецидива воспалительного процесса и повторного образования спаек, но влечет за собой и изменение оптической системы глаза.
По данным предыдущих исследований, показатели глубины передней камеры к 3 месяцам после операции по разработанной технологии, по сравнению со стандартной, увеличились в среднем на 0,25 мм, составив, соответственно 4,42±0,05 и 4,17±0,022 мм (р<0,01) и оставались стабильными в течение всего последующего периода наблюдения [11]. При стандартном расчёте г 70
т 60
§ 40...............
g30...............
20...............
10...............
О- °.2’5.
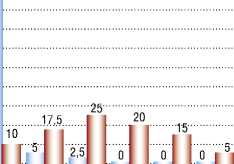
от-2,0 от-1,5 от-1,00 от-0,5 от 0,01 от 0,51 от 1,01 от 1,51 от 2,01
до-1,51 до-1,01 до-0,51 до 0 до 0,5 до 1,0 до 1,50 до 2,0 до 2,5
Основная группа ■ i Контрольная группа
Рис. 1. Распределение рефракционной ошибки (дптр) в исследуемых группах к 3 месяцам после операции Основная группа Контрольная.
оптической силы ИОЛ такое незначительное её смещение приводило к гиперметропическому сдвигу рефракции цели и, очевидно, снижало удовлетворённость пациентов рефракционным результатом при высоких показателях МКОЗ.
Вышеперечисленные особенности разработанной технологии потребовали внесения поправки минус 0,6 дптр (в миопическую сторону) при расчёте диоптрийной силы ИОЛ по формуле Holladay II, и в реальной практике это улучшило рефракционные результаты, при этом достигнутая рефракция находилась в пределах ±0,5 дптр от целевой в 95% случаев.
Заключение
Использование разработанной технологии хирургического лечения катаракты, осложнённой выраженным спаечным процессом при неинфекционном увеите, позволило добиться стабильных анатомо-топографических результатов и минимальной частоты встречаемости рецидива спаечного процесса в переднем сегменте глаза. Расчёт оптической силы ИОЛ по формуле Holladay II с поправкой минус 0,6 дптр у данной группы пациентов позволил снизить рефракционную ошибку с 0,58±0,16 дптр до минус 0,16±0,07 дптр (p<0,001).
Дополнительная информация. Участие авторов. Все авторы внесли значимый вклад в проведение исследования и подготовку статьи, прочли и одобрили финальную версию статьи перед публикацией.


