Расчёт пространственных распределений поглощённой энергии ионизирующего излучения в биологической ткани для протяжённых биоструктур при внутреннем облучении альфа-частицами, электронами и фотонами с различными энергиями: унифицированный подход для применения в ядерной медицине
Автор: Степаненко В.Ф., Богачева В.В., Дорохов А.В., Петухов А.Д., Кучеров В.В., Крылов В.В., Петросян А.П., Кочетова Т.Ю., Шуринов А.Ю., Иванов С.А., Шегай П.В., Каприн А.Д.
Рубрика: Научные статьи
Статья в выпуске: 1 т.34, 2025 года.
Бесплатный доступ
Цель исследования - разработать унифицированный подход для расчётов пространственных распределений поглощённой энергии ионизирующего излучения в пределах и вне биоструктур различной формы и размеров при внутреннем облучении альфа-частицами, электронами и фотонами разных энергий с целью упрощения процедур и сокращения объёма расчётов для дозиметрического обеспечения гарантий качества применения радиофармпрепаратов в ядерной медицине. В исследовании использованы базы данных ФГБУ «НМИЦ радиологии», содержащие информацию о пространственных распределениях в биологической ткани поглощённой энергии, излучаемой точечными изотропными источниками корпускулярного и фотонного излучения. Получены численные данные, характеризующие величины поглощённых долей энергии ионизирующего излучения в пределах и вне объёмов биологических структур, моделируемых сферами и слоями различных размеров при внутреннем облучении альфа-частицами, электронами и фотонами в диапазонах энергий 0,01-10; 0,0005-10 и 0,015-4,0 МэВ соответственно, что охватывает энергетические спектры практически всех радионуклидов, используемых в ядерной медицине. Установлено, что числовые последовательности расчётных значений поглощённых долей энергии (Ф), выраженные в виде зависимостей Ф от отношений размеров биологических структур или расстояний вокруг них к, так называемым, «радиусам 99% поглощения энергии вокруг точечных источников», приобретают унифицированный вид, применимый к биоструктурам различных размеров и форм при внутреннем облучении как корпускулярным, так и фотонным излучением различной энергии. Предложенный подход является универсальным инструментом для расчётов поглощённых доз в пределах и вне объёмов органов и опухолевых образований, на уровне их микроструктур, а также на клеточном и субклеточном уровнях при внутреннем облучении альфа-частицами, электронами и фотонами различных энергий. Данный подход сокращает объём требуемых расчётов и упрощает процедуры, необходимые для дозиметрического сопровождения доклинических/клинических испытаний и применения радиофармпрепаратов в ядерной медицине.
Дозиметрия, внутреннее облучение, радионуклиды, радиофармпрепараты, ядерная медицина, радиобиология, радиология, альфа-частицы, электроны, фотоны, дозовые функции, поглощённая доза, поглощённые доли энергии
Короткий адрес: https://sciup.org/170209555
IDR: 170209555 | УДК: 539.122:504.055 | DOI: 10.21870/0131-3878-2025-34-1-82-94
Calculation of spatial distributions of absorbed energy of ionizing radiation in biological tissue for sources of different shapes and sizes at internal irradiation by alpha-particles, electrons and photons with various energies: a unified approach for use in nuclear medicine
Aim of the study - develop a unified approach for calculating spatial distributions of absorbed energy of ionizing radiation within and outside of biostructures with various shapes and sizes at internal irradiation by corpuscular and photon radiation in order to simplify procedures and to reduce the volume of calculations for dosimetrical support to use of radiopharmaceuticals in nuclear medicine. The data bases, containing information on spatial distributions in biological tissue of absorbed energy, emitted by point isotropic sources of corpuscular and photon radiation, were used. Numerical data characterizing absorbed fractions of energy inside and outside the volumes of biological structures modeled by spheres and layers of different sizes at internal irradiation by alpha particles, electrons and photons in the energy ranges of 0.01-10 MeV, 0.0005-10 MeV and 0.015-4.0 MeV, respectively, were obtained. This almost completely covers the energy spectra of all radionuclides used in nuclear medicine. It has been established that numerical sequences of calculated values of absorbed fractions of energy, expressed as dependences of fractions of energy on the ratios of biological structures' sizes or distances around them to the so-called “radii of 99% absorption of energy around point sources”, becomes a unified form applicable to biostructures of various sizes and shapes at internal irradiation by corpuscular and photon radiation with different energies. The proposed approach is useful tool for calculating absorbed doses inside and outside the volumes of organs and tumor formations, at the level of their microstructures, as well as at the cellular and subcellular levels.
Текст научной статьи Расчёт пространственных распределений поглощённой энергии ионизирующего излучения в биологической ткани для протяжённых биоструктур при внутреннем облучении альфа-частицами, электронами и фотонами с различными энергиями: унифицированный подход для применения в ядерной медицине
Одним из важнейших элементов радиотерапии является планирование и верификация поглощённых доз ионизирующего излучения в очагах (опухолевых образованиях), а также в окружающих опухоль нормальных органах/тканях (органах риска). Дозиметрическое планирование необходимо для обеспечения как эффективности методов радиотерапии, так и их безопасности.
Степаненко В.Ф.* – зав. лаб., д.б.н., проф.; Богачева В.В .– в.н.с., к.б.н.; Дорохов А.В. – инж.-иссл.; Петухов А.Д. – с.н.с., к.б.н.; Кучеров В.В. – зав. отд., к.м.н.; Крылов В.В. – зав. отд., д.м.н.; Петросян А.П. – врач, к.м.н.; Кочетова Т.Ю. – врач-радиолог; Шуринов А.Ю. – с.н.с., к.м.н.; Иванов С.А. – директор, чл.-корр. РАН, д.м.н., проф. кафедры РУДН. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России. Шегай П.В. – зам. ген. директора, к.м.н.; Каприн А.Д. – ген. директор, директор МНИОИ им. П.А. Герцена, зав. каф. РУДН, акад. РАН, д.м.н., проф. ФГБУ «НМИЦ радиологии» Минздрава России.
Этим вопросам уделяется большое внимание не только в соответствующих регулятивных документах международного уровня (ВОЗ, МКРЕИ [1-5]), но и в национальных руководствах РФ [6, 7].
Вместе с тем, применение радиофармпрепаратов (РФП) в ядерной медицине достаточно длительное время, начиная с первых попыток использования РФП, не сопровождалось соответствующим дозиметрическим обеспечением. Это было связано с тем, что методы дозиметрии внутреннего облучения организма человека существенно сложнее методов дозиметрии внешнего облучения и весьма затратны по времени, что усложняло их применение в клинической практике. В результате сложилась парадоксальная ситуация, когда принципы клинической радиобиологии, заключающиеся в том, что терапевтические эффекты и безопасность воздействия на человека ионизирующего излучения непосредственно зависят от поглощённой дозы этого излучения, измеряемого в единицах Гр, замещались в радионуклидной терапии (РНТ) на суррогатный подход, когда вместо поглощённых доз при планировании РНТ использовались так называемые «стандартные введённые активности РФП», измеряемые в единицах МБк. Однако, введение «стандартных активностей РФП» совершенно не означает, что поглощённая доза (в Гр) в очаге или органе риска будет определяться только введённой активностью РФП (в МБк) [8, 9]. Величина поглощённой дозы внутреннего облучения (в Гр) в очаге или органе риска при одной и той же введённой активности РФП существенно зависит также от объёма биологической структуры, в которую поступил РФП, и от динамики его накопления и выведения [8-10].
В последние годы, как это следует из Публикации Европейской ассоциации ядерной медицины [8], Публикации МАГАТЭ 2024 г. [9], Публикации 140 Международной комиссии по радиологической защите [11], Доклада 96 Международной комиссии по радиационным единицам и измерениям [12], подходы к обеспечению эффективности и безопасности РНТ существенно изменились – происходит смена парадигмы в этой области: от введения пациентам эмпирически установленных активностей РФП к индивидуальному дозиметрическому планированию, основанному на оценках доз внутреннего облучения опухолевых образований и органов риска пациентов.
Общий подход к расчётам поглощённых доз внутреннего облучения при использовании РФП в ядерной медицине был рекомендован Медицинским комитетом по дозам внутреннего облучения (Medical Internal Radiation Dose Committee или MIRD) [13]. В соответствии с подходом MIRD, одним из важнейших параметров, используемых при расчётах распределений поглощённых доз внутреннего облучения радионуклидами, является величина «поглощённой доли энергии» (Ф). Величина Ф представляет собой отношение энергии ионизирующего излучения, поглощённой некоторой биоструктурой «мишенью», к энергии, излучаемой некоторой биоструктурой «источником», в объёме которой распределён излучающий радионуклид. Рассматриваются две типичные ситуации внутреннего облучения: а) «самооблучение», когда биоструктуры «источник» и «мишень» совпадают и б) – «взаимное облучение», когда «источник» и «мишень» не совпадают. Как правило, расчёт величин Ф для биоструктур различных размеров и форм, представляемых с помощью соответствующих геометрических моделей, выполняется методами стохастического моделирования взаимодействия с веществом ионизирующего излучения различного вида и разной энергии, что требует значительных объёмов вычислений и больших затрат времени. Как правило, они публикуются в виде соответствующих обширных справочных материалов (см., например, [14]), т.к. в большинстве случаев оперативный расчёт величин Ф весьма затруднён из-за большого объёма необходимых вычислений. В связи с рекомендациями международных организаций [9, 11, 12] о необходимости дозиметрического планирования РНТ в клинической практике с целью обеспечения дозиметрических гарантий безопасности и эффективности РНТ, возрастает актуальность разработок методов дозиметрических расчётов поглощённых доз внутреннего облучения, позволяющих, при сохранении валидности дозиметрических оценок, упростить процедуры и сократить объёмы необходимых вычислений. Унификация и упрощение процедур дозиметрии внутреннего облучения является ключевыми позициями для внедрения в клиническую практику методов дозиметрического обоснования/обеспечения применения РФП с терапевтическими и диагностическими целями [8, 9, 12].
Материалы и методы
Использованы программные средства и базы данных ФГБУ «НМИЦ радиологии» Минздрава России, имеющие государственную регистрацию [15-18]. Расчёт пространственных распределений поглощённых долей Ф для альфа-частиц, электронов и фотонов различной энергии внутри и вне биоструктур в виде сфер и слоёв разных размеров проведён путём аналитического интегрирования изоэнергетических функций точечных изотропных источников ионизирующего излучения (см. рис. 1 со схематической иллюстрацией точечного изотропного источника) по объёмам протяжённых биоструктур с равномерно распределёнными в них точечными источниками в пределах окружающих эти объёмы конгруэнтных поверхностей в биологической ткани (рис. 2 и 3).
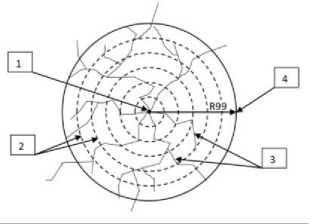
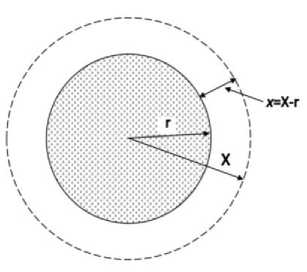
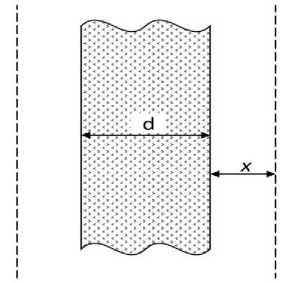
Рис. 3. Биоструктура, моделируемая объёмом в идее слоя в виде слоя, с равномерно распределёнными в объёме точечными источниками, и окружающая биоструктуру конгруэнтная изоэнергетическая поверхность в биологической ткани. d – толщина биоструктуры в виде слоя с равномерно распределёнными в её объёме точечными источниками ионизирующего излучения; x –толщина слоя биологической ткани, прилегающего к излучающей биоструктуре.
Рис. 1. Схематическая иллюстрация размена и поглощения энергии ионизирующего излучения в объёмах биологической ткани, заключённых в пределах сферических изоэнергетических поверхностей, окружающих расположенный в их центре точечный изотропный источник излучения; 1 – точечный изотропный источник ионизирующего излучения; 2 – объёмы биологической ткани, заключённые в пределах изо-энергетических поверхностей различных радиусов (пунктирные линии);
-
3 – схематические изображения траекторий размена и поглощения излучения точечного изотропного источника;
-
4 – изоэнергетическая поверхность (сплошная линия) с радиусом R99, в пределах которой поглощается 99% энергии, излучаемой точечным изо-
Рис. 2. Биоструктура, моделируемая сферическим объёмом, с равномерно распределенными в объёме точечными источниками ионизирующего излучения и окружающая биоструктуру конгруэнтная изоэнергетическая поверхность. r – радиус сферической биоструктуры с равномерно распределенными в её объёме точечными источниками ионизирующего излучения; X – радиальное расстояние от центра излучающей сферической биоструктуры до окружающей её изоэнергетиче-ской поверхности; x=X-r – толщина сферического слоя биологической ткани, окружающего излучающую биоструктуру.
тропным источником.
Плотность и состав биологической ткани соответствует данным, приведённым в Публикации 89 МКРЗ [19]. Нелинейная аппроксимация результатов расчётов аналитическими функциями выполнена с использованием программы Microcal Origin 6.1.
Результаты и обсуждение
Величины поглощённых долей энергии при внутреннем облученииальфа-частицами
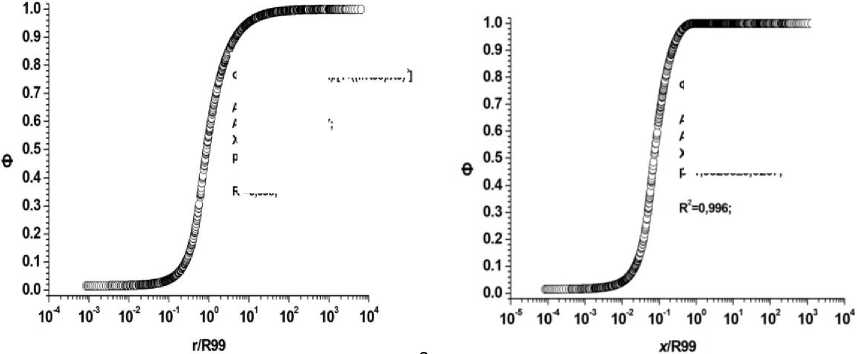
На рис. 4 в графическом виде показаны результаты расчётов поглощённых в биологической ткани долей энергии (Ф) при внутреннем облучении альфа-частицами различных энергий, излучаемыми источниками, представляющими скими объёмами разных радиусов.
собой биоструктуры,
моделируемые сфериче-
O(x/R99)=A2+(A1 •A2)/[1+((x/R99,J/X0)p]
<4r/R99)^+(A1-«MWRWWl
A2=0,9999+0,00168;
A1 =0,0001 ±0,000007:
X0=0,9050+0,0176;
p=1,60458+0.0241;
^=0,998;
42=1,0000+0,00132;
A1=0,0001 ±0,000008;
X0=0,075010,00128;
0=1,9828610,0267;
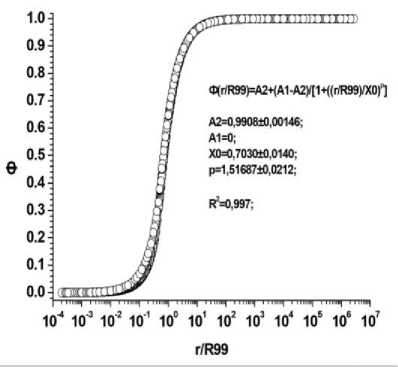
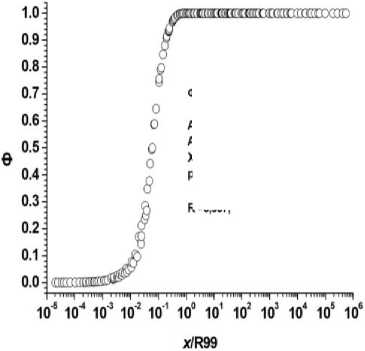
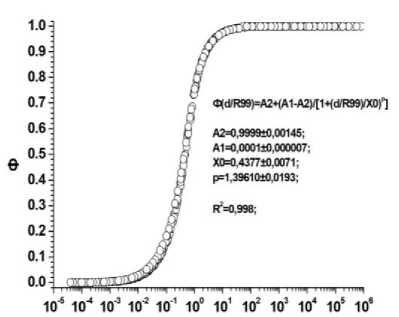
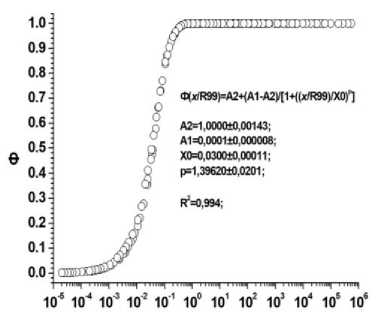
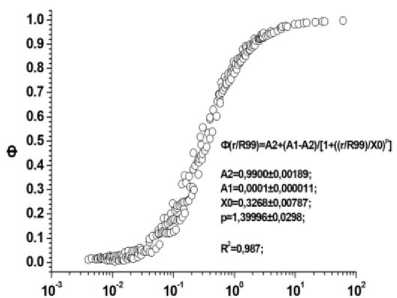
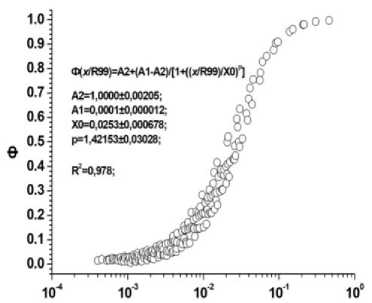
б Рис. 4. Результаты расчётов величин Ф для биоструктур, моделируемых сферическими объёмами, и излучающими альфа-частицы в диапазоне энергий 0,01-10 МэВ. По оси ординат: а) Ф – отношения величин энергий, поглощённых внутри объёмов сфер различных радиусов (r), к энергиям, излучённым этими же источниками («самооблучение»); б) Ф – отношения величин энергий, поглощённых внутри окружающих источники слоёв биологической ткани с различной толщиной (x), к энергиям, излучённым источниками. По оси абсцисс: а) r/R99 – отношения радиусов (r) сфер, содержащих равномерно распределённые в объёмах точечные источники с разными энергиями, к соответствующим этим энергиям величинам R99; б) x/R99 – отношения толщины (x) сферических слоёв-«мишеней», окружающих сферы-источники равномерно распределёнными в объёмах точечными источниками с разными энергиями, к соответствующим этим энергиям величинам R99.
®( A2=0,990010,00143; A1=0: X0=0,4400+0.00796: p=1,3999610,0202; ^=0,997: A2=0,9999+0,00145; A1=0,0001 ±0.000004; X0=0,0440±0,000811; p=1,39600+0,0195; б
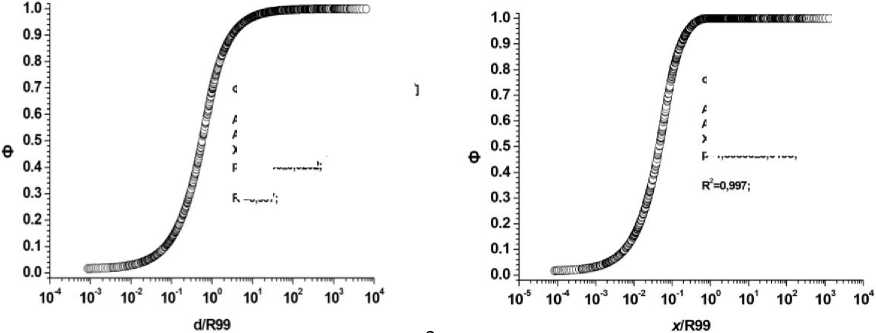
Рис. 5.
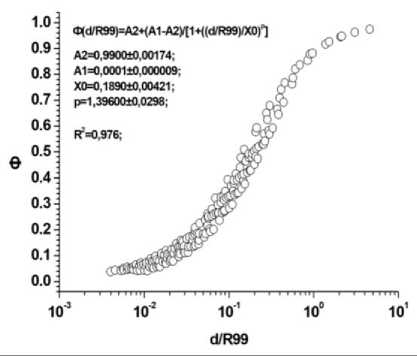
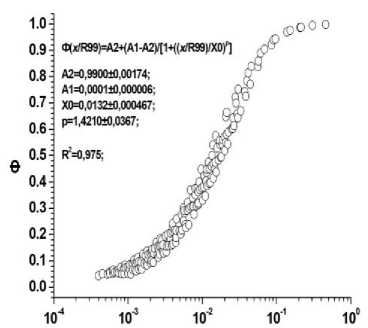
Результаты расчётов величин Ф для источников в виде слоёв из биологической ткани, излучающих альфа-частицы разных энергий. Диапазон энергий альфа-частиц: 0,01-10 МэВ. По оси ординат: а) Ф – отношения величин энергий, поглощённых внутри объёмов слоёв различной толщины (d), к энергиям, излучённым этими же источниками («самооблучение»); б) Ф – отношения величин энергий, поглощённых внутри прилегающих к источникам слоёв биологической ткани с различной толщиной (x), к энергиям, излучённым источниками. По оси абсцисс: а) d/R99 – отношения толщины (d) слоёв, содержащих равномерно распределённые в объёмах точечные излучатели альфа-частиц с разными энергиями, к соответствующим этим энергиям величинам R99; б) x/R99 – отношения толщины (x) слоёв биологической ткани, прилегающих к слоям, излучающим альфа-частицы различных энергий, к соответствующим этим энергиям величинам R99.
На рис. 5 показаны результаты расчётов поглощённых в биологической ткани долей энергии (Ф) при внутреннем облучении альфа-частицами различных энергий, излучаемыми источниками, представляющими собой биоструктуры, моделируемые слоями разной толщины. Величины поглощённых долей энергии при внутреннем облучении электронами На рис. 6 показаны результаты расчётов поглощённых в биологической ткани долей энергии (Ф) при внутреннем облучении электронами различных энергий, излучаемыми источниками, представляющими собой биоструктуры, моделируемые сферическими объёмами разных радиусов.
Рис. 6.
Результаты расчётов величин Ф для источников в виде сфер из биологической ткани, излучающих электроны различных энергий. Диапазон энергий электронов: 0,0005-10 МэВ. По оси ординат: а) Ф – отношения величин энергий, поглощённых внутри объёмов сфер различных радиусов (r), к энергиям, излучённым этими же источниками («самооблучение»); б) Ф – отношения величин энергий, поглощённых внутри окружающих источники слоёв биологической ткани с различной толщиной (x), к энергиям, излучённым источниками. По оси абсцисс: а) r/R99 – отношения радиусов (r) сфер, содержащих равномерно распределённые в объёмах точечные излучатели электронов с разными энергиями, к соответствующим этим энергиям величинам R99; б) x/R99 – отношения толщины (x) сферических слоёв, окружающих сферы, излучающие электроны различных энергий, к соответствующим этим энергиям величинам R99.
qxiRWu+iAHawi+iWROwn A2=0,9958+0.00158: AM; XO=O, 0500+0,0011; H ,7695310,00216; (^=0,997; б d/R99
Рис. 7.
Результаты расчётов величин Ф для источников в виде слоёв из биологической ткани, излучающих электроны разных энергий. Диапазон энергий электронов: 0,0005-10 МэВ. По оси ординат: а) Ф – отношения величин энергий, поглощённых внутри слоёв различной толщины (d), к энергиям, излучённым этими же источниками («самооблучение»); б) Ф – отношения величин энергий, поглощённых внутри прилегающих к источникам слоёв биологической ткани с различной толщиной (x), к энергиям, излучённым источниками. По оси абсцисс: а) d/R99 – отношения толщины (d) слоёв, содержащих равномерно распределённые в объёмах точечные излучатели электронов с разными энергиями, к соответствующим этим энергиям величинам R99; б) x/R99 – отношения толщины (x) слоёв биологической ткани, прилегающих к слоям, излучающим электроны различных энергий, к соответствующим этим энергиям величинам R99.
X/R99 а б На рис. 7 показаны результаты расчётов поглощённых в биологической ткани долей энергии (Ф) при внутреннем облучении электронами различных энергий, излучаемыми источниками, представляющими собой биоструктуры, моделируемые слоями разной толщины. Величины поглощённых долей энергии при внутреннем облучении фотонами На рис. 8 показаны результаты расчётов поглощённых в биологической ткани долей энергии (Ф) при внутреннем облучении фотонами различных энергий, излучаемыми источниками, представляющими собой биоструктуры, моделируемые сферическими объёмами разных радиусов. r/R99 X/R99 а б
Рис. 9.
Результаты расчётов величин Ф для источников в виде слоёв из биологической ткани, излучающих фотоны разных энергий. Диапазон энергий фотонов: 0,0015-4 МэВ. По оси ординат: а) Ф – отношения величин энергий, поглощённых внутри слоёв различной толщины (d), к энергиям, излучённым этими же источниками («самооблучение»); б) Ф – отношения величин энергий, поглощённых внутри прилегающих к источникам слоёв биологической ткани с различной толщиной (x), к энергиям, излучённым источниками. По оси абсцисс: а) d/R99 – отношения толщины (d) слоёв, содержащих равномерно распределённые в объёмах точечные излучатели фотонов с разными энергиями, к соответствующим этим энергиям величинам R99;
б) x/R99 – отношения толщины (x) слоёв биологической ткани, прилегающих к слоям, излучающим фотоны различных энергий, к соответствующим этим энергиям величинам R99. Рис. 8. Результаты расчётов величин Ф для источников в виде сферических объёмов из биологической ткани, излучающих фотоны разных энергий. Диапазон энергий фотонов: 0,015-4 МэВ. По оси ординат: а) Ф – отношения величин энергий, поглощённых внутри сферических источников различных радиусов (r), к энергиям, излучёнными этими же источниками («самооблучение»); б) Ф – отношения величин энергий, поглощённых внутри прилегающих к источникам сферических слоёв биологической ткани с различной толщиной (x), к энергиям, излучённым источниками. По оси абсцисс: а) r/R99 – отношения радиусов (r) сфер, содержащих равномерно распределённые в их объёмах точечные излучатели фотонов с разными энергиями, к соответствующим этим энергиям величинам R99; б) x/R99 – отношения толщины (x) сферических слоёв биологической ткани, прилегающей к источникам, излучающим фотоны различных энергий, к соответствующим этим энергиям величинам R99. а На рис. 9 показаны результаты расчётов поглощённых в биологической ткани долей энергии (Ф) при внутреннем облучении фотонами различных энергий, излучаемыми источниками, представляющими собой биоструктуры, моделируемые слоями разной толщины. В представленном на рис. 5-9 виде (нормировка радиусов сфер-источников (r), толщина слоёв-источников (d) или толщина слоёв-мишеней (x) на величины радиусов 99% поглощения энергии R99) зависимости величин поглощённых долей Ф от r/R99, d/R99 или x/R99 имеют унифицированный сигмоидальный вид и применимы для различных энергий альфа-частиц, электронов, фотонов и размеров биологических структур, моделируемых сферическими объёмами или слоями биологической ткани. Аналитические функции, аппроксимирующие зависимости Ф от d/R99 или x/R99, а также значения их параметров, приведены на полях рисунков. Величины R99 для электронов и фотонов c энергиями в диапазонах 0,0005-10 МэВ и 0,015-4 МэВ соответственно опубликованы нами ранее [20]. В табл. 1 приведены величины R99 для альфа-частиц с энергиями в диапазоне 0,01-10 МэВ. Расчёты выполнены с использованием данных, представленных в [21]. Таблица 1 Энергии альфа-частиц (E) и соответствующие им значения величин R99 в биологической ткани*
E, МэВ
0,010
0,025
0,050
0,080
0,15
0,30
R99, см
1,57x10
-5
3,53x10
-5
6,11x10
-5
8,62x10
-5
1,33x10
-4
2,11 x10
-4
E, МэВ
0,60
0,90
2,0
4,0
7,0
10
R99, см
3,43x10
-4
4,73x10
-4
1,06x10
-3
2,7x10
-3
6,4x10
-3
1,16x10
-2
Примечание: * – Величины R99 для энергий, не совпадающих с энергиями, представленными в табл. 1, можно определять методом линейной интерполяции между двумя ближайшими значениями R99, соответствующими двум соседним энергиям. Сравнение результатов расчётов величин поглощённых долей энергии с имеющимися в доступной литературе данными Сравнение результатов расчётов величин поглощённых долей энергии (Ф), полученных с помощью разработанного унифицированного подхода, с имеющимися в доступной литературе [22-24] величинами Ф, рассчитанными методом Монте-Карло, для биоструктур, излучающих моноэнер-гетические альфа-частицы, электроны и фотоны, показывает, что отношения рассчитанных нами значений (Фрасч) к соответствующим величинам, полученным на основе данных литературы (Флит) составляют:
-
Фрасч/Флит=1,08
±
0,11 для альфа-частиц (энергии - 5,304 МэВ, 6,05 МэВ, 8,75 МэВ, что соответствует энергиям альфа-частиц, излучаемых
210
Po,
212
Bi и
212
Po, радиусы сфер-источников – от 1 до 10 мкм, n=30);
-
Фрасч/Флит=1,06
±
0,09 для электронов (диапазон энергий - 0,1-4 МэВ, радиусы сфер -от 0,134 до 0,985 см, n=42);
-
Фрасч/Флит=1,12
±
0,21для фотонов (диапазон энергий - 0,015-2,75 МэВ, радиусы сфер – от 0,62 до 11,272 см, n=66).
В литературе [22-24] представлены результаты расчётов так называемых S-факторов, выраженных в Гр/(Бк
x
с). Величины S-факторов были пересчитаны в соответствующие величины поглощённых долей энергии Ф и сопоставлены с нашими данными – значениями Ф для соответствующих энергий излучения и сферических биоструктур с этими же радиусами.
Следует особо отметить, что величины поглощённых долей энергии (Ф) для альфа-частиц, рассчитанные с помощью разработанного подхода, были сравнены с имеющимися в доступной литературе немногочисленными данными, характеризующими поглощение энергии альфа-излучения в биологических микроструктурах сферической формы с радиусами, соответствующими объёмам клеток и ядер клеток. То, что при такого рода расчётах рассматриваются биоструктуры именно микрометрических размеров, обусловлено коротким пробегом альфа-частиц (от десятых долей до десятков микрометров - в диапазоне энергий альфа-излучения от 10 кэВ до 10 МэВ).
Следует также отметить, что при моделировании объёмов биологических структур эллипсоидами с объёмами V и площадями поверхностей S возможно использование сферической геометрии с эффективным радиусом сферы r=3
x
V/S [20].
Как было отмечено выше, сравнение проведено только для биоструктур, моделируемых сферическими объёмами. Результаты сравнения рассчитанных нами величин Ф для биоструктур, моделируемых слоями различной толщины, включая сравнение данных о распределениях поглощённой энергии вне протяжённых источников, не представлены из-за отсутствия соответствующих данных в доступной литературе. Заключение Получены численные данные, характеризующие пространственные распределения поглощённых долей энергии корпускулярного и фотонного излучения разной энергии в пределах и вне объёмов протяжённых биологических структур, моделируемых сферами и слоями различных размеров. Расчёты проведены для энергий альфа-частиц, электронов и фотонов в диапазонах 0,01-10 МэВ, 0,0005-10 МэВ и 0,015-4,0 МэВ соответственно, что охватывает энергетические спектры практически всех радионуклидов, используемых в ядерной медицине. Установлено, что числовые последовательности расчётных значений поглощённых долей энергии (Ф), выраженные в виде зависимостей Ф от отношений размеров биологических структур или расстояний вокруг них к так называемым «радиусам 99% поглощения энергии вокруг точечных источников», приобретают унифицированный вид, применимый к биоструктурам различных размеров и форм при внутреннем облучении как корпускулярным, так и фотонным излучением различной энергии. Предложенный подход является универсальным инструментом для расчётов поглощённых доз в пределах и вне объёмов органов и опухолевых образований, на уровне их микроструктур, а также на клеточном и субклеточном уровнях при внутреннем облучении альфа-частицами, электронами и фотонами различных энергий. Данный подход сокращает объём требуемых расчётов и упрощает процедуры, необходимые для дозиметрического сопровождения доклинических/клинических испытаний и применения радиофармпрепаратов в ядерной медицине.