Распространённость диабетической ретинопатии и опыт применения сулодексида в комплексной терапии
Автор: Алферьев Д.В.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 9 т.11, 2025 года.
Бесплатный доступ
В терапии диабетической ретинопатии активно применяются различные подходы, среди которых значительное место занимает комплексная терапия, направленная не только на контроль гликемии, но и на улучшение микроциркуляции и стабилизацию сосудистой стенки сетчатки. Сулодексид — препарат с ангиопротекторным и антикоагулянтным эффектами, доказавший свою эффективность при лечении различных сосудистых заболеваний, включая осложнения сахарного диабета. Клинические исследования показывают, что применение сулодексида в составе комплексной терапии диабетической ретинопатии способствует улучшению микроциркуляторных нарушений и снижению прогрессирования поражения сетчатки. Данная статья посвящена анализу распространенности диабетической ретинопатии и оценке опыта применения сулодексида в комплексной терапии у пациентов, что отражает современные тенденции в управлении данной патологией. Особое внимание уделяется эпидемиологическим аспектам и клиническим результатам терапии, что позволяет подчеркнуть значимость комплексного подхода в снижении риска тяжелых осложнений и улучшении качества жизни пациентов с диабетической ретинопатией. Диабетическая ретинопатия, сахарный диабет, сулодексид, ангиопротекторная терапия. Таким образом, учитывая рост числа пациентов с диабетом и связанной с ним ретинопатией, а также важность своевременного и адекватного лечения, исследование опыта применения сулодексида в комплексной терапии является актуальным и востребованным направлением в офтальмологии и эндокринологии.
Диабетическая ретинопатия, сахарный диабет, сулодексид, ангиопротекторная терапия
Короткий адрес: https://sciup.org/14133784
IDR: 14133784 | УДК: 616.379-008.64-06:617.735-085 | DOI: 10.33619/2414-2948/118/35
Prevalence of Diabetic Retinopathy and the Experience of Using Sulodexide in Comprehensive Treatment
Various therapeutic approaches are used in the management of DR, among which integrated treatment strategies play a crucial role. These are aimed not only at glycemic control but also at improving microcirculation and stabilizing the retinal vascular wall. Sulodexide, a drug with proven angioprotective and anticoagulant properties, has demonstrated efficacy in the treatment of a range of vascular pathologies, including diabetic complications. Clinical studies indicate that sulodexide, when used as part of combination therapy for diabetic retinopathy, contributes to improved microcirculatory function and slows the progression of retinal damage. This article presents an analysis of the prevalence of diabetic retinopathy and an evaluation of the clinical experience of using sulodexide in combination therapy, reflecting current trends in the management of this condition. Special emphasis is placed on epidemiological data and treatment outcomes, highlighting the importance of a comprehensive approach in reducing the risk of severe complications and improving the quality of life for patients with diabetic retinopathy.
Текст научной статьи Распространённость диабетической ретинопатии и опыт применения сулодексида в комплексной терапии
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 616.379-008.64-06:617.735-085
Диабетическая ретинопатия (ДР) является одной из ведущих причин слепоты среди трудоспособного населения во всем мире. Согласно данным Института показателей и оценки здоровья (IHME), бремя болезней, связанных с диабетом, в 2017 году составляло 1014,24 случая на 100 000 населения, что на 17,63% больше, чем в 1999 году, когда этот показатель был 862,2 на 100 000 населения [2]. Такая тенденция роста заболеваемости диабетом наблюдается и в странах СНГ. В частности, в Республике Казахстан в период с 2016 по 2018 год зарегистрировано значительное увеличение заболеваемости всеми формами сахарного диабета (СД). По состоянию на 2018 год уровень заболеваемости СД 2 типа составил 223,93 на 100 000 мужчин и 311,50 на 100 000 женщин. Заболеваемость диабетической ретинопатией в этой же популяции достигла 11,91 на 100 000 мужчин и 17,93 на 100 000 женщин [8].
Глобально, по данным Международной диабетической федерации (IDF), число людей с сахарным диабетом превысило 537 миллионов в 2021 году и прогнозируется рост до 643 миллионов к 2030 году и до 783 миллионов к 2045 году . Диабетическая ретинопатия встречается у примерно третьей части всех пациентов с диабетом, причем значительная часть из них подвергается риску прогрессирующей потери зрения. В мировой практике раннее выявление и адекватное лечение ДР позволяют значительно замедлить или предотвратить развитие тяжелых осложнений и инвалидизации по зрению [1].
Диабетическая ретинопатия (ДР) — одно из наиболее частых и тяжёлых микроангиопатических осложнений сахарного диабета (СД), представляющее собой прогрессирующее поражение сосудов сетчатки, способное приводить к полной и необратимой потере зрения. На сегодняшний день ДР занимает лидирующие позиции среди причин слепоты и значительного снижения остроты зрения у лиц трудоспособного возраста, что обуславливает не только медицинскую, но и выраженную социально-экономическую значимость проблемы [3].
Согласно данным Международной диабетической федерации (IDF), в 2021 году число людей, живущих с сахарным диабетом, превысило 537 миллионов человек по всему миру. Прогнозируемый рост к 2030 году составит до 643 миллионов, а к 2045 — до 783 миллионов пациентов [4]. Диабетическая ретинопатия выявляется у приблизительно 30–35% всех больных СД, при этом у 10% из них развивается зрительно-значимая форма заболевания, включая пролиферативную ретинопатию и диабетический макулярный отёк, что требует немедленного вмешательства [5].
Ситуация усугубляется тем, что ДР может длительное время протекать бессимптомно, особенно на ранних стадиях. Это затрудняет раннюю диагностику и своевременное начало терапии. Недостаточная осведомлённость пациентов, низкая доступность офтальмологических скринингов в ряде стран, а также коморбидное течение с другими сосудистыми и метаболическими нарушениями существенно повышают риск инвалидизации [6]. Согласно данным Института показателей и оценки здоровья (IHME), бремя заболеваний, связанных с сахарным диабетом, в глобальном масштабе возросло на 17,63% за период с 1999 по 2017 год [7].
В странах СНГ также наблюдается устойчивая тенденция роста заболеваемости как сахарным диабетом, так и его сосудистыми осложнениями. Например, в Республике
Казахстан в период с 2016 по 2018 год заболеваемость СД 2 типа составила 223,93 на 100 000 мужчин и 311,50 на 100 000 женщин, тогда как частота выявления диабетической ретинопатии в этой же популяции достигла 11,91 на 100 000 мужчин и 17,93 на 100 000 женщин .
Современные принципы ведения пациентов с ДР включают комплексный подход, предполагающий не только достижение компенсации углеводного обмена, но и воздействие на патофизиологические механизмы сосудистого поражения сетчатки: улучшение микроциркуляции, снижение проницаемости сосудистой стенки, предотвращение пролиферации и образования новообразованных сосудов. Особый интерес в этом контексте представляет применение ангиопротекторных средств, обладающих также антикоагулянтным и противовоспалительным действием.
Сулодексид — это гликозаминогликановый препарат, обладающий выраженными ангиопротекторными, антитромботическими и противовоспалительными свойствами. Он зарекомендовал себя в терапии сосудистых осложнений при диабете, таких как диабетическая нефропатия, ангиопатии нижних конечностей, а в последнее десятилетие всё активнее изучается его эффективность при ретинопатии. Согласно результатам ряда клинических исследований, применение сулодексида способствует снижению уровня сосудистого эндотелиального фактора роста (VEGF), улучшению реологических свойств крови и снижению выраженности отёка сетчатки [8, 9].
Таким образом, в условиях нарастающей глобальной распространённости диабета и его тяжёлых офтальмологических осложнений, исследование эффективности комплексной терапии с использованием сулодексида представляет собой актуальное и перспективное направление. Оно имеет значение как для клинической практики, так и для оптимизации стратегии ведения пациентов с ДР, направленной на снижение риска слепоты и улучшение качества жизни больных.
Цель: оценить клиническую эффективность применения препарата сулодексид в составе комплексной терапии у пациентов с диабетической ретинопатией.
Материал и методы исследования
Настоящее исследование базируется на анализе данных, полученных в процессе наблюдения и лечения пациентов с диагнозом, диабетическая ретинопатия (ДР) на базе офтальмологического лазерного центра. Исследование включало как ретроспективный анализ статистических показателей, так и проспективную оценку клинической эффективности комплексной терапии с применением препарата Вессел Дуэ Ф (сулодексид).
-
1. Анализ статистических данных. Проанализированы данные по обращаемости пациентов с сахарным диабетом и осложнённой диабетической ретинопатией в медицинском центре за последние 3 года. Учитывались показатели первичного выявления ДР, количество направлений на лечение, а также доля пациентов, проходивших курс терапии с применением ангиопротекторов.
-
2. Применение препарата Вессел Дуэ Ф. На базе офтальмологического центра был проведён курс комплексного лечения пациентов с различными стадиями ДР с использованием препарата Вессел Дуэ Ф. Схемы терапии разрабатывались индивидуально, с учётом стадии ретинопатии, сопутствующих патологий и общего состояния пациента.
-
3. Офтальмологическое наблюдение — циклоскопия. Всем пациентам с ДР, участвующим в исследовании, проводилась циклоскопия (осмотр сетчатки и заднего сегмента глаза с использованием широкоугольных методов визуализации) до и после курса лечения Вессел Дуэ Ф. Оценивались следующие параметры: выраженность микроаневризм и кровоизлияний, наличие и степень отёка макулы, состояние сосудистой стенки, динамика пролиферативных изменений.
-
4. Сравнительный анализ с группой пациентов, прошедших лазерное лечение.
Группа 1: Пероральный приём — по 1 капсуле 2 раза в день в течение 50 дней.
Группа 2: Внутримышечные инъекции — 2 мл препарата в течение 10 дней, затем пероральный приём по 1 капсуле 2 раза в день в течение 50 дней.
Группа 3: Подкожные инъекции в височную область — по 1 мл с каждой стороны в течение 10 дней, затем пероральный приём по аналогичной схеме.
Дополнительно была сформирована группа пациентов, которым проводилось лазерное коагуляционное лечение ДР. Им также выполнялась циклоскопия до и после процедуры, с аналогичной оценкой морфофункционального состояния сетчатки. Это позволило провести сравнительный анализ эффективности лазерной терапии и медикаментозного ангиопротекторного лечения.
Методы статистической обработки:
-
– для количественной оценки результатов использовались методы описательной статистики, включая расчёт средних величин, стандартных отклонений и доверительных интервалов.
-
– для сравнения параметров до и после лечения применялись парные t-тесты и U-критерий Манна–Уитни.
-
– достоверность различий принималась при уровне значимости p < 0,05.
Обработка данных проводилась с использованием программы Statistica 12.0 (StatSoft Inc., США) и Microsoft Excel.
При анализе обращаемости пациентов на циклоскопию за трёхлетний период (2020– 2022 гг.) отмечалась тенденция к росту заболеваемости диабетической ретинопатией как в абсолютных, так и в относительных показателях.
Таблица 1
ДИНАМИКА ЗАБОЛЕВАЕМОСТИ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИЕЙ ПО ДАННЫМ ОФТАЛЬМОЛОГИЧЕСКОГО ЦЕНТРА за 2020–2022 гг.
|
Год |
Всего пациентов |
Из них с ДР |
% пациентов с ДР |
|
|
2020 |
2351 |
280 |
11,9 |
|
|
2021 |
2 154 |
337 |
15,6 |
|
|
2022 |
2 464 |
413 |
16,8 |
Анализ данных, представленных в Таблице 1, свидетельствует о стабильной тенденции к увеличению удельного веса пациентов с диабетической ретинопатией среди всех обратившихся. Если в 2017 году доля пациентов с ДР составляла 11,9%, то уже в 2019 году она увеличилась до 16,8 %, что указывает на рост выявляемости заболевания либо на общее ухудшение течения сахарного диабета в популяции пациентов, проходящих офтальмологическое обследование. Рост показателей может быть обусловлен как увеличением общей численности пациентов с длительным анамнезом СД, так и улучшением методов диагностики и скрининга, включая циклоскопию. Эти данные подчёркивают необходимость своевременного выявления ретинопатии и раннего начала патогенетически обоснованной терапии, включая применение ангиопротекторных препаратов. Диаграмма ниже иллюстрирует распределение пациентов с диабетической ретинопатией по различным стадиям и фазам на основании собственных данных (%) (Рисунок 1).
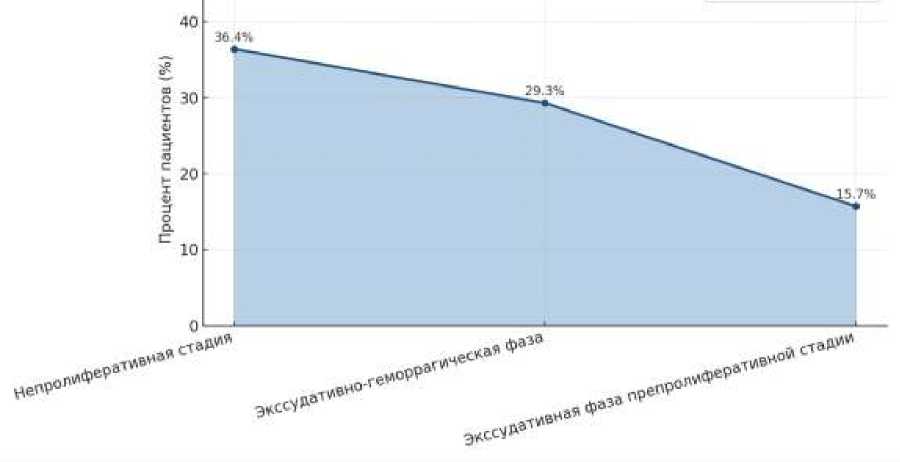
Рисунок 1. Распределение пациентов с диабетической ретинопатией
Анализ распределения пациентов с диабетической ретинопатией по стадиям и фазам, представленный на диаграмме, свидетельствует о том, что наибольший удельный вес приходился на пациентов с непролиферативной стадией заболевания — 36,4 %. Это указывает на то, что большинство больных обращаются за медицинской помощью на ранних этапах развития ретинопатии, когда преобладают микроаневризмы, точечные кровоизлияния и минимальные признаки нарушения сосудистой проницаемости.
На втором месте по частоте встречаемости находились пациенты с экссудативногеморрагической фазой — 29,3 %. Эта фаза характеризуется более выраженными изменениями сосудистой стенки, наличием твердых и мягких экссудатов, кровоизлияний в сетчатку и стекловидное тело, что свидетельствует о прогрессировании патологического процесса.
Третью позицию заняли пациенты с экссудативной фазой препролиферативной стадии — 15,7 %. Данная стадия считается предвестником тяжёлых осложнений, включая развитие пролиферативной ретинопатии и необратимой утраты зрения.
Таким образом, приведённые данные подчёркивают важность раннего выявления диабетической ретинопатии, регулярного офтальмологического контроля и своевременного начала комплексного лечения, направленного на стабилизацию сосудистой стенки и улучшение микроциркуляции в сетчатке. Пациентам проводилось лечение по одной из трёх схем введения препарата Вессел Дуэ Ф (сулодексид), отличающихся по способу и кратности введения показана в Таблице 2.
Таблица 2
СХЕМЫ ВВЕДЕНИЯ ПРЕПАРАТА СУЛОДЕКСИД
|
Способ введения |
Описание |
|
|
Схема 1 |
Внутримышечно + перорально |
Внутримышечно по 2 мл в течение 10 дней, затем внутрь по 2 капсулы в сутки 25 дней. |
|
Схема 2 |
Подкожно (виски) + внутримышечно + перорально |
По 0,5 мл подкожно с обеих сторон (всего 1 мл), оставшиеся 1 мл — внутримышечно. Курс 10 дней, затем внутрь по 2 капсулы в сутки 25 дней. |
|
Схема 3 |
Подкожно (виски) + перорально |
По 1 мл с каждой стороны в височную область (всего 2 мл в сутки) в течение 10 дней, затем внутрь по 2 капсулы в сутки 25 дней. |
На Рисунке 2 представлена диаграмма, отражающая распределение пациентов в зависимости от схемы консервативного лечения препаратом Вессел Дуэ Ф, выраженное в процентном соотношении.
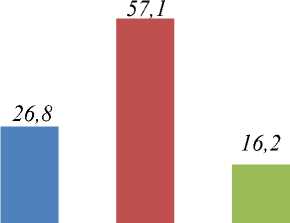
Рисунок 2. Результаты консервативного лечение Вессел Дуэ Ф (%)
-
■ подкожно в область виска + перорально
-
■ внутримышечно + перорально
-
■ перорально
Наиболее распространённой оказалась комбинированная схема, включающая внутримышечное введение препарата с последующим пероральным приёмом, — данный вариант был применён у 57,1% пациентов. Подкожное введение Вессел Дуэ Ф в височную область с последующим пероральным приёмом использовалось у 26,8% пациентов. Минимальная доля (16,2%) пришлась на исключительно пероральное применение препарата. Полученные данные свидетельствуют о преимущественном использовании парентеральнопероральных схем, вероятно, в связи с их большей клинической эффективностью. Лазерное лечение ДР проводилось у пациентов с препролиферативной и пролиферативной стадией. Перед операциями проводилось консервативное лечение Вессел Дуэ Ф по 3 схеме.

Рисунок 3 Состояние глазного дна до консервативного и лазерного лечения

Рисунок 4 Состояние глазного дна после консервативного и лазерного лечения
Результаты лечения.
По завершении курса консервативной терапии все пациенты отмечали улучшение общего состояния, у части из них наблюдалось уменьшение выраженности болевого синдрома в нижних конечностях, что способствовало повышению уровня повседневной активности и качества жизни. В ходе клинического и офтальмологического наблюдения зафиксировано достоверное снижение выраженности макулярного отёка, уменьшение количества и площади ретинальных геморрагий, а также твёрдого экссудата.
Наиболее выраженный терапевтический эффект отмечен при применении третьей схемы лечения, включающей подкожное введение препарата в височную область с последующим пероральным приёмом. Однако данная схема характеризуется повышенной болезненностью инъекций, связанной с объёмом вводимого препарата, что ограничивает её применение у пациентов с низким болевым порогом.
Проведение консервативной терапии позволило значительно сократить количество сеансов лазерной коагуляции сетчатки — с 5–6 до 2–3, что указывает на стабилизацию патологического процесса и повышение эффективности медикаментозного вмешательства. У пациентов с непролиферативной стадией диабетической ретинопатии зафиксировано улучшение остроты зрения на 10–20%, у больных с препролиферативной стадией — на 5– 10%. У пациентов с пролиферативной формой заболевания острота зрения в ходе медикаментозного лечения оставалась без существенной динамики, однако положительный эффект (до 10%) был зарегистрирован после проведения сеансов лазерной коагуляции (Рисунок 3).
Вывод
Применение препарата Вессел Дуэ Ф в составе комплексной терапии диабетической ретинопатии способствует снижению активности патологического ангиоретинального процесса, уменьшению площади поражения сетчатки и, как следствие, необходимости в проведении объемного лазерного вмешательства, что подтверждает его высокую клиническую эффективность.


