Растворимость фосфатов редкоземельных металлов в карбонатно-щелочных системах
Автор: Герасв С.А., Литвинова Т.Е., Масанина М.Н., Гордиманова Э.А.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 1 т.24, 2024 года.
Бесплатный доступ
Статья посвящена исследованию процесса растворения фосфатов некоторых редкоземельных металлов (РЗМ) в карбонатно-щелочных системах. В качестве объекта исследования рассмотрены модельные осадки фосфатов тяжелых РЗМ - гольмия и иттербия; РЗМ средней массы - самария и гадолиния; легкого РЗМ - неодима, а также иттрия, который не является лантаноидом. Фосфаты РЗМ представляют собой примесные компоненты, входящие в состав промышленного отхода фосфогипса (ФГ). По различным оценкам ежегодно в России образуется от 10 до 15 млн тонн такого отхода, что влечет за собой возникновение экологических проблем в местах его захоронения. Для рационального использования минерального сырья необходимо разработать такое решение, которое позволит переработать фосфогипс в коммерчески ценные продукты, одним из которых может быть концентрат редкоземельных металлов. Редкоземельные металлы получили широкое применение в различных отраслях: оборона, энергетика, электроника, металлургия, катализ и другие. Однако малые объемы производства и отсутствие полного цикла производства некоторых РЗМ вынуждают осуществлять их закупку за рубежом. Таким образом, исследование направлено на достижение экономической стабильности и технологического суверенитета Российской Федерации. В статье представлено описание влияния температуры, концентрации карбонатного раствора, межфазного отношения и скорости перемешивания на процесс растворения фосфатов РЗМ. В рассматриваемом концентрационном диапазоне при температуре 90 °С максимальные равновесные степени извлечения в раствор составили: E(Ho) = 75,6 %; E(Yb) = 85,5 %; E(Nd) = 62,5 %; E(Gd) = 71,6 %; E(Y) = 73,1 %; E(Sm) = 46,1 %. Результаты экспериментального исследования относятся к части термодинамического анализа системы REEPO4 - K2CO3, которые в дальнейшем могут быть использованы при моделировании процесса попутного извлечения РЗМ из техногенных отходов, в частности фосфогипса, методом жидкостной карбонатно-щелочной конверсии.
Редкоземельные металлы, лантаноиды, фосфогипс, карбонат калия, изотермы растворимости
Короткий адрес: https://sciup.org/147243229
IDR: 147243229 | УДК: 669 | DOI: 10.14529/met240101
The dissolution of the rare-earth phosphates in carbonate-alkaline media
The article is dedicated to the dissolution process of some rare-earth phosphates in carbonate-alkaline media. The object of the study are model sediments of rare-earth phosphates. Different groups of the rare earth elements (REE) have been researched according to their masses: heavy-weight - holmium and ytterbium; medium-weight - samarium and gadolinium; light-weight - neodymium and yttrium though it does not belong to lanthanoids. REE-phosphates are impurity and taken place into technogenic waste phosphogypsum (PG). It is considered to be the PG has being be produced from 10 to 15 million tons per year. Because of the PG goes to disposal site, it causes ecological issues. For the rational use of natural raw materials, it is necessary to develop a solution that allows the phosphogypsum process into commercially valuable products. Concentrate of rare earth metals may be one of these. REE are widely used in various industries: defense, energy, electronics, metallurgy, catalysis and others. However, there are low-level production and incomplete production cycle in the several REE industry, this it is in need of import. Therefore, the study is aimed at achieving economic stability and technological sovereignty of the Russian Federation. The article demonstrates an illustration of the influence of temperature, concentration of carbonate solution, liquid to solid ratio and intensity of mixing on the REE-phosphates solubility. In the concentration range under consideration at a temperature of 90 °C, the maximum equilibrium degrees of extraction into solution were: E(Ho) = 75.6 %; E(Yb) = 85.5 %; E(Nd) = 62.5 %; E(Gd) = 71.6 %; E(Y) = 73.1 %; E(Sm) = 46.1 %. The results of this research are part of the thermodynamic analysis of the REEPO4 - K2CO3 system, which can subsequently be used to model the process of associated REE extraction from industrial waste (phosphogypsum, for example) by liquid carbonating conversion method.
Текст научной статьи Растворимость фосфатов редкоземельных металлов в карбонатно-щелочных системах
Одно из актуальных направлений для исследований в области переработки минерального сырья – это повышение комплексности переработки [1, 2]. В промышленном масштабе до сих пор не внедрен ни один способ, который позволил бы рационально использовать апатитовый концентрат при переработке его в ортофосфорную кислоту [3, 4]. Часть производств организована по дигидратному методу (1), что влечет за собой образование отхода дигидрата сульфата кальция, другая часть производств – по полугидратному методу (2), приводящему к появлению отхода полугидрата сульфата кальция [5, 6]:
Ca5 (PO 4 )3 F + 5H 2 SO 4 + 10H 2 O ^ 5CaSO 4 • 2H 2 O Ф + 3H 3 PO 4 + HF T ; (1)
Ca5(PO 4 )3F + 5H 2 SO 4 + 2,5H 2 O ^ 5CaSO 4 • 0,5H 2 O Ф + 3H 3 PO 4 + HF T . (2)
Дигидрат и полугидрат сульфата кальция имеют схожий состав, отличающийся лишь содержанием структурной воды. В случае захоронения открытым способом эти отходы и вовсе могут иметь одинаковый состав в силу протекания процессов дегидратации (3) и гидратации (4), обусловленных аналогичным влиянием условий окружающей среды на них [7, 8]:
CaSO4 • 2H 2 O ^ CaSO4 • 0,5H 2 O + 1,5H 2 O; (3)
CaSO4 • 0,5H2O + 1,5H2O ^ CaSO4 • 2H 2 O. (4)
Таким образом, полугидрат и дигидрат сульфата кальция следует рассматривать как одну группу отходов (фосфогипс), области применения и способы переработки которых должны быть основаны на общем подходе.
Одним из путей утилизации фосфогипса в мировой практике является использование его в качестве добавки в строительные смеси, материала для дорожного покрытия или, например, подкисляющего агента в сельском хозяйстве. Однако применение отхода в качестве добавки в лучшем случае решает только проблему утилизации и никоим образом не позволяет увеличить глубину переработки исходного сырья, что приводит к потере ценных компонентов [9, 10].
Согласно данным рентгенофазового анализа различных проб отвального фосфогипса, в его состав входит от 0,1 до 0,8 % редкоземельных металлов в пересчете на оксиды [11, 12], причем нахождение их зафиксировано преимущественно в виде фосфата трехвалентного металла [13, 14]. Хотя ФГ содержит относительно небольшое количество РЗМ, тем не менее он является перспективным источником для их извлечения, поскольку:
-
1) является безопасным вторичным сырьем с точки зрения радиационного фона [15];
-
2) в сравнении с другими РЗМ-содержа-щими источниками, расположенными на территории Российской Федерации, отвалы ФГ являются доступными [16, 17].
Например, в рудах месторождения Томтор (Якутия) содержится изобилие редкоземельных металлов: от 7 до 10 % РЗМ в пересчете на оксидную форму, тем не менее из-за отсутствия инфраструктуры вблизи месторождения добыча и переработка ископаемого сырья не представляется возможной [18].
Существует множество способов химической переработки ФГ, основанных на кислотном выщелачивании. Технологические схемы предполагают получение РЗМ и гипса как потенциального строительного материала [19, 20]. Комплексной переработки эти методы не предусматривают и не приводят к сокращению количества отвалов [21].
Карбонатная конверсия фосфогипса предполагает его обработку крепкими растворами карбонатов натрия или аммония с получением сульфата щелочного металла или аммония и фосфомела (конверсионного мела) [22, 23]. К недостаткам способа следует отнести неудовлетворительные реологические показате- ли и фильтруемость мелкодисперсной пульпы фосфомела и потери РЗМ [24].
Прием использования карбонатно-щелочных сред является перспективным для переработки фосфатно-карбонатных сырьевых источников [25–27] за счет образования растворимых карбонатных комплексов состава REE (CO 3 ) 2 [28–30].
Тем не менее поведение малорастворимых соединений РЗМ в карбонатно-щелочных средах изучено далеко не в полной мере [31, 32] и носит, скорее, отрывочный характер.
В этой связи необходимо осуществить экспериментальное подтверждение теоретических исследований с целью определения практических значений растворимости фосфатов различных групп РЗМ: тяжелых – гольмия и иттербия; средних – самария и гадолиния; легких – неодима, а также иттрия, который не является лантаноидом [33].
Цель настоящего исследования – установить влияние ряда параметров на растворимость фосфатов РЗМ в карбонатно-щелочных средах: температуры, времени, концентрации карбоната калия, межфазного отношения и скорости перемешивания.
Методология
Изучено влияние температуры, скорости и продолжительности перемешивания, концентрации карбоната в растворе на растворимость фосфатов гольмия, иттербия, неодима, гадолиния, иттрия и самария.
В качестве исходных образцов были отобраны навески модельных фосфатов гольмия, иттербия, самария, гадолиния, неодима и иттрия, которые были предварительно получены осаждением РЗМ ортофосфорной кислотой (0,2 М) из нитратных сред (0,2 М):
REE 3+ + H 3 PO 4 ^ REE PO 4 Ф + 3H + . (5)
После осаждения модельные осадки направлялись на фильтрование, промывку и сушку, а также на рентгенофазовый анализ для подтверждения состава.
Предварительное исследование растворимости фосфатов редкоземельных металлов было опробовано в среде карбоната калия и аммония, а также в среде карбоната и гидрокарбоната натрия. В ряду: карбонат калия, карбонат аммония, карбонат натрия, гидрокарбонат натрия наблюдается снижение растворимости фосфатов РЗМ, что может указывать на влияние природы катиона. Снижение растворимости в среде гидрокарбонат-иона, вероятно, связано с малой стабильностью гидрокарбонатных комплексов РЗМ, вследствие чего экспериментальные исследования, представленные в данной статье, проводились именно в среде карбоната калия.
Изучение растворимости было проведено в изотермических условиях на лабораторном оборудовании HEL Auto-MATE Reactor System.
Параметры, при которых осуществлялось построение изотерм растворимости, выбирались из следующих соображений.
-
1. Температура
-
2. Время
-
3. Концентрация карбонатного раствора
-
4. Межфазное отношение
-
5. Интенсивность перемешивания
Большинство известных способов переработки фосфогипса в мел методом жидкостной карбонатно-щелочной конверсии подразумевают ведение процесса при температуре 50–90 °С [34]. Выбор температуры 90 °С для исследования влияния концентрации на степень извлечения РЗМ обусловлен увеличением скорости процесса (согласно уравнению Аррениуса) и смещением химического равновесия в сторону образования карбонатного комплекса (принцип Ле Шателье), поскольку процесс является эндотермическим.
Изотермы растворимости представляют собой зависимость равновесной концентрации (степени извлечения) РЗМ от концентрации карбонатного раствора. В этой связи время должно быть подобрано таким образом, чтобы дальнейшее его увеличение не приводило к росту растворимости.
Растворимость карбоната калия в воде составляет 110,5 г на 100 г воды, следовательно, технически представляется возможным исследовать растворимость осадков РЗМ в широком диапазоне его концентрации, в то время как растворимость карбоната натрия (21,8 г на 100 г воды) и карбоната аммония (96 г на 100 г воды) значительно ниже и не позволит рассмотреть поведение фосфатов РЗМ в области высоких концентраций.
Межфазное отношение (ж : т) оказывает существенное влияние на растворимость, причем попытки проведения эксперимента при стехиометрических соотношениях не привели к ожидаемому результату.
Параметр обеспечивает интенсификацию процесса растворения и влияет на отвод про- дуктов (карбонатных комплексов РЗМ) с поверхности твердого фосфата РЗМ. Экспериментально было установлено, что число оборотов оказывает воздействие на процесс растворения и при значении выше 650 об/мин возрастания степени извлечения не наблюдается. Растворение REEPO4, равно как и REE2(CO3)3, протекает в диффузионном режиме. Скорость перемешивания, учитывая опыт, установлена 650 об/мин.
Анализ концентрации РЗМ в растворе производился методом трилонометрического титрования в присутствии индикатора арсеназо (III) по формуле
_ C Трилон Б ' V T рилон Б
C REE = у ,
V a
где C Трилон Б – концентрация титранта, экв/л; V Трилон Б – объем трилона Б, ушедшего на титрование пробы, мл; V a – объем аликвоты, взятой на анализ, мл.
Результаты эксперимента
Согласно анализу термодинамических параметров (энтальпия, энтропия, энергия Гиббса), фосфаты редкоземельных металлов способны растворяться в среде карбонат-иона, причем наиболее вероятными продуктами процесса являются карбонатные комплексы [35]. При этом реакция имеет эндотермический характер, а значит, повышение температуры позволит не только повысить скорость, но и сместить химическое равновесие в сторону образования комплекса. На примере фосфата иттербия (III) (рис. 1) представлено несколько кинетических кривых при разных T . Увеличение температуры приводит к увеличению скорости, а также к увеличению степени извлечения в раствор в состоянии системы, близком к равновесному.
Скорость перемешивания пульпы (рис. 2) и межфазное отношение (рис. 3) оказывают воздействие на процесс растворения фосфатов редкоземельных металлов. Анализ экспериментально полученных зависимостей для фосфатов гольмия (III), иттербия (III) и неодима (III) свидетельствует о том, что при n > 500 об/мин и ж : т > 2000 мл/г дальнейшее увеличение этих параметров не проводит к возрастанию E , таким образом, построение изотерм растворимости осуществлялось при n = 650 об/мин и ж: т = 2100 мл/г.
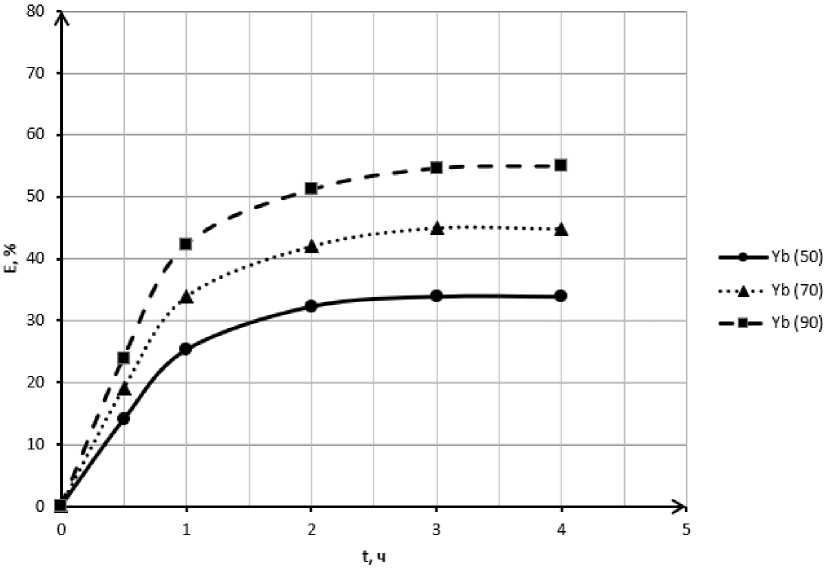
Рис. 1. Влияние температуры на растворимость YbPO 4 Fig. 1. An influence of temperature on YbPO 4 dissolution
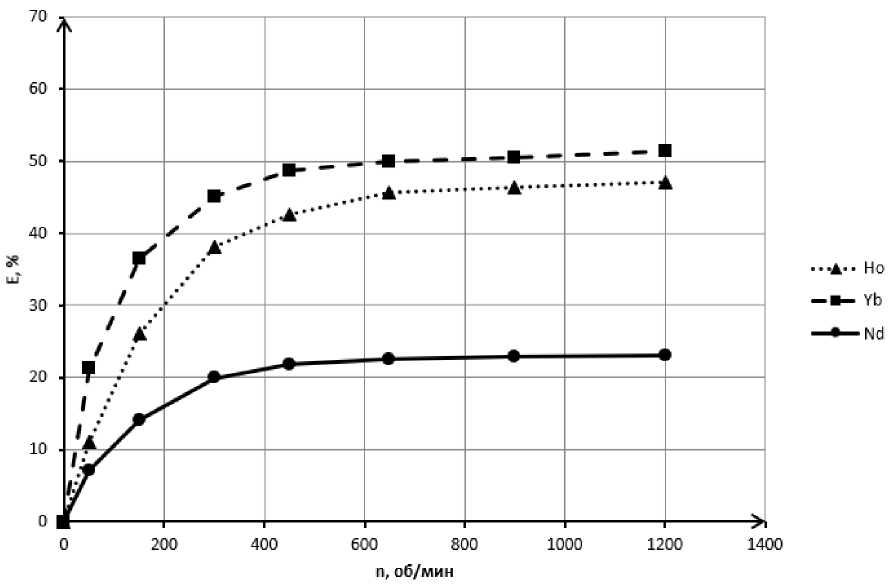
Рис. 2. Влияние скорости перемешивания на растворимость REE PO 4 Fig. 2. An influence of mixing rate on REE PO 4 dissolution
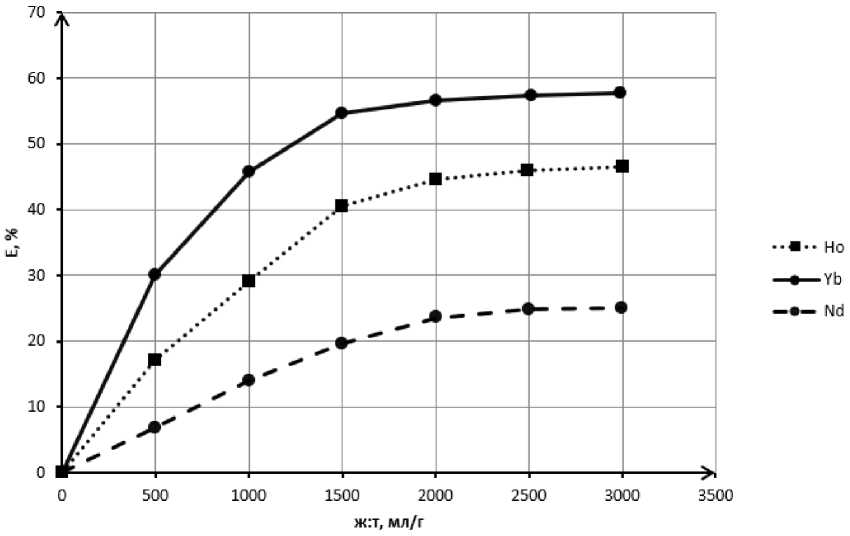
Рис. 3. Влияние межфазного отношения на растворимость REE PO 4 Fig. 3. An influence of liquid to solid ratio on REE PO 4 dissolution
Известные литературные данные полагают полное растворение REEPO4 в карбонатных средах уже при 1 М K2CO3, однако использование раствора такой концентрации не приводит к полному растворению, поэтому рассмотрено влияние концентрации карбонат- иона на растворимость. Эксперимент проводили при T = 90 °C, скорости перемешивания 650 об/мин, ж :т = 2100 мл/г и продолжительности перемешивания 6 ч. На рис. 4 показаны зависимости E-C для фосфата иттербия (III).
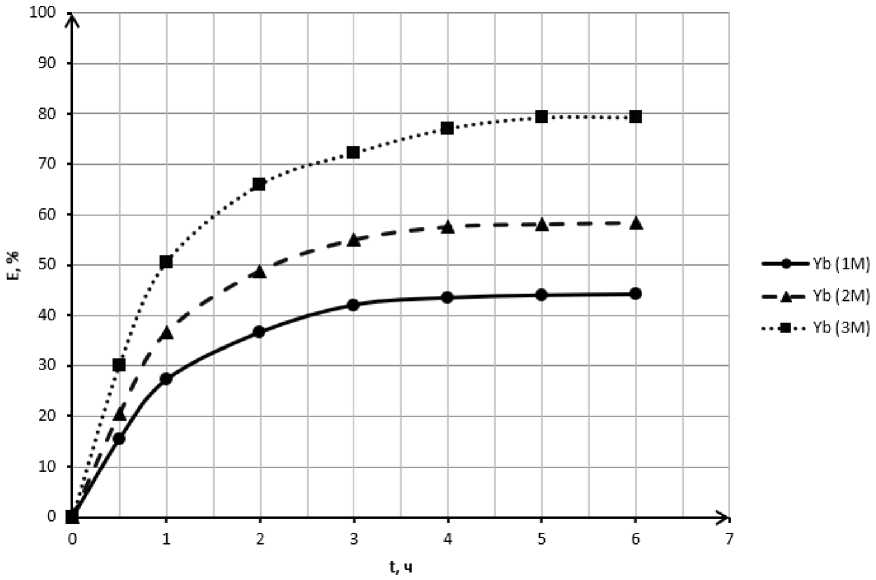
Рис. 4. Влияние концентрации карбонат-иона на растворимость YbPO 4 Fig. 4. An influence of carbonate-ion concentration on YbPO 4 dissolution
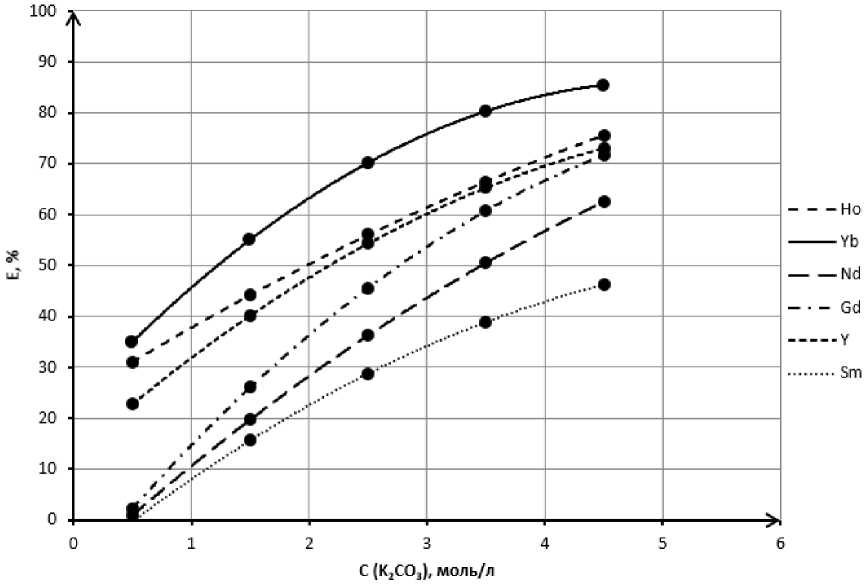
Рис. 5. Изотермы растворимости REE PO 4 в карбонатно-щелочной среде
Fig. 5. Isotherms of REE PO 4 dissolution in carbonate-alkaline media
Степень извлечения некоторых редкоземельных металлов в раствор при различной концентрации карбоната калия
Degree of extraction of some rare earth metals into solution at different potassium carbonate concentrations
1-я стадия:
2 REE PO 4 + 3CO 3 2 - → REE 2 (CO 3 ) 3 + 2PO 3 4 - ; (7) 2-я стадия:
REE 2 (CO 3 ) 3 + CO 3 2 - → 2 REE (CO 3 ) 2 - ; (8)
Σ :
REE PO 4 + 2CO 3 2 - → REE (CO 3 ) 2 - + PO 3 4 - . (9)
Отрицательное значение стандартной энергии Гиббса процесса комплексообразования РЗМ указывает на возможность протекания процесса, однако растворение при стандартных условиях на протяжении длительного времени (более суток) не приводит к переходу РЗМ в жидкую фазу, что свидетельствует о том, что скорость процесса низка при данных условиях. Таким образом, вести процесс следует при повышенной температуре.
Установлено влияние межфазного отношения, которое также указывает на протекание процесса с низкой скоростью при стехиометрических соотношениях. Такое влияние может свидетельствовать о том, что процесс комплексообразования – последовательный процесс перехода фосфата в карбонат, а карбоната – в комплекс.
Выводы
Растворение осадков РЗМ в среде карбо-нат-иона технически осуществимо, причем в случае попутного извлечения редких земель из фосфогипса возможно достичь равновесной концентрации рассмотренных металлов в растворе, поскольку время конверсии фосфогипса по ранее разработанной технологии совпадает с равновесным временем, при котором были экспериментально получены изотермы.
С учетом результатов, опубликованных ранее, метод растворения осадков РЗМ в среде карбонат-иона является универсальным, поскольку позволяет перевести РЗМ в жидкую фазу из осадков, образованных различными анионами: сульфатами, карбонатами, фосфатами.
Применительно к технологии жидкостной карбонатно-щелочной конверсии фосфогипса представляется целесообразным ведение процесса конверсии при тех же параметрах, что и ранее разработанных, за исключением межфазного отношения (его необходимо увеличить).
Дальнейшее выделение РЗМ из щелока возможно осуществить за счет разрушения карбонатных комплексов с образованием вторичных осадков РЗМ, однако в литературе описана трудность разделения смеси РЗМ на отдельные элементы, которая вызвана малым различием в ионном радиусе атома (различия в радиусе атомов соседних элементов составляют всего лишь 0,01–0,03 Å) [12]. Таким образом, их разделение методом осаждения является перспективной и сложной задачей.
Список литературы Растворимость фосфатов редкоземельных металлов в карбонатно-щелочных системах
- Chernysh Y., Yakhnenko O., Chubur V., Roubík H. Phosphogypsum Recycling: A Review of Environmental Issues, Current Trends, and Prospects. Appl. Sci. 2021;11:1575. DOI: 10.3390/app11041575
- Gschneidner K.A., Jr. The Rare Earth Crisis – The Supply/Demand Situation for 2010–2015. Mater. Matters. 2011;6:32–37.
- Cheremisina O., Sergeev V., Ponomareva M., Ilina A., Fedorov A. Kinetics Study of Solvent and Solid-Phase Extraction of Rare Earth Metals with Di-2-Ethylhexylphosphoric Acid. Metals. 2020;10:687. DOI: 10.3390/met10050687
- Sergeev I.B., Ponomarenko T.V. Incentives for creation the competitive rare-earth industry in Russia in the context of global market competition. Journal of Mining Institute. 2015;211:104.
- Cheremisina O., Sergeev V., Fedorov A., Alferova D. Concentration and Separation of Heavy Rare-Earth Metals at Stripping Stage. Metals. 2019;9:1317. DOI: 10.3390/met9121317
- Husein Malkawi D.A., Husein Malkawi A.I., Bani-Hani K.A. Slope Stability Analysis for the Phosphogypsum Stockpiles: A Case Study for the Sustainable Management of the Phosphogypsum Stacks in Aqaba Jordan. Sustainability. 2022;14(23):15763. DOI: 10.3390/su142315763
- Bingqi W., Lin Y., Tong L., Jianxin C. Study on the Kinetics of Hydration Transformation from Hemihydrate Phosphogypsum to Dihydrate Phosphogypsum in Simulated Wet Process Phosphoric Acid. ACS Omega. 2021;6(11):7342–7350. DOI: 10.1021/acsomega.0c05432
- Cheremisina O., Ponomareva M., Sergeev V., Mashukova Y., Balandinsky D. Extraction of Rare Earth Metals by Solid-Phase Extractants from Phosphoric Acid Solution. Metals. 2021;11:991. DOI: 10.3390/met11060991
- Li P., Zhang X., Zhong M., Fan Z., Xiong J., Zhang Z. Phosphogypsum-Based Ultra-Low Basicity Cementing Material. Materials. 2022;15:6601. DOI: 10.3390/ma15196601
- Kim P., Anderko A., Navrotsky A., Riman R.E. Trends in Structure and Thermodynamic Properties of Normal Rare Earth Carbonates and Rare Earth Hydroxycarbonates. Minerals. 2018;8:106. DOI: 10.3390/min8030106
- Kurkinen S., Sami Virolainen S., Sainio T. Recovery of rare earth elements from phosphogypsum waste in resin-in-leach process by eluting with biodegradable complexing agents. Hydrometallurgy. 2021;201:105569. DOI: 10.1016/j.hydromet.2021.105569
- Pathapati S.V.S.H., Free M.L., Sarswat P.K. A Comparative Study on Recent Developments for Individual Rare Earth Elements Separation. Processes. 2023;11:2070. DOI: 10.3390/pr11072070
- Salavati-Niasari M., Javidi J., Davar F. Sonochemical synthesis of Dy2(CO3)3 nanoparticles, Dy(OH)3 nanotubes and their conversion to Dy2O3 nanoparticles. Ultrason. Sonochem. 2010;17:870–877. DOI: 10.1016/j.ultsonch.2010.02.013
- Kaczorowska M.A. The Latest Achievements of Liquid Membranes for Rare Earth Elements Recovery from Aqueous Solutions – A Mini Review. Membranes. 2023;13:839. DOI: 10.3390/membranes13100839
- Mukaba J.-L., Eze C.P., Pereao O., Petrik L.F. Rare Earths’ Recovery from Phosphogypsum: An Overview on Direct and Indirect Leaching Techniques. Minerals. 2021;11:1051. DOI: 10.3390/min11101051
- Cheremisina O.V., Sergeev V., Fedorov A.T., Alferova D.A. Separation of rare-earth metals and titanium in complex apatite concentrate processing. Obogashchenie Rud. 2020;5:30–34. DOI: 10.17580/or.2020.05.05
- Pyagai I., Zubkova O., Babykin R., Toropchina M., Fediuk R. Influence of Impurities on the Process of Obtaining Calcium Carbonate during the Processing of Phosphogypsum. Materials. 2022;15:4335. DOI: 10.3390/ma15124335
- Okrugin A., Zhuravlev A. Mineralogical and Geochemical Evidence of Paragenetic Unity of Igneous Silicate and Carbonatite Rocks of the Tomtor Massif in the North-East of the Siberian Platform. Minerals. 2023;13:211. DOI: 10.3390/min13020211
- Daminescu D., Duteanu N., Ciopec M., Negrea A., Negrea P., Nemeş N.S., Pascu B., Lazău R., Berbecea A. Kinetic Modelling the Solid–Liquid Extraction Process of Scandium from Red Mud: Influence of Acid Composition, Contact Time and Temperature. Materials. 2023;16:6998. DOI: 10.3390/ma16216998
- Guan Q., Sui Y., Liu C., Wang Y., Zeng C., Yu W., Gao Z., Zang Z., Chi R.-a. Characterization and Leaching Kinetics of Rare Earth Elements from Phosphogypsum in Hydrochloric Acid. Minerals. 2022;12:703. DOI: 10.3390/min12060703
- Zeng Cx., Guan Qj., Sui Y. Kinetics of nitric acid leaching of low-grade rare earth elements from phosphogypsum. J. Cent. South Univ. 2022;29(6):1869–1880. DOI: 10.1007/s11771-022-5049-y
- Li X., Lv X., Xiang L. Review of the State of Impurity Occurrences and Impurity Removal Technology in Phosphogypsum. Materials. 2023;16:5630. DOI: 10.3390/ma16165630
- Balaram V. Potential Future Alternative Resources for Rare Earth Elements: Opportunities and Challenges. Minerals. 2023;13:425. DOI: 10.3390/min13030425
- Lv X., Xiang L. The Generation Process, Impurity Removal and High-Value Utilization of Phosphogypsum Material. Nanomaterials. 2022;12:3021. DOI: 10.3390/nano12173021
- Millero F., Schreiber D. Use of the ion pairing model to estimate activity coefficients of the ionic components of natural waters. American Journal of Science. 1982;282:1508–1540. DOI: 10.2475/ajs.282.9.1508
- Lee J.H., Robert H.B. Examination of comparative rare earth element complexation behavior using linear free-energy relationships. Geochimica et Cosmochimica Acta. 1992;56:1127–1137. DOI: 10.1016/0016-7037(92)90050-S
- Liu X., Byrne R.H. Comprehensive Investigation of Yttrium and Rare Earth Element Complexation by Carbonate Ions Using ICP–Mass Spectrometry. Journal of Solution Chemistry. 1998;27:803–815. DOI: 10.1023/A:1022677119835
- Luo Y.R., Byrne R.H. The Ionic Strength Dependence of Rare Earth and Yttrium Fluoride Complexation at 25°C. Journal of Solution Chemistry. 2000;29:1089–1099. DOI: 10.1023/A: 1005186932126
- Ohta A., Kawabe I. Rare earth element partitioning between Fe oxyhydroxide precipitates and aqueous NaCl solutions doped with NaHCO3: Determinations of rare earth element complexation constants with carbonate ions. Geochemical journal. 2000;34:439–454. DOI: 10.2343/geochemj.34.439
- Rao R., Chatt A. Studies on Stability Constants of Europium(III) Carbonate Complexes and Application of SIT and Ion-Pairing Models. Radiochimica Acta. 1991;54(4):181–188. DOI: 10.1524/ract.1991.54.4.181
- Devine C.D. The stability constants of some carboxylate complexes of the trivalent lanthanons; 1969. DOI: 10.2172/4619812
- Han K. Characteristics of Precipitation of Rare Earth Elements with Various Precipitants. Minerals. 2020;10:178. DOI: 10.3390/min10020178
- Jowitt S.M. Mineral economics of the rare-earth elements. MRS Bulletin. 2022;47:276–282. DOI: 10.1557/s43577-022-00289-3
- Kang C.-U., Ji S.-W., Jo H. Recycling of Industrial Waste Gypsum Using Mineral Carbonation. Sustainability. 2022;14:4436. DOI: 10.3390/su14084436
- Chirkst D.E., Cheremisina O.V. Solubility of cerium (III) phosphate at different temperatures and concentrations of ortho-phosphoric acid. Journal of Mining Institute. 2006;169(4):227–230.


