Растворимость в системах вода - оксиэтилированный нонилфенол - (NH4)2SO4
Автор: Станкова Анастасия Вадимовна, Елохов Александр Михайлович, Катаева Дарья Андреевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 3 т.10, 2018 года.
Бесплатный доступ
В работе описано применение системного подхода к оптимизации температурно-концентрационных параметров экстракции в системах вода - поверхностно-активное вещество - неорганический высаливатель, основанного на анализе политермической фазовой диаграммы соответствующей тройной системы. Визуально-политермическим методом и изотермическим методом сечений изучена растворимость в системах вода - неонол АФ-9-12 (или неонол АФ-9-25) - сульфат аммония в интервале температур 25-80 °С, где неонол АФ-9-12 (неонол АФ-9-25) - оксиэтилированные нонилфенолы со степенью оксиэтилирования 12 и 25 соответственно. Установлено, что область расслаивания увеличивается с ростом температуры вследствие увеличения высаливающей способности сульфата аммония и снижения гидратации мицелл ПАВ. Максимальные различия в концентрационных границах области расслаивания наблюдаются при температуре выше 40 °С, в расслаивающихся смесях, содержащих неонол АФ-9-25, концентрация воды ниже, чем для системы с неонолом АФ-9-12 при той же температуре вследствие большей степени гидратации неонола АФ-9-25. Также для системы с неонолом АФ-9-12 увеличение температуры выше 84 °С приводит к образованию расслаивания в двойной системе вода - неонол АФ-9-12 и высаливанию указанной гетерогенной подсистемы. Показано, что на температурно-концентрационные границы области расслаивания также влияет степень оксиэтилирования ПАВ, рост которой сопровождается увеличением гидратации мицелл ПАВ и снижением их способности к высаливанию при фиксированной температуре. На основании диаграмм растворимости установлены оптимальные параметры экстракции в системе вода - неонол АФ-9-12 - сульфат аммония при 25 и 60 °С и показано, что рост температуры приводит к уменьшению объема экстракта и увеличению интервала кислотности, при котором существует расслаивание вследствие увеличения высаливающей способности соли и введения дополнительного количества анионов - высаливателей с кислотой. Полученные данные обуславливают перспективность использования изученных систем в экстракции при температуре выше комнатной.
Поверхностно-активные вещества, расслаивающиеся системы, мицеллярная экстракция, высаливание
Короткий адрес: https://sciup.org/147233100
IDR: 147233100 | УДК: 544.344 | DOI: 10.14529/chem180304
Solubility in the water - oxyethylated nonylphenol - (NH4)2SO4 systems
The paper describes system approach application to optimization of temperature-concentration extraction parameters in water - surfactant - inorganic salting-out agent systems, based on analysis of the polythermic phase diagram of the corresponding ternary system. Solubility in water - Neonol AF-9-12 (or Neonol AF-9-25) - ammonium sulfate systems has been studied in the range 25-80 °C by visual polythermal and isothermal section methods, where Neonol AF-9-12 and Neonol AF-9-25 are oxyethylated nonylphenols with oxyethylation degree of 12 and 25, respectively. It has been established that the delamination region increases when temperature grows, because of increasing salting-out ability of ammonium sulfate and decreasing hydration of surfactant micelles. The maximum differences in delamination region concentration boundaries have been observed at temperatures above 40 °C. In the delaminating mixtures containing Neonol AF-9-25, the water concentration is lower than that for the system with Neonol AF-9-12 at the same temperature, due to greater hydration degree of Neonol AF-9-25. Besides, for the system with Neonol AF-9-12 increase in temperature above 84 °C leads to formation of delamination in water - Neonol AF-9-12 binary system and salting-out of this heterogeneous subsystem. It has been shown that temperature-concentration delamination region boundaries are affected by surfactant oxyethylation degree, the growth of which is accompanied by increase in hydration of surfactant micelles and decrease in their salting-out ability at fixed temperature. On the basis of solubility diagrams, the optimal extraction parameters in the water - Neonol AF-9-12 - ammonium sulfate system at 25 and 60 °C have been established, and it has been shown that temperature increase leads to decreasing extract volume and widening of acidity interval at which separation is observed, due to increasing salting-out ability of the salt and additional number of anions - salting-out agents with an acid. This determines the use of the studied systems for extraction at higher than room temperature.
Текст научной статьи Растворимость в системах вода - оксиэтилированный нонилфенол - (NH4)2SO4
Водорастворимые полимеры и оксиэтилированные поверхностно-активные вещества находят широкое применение при экстракции биологически активных веществ [1–3], антибиотиков [4–6], органических и неорганических загрязнителей окружающей среды [7–9].
Для получения расслаивающихся систем на основе водорастворимых полимеров используют поливинилпирролидон [10], триблоксополимеры оксида этилена и оксида пропилена [11], поли-пропиленгликоль [12] или полиэтиленгликоли с различной молекулярной массой [13–15]. В качестве высаливателей применяют преимущественно сульфаты и фосфаты щелочных металлов, аммония и магния. Способность к высаливанию полиэтиленгликолей при неизменной температуре и одном высаливателе возрастает с уменьшением молекулярной массы ПЭГ, что связано с повышением гидрофобности молекул полимера.
Среди неионных ПАВ наиболее изученными являются синтамиды (полиэтиленгликолевые эфиры моноэтаноламидов синтетических жирных кислот, CnH2n+1CONHCH2CH2O(C2H4O)mH, m = 5–6, где n=10–16 для синтамида-5 и n = 7–17 для синтамида-5к) [16, 17] и синтанолы – моноалкиловые эфиры полиэтиленгликоля (CnH2n-1O(C2H4O)mH, m = 8–10, где n = 12–14 для син-танола АЛМ-10 и n = 10–18 для синтанола ДС-10) [18]. Синтамиды способны эффективно вы- саливаться многими солями, образуя области расслаивания, располагающиеся достаточно близко к вершине воды (табл. 2) [17]. Область расслаивания в системах с синтанолами находится по воде ниже, чем для систем, содержащих синтамиды. Кроме того, при концентрации ПАВ более 40 % происходит образование вязких неподвижных гелей [18]. Другими примерами неионных ПАВ являются ОП-10 – оксиэтилированные алкилфенолы (CnH2n+1C6H4O(C2H4O)mH, где n = 8–10, m = 10–12) [19] и Triton X – оксиэтилированные октилфенолы (C8H17C6H4O(C2H4O)n) [20], системы на основе которых применяются для экстракции ионов металлов в присутствии органических комплексообразователей.
Так как основной гидрофильной группой, обуславливающей растворимость оксиэтилиро-ванных ПАВ в воде, является полиоксиэтиленовый фрагмент, то действие солей на них аналогично явлениям, наблюдающимся в растворах ПЭГ. Косвенно оценку способности высаливания ПАВ близкой структуры можно произвести на основании величины гидрофильнолипофильного баланса или температуры помутнения их водных растворов. Согласно справочным данным [21], температура помутнения 1%-ного раствора синтамида-5 равна 45±2 ºС, в то время как для синтанолов она существенно выше, что подтверждается данными по высаливанию этих ПАВ сульфатом аммония.
Оксиэтилированные нонилфенолы (неонолы) не получили широкого распространения в экстракции, в связи с чем представляло исследовать возможность разработки экстракционных систем на основе неонолов с различной степенью оксиэтилирования. Ранее изучена высаливающая способность неорганических солей по отношению к неонолам АФ-9-12 и АФ-9-25 [22] и установлено, что расслаивание наблюдается в системах с сульфатами аммония, алюминия, магния, натрия, с карбонатом, фторидом и нитратом аммония. В качестве высаливателя рекомендован сульфат аммония вследствие его высокой растворимости и высаливающей способности аниона.
Объекты и методы исследования
В работе использованы неионные ПАВ – оксиэтилированные нонилфенолы (C 9 H 19 C 6 H 4 O(C 2 H 4 O) n H, где n = 12 для неонола АФ-9-12 и n =25 для неонола АФ-9-25, ТУ 2483-077-05766801-98), сульфат аммония квалификации ч.д.а, дистиллированная вода.
Растворимость в системе вода – неонол АФ-9-12 (АФ-9-25) – сульфат аммония изучена изотермическим методом сечений [23] и визуально-политермическим методом [24]. Изотермический метод сечений основан на определении показателя преломления жидкой фазы смесей, находящихся в некотором сечении треугольника состава. Концентрационные параметры фазовых переходов определяли по изломам кривых на графике зависимости показателя преломления от концентрации одного из компонентов системы. Показатель преломления измеряли на рефрактометре ИРФ-454Б2М с точностью 0,0005. Погрешность определения растворимости равна 0,5 %.
Визуально-политермический метод заключается в фиксировании температуры помутнения смесей-навесок, соответствующих определенным сечениям треугольника состава, при нагревании с заданной скоростью 1 ° С/5 мин и периодическом встряхивании. Температуру помутнения устанавливали по появлению устойчивой опалесценции. Точность измерений составила ±1 °С.
Изучение влияния неорганических кислот на устойчивость расслаивания проводили в градуированных пробирках с притертыми пробками. Для этого в пробирку вносили 4 мл ПАВ с концентрацией 250 г/л, 3,0 г сульфата аммония, расчетный объем серной или хлороводородной кислоты с концентрацией 5 моль/л. Общий объем смеси доводили дистиллированной водой до 20 мл и встряхивали в течение трех минут. После установления равновесия определяли относительный объем фазы ПАВ (V отн ) как отношение объема фазы ПАВ к общему объему системы.
Влияние кислот на расслаивание при 60 °С проводили аналогично, подготовленные пробирки термостатировали в течение 15–20 минут, после чего охлаждали до комнатной температуры и фиксировали относительный объем фазы ПАВ (V отн ).
Результаты и их обсуждение
Изотермическим методом сечений изучена растворимость в системах вода – неонол АФ-9-12 (АФ-9-25) - сульфат аммония при 25 ° С.
Установлено, что неонолы неограниченно растворяются в воде, образуя при этом вязкие гомогенные смеси, а сульфат аммония в ПАВ практически не растворяется. Область вблизи вершины ПАВ подробно не изучалась ввиду высокой вязкости растворов и длительного установления равновесия.
Полученные диаграммы растворимости (рис. 1) имеют одинаковую топологию, обнаружены следующие области: гомогенная (L), расслаивания (L 1 +L 2 ), монотектического равновесия (L 1 +L 2 +S), кристаллизации сульфата аммония (L+S). Области расслаиваниях в обеих системах располагаются достаточно близко к вершине воды и смещены к стороне сульфат аммония – вода. Области кристаллизации соли незначительны. Критические точки, определенные по правилу Алексеева, отмечены на диаграммах серым цветом.
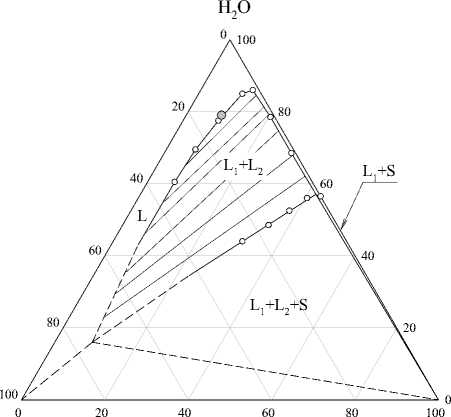
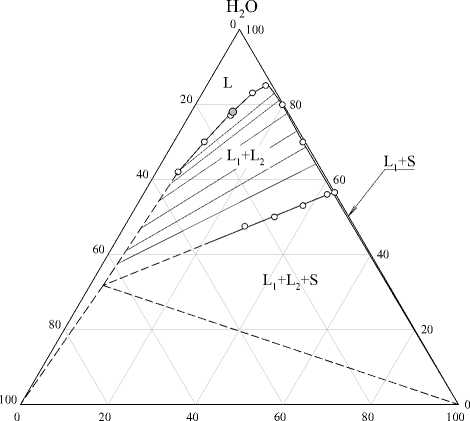
Неонол АФ-9-12 (NH4)2SO4 Неонол АФ-9-25 (NH4)2SO4 а) б)
Рис. 1. Диаграммы растворимости систем вода – неонол АФ-9-12 – сульфат аммония (а) и вода – неонол АФ-9-25 – сульфат аммония (б) при 25 °С [22]
Обращает на себя внимание факт различного положения предельной ноды монотектического равновесия для двух систем. Содержание воды в фазе ПАВ в области монотектического равновесия для системы с неонолом АФ-9-25 существенно больше, чем аналогичная величина для неонола АФ-9-12, что может быть связано с различной степенью гидратации мицелл ПАВ. Неонол АФ-9-25, вследствие большей степени оксиэтилирования, гидратируется сильнее, чем неонол АФ-9-12, что сопровождается переносом большего количества воды в фазу ПАВ.
Известно, что повышение температуры осуществления процесса экстракции позволяет увеличить концентрацию воды в экстракционной системе, при этом наблюдается уменьшение относительного объема фазы ПАВ и времени установления равновесия [25]. Представляло интерес определить влияние температуры на область расслаивания в изученных системах.
На рис. 2 представлены границы области расслаивания в системах вода – неонол АФ-9-12 (неонол АФ-9-25) – сульфат аммония в интервале температур 25–80 ºС. Установлено, что с ростом температуры область расслаивания приближается к вершине воды и двойной подсистеме ПАВ - вода, то есть наблюдается ее расширение. При этом имеются различия в температурноконцентрационных параметрах границ области расслаивания между неонолами АФ-9-12 и АФ-9-25. При температурах близких к комнатной (до 40 °С) концентрационные границы области расслаивания практически идентичны для обеих систем, что обусловлено высокой высаливающей способностью сульфат-иона, который в свою очередь нивелирует различие в способности к высаливанию для обоих ПАВ [23]. Последующее увеличение температуры приводит к дифференцированию неонолов по способности к высаливанию. В системе с неонолом АФ-9-12 область расслаивания расширяется и при достижении температуры 84 °С, отвечающей нижней критической температуре растворения (НКТР) в системе неонол АФ-9-12 – вода, область рас- слаивания касается двойной подсистемы ПАВ – вода. В случае системы с неонолом АФ-9-25 увеличение температуры выше 40 °С не приводит к существенным изменениям в расширении гр
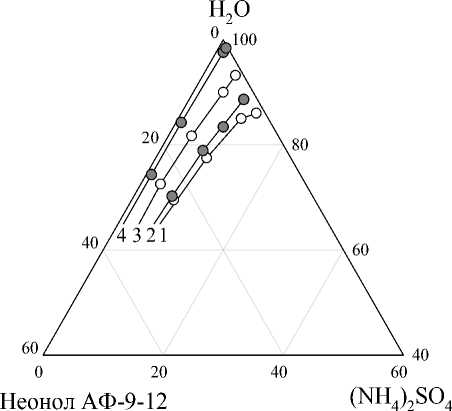
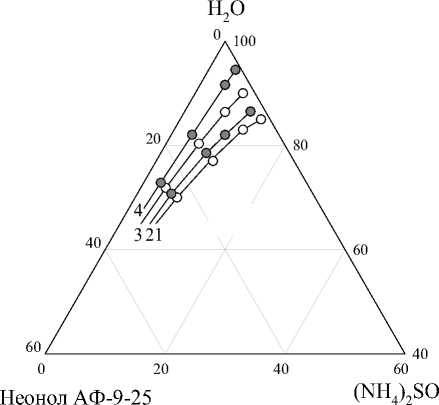
-
а) б)
Рис. 2. Граница области расслаивания в системах вода – неонол АФ-9-12 – сульфат аммония (а) и вода – неонол АФ-9-25 – вода (б) при различных температурах (°С): 1 – 25; 2 – 40; 3 – 60; 4 – 80
Наблюдаемые закономерности связаны с увеличением высаливающей способности соли и одновременным снижением степени гидратации мицелл ПАВ с ростом температуры. Температурная дегидратация мицелл ПАВ и их последующая их агрегация зависит от степени гидрофильности молекул ПАВ, которую можно оценить величиной гидрофильно-липофильного баланса (ГЛБ) или НКТР системы ПАВ – вода. Вычисленные значения ГЛБ по Девису [22] и НКТР двойных систем ПАВ – вода представлены в табл. 1. Неонол АФ-9-25 даже при температурах выше 60 °С гидратирован в большей степени чем неонол АФ-9-12, поэтому его способность к высаливанию несколько ниже, чем у неонола АФ-9-12.
Таблица 1
Основные характеристики, определяющие способность к высаливанию неонолов
|
ПАВ |
ГЛБ |
НКТР, °С |
|
Неонол АФ-9-12 |
6.93 |
84 |
|
Неонол АФ-9-25 |
11.22 |
> 100 |
Оптимальные параметры проведения экстракции в системе вода – неонол АФ-9-12 – сульфат аммония при 25 ° С определены ранее [22]. Представляло интерес установить влияние температуры основные характеристики расслаивания при неизменных концентрационных параметрах системы (табл. 2).
Таблица 2
Параметры экстракции в системах вода – неонол АФ-9-12 – сульфат аммония
|
Концентрация компонентов, мас. % |
(NH 4 ) 2 SO 4 |
15,0 |
|
|
ПАВ |
5,0 |
||
|
Вода |
80,0 |
||
|
Температура, °С |
25 |
60 |
|
|
V отн |
0,10 |
0,07 |
|
|
Сmax, моль/л |
HCl |
< 0,6 |
< 1,5 |
|
H 2 SO 4 |
< 0,8 |
< 2,0 |
|
*Сmax – максимальная концентрация, при которой существует расслаивание.
Увеличение температуры приводит к уменьшению относительного объема экстракта ввиду роста высаливающей способности сульфата аммония. Другим положительным моментом является расширение интервала кислотности при 60 °С. При введении кислот происходит частичное протонирование оксиэтиленовых фрагментов молекул ПАВ, вследствие чего снижается их способность к высаливанию, что в итоге приводит к гомогенизации системы. Рост температуры сопровождается увеличением высаливающей способности сульфата аммония, поэтому гомогенизация происходит при большем содержании кислот в смеси. Следует отметить, что при введении серной кислоты интервал существования расслаивания больше, чем при введении хлороводородной кислоты, так как высаливающее действие сульфат-иона выше, чем хлорид-иона.
Выводы
Таким образом, полученные данные по растворимости в системах вода – оксиэтилированный нонилфенол – сульфат аммония при различных температурах позволили оценить влияние степени оксиэтилирования ПАВ и температуры на особенности расслаивания в системе и оптимизировать параметры проведения жидкостной экстракции при температуре 25 и 60 °С.
Список литературы Растворимость в системах вода - оксиэтилированный нонилфенол - (NH4)2SO4
- Saitoh, T. Use of surfactant-mediated phase separation (cloud point extraction) with affinity ligands for the extraction of hydrophilic proteins / T. Saitoh, W.L. Hinze // Talanta. - 1995. - V. 42. - № 1. - P. 119-127. DOI: 10.1016/0039-9140(94)00227-J
- Akita, S. Cloud-point extraction of organic compounds from aqueous solutions with nonionic surfactant / S. Akita, H. Takeuchi // Separation Science and Technology. - 1995. - V. 30, № 5. - P. 833-846. DOI: 10.1080/01496399508013895
- Cloud point extraction applied to casein proteins of cow milk and their identification by mass spectrometry / A.S. Lopes, J.S. Garcia, R.R. Catharino, et al. // Analytica chimica acta. - 2007. - V. 590, № 2. - P. 166-172. DOI: 10.1016/j.aca.2007.03.043
- Madej, K. Microwave-assisted and cloud-point extraction in determination of drugs and other bioactive compounds / K. Madej // TrAC Trends in Analytical Chemistry. - 2009. - V. 28, № 4. - P. 436-446. DOI: 10.1016/j.trac.2009.02.002
- Use of aqueous two-phase systems for in situ extraction of water soluble antibiotics during their synthesis by enzymes immobilized on porous supports / O. Hernandez-Justiz, R. Fernandez-Lafuente, M. Terreni et al. // Biotechnology and bioengineering. 1998. - V. 59, № 1. - P. 73-79.
- Liquid-liquid extraction by mixed micellar systems: a new approach for clavulanic acid recovery from fermented broth / V.C. Santos, F.A. Hasmann, A. Converti et al. // Biochemical Engineering Journal. - 2011. - V. 56, № 1-2. - P. 75-83.
- DOI: 10.1016/j.bej.2011.05.011
- Altunay, N. A New Micellar Mediated Cloud-Point Extraction Procedure for Sensitive and Selective Determination of Trace Amounts of Total Iodine in Milk-Based Nutritional Products by Means of Indirect Spectrophotometry / N. Altunay, R. Gürkan // Food Analytical Methods. - 2016. - V. 9, № 2. - P. 505-518.
- DOI: 10.1007/s12161-015-0220-9
- El-Hay, S.S.A. Determination of thorium (IV) in real samples by spectrophotometry after micelle-mediated cloud point extraction / S.S.A. El-Hay, A.A. Gouda // Journal of Radioanalytical and Nuclear Chemistry. - 2016. - V. 310, № 1. - P. 191-200.
- DOI: 10.1007/s10967-016-4780-y
- Removal of crystal violet dye from aqueous solution using triton X-114 surfactant via cloud point extraction / A. Appusamy, I. John, K. Ponnusamy et al. // Engineering Science and Technology, an International Journal. - 2014. - V. 17, № 3. - P. 137-144.
- DOI: 10.1016/j.jestch.2014.04.008
- Extraction and preconcentration of anthocyan dye from aqueous solutions with water-soluble poly-N-vinylamides / E.V. Churilina, G.V. Shatalov, Y.I. Korenman, et al. // Russian Journal of Applied Chemistry. - 2008. - V. 81, № 4. - P. 726-729.
- DOI: 10.1134/S1070427208040320
- Liquid-liquid equilibrium phase diagrams of new aqueous two-phase systems: Ucon 50-HB5100 ammonium sulfate water, Ucon 50-HB5100 poly(vinyl alcohol) water, Ucon 50-HB5100 hydroxypropyl starch water, and poly(ethylene glycol) 8000 poly(vinyl alcohol) water / M. Pereira, Y.T. Wu, P. Madeira et al. // Journal of Chemical Engineering Data. - 2004. - V. 49, № 1. - P. 43-47.
- DOI: 10.1021/je034038d
- Zhao, X. Liquid-liquid equilibrium of aqueous two-phase systems containing poly (propylene glycol) and salt ((NH4)2SO4, MgSO4, KCl, KAc): experiment and correlation / X. Zhao, X. Xie, Y. Yan // Thermochimica Acta. - 2011. - V. 516, № 1. - P. 46-51.
- DOI: 10.1016/j.tca.2011.01.010
- Extraction of complexes of lanthanides and actinides with Arsenazo III in an ammonium sulfate-poly (ethylene glycol)-water two-phase system / V. Shkinev, N. Molochnikova, T. Zvarova et al. // Journal of Radioanalytical and Nuclear Chemistry. - 1985. - V. 88, № 1. - P. 115-120.
- Snyder, S.M. Phase compositions, viscosities, and densities for aqueous two-phase systems composed of polyethylene glycol and various salts at 25ºC / S.M. Snyder, K.D. Cole, D.C. Szlag // Journal of Chemical and Engineering Data. - 1992. - V.37, № 2. - P.268-274.
- Liquid-liquid extraction in the absence of usual organic solvents: application of two-phase aqueous systems based on a water-soluble polymer / T.I. Zvarova, V.M. Shkinev, G.A. Vorob'eva et al. // Microchimica Acta. - 1984. - V. 84, № 5-6. - P. 449-458.
- Phase and extraction equilibria in water - syntamide-5 - ammonium sulfate and water - syntamide-5k - ammonium sulfate systems / A.V. Golovkina, A.E. Lesnov, O.S. Kudryashova et al. // Russian Journal of Physical Chemistry A. - 2013. - V. 87, № 9. - P. 1502-1505.
- DOI: 10.1134/S0036024413080128
- Двухфазные водные системы на основе полиэтиленгликолевых эфиров моноэтаноламидов синтетических жирных кислот и неорганических высаливателей / А.Е. Леснов, А.В. Головкина, О.С. Кудряшова, и др. // Химия в интересах устойчивого развития. - 2016. - Т. 24, № 1. - С. 29-33.
- Phase equilibria in the water - alkali metal or ammonium sulfate - synthanol systems / O.S. Kudryashova, S.A. Denisova, M.A. Popova, et al. // Russian Journal of Inorganic Chemistry. - 2013. - V. 58, № 2. - P. 246-249.
- DOI: 10.1134/S0036023612120121
- Шестопалова, Н.Б. Влияние солей натрия на фазовое разделение в системе «(ОП-10)-Н2О» / Н.Б. Шестопалова, Р.К. Чернова // Вестник Тамбовского государственного технического университета. - 2014. - Т. 20, № 2. - С. 322-328.
- Salabat, A. Liquid-liquid equilibria of aqueous two-phase systems composed of TritonX-100 and sodium citrate or magnesium sulfate salts / A. Salabat, S.T. Moghadam, M.R. Far // Calphad: Computer Coupling of Phase Diagrams and Thermochemistry. - 2010. - V. 34, № 1. - P. 81-83.
- DOI: 10.1016/j.calphad.2009.12.004
- Абрамзон, А.А. Поверхностно-активные вещества. Справочник / А.А. Абрамзон, В.В. Бочаров, Г.М. Гаев. - Л.: Химия, 1979. - 376 с.
- Specific Features of the Salting-out of Oxyethylated Nonylphenols Using Inorganic Salts at 25 °С / A.V. Stankova, A.M. Elokhov, S.A. Denisova., O.S. Kudryashova, et al. // Russian Journal of Physical Chemistry A. - 2017. - V. 91, № 5. - P. 880-886.
- DOI: 10.1134/S0036024417050247
- Никурашина, Н.И. Метод сечений. Приложение к изучению многофазного состояния многокомпонентных систем. / Н.И. Никурашина, Р.В. Мерцлин. - Cаратов: Саратов. ун-т, 1969. - 122 с.
- Аносов, В.Я. Основы физико-химического анализа / В.Я. Аносов, М.И. Озерова, Ю.Я. Фиалков. - М.: Наука, 1976. - 504 с.
- Elokhov, A.M. Salting Out Of Potassium Bis(Alkylpolyoxyethylene)Phosphate With Ammonium Salts As The Base of Micellar Extraction Processes Development / A.M. Elokhov, A.E. Lesnov, O.S. Kydryashova // Russian Journal of General Chemistry. - 2015. - V. 85, № 11. - P. 2657-2662.
- DOI: 10.1134/S1070363215110250


