Равновесные параметры газовых смесей H2-H2O-CO-CO2-CH4 в отсутствии и присутствии углерода
Автор: Чернуха Александр Сергеевич, Кузнецов Юрий Серафимович, Качурина Ольга Ивановна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 4 т.16, 2016 года.
Бесплатный доступ
Внедоменное бескоксовое прямое получения железа (процесс «Мидрекс») осуществляется при 1000…1100 °C с использованием природного газа. Процессы конверсии основного компонента природного газа - метана: CH4 = C + 2H2, CH4 + CO2 = 2H2 + 2CO, CH4 + H2O = CO + 3H2 приводят к получению восстановительного газа и сажистого углерода при определенном соотношении молярных долей CO и CO2. Термодинамическая возможность протекания процессов восстановления оксида металла в сложной газовой смеси определяется соотношением кислородных потенциалов оксида и газовой атмосферы: (πo = RT ln pO2)оксид > (πo = RT ln pO2)газ. смесь. Кислородный потенциал газовой смеси количественно оценивается величиной равновесного давления кислорода, а кислородный потенциал оксида упругостью его диссоциации. Присутствие в рассматриваемой газовой фазе очень малого количества кислорода определяется реакциями диссоциации CO2 и H2O: lg[pO2, атм] = 2 lg(xH2O / xH2) - 25708 / T + 5,653; lg[pO2, атм] = 2 lg(xCO2 / xCO) - 29529 / T + 9,149. В работе определен кислородный потенциал газовых смесей H2-H2O-CO-CO2-CH4 в зависимости от их состава в интервале температур 800…1500 К. Полученные результаты позволяют оценить влияние присутствия метана на восстановительные свойства газовых смесей по отношению не только к оксидам железа.
Водяной газ, кислородный потенциал, метан, восстановление оксидов
Короткий адрес: https://sciup.org/147157062
IDR: 147157062 | УДК: 544.342-13 | DOI: 10.14529/met160401
Equilibrium parameters of gas mixtures H2-H2O-CO-CO2-CH4 in the absence and presence of carbon
Cokeless direct iron-making outside the blast furnace (the “Midrex” process of) is carried out at 1000-1100 °C using natural gas. Processes of conversion of natural gas component, methane, namely CH4 = C + 2H2, CH4 + CO2 = 2H2 + 2CO, CH4 + H2O = CO + 3H2 result in a reduction gas and sooty carbon at a certain ratio of mole fractions of CO and CO2. The thermodynamic possibility of reduction of the metal oxide in the complex gas mixture is determined by the ratio of the oxygen potential of the gas atmosphere and oxide: (πo = RT ln pO2)oxide > (πo = RT ln pO2)gas mixture. The reduction potential of the gas mixture is estimated by equilibrium pressure of oxygen, and the oxygen potential of the oxide is estimated by its dissociation tension. The presence of a very small amount of oxygen in the gas phase is determined by reactions of dissociation of CO2 and H2O: lg[pO2, atm] = 2 lg(xH2O / xH2) - 25708 / T + 5,653; lg[pO2, atm] = 2 lg(xCO2 / xCO) - 29529 / T + 9,149. The paper describes determination of oxygen potential of the gas mixtures H2-H2O-CO-CO2-CH4 depending on their composition in the temperature range of 800-1500 K. The obtained results allow to evaluate the effect of presence of methane in the gas mixtures on their reducing properties not only in relation to the iron oxides.
Текст научной статьи Равновесные параметры газовых смесей H2-H2O-CO-CO2-CH4 в отсутствии и присутствии углерода
В науке и технике важную роль играют различные диаграммы, позволяющие наглядно и компактно представить информацию по параметрам состояния различных систем и понять смысл и тенденции возможных процессов. Особое место диаграммам фазовых равновесий отводится при анализе металлургических процессов, а в ряде случаев они являются базой теоретических, лабораторных и промышленных исследований. Возможные параметры равновесного водяного газа H2–H2O–CO–CO2 давно и достаточно точно определены. Некоторые особенности в графической интерпретации параметров равновесного водяного газа и характеристик взаимодействия его с углеродом опубликованы в работах [1–4]. Однако в этих работах авторы придерживались общепринятого пред- положения – не учитывали возможность образования метана по реакциям:
2H 2 + 2CO = CH 4 + CO 2 ,
C + 2H 2 = CH 4 .
В силу повышенного интереса к твёрдофазному восстановлению металлов следует определить целесообразность учёта присутствия в газовой фазе метана.
Гомогенное равновесие
«водяной газ – метан»
Такая однофазная трехкомпонентная система (пять веществ минус две независимые реакции) при заданной температуре и постоянном давлении имеет по правилу фаз Гиббса две степени свободы. Для определения параметров газовой смеси H2–H2O–CO–CO2–CH4 необходимо рассчитать совместное равнове- сие двух независимых реакций (здесь и да- лее справочные величины ArGТ определяются в Дж):
H 2 + CO 2 = H 2 O + CO,
A rG°T (I) = 36 580 - 33,465 Т ; (I)
2H 2 + 2CO = CH 4 + CO 2 ,
A rG°T (II) = - 262 365 + 287,23 Т . (II)
Для этого решается система трех уравнений с четырьмя неизвестными:
x H 2 O x CO
KI = xH2 xCO2
K
II =
x CH 4 x CO 2
222 x H 2 x CO P
xh2 + x h2o + xco + xco2 + xch4 = 1 . (3) Важная особенность равновесной газовой смеси – при любой температуре возможно множество концентраций компонентов смеси, удовлетворяющих константам равновесия KI и KII [2–4]. По этой причине невозможно представлять графически составы равновесного водяного газа. Однако можно получить газо- вую смесь нужного состава, если задать ка- кой-либо исходный технологический пара- метр. Например, нагреванием смеси H2 и CO2
исходного состава
x H 2
I x CO 2 Асх
a 0 при кон- d 0
центрациях x CO = x Н2О = 0 [3] (или нагреванием смеси H 2 O и CO известного состава при исходных концентрациях x Н2 = x co2 = 0).
Рассмотрим решение системы уравнений (1)–(3) для случая нагревания смеси ( a 0 моль H 2 + d 0 моль CO 2 ) при P = 1 атм. При этом целесообразно оценить количества всех компонентов получающейся смеси:
|
H 2 |
+ CO 2 = |
H 2 O |
+ |
CO |
|
a 0 |
d 0 |
– |
– |
|
|
( a 0 – x – y ) |
( d 0 – x + y/ 2) |
x |
( x – y ) |
|
|
2H 2 |
+ 2CO = |
CH 4 |
+ |
CO 2 |
|
a 0 |
– |
– |
d 0 |
|
|
( a 0 – x – y ) |
( x – y ) |
y/ 2 |
( d 0 |
– x + y/ 2) |
Здесь в первой строке после уравнений реакций показаны количества веществ в начальном состоянии, во второй строке – в равновесном состоянии: x и y – расходы H2 и CO2 по реакциям (I) и (II), x – получено H2O и CO, y – расход CO, y/2 – получено CH4 и CO2. При нагревании исходной смеси (H2 + CO2) общее количество газов изменяется и в состоянии равновесия оно составляет
∑ = a 0 + d 0 – y . (4)
Вместо весьма сложного решения в общем виде системы уравнений (1)–(3) возможно такое численное решение. Из константы равновесия реакции (I) и условия нормировки с учетом принятых обозначений:
A = y, B = a0 -1, C = d0 -1, xxx
D = B - C + — , E = 2 BC - —
2 KI получаем уравнение для соотношения между величинами A = y/x и x
A = D ± VD2 + E .(5)
Из множества возможных сочетаний вычисленных величин y и заданных x следует найти такое, которое удовлетворяет константе равновесия реакции (II). Равновесные концентрации компонентов газовой смеси определяются соотношениями:
a x h2 = —
—
- x - y _ x _ x - y
2 , x h2o = ^ , x CO = ^ ,
_ d0 -x -0,5y _ 0,5y xCO2 = у , x CH4 = у
На рис. 1–3 показаны результаты вычисления концентраций H2 и CO в равновесных смесях H2–H2O–CO–CO2–CH4 в сравнении с равновесными параметрами водяного газа H2–H2O–CO–CO2, получающегося при нагревании тех же исходных смесей (H2 + CO2) без учета реакции образования метана (II). На рис. 4 показано влияние состава исходной смеси на суммарные концентрации газов-восстановителей и газов-окислителей.
Обнаруживается ожидаемый эффект – в интервале температур 1000…1500 К молярная доля метана не превышает ~ 10–3…10–7, лишь при температурах ниже ~ 950 К имеет смысл учитывать образование метана. Например, при нагревании исходной смеси (H2, a 0 моль – CO 2 , b 0 моль) до 800 К молярная доля метана при изменении соотношения a 0 / b 0 от 0 до 9 определяется кривой с максимумом 0,1669 при a 0 / b 0 = ~ 4, рис. 4). Это объясняется малой величиной константы равновесия реакции (II) при высоких температурах: 5,03·10–2 при 1000 К и 1,36·10–6 при 1500 К, тогда как при 800 К она равна 134,1 атм–2. Этим же объясняется практически незначимое при температурах выше ~ 950 К влияние метана
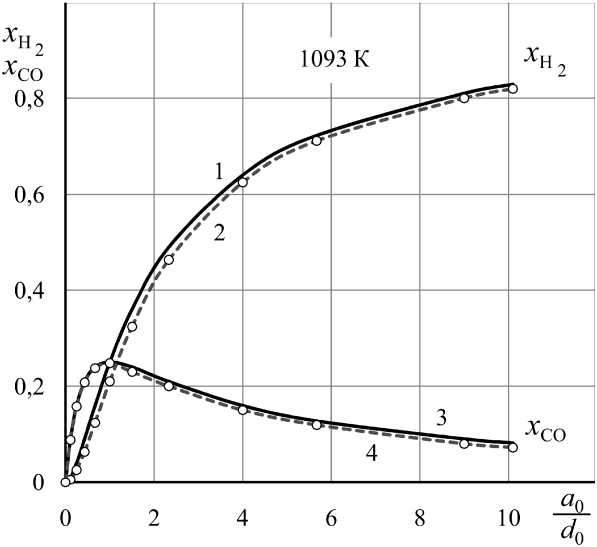
Рис. 1. Концентрации газов-восстановителей в газовых смесях, получающихся при нагревании (H 2 , a 0 – CO 2 , b 0 моль) до 1093 К: 1, 3 – водяной газ H 2 –H 2 O–CO–CO 2 [3]; 2, 4 – смесь H 2 –H 2 O–CO–CO 2 –CH 4
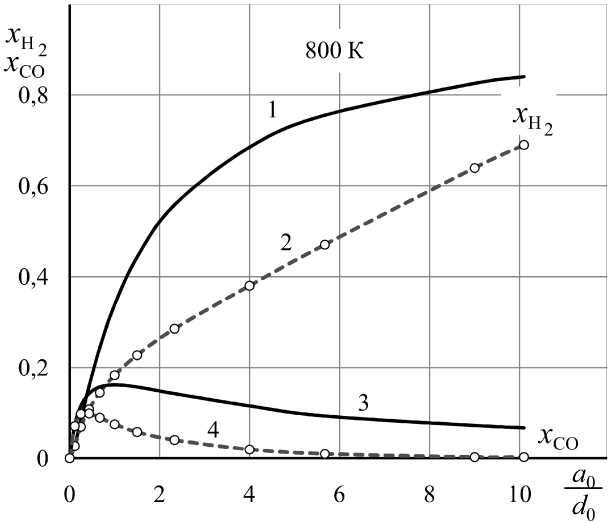
Рис. 2. Концентрации газов-восстановителей в газовых смесях, получающихся при нагревании (H 2 , a 0 – CO 2 , b 0 моль) до 800 К: 1, 3 – водяной газ H 2 –H 2 O–CO–CO 2 [3]; 2, 4 – смесь H 2 –H 2 O–CO–CO 2 –CH 4
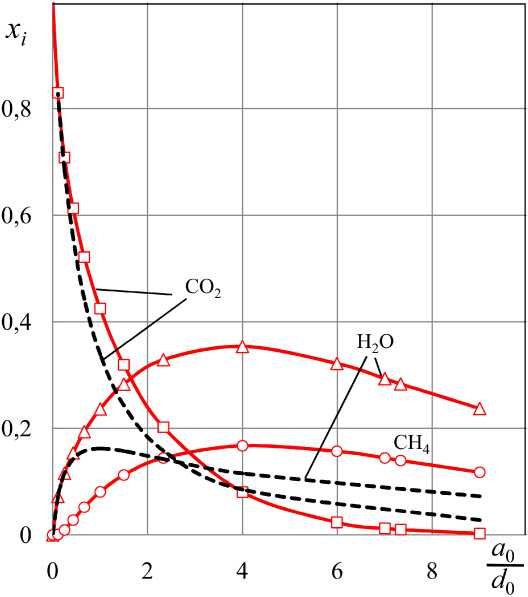
Рис. 3. Концентрации H 2 O, CO 2 и CH 4 в газовых смесях, получающихся при нагревании (H 2 , a 0 – CO 2 , b 0 моль) до 800 К: штриховые линии – водяной газ H 2 –H 2 O–CO–CO 2 [3]; сплошные – смесь
H 2 –H 2 O–CO–CO 2 –CH 4
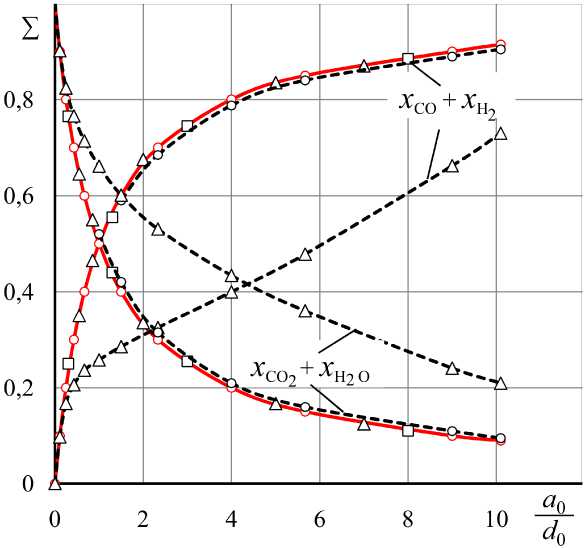
Рис. 4. Суммы концентраций восстановителей и окислителей: сплошные линии – водяной газ при любых температурах; штриховые – H 2 –H 2 O–CO–CO 2 –CH 4 при Т > 950 К; штриховые линии с точками (∆) при Т = 800 К
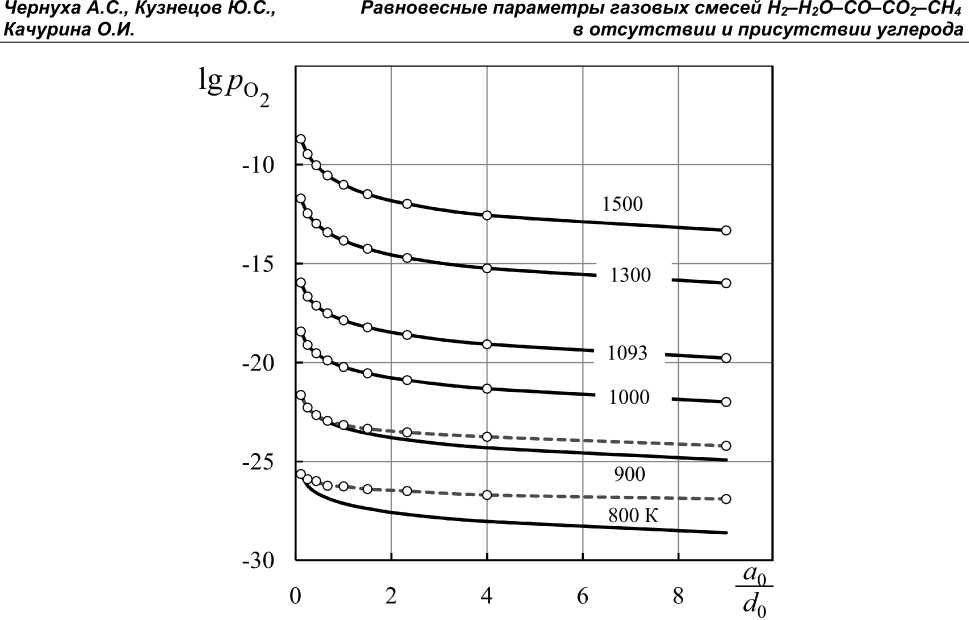
Рис. 5. Кислородный потенциал газовых смесей, получающихся при нагревании исходной смеси (H 2 , a 0 – CO 2 , b 0 моль): сплошные линии – водяной газ H 2 –H 2 O–CO–CO 2 [3]; точки и штриховые линии – смесь H 2 –H 2 O–CO–CO 2 –CH 4
на восстановительные свойства газовой смеси H 2 –H 2 O–CO–CO 2 –CH 4 , которые количественно оцениваются кислородным потенциалом n o = RT In p O2, или величиной 1g( p O2, атм).
Расчетные формулы для логарифма равновесного давления кислорода [3, 4]:
2H 2 O = 2H 2 + O2, A rG°T = 492 230 - 108,24 T ;
2CO 2 = 2CO + O2, A r G T = 565 390 - 175,17 T .
На рис. 5 результаты вычислений lg( pO , атм) показаны в сравнении с равно- весными параметрами водяного газа H2–H2O– CO–CO2, получающегося при нагревании тех же исходных смесей (H2 + CO2) без учета реакции образования метана [3]. Лишь при температурах ниже ~ 950 К равновесное давле- ние кислорода смесей H2–H2O–CO–CO2–CH4 отличается от равновесного давления кислорода водяного газа, вычисленного без учета образования метана. Восстановление Fe3O4 до FeO, например, при 1000 К начинается, если lg( pO , атм) ≤ –19,84, при 1500 К, если lg( pO , атм) ≤ –8,72. Восстановление FeO до Fe при 1000 К начинается, если lg( pO , атм) ≤ ≤ –20,72, при 1500 К, если lg( pO , атм) ≤ ≤ –11,63. В существующих технологиях восстановление железа из железорудной составляющей шихты осуществляется при температурах выше 1000 К, поэтому для упрощения расчетов параметров таких процессов можно не учитывать образование метана.
Гетерогенное равновесие
«водяной газ – метан – углерод»
В присутствии углерода в качестве самостоятельной фазы метан получается не только по реакции (II), но и в результате взаимодействия водорода с углеродом. Определение параметров равновесия смеси (H 2 –H 2 O–CO– CO 2 –CH 4 –C) связано c учетом совместного равновесия пяти реакций:
H 2 + CO 2 = H 2 O + CO,
Д rGT (I) = 36 580 - 33,465 T;(I)
2H 2 + 2CO = CH 4 + CO 2 ,
Д rGT (II) = -262 365 + 287,23 T;(II)
C + CO 2 = 2CO,
Д rGT (III) = 172140 - 177,7T;(III)
C + H 2 O = CO + H 2 ,
Д rGT (IV) = 135 560 -144,235 T;(IV)
C + 2H 2 = CH 4 ,
Д rGT (V) = -90 225 +109,53 T.(V)
Для расчетов следует взять три независимые реакции, например (I), (IV) и (V). Рассматриваемая двухфазная трехкомпонентная (шесть веществ минус три независимые реакции) система при заданной температуре и давлении 1 атм имеет по правилу фаз Гиббса одну сте- пень свободы. Поэтому из системы четырех уравнений:
x H 2 O x CO x H 2 x CO
KI = , KIV = xH2 xCO2
Kv = ^CIH^, ZXi = 1(6)
x H2
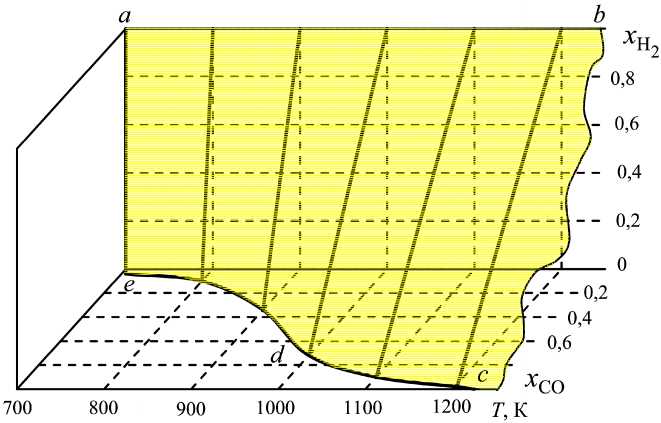
концентрации всех компонентов газовой смеси можно определить, задавая концентрацию одного из пяти компонентов. В работе [2] не учитывалась возможность образования метана, а результаты расчетов иллюстрировались трехмерной диаграммой и изотермическими сечениями этой диаграммы, показывающими соотношения концентраций H 2 и CO, рис. 6, a и 7. В этом случае соотношения между x H от x СО можно аппроксимировать прямыми линиями,
а)
700 800 900 1000 1100 1200 ^ к
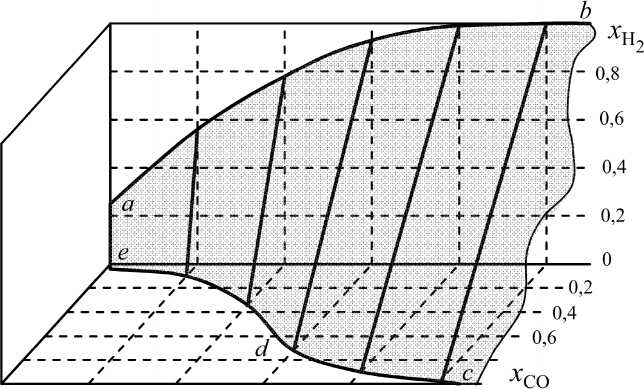
Рис. 6. Влияние учета реакций образования метана на соотношение между концентрациями H 2 и CO: a – системы H 2 –H 2 O–CO–CO 2 –C [2]; б – системы H 2 –H 2 O–CO–CO 2 –CH 4 –C
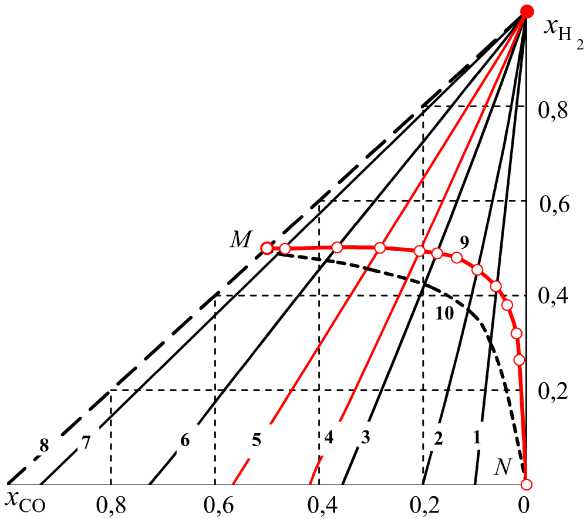
Рис. 7. Концентрации Н 2 и СО в системах Н 2 –Н 2 О–СО–СО 2 –С [2]: линия 1 – определяет все возможные состояния при 800, 2 – 850, 3 – 900, 4 – 917, 5 – 955, 6 – 1000, 7 – 1100, 8 – выше 1300 К; линия 9 – определяет состояния систем при нагревании (Н 2 О–С) [2], линия 10 – определяет состояния систем при нагревании (Н 2 О–С) с учетом образования метана
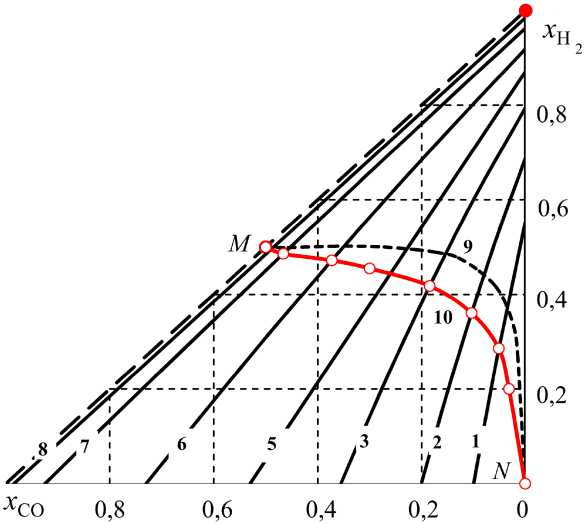
Рис. 8. Концентрации Н2 и СО в системах Н2–Н2О–СО–СО2–СН4–С: линия 1 определяет все возможные состояния при 800, 2 – 850, 3 – 900, 5 – 950, 6 – 1000, 7 – 1100, 8 –1200 К и выше; линия 9 – состояния систем без метана при нагревании (Н2О–С) [2], линия 10 – состояния систем при нагревании (Н2О–С) с учетом метана соединяющими точку с координатами xH = 1 и xСО = 0 с точками, координаты которых оп-
ределяются параметрами равновесия системы CO–CO 2 –C. При решении системы уравнений (6) для сравнения с результатами работы [2]
выведено уравнение для соотношения между
x H и x СО при заданной температуре с учетом
образования метана:
x H 2
- 0,5
' K IV + X CO "
V K IV K V 7
+
+. 0,25
K IV + X CO ^ + 1 X CO v K iv K v 7
—
( x C 2 O K III )
K V
. (7)
Результаты расчетов показаны криволинейной поверхностью abcde на рис. 6, б и прямыми линиями 1–8 изотермических сечений этой поверхности на рис. 8. Координаты точек пересечения изотерм с осью x H ( x CO = 0) определяют концентрацию водорода в системе H 2 –CH 4 –C. При температурах T ≥ 1000 К поверхности abcde и изотермические линии на рис. 6–8 не отличаются. Однако при температурах ниже 1000 К положения изотерм различаются и становятся существенными различия при температурах ниже ~ 950 К. Это обстоя-
тельство еще раз подтверждает допустимость не учитывать образование метана при температурах выше ~ 950 К.
В практических технологиях процессы восстановления оксидов металлов чаще всего осуществляются в многокомпонентных газовых смесях нужного состава в присутствии углерода. Получать газовые атмосферы строго контролируемого состава в присутствии углерода можно различными способами. Наибольший интерес представляет возможность создания атмосферы водяного газа нагреванием паров воды в контакте с углеродом. В частности, в работах [5, 6] анализируются особенности восстановления оксидов с использованием углерода и паров воды. В предлагаемых «колпаковых» устройствах [7, 8] организуется постоянная подпитка системы парами воды. В таких открытых системах имеет место обмен с окружающей средой газом, и это исключает возможность установления равновесия. Однако информация о предельно возможных (равновесных) параметрах закрытых систем позволяет судить о влиянии различных факторов на протекание и неравновесных процессов. В работе [2] приведены результаты термодинамического расчета параметров водяного газа, получающегося при нагрева-
Параметры газовой фазы, получающейся при нагревании 1 моля паров воды в контакте с избытком углерода, P = 1 атм
|
T , К |
800 |
850 |
900 |
1000 |
1093 |
1200 |
|
x H 2 |
0,2858 |
0,3603 |
0,4179 |
0,4719 |
0,4859 |
0,4933 |
|
x H 2 О |
0,3040 |
0,2347 |
0,1662 |
0,0620 |
0,0199 |
0,0057 |
|
x СО |
0,0512 |
0,1041 |
0,1845 |
0,3730 |
0,4660 |
0,4932 |
|
x СО 2 |
0,2381 |
0,2144 |
0,1740 |
0,0713 |
0,0191 |
0,0040 |
|
x СH 4 |
0,1208 |
0,0864 |
0,0572 |
0,0218 |
0,0092 |
0,0040 |
|
E n |
1,203 |
1,3025 |
1,4314 |
1,7314 |
1,9078 |
1,9733 |
|
A n h2o |
0,6343 |
0,6943 |
0,7621 |
0,8927 |
0,9620 |
0,9888 |
|
A n C(CH 4 ) |
0,1453 |
0,1126 |
0,0819 |
0,0378 |
0,0175 |
0,0077 |
|
A n C(CO) |
0,0616 |
0,1356 |
0,2641 |
0,6458 |
0,8890 |
0,9732 |
|
A n C(CO 2 ) |
0,2864 |
0,2793 |
0,2491 |
0,1234 |
0,0364 |
0,0078 |
|
EA n C |
0,4933 |
0,5275 |
0,5951 |
0,8070 |
0,9429 |
0,9877 |
|
lg( p O 2 , атм) |
–26,42 |
–25,45 |
–23,71 |
–21,82 |
–20,64 |
–19,65 |
|
lg( p O 2 , атм) без метана* |
– |
–25,04 |
–23,76 |
–21,84 |
–20,64 |
–19,65 |
Примечание. * Вычислено без учета реакций образования метана [2].
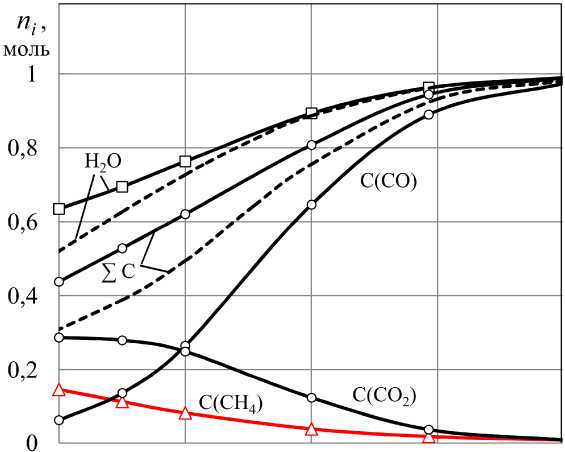
Рис. 9. Расход паров воды и углерода при нагревании смеси (Н 2 О, 1 смоль – С): сплошные линии – с учетом образования метана, штриховые – без метана; C(CH 4 ), C(CO 2 ), C(CO) – расход углерода на образование CH 4 , CO 2 и CO; ∑C – суммарный расход углерода;
Н 2 О – расход воды
нии до разных температур исходной системы C–H 2 O без учета образования метана. Эти параметры представлены политермической линией 9 на рис. 7 и 8. Результаты аналогичных расчетов с учетом двух реакций образования метана приведены в таблице и показаны на рис. 7 и 8 политермической линией 10. Из сравнения положений линий 9 и 10 следует, что образование метана незначительно снижает концентрацию водорода и приводит к увеличению концентрации монооксида СО. Однако, важнейшая технологическая характеристика lg( p O , атм) газовой смеси, получающейся при нагревании паров воды в контакте с углеродом, существенно не изменяется с учетом реакций образования метана, рис. 5.
На рис. 9 представлены результаты расчетов расхода паров воды и углерода при нагревании исходной системы (Н2О, 1 смоль – С). При нагревании до 800 К в равновесной газовой смеси Н2–Н2О–СО–СО2–СН4 xH = 0,2858, xCO = 0,0512 (см. рис. 7), lg( pO , атм) = –26,42. Расход паров воды составляет около 63 %, а углерода – лишь 42 % от максимально возможного расхода. При этом около трети общего количества израсходованного углерода переходит в газовую фазу с образованием метана, около двух третей – с образованием СО. При нагревании до 1200 К расходы паров воды и углерода достигают максимально возможных величин – по 1 молю. При этом весь углерод переходит в газовую фазу только с образованием СО, все пары воды восстанавливаются до водорода. Получающаяся газовая фаза представляет собой эквимолярную смесь Н2–СО со следами Н2О, СО2 и СН4 с высоким восстановительным потенциалом lg( pO , атм) = –19,65.
Выводы
При температурах ниже ~ 950 К в водяном газе в отсутствии углерода в качестве самостоятельной фазы возможно образование метана, что незначительно снижает восстановительную способность газовой фазы. При температурах выше 950 К при количественной оценке параметров водяного газа можно не учитывать возможность образования метана. При нагревании до температур выше ~ 1200 К паров воды в контакте с избытком углерода получается смесь только Н 2 и СО с равными концентрациями компонентов.
Список литературы Равновесные параметры газовых смесей H2-H2O-CO-CO2-CH4 в отсутствии и присутствии углерода
- Строкина, И.В. Изменения окислительно-восстановительных свойств газовой фазы системы C-O2-H2/И.В. Строкина, Н.Ф. Якушевич//Изв. вузов. Черная металлургия. -2011. -№ 6. -С. 3-5.
- Кузнецов, Ю.С. Системный анализ процессов восстановления оксидов железа в атмосфере водяного газа в присутствии углерода // Ю.С. Кузнецов, Г.Г. Михайлов, О.И. Качурина // Металлы. ИМЕТ РАН. - 2014. - № 2. - С. 10-15.
- Reduction of Iron Oxides in a Humid Atmosphere/G.P. Vyatkin, G.G. Mikhailov, Yu.S. Kuznetsov et al.//Steel in Translation. -2012. -Vol. 42, no. 2. -P. 103-106 DOI: 10.3103/S0967091212020301
- Кузнецов, Ю.С. Окислительно-восстановительный потенциал газовых фаз // Ю.С. Кузнецов, О.И. Качурина // Современные проблемы электрометаллургии стали: материалы XVI Междунар. науч. конф. / под ред. В.Е. Рощина. - Челябинск: Издат. центр ЮУрГУ, 2015. - Ч. 1. - С. 75-82.
- Дигонский, С.В. Роль водорода в восстановлении оксидов металлов твердым углеродом/С.В. Дигонский, В.В. Тен//Альтернативная энергетика и экология. -2009. -№ 11 (79). -С. 45-55.
- Дигонский, С.В. Карботермическое восстановление оксидного сырья в неравновесных химических системах/С.В. Дигонский//Технология металлов. -2008. -№ 8. -С. 3-7.
- Пат. 2111271 С1 Российская Федерация. Способ получения металлов из их сульфидов/С.В. Дигонский, Н.А. Дубинин, Е.Д. Кравцов. -Заявл. 22.10.96, опубл. 20.05.98.
- Пат. 2033431 С1 Российская Федерация. Способ получения металлов/В.В. Дигонский, С.В. Дигонский, В.Е. Горбовский. -Заявл. 02.04.91, опубл. 20.04.95.


