Разработка и стандартизация липосомальной формы 4-тиоурендоиминометилпиридиний перхлората с использованием природных триацилглицеринов
Автор: Павлов И.А.
Журнал: Природа Внутренней Азии @nature-inner-asia
Рубрика: Фармакология
Статья в выпуске: 1 (34), 2026 года.
Бесплатный доступ
Разработка новых лекарственных форм противотуберкулезных препаратов является актуальной задачей для регионов с высокой заболеваемостью, включая Республику Бурятия. В работе представлены результаты создания липосомальной формы 4-тиоурендоиминометилпиридиния перхлората (Перхлозон), характеризующегося липофильностью и ограниченной биодоступностью. Для модификации липидного бислоя использованы природные триацилглицерины — жир сурка сибирского (Marmota sibirica Radde) и экстракт околоплодной пленки кедрового ореха (Pinus sibirica). Методом ГХ-МС установлен жирнокислотный состав исходного сырья: в подкожном жире сурка идентифицировано 36 жирных кислот, в экстракте пленки кедрового ореха — 20. Из подкожного жира сурка получен концентрат полиненасыщенных жирных кислот методом комплексообразования с мочевиной, содержание линоленовой кислоты в котором достигло 45,3 %, линолевой — 21,7 %. Оптимизирована технология получения липосом методом гидратации тонкой пленки: установлено оптимальное время ультразвуковой обработки (7 мин), обеспечивающее степень включения препарата 56,5 % и средний размер везикул 445±55 нм. Разработаны методики стандартизации готовой формы с использованием УФ-спектрофотометрии (аналитическая длина волны 317 нм) и ВЭЖХ, позволяющие подтвердить подлинность и определить содержание действующего вещества. Полученные результаты служат основой для проекта фармакопейной статьи предприятия.
Липосомы, липосомальная доставка, «Перхлозон», жир сурка сибирского, кедровый орех, полиненасыщенные жирные кислоты, стандартизация
Короткий адрес: https://sciup.org/148333180
IDR: 148333180 | УДК: 615.451.3:547.915:665.3 | DOI: 10.18101/2542-0623-2026-1-94-105
Development and standardization of a liposomal 4-thiourendiminomethylpyrid inium perchlorate using natural triacylglycerols
Development of new dosage forms of anti-tuberculosis drugs is a pressing issue for regions with a high incidence of this disease, including the Republic of Buryatia. The article presents the results of the development of 4-thiourendoiminomethylpyridinium perchlorate (Perchlozon) liposomal formulation, characterized by lipophilicity and limited bioavailability. We used natural triacylglycerols — Siberian marmot (Marmota sibirica Radde) fat and pine nut (Pinus sibirica) pellicle extract — to modify the lipid bilayer. The fatty acid composition of the starting materials was determined using GC-MS: 36 fatty acids were identified in marmot subcutaneous fat and 20 — in pine nut membrane extract. We obtained a polyunsaturated fatty acid concentrate from marmot subcutaneous fat via complexation with urea; the linolenic acid content reached 45.3 % and the linoleic acid content — 21.7 %. The technology for producing liposomes via thin film hydration was optimized: optimal ultrasonic treatment time ensuring a drug incorporation rate of 56.5% was 7 min with an average vesicle size of 445±55 nm. We developed methods for standardizing the finished product using UV spectrophotometry (analytical wavelength — 317 nm) and HPLC, allowing for confirmation of authenticity and determination of the active ingredient content. The results obtained serve as the basis for the draft corporate pharmacopoeial monograph.
Текст научной статьи Разработка и стандартизация липосомальной формы 4-тиоурендоиминометилпиридиний перхлората с использованием природных триацилглицеринов
Высокий уровень заболеваемости туберкулезом в регионе Внутренней Азии, в частности в Республике Бурятия, где показатели превышают среднероссийские (154,8 на 100 тыс. населения), требует совершенствования подходов к фармакотерапии. Одним из перспективных направлений является применение липосомальных систем доставки, позволяющих повысить биодоступность труднорастворимых соединений и обеспечить пролонгированное действие препарата [Барсуков, 1998].
Объектом исследования выбран отечественный противотуберкулезный препарат 4-тиоурендоиминометилпиридиний перхлорат (Перхлозон), обладающий высокой активностью в отношении Mycobacterium tuberculosis , включая поли-резистентные штаммы (патент РФ № 1621449)1. Соединение внесено в Государственную фармакопею РФ XV издания (ФС.2.1.0484). «Перхлозон» является липофильным веществом (логарифм коэффициента распределения logP > 2), что обусловливает его низкую растворимость в воде (0,15 мг/мл) и, как следствие, ограниченную биодоступность при пероральном приеме. Включение липофильных соединений в липосомы является общепризнанным подходом для улучшения их фармакокинетических параметров за счет солюбилизации в липидном бислое и защиты от метаболической инактивации.
Целесообразность использования в составе липосомальной мембраны природных липидов, богатых полиненасыщенными жирными кислотами (ПНЖК), обусловлена их биосовместимостью и способностью модулировать текучесть мембраны. В качестве региональных источников ПНЖК выбраны жир сурка сибирского ( Marmota sibirica Radde), традиционно применяемый в народной медицине Забайкалья при легочных заболеваниях [Эрэгдэндагва, 1986], и околоплодная пленка семян сосны сибирской ( Pinus sibirica ), являющаяся отходом переработки кедрового ореха и потенциальным источником биологически активных липидов [Ширеторова, 2002].
Цель настоящей работы — разработка состава, технологии и методов стандартизации липосомальной формы 4-тиоурендоиминометилпиридиний перхлората с использованием концентратов ПНЖК из природного сырья.
Материалы и методы исследования
Объекты исследования. Образцы подкожного, полостного и бурого жира сурка сибирского отобраны в Джидинском районе Республики Бурятия. Экстракт липидов из околоплодной пленки кедрового ореха получен методом Блайя — Дайэра [Bligh, Dyer, 1959]. Субстанция 4-тиоурендоиминометилпиридиния перхлората (Перхлозон) предоставлена Иркутским институтом химии им. А. Е. Фаворского СО РАН, содержание основного вещества 99,2%. Фосфолипиды выделяли из куриных яиц по методу Фолча [Кейтс, 1975].
Анализ жирнокислотного состава. Метиловые эфиры жирных кислот получали по методике Stoffel с соавт. (1959). Анализ выполняли на хромато-масс-спек-трометре Hewlett-Packard 6890 с квадрупольным детектором HP 5973, колонка CP-Wax (30 м × 0,25 мм), газ-носитель — гелий. Идентификацию проводили по библиотеке масс-спектров NIST.
Получение концентрата ПНЖК. Жир сурка омыляли спиртовым раствором КОН, свободные жирные кислоты (СЖК) экстрагировали гексаном.
Концентрирование ПНЖК осуществляли методом комплексообразования с мочевиной [Swern, 1955]. Изучали влияние соотношения мочевина:СЖК (2:1, 3:1, 4:1, 5:1), температуры кристаллизации (0, –5, –10, –20 °С) и времени (12, 24, 48 ч) на выход и состав целевой фракции.
Приготовление липосом. Липосомы получали методом гидратации тонкой липидной пленки. Липидную смесь (фосфолипиды, концентрат ПНЖК или экстракт пленки, α-токоферол) растворяли в хлороформе и упаривали на роторном испарителе при 40°С. Пленку гидратировали трис-буферным раствором (pH 7,4), содержащим «Перхлозон» (1,5 мг/мл). Суспензию обрабатывали ультразвуком на диспергаторе УЗДН-А (22 кГц) в ледяной бане, варьируя время обработки от 3 до 10 мин. Недиспергированные липиды осаждали центрифугированием (3000 об/ мин, 90 мин).
Определение степени включения. Липосомальную суспензию наносили на колонку (1×20 см) с Сефадексом G-50, элюировали физиологическим раствором. Собирали фракции по 2 мл, измеряли оптическую плотность при 317 нм (спектрофотометр Apel PD 303 UV). Для разрушения липосом к пробам добавляли 5 %-ный раствор дезоксихолата натрия. Степень включения (η, %) рассчитывали по формуле: η = (D1·V1) / (D1·V1 + D2·V2) × 100%, где D1 и D2 — оптическая плотность липосомальной и свободной фракций после разрушения, V1 и V2 — их объемы.
Определение размеров липосом. Средний гидродинамический диаметр везикул оценивали методом спектротурбидиметрии по углу наклона зависимости lgD от lgλ в диапазоне 400–700 нм [Трофимов, Нисневич, 1990]. Дополнительно проводили микроскопию (микроскоп МС-300, увеличение ×1000).
Идентификация и количественное определение « Перхлозона » . УФ-спектры регистрировали в диапазоне 200–400 нм. ВЭЖХ-анализ выполняли на хроматографе Agilent 1 200 с масс-детектором (ионная ловушка), колонка Zorbax SB-C18, подвижная фаза ацетонитрил-вода (60:40), скорость потока 1 мл/мин, детекция при 317 нм. Калибровочный график строили для растворов «Перхлозона» с концентрацией 5–50 мкг/мл.
Результаты и обсуждение
Характеристика липидного сырья. Проведено сравнительное исследование трех типов жировой ткани сурка сибирского. Установлено, что подкожный жир характеризуется наиболее высокими значениями йодного числа (110–112 г I2/100 г) и низкими показателями окисленности (перекисное число 0,03–0,04), что свидетельствует о его высоком качестве и степени ненасыщенности. Полостной и бурый жиры уступают по этим показателям (йодное число 108–109 и 72–75 соответственно) (табл. 1).
Методом ГХ-МС в жире сурка идентифицировано 36 жирных кислот (табл. 2). Доминирующими компонентами являются олеиновая (C18:1n9, 46-58%), линолевая (C18:2n6, 5-9%) и а-линоленовая (C18:3n3, 11-18%) кислоты. Суммарное содержание ненасыщенных жирных кислот в подкожном жире достигает 80%, что значительно выше, чем у большинства наземных млекопитающих, и сопоставимо с жирами рыб. Полученные данные согласуются с результатами исследований жира других видов сурков [Машкин, Батурин, 1993; Florant et al., 1990], что подтверждает видоспецифичность липидного метаболизма этих животных, адаптированного к длительной зимней спячке.
Таблица 1
Физико-химические показатели жира сурка и околоплодной пленки кедрового ореха
|
Показатель |
Сурок (подкожный / полостной / бурый) |
Околоплодная пленка кедрового ореха |
|
Цвет |
светло-желтый / светло-желтый/бурый |
желтый |
|
Запах |
слабый, специфический |
специфический |
|
Йодное число, г/100 г |
112/ 108/ 72 |
110–120 |
|
Перекисное число, г/100 I2 |
0,04/ 0,09/ 0,19 |
0,30 |
|
Кислотное число |
0,5 |
2,5 |
|
Число омыления |
188,85 |
112 |
Таблица 2
Жирнокислотный состав подкожного жира сурка сибирского ( Marmota sibirica Radde), процент от суммы
|
Жирная кислота |
Содержание, % (M±m, n=5) |
|
C16:0 (пальмитиновая) |
15,57±0,29 |
|
C16:1n7 (пальмитолеиновая) |
1,92±0,20 |
|
C18:0 (стеариновая) |
0,02±0,01 |
|
C18:1n9 (олеиновая) |
46,41±3,69 |
|
C18:2n6 (линолевая) |
8,35±1,03 |
|
C18:3n3 (линоленовая) |
18,79±2,01 |
|
Сумма насыщенных |
18,24 |
|
Сумма мононенасыщенных |
52,61 |
|
Сумма полиненасыщенных |
28,30 |
Исследование экстракта околоплодной пленки кедрового ореха показало, что его липидный комплекс содержит 20 жирных кислот (табл. 3). Сумма ненасыщенных кислот составляет 64,6%, из которых на долю олеиновой кислоты приходится 52,7%, линолевой — 5,4%. Высокое содержание липидов (22,5%) в пленке делает этот отход переработки перспективным сырьем для получения биологически активных добавок, однако по содержанию ПНЖК (особенно линоленовой кислоты) пленка уступает жиру сурка. В связи с этим для дальнейшей работы по получению концентрата ПНЖК был выбран подкожный жир сурка.
Анализ жирнокислотного состава полученного концентрата (табл. 4) показал значительное обогащение ПНЖК по сравнению с исходным жиром. Содержание линоленовой кислоты возросло до 45,3%, линолевой — до 21,7 %. Сумма ПНЖК достигла 73,3 %, что позволяет использовать данный концентрат в качестве функционального компонента липосомальной мембраны.
Жирнокислотный состав экстракта околоплодной пленки кедрового ореха ( Pinus sibirica ), процент от суммы
Таблица 3
|
Жирная кислота |
Содержание, % (M±m, n=3) |
|
C16:0 (пальмитиновая) |
18,42±0,28 |
|
C18:0 (стеариновая) |
10,63±0,07 |
|
C18:1n9 (олеиновая) |
52,74±0,46 |
|
C18:2n6 (линолевая) |
5,36±0,38 |
|
Сумма насыщенных |
35,36 |
|
Сумма ненасыщенных |
64,64 |
Таблица 4
Жирнокислотный состав концентрата ПНЖК из жира сурка сибирского
|
Жирная кислота |
Содержание, % |
|
C16:1n7 |
1,36 |
|
C16:3n4 |
1,29 |
|
C18:1n9 |
6,30 |
|
C18:2n6 |
21,74 |
|
C18:3n3 |
45,31 |
|
Сумма ПНЖК |
73,3 |
Получение концентрата ПНЖК из жира сурка. Для обогащения липосомальной мембраны эссенциальными жирными кислотами из подкожного жира сурка получен концентрат ПНЖК методом комплексообразования с мочевиной. Установлены оптимальные условия процесса, обеспечивающие максимальный выход целевого продукта (рис. 1–3): соотношение мочевина : свободные жирные кислоты = 4 : 1, температура кристаллизации -10°С, продолжительность 24 ч. Выход концентрата (некарбамидной фракции) составил 65% массы исходных СЖК.
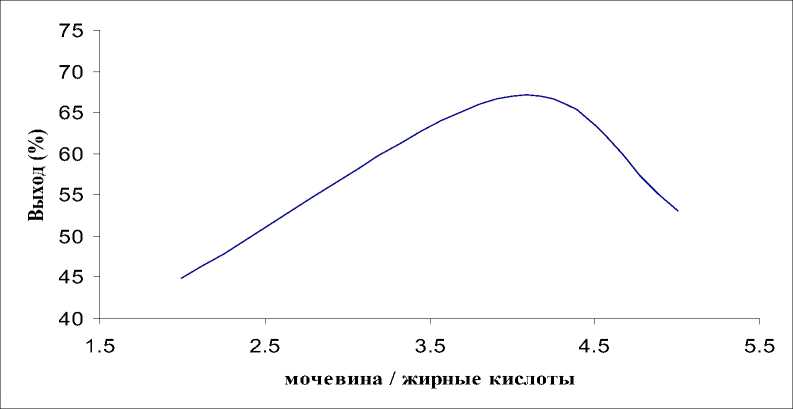
Рис. 1. Влияние соотношения мочевина : СЖК на выход концентрата ПНЖК (T = –10°C, 24 ч)
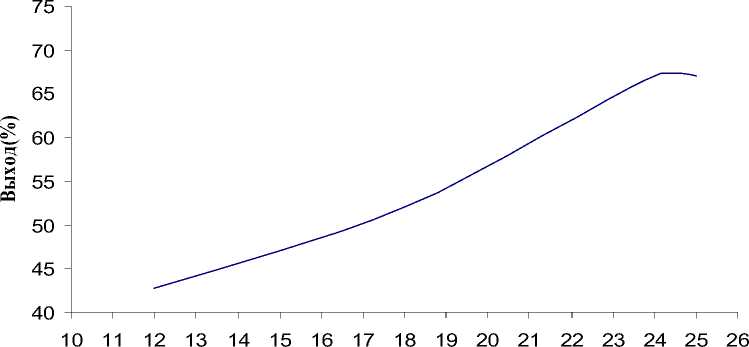
Время (часы)
Рис. 2. Влияние температуры кристаллизации на выход концентрата ПНЖК (соотношение 4:1, 24 ч)
Разработка технологии получения липосом. Выбор метода гидратации тонкой липидной пленки для получения липосом обусловлен его простотой, воспроизводимостью и возможностью масштабирования. Данный метод позволяет включать как гидрофильные, так и липофильные вещества. В случае липофильного «Перхлозона» предполагается его локализация в гидрофобной области бислоя.
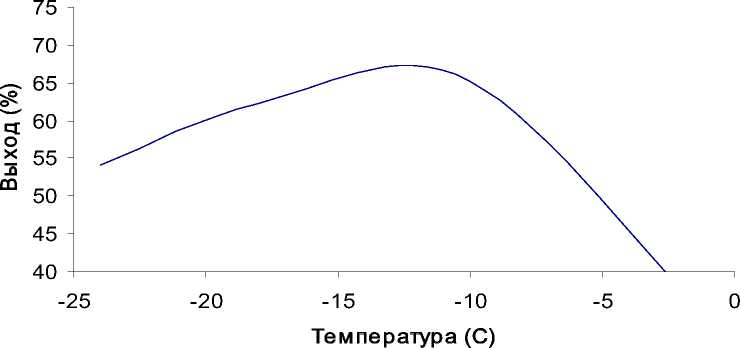
Рис. 3. Влияние времени кристаллизации на выход концентрата ПНЖК (соотношение 4:1, T = –10°C)
Состав липидной смеси подобран экспериментально. Основу составляют фосфолипиды (10% массы готовой формы) как структурообразующий компонент. Концентрат ПНЖК добавлен в количестве 66,7% массы фосфолипидов для модификации текучести мембраны и придания ей дополнительных биоактивных свойств. а-токоферол (5% суммы липидов) введен в качестве антиоксиданта для предотвращения пероксидного окисления ПНЖК.
Ключевым технологическим параметром, влияющим на размер везикул и эффективность включения, является время ультразвуковой обработки. Результаты эксперимента представлены в таблице 5.
Таблица 5
Зависимость характеристик липосом от времени ультразвуковой обработки (M±m, n=5)
|
Время, мин |
Степень включения, % |
Средний диаметр, нм |
|
3 |
87±5 |
1000±150 |
|
5 |
76±4 |
720±98 |
|
7 |
56,5±4,1 |
445±55 |
|
9 |
27,9±4,8 |
220±48 |
Увеличение времени обработки свыше 7 минут приводит к резкому снижению степени включения, что, вероятно, связано с деструкцией везикул и высвобождением препарата в среду. В связи с этим время 7 минут выбрано как оптимальное, обеспечивающее приемлемый баланс между размером частиц (445±55 нм) и степенью загрузки.
Стандартизация готовой формы. Разработка методик стандартизации включала выбор параметров идентификации и количественного определения «Перхло-зона» в составе липосом.
Идентификация. УФ-спектр «Перхлозона» характеризуется максимумом поглощения при 317 нм, обусловленным наличием сопряженной системы связей в молекуле. Сравнение спектров исходного раствора субстанции, раствора в трис-буфере и липосомальной суспензии после разрушения показало идентичность положения максимума, что свидетельствует об отсутствии химического взаимодействия препарата с компонентами липосомальной мембраны. Дополнительно идентификацию проводили методом ВЭЖХ по времени удерживания (Rt = 4,2 мин) и совпадению масс-спектров с библиотечным (рис. 4).
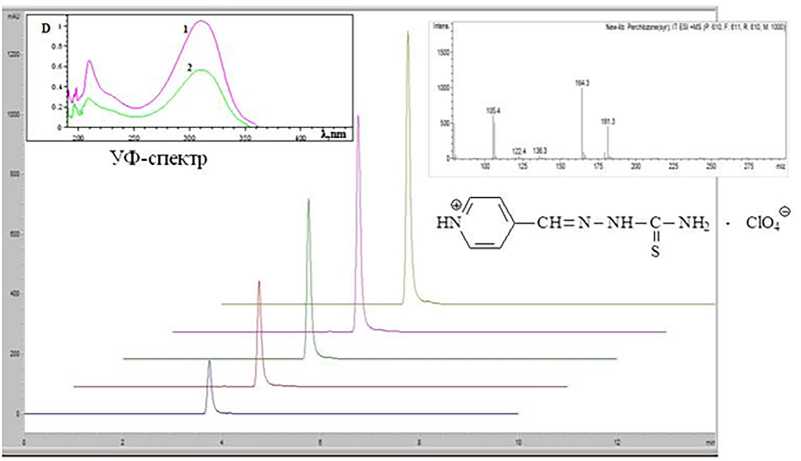
Рис. 4. УФ и масс-спектр контрольного раствора «Перхлозона»
1 — стандартный раствор 4-тиоурендоиминометилпиридиний перхлората; 2 — 4-тиоурендоимино-метилпиридиний перхлората в образце после разрушения липосомальной оболочки
Количественное определение. Для определения содержания «Перхлозона» в липосомах использовали метод УФ-спектрофотометрии после разрушения везикул дезоксихолатом натрия. Предварительно строили калибровочный график в диапазоне концентраций 5–50 мкг/мл (R² = 0,999). Удельный показатель поглощения (E¹%₁см) рассчитан и составил 8 210. Параллельно проводили определение методом ВЭЖХ с использованием внешнего стандарта. Метрологические характеристики методик представлены в таблице 6. Оба метода характеризуются удовлетворительной воспроизводимостью (относительная ошибка < 1 %).
Содержание «Перхлозона» в готовой форме составило в среднем 39,0% от теоретически загруженного количества (1,5 мг/мл липосомальной суспензии соответствует 0,585 мг/мл включенного препарата). Данная концентрация является экспериментально достигнутой для выбранного метода получения и может служить основой для установления нормы содержания в проекте нормативной документации.
Таблица 6
Метрологические характеристики методик количественного определения «Перхлозона» в липосомах (n=5, P=0,95)
|
Метод |
Найдено, % |
S² |
S |
Δx |
ε, % |
|
УФ-спектрофотометрия |
38,996 |
0,014 |
0,118 |
0,136 |
0,35 |
|
ВЭЖХ |
39,028 |
0,012 |
0,111 |
0,128 |
0,33 |
Разработка проекта нормативной документации
На основании проведенных исследований разработан проект фармакопейной статьи предприятия «Липосомальная форма Перхлозона». В проекте регламентируются следующие показатели качества:
-
- описание: опалесцирующая суспензия беловато-желтоватого цвета;
-
- подлинность: совпадение УФ-спектра поглощения раствора препарата после разрушения липосом со спектром стандартного образца (максимум при 317 нм); время удерживания основного пика на ВЭЖХ должно соответствовать стандарту;
-
- размер частиц: средний диаметр везикул должен находиться в пределах 350–550 нм (метод спектротурбидиметрии или лазерной дифракции);
-
- степень включения: не менее 50 % от теоретического содержания (метод гель-фильтрации с УФ-детекцией);
-
- количественное определение: содержание «Перхлозона» должно составлять 0,55–0,65 мг/мл (метод УФ-спектрофотометрии или ВЭЖХ);
-
- микробиологическая чистота: соответствует требованиям ГФ XV для нестерильных лекарственных форм.
Обсуждение результатов
В ходе выполнения работы последовательно решены задачи, направленные на создание новой лекарственной формы известного противотуберкулезного средства. Первоначально проведена оценка региональных источников липидов — жира сурка и отходов переработки кедрового ореха. Данные ГХ-МС подтвердили высокое содержание ПНЖК в обоих объектах, однако для дальнейшего использования был выбран жир сурка, так как он позволяет получить высокообогащенный концентрат эссенциальных кислот. Полученный концентрат с содержанием линолевой и линоленовой кислот более 65 % может рассматриваться как самостоятельная биологически активная добавка, а в контексте данной работы — как модификатор липосомальной мембраны.
Выбор метода гидратации пленки для получения липосом обусловлен его технологичностью и эффективностью для включения липофильных веществ, к которым относится «Перхлозон». Варьирование времени ультразвуковой обработки позволило найти компромисс между степенью включения и размером везикул. Полученные везикулы размером около 450 нм относятся к крупным моноламеллярным или олиголамеллярным структурам, способным эффективно захватывать липофильные соединения в бислой (рис. 5).

Рис. 5. Микрофотографии липосом (увеличение 10×100)
Разработанные методики стандартизации (УФ-спектрофотометрия и ВЭЖХ) являются общепринятыми для данного класса соединений и позволяют надежно контролировать качество препарата на всех этапах производства. Совпадение результатов, полученных двумя независимыми методами, подтверждает их правильность. Таким образом, цель исследования — разработка состава, технологии и методов стандартизации липосомальной формы «Перхлозона» — может считаться достигнутой. Полученная композиция требует дальнейших доклинических исследований для подтверждения повышения биодоступности и терапевтической эффективности in vivo.
Заключение
-
1. Исследован жирнокислотный состав жира сурка сибирского и экстракта околоплодной пленки кедрового ореха. Показано, что подкожный жир сурка
-
2. Оптимизирована методика получения концентрата ПНЖК из жира сурка методом комплексообразования с мочевиной. Установлены оптимальные параметры (соотношение 4:1, -10°С, 24 ч), позволяющие получить продукт с содержанием ПНЖК 73,3 %.
-
3. Разработаны состав и технология получения липосом с включением 4-тио-урендоиминометилпиридиний перхлората и концентрата ПНЖК. Определено оптимальное время ультразвуковой обработки (7 мин), обеспечивающее степень включения 56,5% и размер везикул 445±55 нм.
-
4. Разработаны и валидированы методики идентификации и количественного определения «Перхлозона» в липосомах методами УФ-спектрофотометрии и ВЭЖХ. Относительная ошибка определений не превышает 0,35%.
-
5. На основании полученных результатов разработан проект фармакопейной статьи предприятия, регламентирующий основные показатели качества новой лекарственной формы.
содержит до 80 % ненасыщенных жирных кислот и является перспективным сырьем для получения концентрата ПНЖК.


