Разработка и валидация методик хроматографического определения для идентификации, количественной оценки препаратов карбоновых кислот
Автор: Бакина К.Д., Зеленова М.П., Потехина Е.А., Топорец Т.А., Симонян Е.В.
Журнал: Мировая наука @science-j
Рубрика: Основной раздел
Статья в выпуске: 6 (15), 2018 года.
Бесплатный доступ
В статье описываются результаты исследований, проведенных с целью разработки и валидации методик хроматографического определения для идентификации и количественной оценки препаратов карбоновых кислот. В ходе исследований изучена подвижность веществ в растворителях с различной элюирующей способностью. Экспериментально установлено, что наиболее эффективными для идентификации изучаемых веществ являются смеси растворителей с величиной диэлектрической проницаемости равной 0,6. На основании полученных элюотропных рядов были предложены различные бинарные системы растворителей, из которых оптимальными свойствами обладала система этилацетат - спирт этиловый. Для дальнейшей модификации предложенного метода проводилось исследование по влиянию процесса импрегнирования пластинок поверхностно - активными веществами. Для этого целесообразно использовать катионоактивные четвертичные аммониевые основания, в частности цетилпиридиния хлорид.
Жидкостная адсорбционная хроматография, элюирующая способность, растворитель, элюотропные ряды, детектирование
Короткий адрес: https://sciup.org/140263645
IDR: 140263645
Development and validation chromatographic determination techniques for the identification and quantification of carboxylic acid preparations
The article describes the results of the studies carried out for the purpose of developing and validating chromatographic determination techniques for the identification and quantification of carboxylic acid preparations. In the course of the studies, the mobility of the substances in solvents with a different eluting ability was studied. It has been experimentally established that the mixtures of the solvents with a dielectric constant equaled 0.6 are the most effective for the identification of the studied substances. Various binary systems of solvents have been proposed on the basis of obtained eluotropic series, of which the ethyl acetate - ethyl alcohol system has the optimal properties. The study of the influence of the impregnation of plates with surface active agents was made for the further modification of the proposed method. Cationic quaternary ammonium bases, particularly cetylpyridinium chloride, are appropriate to use for this purpose.
Текст научной статьи Разработка и валидация методик хроматографического определения для идентификации, количественной оценки препаратов карбоновых кислот
Выбор элюента в жидкостной адсорбционной хроматографии играет более значимую роль, чем выбор неподвижной фазы. Растворитель напрямую участвует в самом процессе разделения, в связи с чем, изменяя природу растворителей подвижной фазы, возможно в широких пределах изменять удерживание и селективность разделения на одних и тех же адсорбентах. Для получения оптимальных значений R f экспериментально подбирают растворители с определенной элюирующей способностью. Самый простой способ получения подвижной фазы с любой элюирующей способностью состоит в смешивании двух растворителей с разной полярностью [1]. Основной целью исследования была разработка унифицированного метода идентификации для некоторых лекарственных препаратов – производных карбоновых кислот. В качестве объекта исследования нами были выбраны кислота янтарная, фумаровая, никотиновая и глутаминовая. В ходе исследования изучена подвижность веществ в растворителях с различной элюирующей способностью. Результаты представлены в таблице 1.
Таблица 1 - Подвижность некоторых производных карбоновых кислот в растворителях с различной элюирующей способностью
|
Растворитель |
5 я ° о у 2 К У я 8 Я О |
8 я я 8 ся м |
5 я S ^ 5 е |
о я я н |
§ я 2 н я о я к |
|
Бензол |
2,3 |
0,05 |
0 |
0 |
0 |
|
Толуол |
2,3 |
0 |
0 |
0 |
0 |
|
Диэтиловый эфир |
4,2 |
0,45 |
0,19 |
0,01 |
0,88 |
|
Хлороформ |
4,8 |
0 |
0 |
0,03 |
0,03 |
|
Этилацетат |
6,0 |
0 |
0,08 |
0,78 |
0,16 |
|
Кислота ледяная уксусная |
6,2 |
0,84 |
- |
- |
0,6 |
|
Пиридин |
12,9 |
0,05 |
0,03 |
0 |
0,48 |
|
Изоамиловый спирт |
15,2 |
0,65 |
0 |
0,2 |
0,13 |
|
Аммиак |
16,5 |
0,98 |
0,98 |
0,98 |
0,96 |
|
Бутанол |
17,8 |
0,7 |
0,05 |
0,03 |
0,12 |
|
Ацетон |
20,7 |
0,8 |
0,15 |
0 |
0,09 |
|
Изопропанол |
21,8 |
0 |
0 |
0 |
0,15 |
|
Этанол |
24,5 |
0,8 |
0,38 |
- |
0,8 |
|
ДМФА |
36,7 |
0,95 |
0 |
- |
- |
|
Ацетонитрил |
37,5 |
0,74 |
0,2 |
0 |
0,073 |
|
Вода |
78,5 |
0,96 |
0,98 |
0,99 |
0,99 |
Величина Rf 0,4 – 0,7 наблюдалась при использовании растворителей с величиной диэлектрической проницаемости не более 20. На основании полученных данных предложены бинарные системы растворителей с рассчитанной элюирующей способностью. Расчет проводили по формуле [3]:
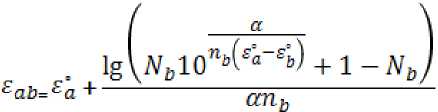
, где
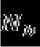
– мольная доля более сильного растворителя;
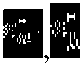
– значения для чистых растворителей;
(≈Ax) – площадь, необходимая для размещения молекулы растворителя B на поверхности;
a - параметр активности;
Параметр Nb рассчитывали по формуле:
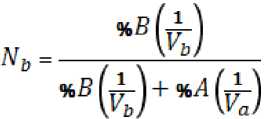
, где
∨ а
- величины, обратные мольной доле.
Экспериментально установлено, что наиболее эффективными для идентификации изучаемых веществ являются смеси растворителей с величиной диэлектрической проницаемости равной 0,6. В дальнейшем, для выбора оптимальных соотношений растворителей, формулу преобразовали:
1 (IQ ® / п ( Е а - Е в ) - 1)
∨ в
А
В
(1Q
а п ( Е Q - а пЕ а )
∨
а
- 1)
∨ в
Для более эффективной работы, была написана программа на основе VisualBasic. Электронная таблица преобразуется посредством объектноориентированной модели кода и данных, которые мгновенно обрабатываются. Таблица становится интерфейсом кода, позволяя легко работать изменять его и управлять расчётами. Смешением двух растворителей с разной полярностью можно приготовить систему с любой элюирующей способностью. На основании полученных элюотропных рядов были предложены различные бинарные системы растворителей, из которых оптимальными свойствами обладала система этилацетат – спирт этиловый. Хроматографирование проводили в данной бинарной системе растворителей с различным соотношением более полярного растворителя (спирта этилового), от 10 до 90% по объему, результаты определения приведены в таблице 2.
Таблица 2 - Определение подвижности кислоты янтарной в системе растворителей этилацетат - спирт этиловый
|
Соотношение растворителей этилацетат: спирт этиловый |
Элюирующая способность системы |
Величина R f кислоты янтарной |
|||
|
Кислота никотиновая |
Кислота глутаминовая |
Кислота фумаровая |
Кислота янтарная |
||
|
9:1 |
0,779 |
0,345 |
0,730 |
0,223 |
0,764 |
|
8:2 |
0,815 |
0,405 |
0,734 |
0,307 |
0,802 |
|
7:3 |
0,833 |
0,412 |
0, 740 |
0,207 |
0,805 |
|
6:4 |
0,850 |
0,388 |
0,738 |
0,212 |
0,812 |
|
5:5 |
0,855 |
0,371 |
0,741 |
0 |
0,815 |
|
4:6 |
0,862 |
0,367 |
Хвост |
0 |
0,823 |
|
3:7 |
0,868 |
Хвост |
Хвост |
0 |
0,823 |
|
2:8 |
0,872 |
Хвост |
Хвост |
0 |
0,834 |
|
1:9 |
0,877 |
Хвост |
Хвост |
0 |
0,830 |
|
0:10 |
0,88 |
0 |
Хвост |
0 |
0,843 |
|
10:0 |
0,48 |
0 |
Хвост |
0 |
0 |
Доказано, что введение более полярного для кислоты янтарной вызывает сначала резкое увеличение элюирующей способности системы, но дальнейшее возрастание его концентрации практически не изменяет свойств системы, носит асимптотический характер, что согласуется с литературными данными. Крутизна начального подъема экспоненциальной кривой тем больше, чем больше различия в полярности обоих растворителей. Кислота фумаровая при соотношении растворителей 1:1 и с дальнейшим увеличением концентрации спирта этилового остается на старте, а для кислоты никотиновой и глутаминовой происходит неполный отрыв вещества от линии старта.
Детектирование осуществляли 0,1% спиртовым раствором метилового красного, а для проявления кислоты глутаминовой использовали раствор 0,1% нингидрина в спирте этиловом с дальнейшим нагреванием на плитке [2].
Для дальнейшей модификации предложенной методики мы проводили исследование по влиянию процесса импрегнирования пластинок поверхностно - активными веществами. Для этого целесообразно использовать катионоактивные четвертичные аммониевые основания, в частности цетилпиридиния хлорид. Известно, что изотерма адсорбции катионных ПАВ имеет два плато: первое характеризует нейтрализацию заряда поверхности силикагеля, при этом мономеры катионного ПАВ замещают адсорбированные молекулы воды, а второе отвечает за образование гемимицелл на поверхности за счет гидрофобных взаимодействий между хвостами мономеров поверхностно-активных веществ [4]. Мицелярные свойства цетилпиридиния хлорида (ЦПХ) подходят для использования в хроматографии: точка Крафта (температура, выше которой возможно мицеллообразование) составляет 19,5°С, а критическая концентрация мицеллообразования 9,0Л0-4 моль/л. В связи с этим мы предложили проводить идентификацию наших производных карбоновых кислот следующим образом. Хроматографическую пластинку «Сорбфил» помещали в камеру с раствором цетилпиридиния хлорида 0,001 %. После того, как фронт растворителей достигнет линии финиша, пластинку вынимали, высушивали в течение 2 часов, а затем на линию старта наносили по 5 мкл 0,1% водно-спиртовых растворов (1:1) кислоты фумаровой, янтарной, никотиновой, глутаминовой и хроматографировали после высушивания восходящим методом в камере, предварительно насыщенной системой растворителей этилацетат – спирт этиловый (8:2). Затем пластинку вынимали, высушивали и детектировали. На хроматограмме наблюдались четкие пятна овальной формы.
Список литературы Разработка и валидация методик хроматографического определения для идентификации, количественной оценки препаратов карбоновых кислот
- Бёккер, Ю. Хроматография. Инструментальная аналитика: методы хроматографии и капиллярного электрофореза / Ю. Бёккер. - Москва: Техносфера, 2009. - 458 с.
- Ворожейкин, С.Б. Тонкослойная хроматография аминокислот в мицеллярных подвижных фазах на силикагеле / С.Б. Ворожейкин, Е.С. Башко, С.Н. Штыков // Сорбционные и хроматографические процессы. - 2011. - Т.11, № 6. - С. 840-847.
- Шаповалов, Е.Н. Хроматографические методы анализа: метод. пособие / Е.Н. Шаповалов, А.В. Пирогов. - Москва: Изд-во МГУ им. М. В. Ломоносова, 2007. - 110 с.
- Kung, K.H.S. Fourier transform infrared spectroscopic study of the adsorption of cetyltrimethylammonium bromide and cetylpyridinium chloride on silica / K.H.S. Kung, K.F. Hayes // Langmuir. - 1993. - Vol. 9, №1. - P. 263-267


