Разработка металл-хелатного сорбента на основе стеарата никеля (II)
Автор: Шрейнер Екатерина Владимировна, Кельциева О.А., Шустов В.Э., Суходолов Н.Г., Шиловских В.В., Ширкин А.Ю., Александрова М.Л., Жаковская З.А., Подольская Е.П.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Физика и химия приборостроения
Статья в выпуске: 4 т.25, 2015 года.
Бесплатный доступ
Работа посвящена получению и охарактеризации нового металл-хелатного сорбента на основе стеарата никеля(II). Показано, что данные структуры обладают необходимыми поверхностными и сорбционными свойствами для их использования при проведении пробоподготовки соединений, содержащих в своем составе различные активные гетероатомы (фосфор и хлорсодержащие пестициды).
Металл-аффинная хроматография, металл-хелатный сорбент, пленки ленгмюра-блоджетт, анализ пестицидов
Короткий адрес: https://sciup.org/14264993
IDR: 14264993 | УДК: 543.544.414;
Development of new metal-chelate sorbent based on stearate nickel (II)
The work is devoted to the preparation and characterization of new metal-chelate sorbent based on stearate nickel(II). The collapsed structure on the basis of nickel stearate have been received by the method of Langmuir-Blodgett. Its surface properties have been studied: data obtained on the structure surfaces using scanning electron microscopy, the zeta potential is determined by the Helmholtz-Smoluchowski theory without introducing amendments. Also the sorption properties of the new sorbent have been investigated: the sorption isotherm of albumin chicken on metal-chelate sorbent based nickel stearate have been shown. Also, it have been presented that these structures have the necessary surface and sorption properties for their use during the sample preparation of toxic substances containing in its composition different active heteroatoms. As such compounds, we selected the widely used pesticides: nitrogen (glyphosate and its major metabolite aminomethylphosphonic acid) and chlorine (main persistent organic pollutant - dieldrin). Also the method of inductively coupled plasma mass spectrometry and gas chromatography with electron capture detector have been used in our study.
Текст научной статьи Разработка металл-хелатного сорбента на основе стеарата никеля (II)
Металл-аффинная хроматография является методом концентрирования соединений в зависимости от их химической природы, а именно наличия в структуре активных гетероатомов, что делает этот метод достаточно специфичным и применимым для обогащения образцов строго определенными химическими соединениями или же их метаболитами [1]. На сегодняшний день металл-аффинная хроматография (МАХ) прочно заняла свое место среди других методов предварительного разделения сложных смесей, таких как жидкостная обращенно-фазовая, ионообменная, аффинная хроматографии и гель-электрофорез [2, 3]. Однако существующие коммерческие металл-аффинные сорбенты имеют недостатки: возможность вымывания металла из сорбента во время элюирования, высокий уровень неспецифичной сорбции, и, как следствие, низкую селективность [4]. Металл-аффинная хроматография в настоящее время активно используется в протеомных исследованиях [5, 6], но потенциал метода достаточно высок и он может быть использован для анализа химических веществ, имеющих в своем составе гетероатомы, например пестицидов и их метаболитов. Согласно принципу Пирсона [7], каждый металл обладает определенным сродством к гетероатомам, содержащимся в функциональных группах органических и био-органических соединений.
Металл-аффинные сорбенты по своим структурным особенностям должны отвечать следующим требованиям: ионы металла должны быть доступны для исследуемых молекул, должны находиться в активной форме и не должны переходить в раствор вместе с исследуемым веществом. К таким структурам можно отнести уникальные пленки, полученные по методу Ленгмюра—Блоджетт (ПЛБ) [8], которые в последние годы находят широкое практическое применение в различных областях науки и техники. С помощью данного метода получают мономолекулярные слои стеариновой кислоты, содержащие ионы металла за счет образования ковалентных связей, а коллапсирование пленок позволяет наработать достаточное количество материала для проведения экспериментов, при этом свойства поверхности монослоев не меняются [9].
Ранее нами был разработан и охарактеризован металл-хелатный сорбент на основе стеарата железа (III) (МХС Fe(III))и показана возможность его применения для селективной экстракции таких классов веществ как: фосфорилированные белки и пептиды, аддукты фосфорорганических веществ (зарин, зоман) с белками крови, перфтороктановая сульфокислота (ПФОСК) [10, 11]. Однако представлялось интересным разработать металл-аффинный сорбент на основе ПЛБ, содержащий двухвалентный металл, например никель, который по принципу Пирсона имеет сродства к азоту и галогенам.
Таким образом, целью данной работы была разработка и охарактеризация нового металл-аффинного сорбента на основе стеарата никеля и исследование возможности специфичной экстракции ряда соединений, имеющих в своем составе азот или хлор.
МАТЕРИАЛЫ И МЕТОДЫ
Получение пленок МХС Ni(II)
В качестве субфазы использовали 10–4 М водный раствор нитрата никеля объемом 1.5 л (для ванны размером 750×140×8 мм). При помощи подвижных барьеров рабочую площадь ограничили до 10 дм2. На субфазу наносили 1 мл насыщенного раствора стеариновой кислоты в н-гексане. После испарения гексана с водной субфазы на поверхности образовывался монослой стеариновой кислоты, который после взаимодействия с ионами субфазы коллапсировали и собирали с поверхности раствора.
Сканирующая электронная микроскопия
Исследования проводили на растровом электронном микроскопе Inspect S ("FEI", США), позволяющем получать изображение поверхности исследуемых объектов с разрешением не хуже 3 нм. В качестве источника для формирования электронного пучка был использован вольфрамовый катод, ускоряющие напряжения были выбраны из диапазона 1–10 кВ, при этом диаметр сфокусированного электронного пучка лежал в диапазоне 1–3 нм.
Стандартизация МХС Ni(II)
По 100 монослоев стеарата металла с минимальными потерями переносили в предварительно взвешенные микропробирки объемом 1.5 мл. При переносе с помощью фильтровальной бумаги максимально удаляли излишек жидкой фазы. Затем микропробирки помещали в вакуумный эксикатор на три дня ( Р = 15 мм.рт.ст.). После чего микропробирки повторно взвешивали и по разнице определяли массу сорбента.
Определение электрокинетического потенциала МХС Ni(II)
В колбу на 50 мл поместили 15 монослоев сорбента. При микроэлектрофоретических исследованиях регуляторами рН служили растворы HCl и KOH. Дисперсию пленок получали в ультразвуковом диспергаторе при частоте 44 МГц в течение 3 мин. Приготовили растворы КCl с различным значением pH для двух концентраций электролита, после чего провели измерения электропроводности и электрофоретической подвижности с помощью прибора Zetaciser NANO ZC.
Построение изотермы адсорбции альбумина курицы на МХС Ni(II)
В микропробирки, каждая из которых содержала по 5 монослоев ПЛБ Ni(II), добавляли 500 мкл раствора белка с различной концентрацией и перемешивали в течение 30 мин. Далее растворы центрифугировали и отбирали по 250 мкл супернатанта, к которому добавляли 1.25 мл реактива Бредфорда и измеряли поглощение при длине волны 595 нм против соответствующего контроля. Концентрацию белка рассчитывали по ранее построенному калибровочному графику.
Металл-аффинная хроматография на МХС Ni(II)
В спиновую колонку (диаметр пор 0.45 нм) поместили 100 дм2 ПЛБ Ni(II), промыли последовательно 100 мкл ацетонитрила, центрифугировали 2 мин при 3000 об./мин, супернатанты отбросили. Затем сорбент промыли 100 мкл 0.1 % водного раствора трифторуксусной кислоты, центрифугировали 2 мин при 3000 об./мин, супернатант также отбросили. После этого в спиновую колонку с сорбентом добавили 50 мкл раствора целевого вещества (концентрация водных растворов глифосата и АМФК 1 мг/мл, дильдрина 1 мкг/мл) и 50 мкл 0.1 % водного раствора трифторуксусной кислоты и оставили на 15 мин, после чего спиновую колонку центрифугировали 5 мин при 3000 об./мин., супернатант отобрали в чистую микропробирку для последующего анализа. К сорбенту добавили 100 мкл 0.1% водного раствора трифторуксусной кислоты для промывки, оставили на 10 мин, после чего микропробирку центрифугировали 5 мин при 3000 об./мин и супернатант отобрали в чистую микропробирку. Элюирование с сорбента проводили последовательно 100 мкл 0.1 % раствора трифторуксусной кислоты в ацетонитриле и при необходимости 100 мкл 0.5 % водного раствора пиперидина с отбором фракций в чистые микропробирки. В случае дильдрина использовали последовательное элюирование следующими растворителями: 100 мкл 0.4 М водного раствора аммиака, 100 мкл 0.015 % ПФОСК в 0.5 % водном растворе пиперидина.
Количественный анализ методом атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой
Количественный анализ глифосата и аминометилфосфоновой кислоты проводили на атомноэмиссионном спектрометре с индуктивно связанной плазмой Optima 2100DV ("Perkin Elmer", США) с использованием многоэлементного стандарта IV-ICPMS-71A 10.00 μg/mL ea: Ag, Al, As, B, Ba, Be, Cd, Ca, Co, Cr, Cs, Cu, Dy, Er, Eu, Fe, Ga, Gd, Ho, K, La, Lu, Mg, Mn, Na, Nd, Ni, P, Pb, Pr, Rb, S, Se, Sr, Th, Tl, Tm, U, V, Yb, Zn ("Inorganic Ventures", США). Параметры анализа: скорость
а б
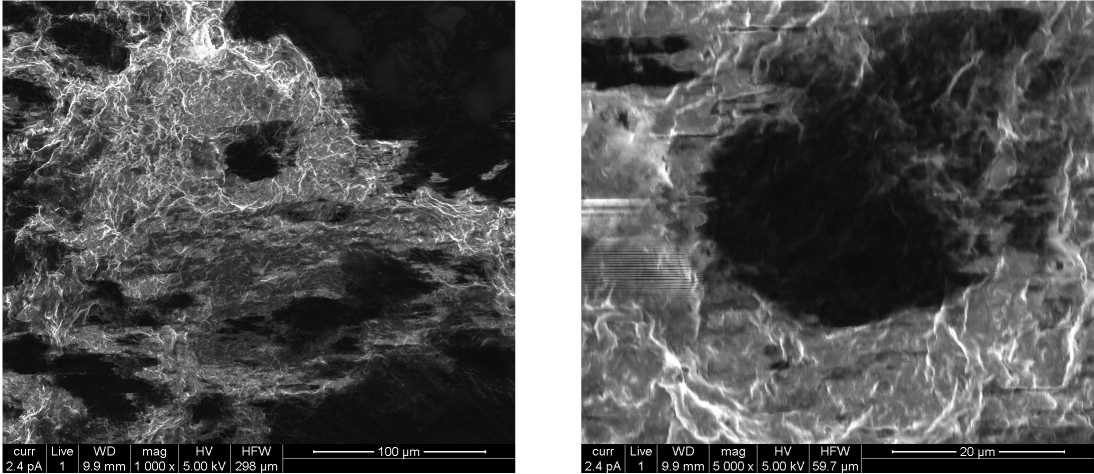
Рис. 1. Микрофотографии структуры коллапсированных пленок МХС Ni(II). а — увеличение в 1000 раз; б — увеличение в 5000 раз
потока образца 1.50 мл/мин; скорость плазмообразующего потока 15 л/мин; скорость вспомогательного потока 0.2 л/мин; скорость распыляющего потока 0.8 л/мин; мощность высокочастотного генератора 1300 Вт; обзор аксиальный; расчет интенсивности — площадь пика; рабочая длина волны для определения фосфора 617 нм.
Количественный хроматографический анализ дильдирина методом ГХ
Количественный анализ дильдрина проводили в следующих условиях: газовый хроматограф Shimadzu GC-2010 с автодозатором АОС-20i. Колонка SPB-608 (30 м × 0.25 мм). Анализ проводили в режиме программирования температур. Начальная температура колонки 90 °С, время удерживания 1 мин, дальнейший подъем температуры до 250 °С со скоростью 10 °С/мин, время удерживания 5 мин, далее подъем температуры до 280 °С со скоростью 5 °С/мин, время удерживания 5 мин. Объем вводимой в хроматограф пробы составлял 1 мкл. Для построения калибровочного графика использовали метод внешнего стандарта.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Металл-хелатный сорбент (МХС) на основе стеарата никеля(II) получали по методу Ленгмюра—Блоджетт. В специальной ванне на поверхность водной субфазы наносили по каплям раствор ПАВ в подходящем неполярном легколетучем органическом растворителе. Раствор ПАВ растекается по поверхности воды, образуя монослой, ограниченный бортами ванны и подвижными барьерами, которые могут регулировать поверхностное давление в образовавшемся монослое.
В качестве субфазы использовали 10–4 М водный раствор нитрата никеля, в качестве ПАВ на субфазу наносили насыщенный раствор стеариновой кислоты в гексане. После испарения гексана с водной субфазы на поверхности образовывался монослой стеариновой кислоты, который после прохождения реакции с ионами субфазы медленно сжимали с помощью подвижных барьеров. При достижении определенного давления монослой коллапсировал (ломался), и отдельные части монослоя наползали друг на друга. Таким образом, были получены многослойные регулярные структуры, состоящие из продуктов взаимодействия стеариновой кислоты с ионами металла субфазы. Полученные частицы собирали с поверхности раствора в микропробирку для дальнейших исследований.
Для установления структуры коллапсированных монослоев Ni(II) препараты были нанесены на кремневую подложку и исследованы методом сканирующей электронной микроскопии (СЭМ).
На представленных фотографиях хорошо видна складчатая структура коллапсированных монослоев стеарата никеля (рис. 1, а), наблюдается мягкость и эластичность складчатых коллапсированных монослоев. Кроме того, при большем увеличении (рис. 1, б) также различимы участки с гладкой поверхностью. Это подтверждает доступность структуры для молекул аналита.
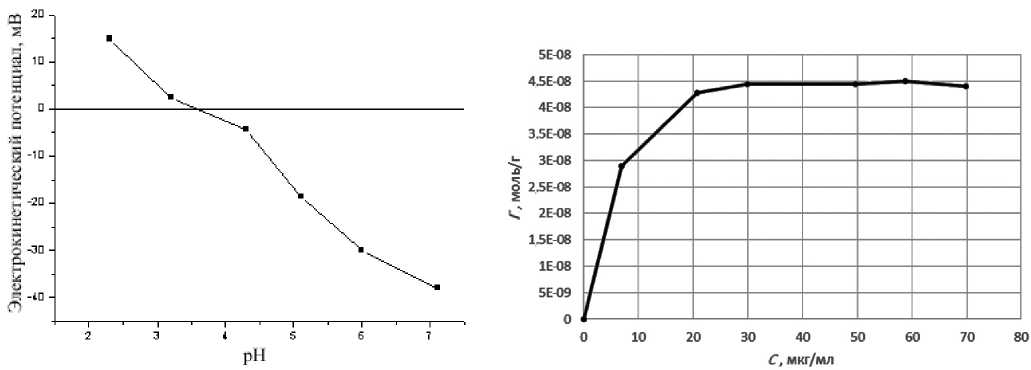
Рис. 3. Изотерма сорбции альбумина курицы на МХС Ni(II)
Рис. 2. Зависимость электрокинетического потенциала МХС Ni(II) от рН раствора KCl 10–4 моль/л
Для определения сорбционных свойств, полученных МХС, необходима информация о его точной массе. Однако в силу специфики метода получения структур, содержащих Ni(II), с высокой точностью определяется площадь, занимаемая пленкой, и соответственно представляется необходимым определить точную массу монослоя определенной площади, что позволит в дальнейшем определять массу сорбента по площади полученного монослоя, т. е. стандартизировать полученные сорбенты. Эксперимент показал, что усредненная масса 1 дм2 составляет 0.022 ± 0.003 мг. В дальнейших экспериментах массу сорбента рассчитывали по площади соответствующего монослоя.
Одним из параметров, характеризующих электрические и структурные свойства поверхности, является электрокинетический потенциал (ξ-потенциал), который измеряли методом микроэлектрофореза в растворе KCl с концентрацией 10–4 моль/л, используя прибор Zetasizer NANO ZC. В ходе эксперимента электрокинетический потенциал определяли по методу микроэлектрофореза и рассчитывали по формуле Гельмгольца— Смолуховского без введения поправок (рис. 2).
Как следует из приведенных данных, в кислой области рН поверхность сорбентов заряжена положительно. По мере уменьшения кислотности среды положительный заряд уменьшается и становится равен нулю при рН ≈ 3.9 (изоэлектрическая точка). При дальнейшем уменьшении кислотности наблюдается рост значений электрокинетического потенциала. На основании полученных данных можно сделать вывод, что успешная сорбция будет проходить в кислой среде при рН ниже изоэлектрической точки.
Для изучения сорбционных свойств полученной структуры было проведено исследование изотермы сорбции альбумина курицы. Результаты представлены на рис. 3. На изотерме сорбции альбумина курицы, наблюдается одно плато, значение предельной сорбции достигается постепенно, и можно сделать вывод, что с точки зрения сорбционных свойств рассматриваемая структура может быть использована в качестве сорбента, т. к. при низких концентрациях аналита наблюдается практически полная сорбция и выход на плато насыщения наступает при достаточно высоких концентрациях белка в исходном образце. Сорбционная емкость МХС Ni(II) по альбумину курицы составила 1.38 мкмоль/г.
Чтобы продемонстрировать возможность использования исследуемой структуры, как металл-хелатного сорбента на стадии пробоподготовки для специфичного выделения аналитов, был проведен эксперимент по экстрации ряда пестицидов из водной среды методом металл-аффинной хроматографии. Как упоминалось выше, никель имеет сродство к таким элементам, как азот и хлор, поэтому в качестве азотсодержащих пестицидов нами были выбраны глифосат и его основной метаболит — аминометилфосфоновая кислота (АМФК), а хлорсодержащего — дильдрин. Исследования проводились в условиях классической металл-аффинной хроматографии.
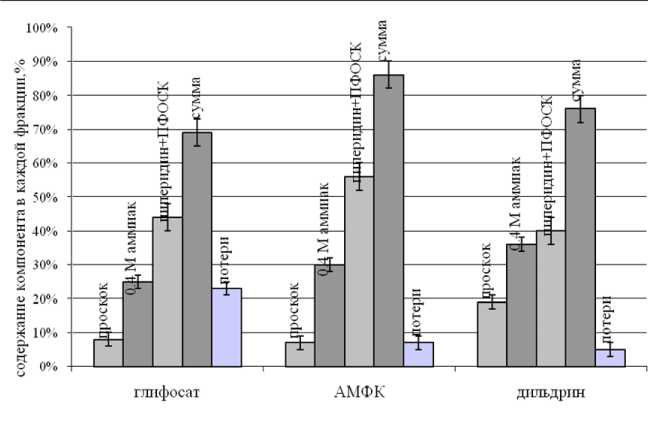
Рис. 4. Диаграмма степеней извлечения глифосата, АМФК и дильдрина из водной среды
Для достижения равновесия в системе сорбент—раствор пестицида проводили инкубирование раствора глифосата, АМФКА и дильдрина с сорбентом в течение 15 мин при постоянном перемешивании. Последовательное элюирование компонентов с сорбента проводили раствором 0.4 М аммиака и 0.015 % раствором перфтороктан-сульфоновой кислоты (ПФОСК) в 0.5 % пиперидине. Количественный анализ проводили с помощью метода ИСП-МС для азотсодержащих пестицидов и ГХ-ЭЗД для дильдрина.
Результаты представлены на рис. 4. На представленных диаграммах показано, что суммарная степень извлечения глифосата, АМФК и дильдри-на из водных растворов составила 69 %, 86 % и 77 % соответственно.
Таким образом, был разработан и охарактеризован новый металл-аффинный сорбент на основе коллапсированных монослоев стеарата никеля(II) и продемонстрирована возможность его использования для выделения ряда пестицидов из водных сред.
Список литературы Разработка металл-хелатного сорбента на основе стеарата никеля (II)
- Кельциева О.А., Гладилович В.Д., Подольская Е.П. Металл-аффинная хроматография. Основы и применение//Научное приборостроение. 2013. Т. 23, № 1. С. 74-85.
- Lv G.S., Hua G.C., Fu X.Y. Expression of milk-derived antihypertensive peptide in Escherichia coli//J. Dairy Sci. 2003. Vol. 86. P. 1 927-1 931 DOI: /10.3168/jds.S0022-0302(03)73779-5
- Stasyk T., Huber L.A. Zooming in: Fractionation strategies in Proteomics//Proteomics. 2004. Vol. 4. P. 3 704-3 716 DOI: /10.1002/pmic.200401048
- Cheung R.F., Wong J.H. Tzi B.N. Immobilized metal ion affinity chromatography:a review on its applications//Appl Microbiol Biotechnol. 2012. Vol. 96. P. 1 411-1 420 DOI: 10.1007/s00253-012-4507-0
- Mateo C., Fernández-Lorente G., Cortés E., et al. One-step purification, covalent immobilization, and additional stabilization of poly-His-tagged proteins using novel heterofunctional chelate-epoxy supports//Biotechnology and Bioengineering. 2001. Vol. 76, no. 3. P. 269-276 DOI: 10.1002/bit.10019
- Lorena O.-M. L., Benavente F., Medina-Casanellas S., et al. Study of immobilized metal affinity chromatography sorbents for the analysis of peptides by on-line solid-phase extraction capillary Electrophoresis-mass spectrometry//Electrophoresis. 2015. Vol. 36, no. 6. P. 962-970 DOI: 10.1002/elps.201400374
- Porath J., Carlsson J., Olsson I., Belfrage G. Metalchelate affinity chromatography. A new approach to protein fractionation//Nature. 1975. Vol. 258. P. 598-599 DOI: 10.1002/elps.201400374
- Ковальчук М.В., Клечковская В.В., Фейгин Л.А. Молекулярный конструктор Ленгмюра-Блоджетт//Природа. 2003. Т. 11. С. 11-19.
- Суходолов Н.Г., Гладилович В.Д., Колоницкий П.Д. и др. Исследование электрокинетических свойств регулярных мультимолекулярных сорбентов на основе стеаратов трехвалентных металлов//Научное приборостроение. 2013. Т. 23, № 1. С. 123-129.
- Кельциева О.А., Гладилович В.Д., Прусаков А.Н. и др. Регулярные мультимолекулярные сорбенты (РММС). Получение, изучение поверхностных и сорбционных свойств//Научное приборостроение. 2012. Т. 22, № 4. С. 50-55.
- Гладилович В.Д., Шрейнер Е.В., Дубровский Я.А. и др. Исследование специфичных свойств регулярного мультимолекулярного сорбента Fe(III)//Научное приборостроение. 2013. Т. 23, № 1. С. 106-114.


