Разработка методики количественного определения Зовиракса
Автор: Илларионова Елена Анатольевна, Иноземцев Павел Олегович, Сыроватский Игорь Петрович
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Медицина
Статья в выпуске: SC, 2012 года.
Бесплатный доступ
Разработана унифицированная методика спектрофотометрического определения зовиракса (ацикловира) в субстанции, отличающаяся использованием в качестве образца сравнения калия феррицианида. Обоснованы оптимальные условия определения: растворитель - 0,1 М раствор натрия гидроксида, аналитическая длина волны - 261 нм. Определены коэффициенты пересчета. Относительное стандартное отклонение разработанной методики для субстанции составило 0,005.
Спектрофотометрия, внешний образец сравнения, коэффициент пересчета, зовиракс, ацикловир, калия феррицианид
Короткий адрес: https://sciup.org/148181425
IDR: 148181425 | УДК: 543.42.062
The development of the methodology of quantitation determination of Zovirax
A unified procedure has been developed for the spectrophotometric determination of zovirax (aciclovir) in the substance using potassium ferrocyanide as reference sample. The best conditions for substance determination have been substantiated as follows: 0,1M NaOH as a solvent and an analytical wavelength of 261 nm. The coefficients of recalculation have been determined. The relative standard deviation of the developed methodology is 0,005 for the substance.
Текст научной статьи Разработка методики количественного определения Зовиракса
Одними из широко применяемых в медицине лекарственных средств являются производные пу- рина, обладающие противовирусным действием [2]. Одним из таких препаратов является зовиракс, или ацикловир (2-амино-1,9-дигидро-9-[(2-гидроксиэтокси)-метил]-6Н-пурин-6-OH) .
ацикловир
Частое применение этого препарата требует особого внимания к его качеству. Анализ НД показал, что для количественного определения ацикловира применяется ацидиметрия в среде ледяной уксусной кислоты и уксусного ангидрида, являющаяся высокотоксичным методом [1]. Цель настоящего исследования разработать новую методику количественного определения зовиракса спектрофотометрическим методом с использованием внешнего образца сравнения.
Материалы и методы
В работе использовали: субстанцию ацикловира, отвечающую требованиям нормативного документа, калия феррицианид (чда), 0,1 М раствор натрия гидроксида, приготовленный из фиксанала, 0,1 М раствор кислоты хлористоводородной, приготовленный из фиксанала, спирт этиловый 95%.
Электронные спектры регистрировали на спектрофотометре Specord UV VIS. Оптическую плотность растворов измеряли на спектрофотометрах СФ-26 и СФ-46 в кюветах 1 см на фоне растворителя. Величину рН контролировали с помощью универсального ионометра ЭВ-74.
Результаты исследований обработаны статистически с использованием пакета программ Microsoft Excel для Windows XP. Проверка распределения, которому подчиняются результаты исследования, дала возможность использовать для анализа критерий Стьюдента. Критический уровень значимости при проверке статистических гипотез Р = 0,05.
Результаты и обсуждение
С целью оптимизации условий спектрофотометрического определения ацикловира нами были изучены спектры поглощения растворов ацикловира в интервале рН 1,1-13,0 (рис. 1).
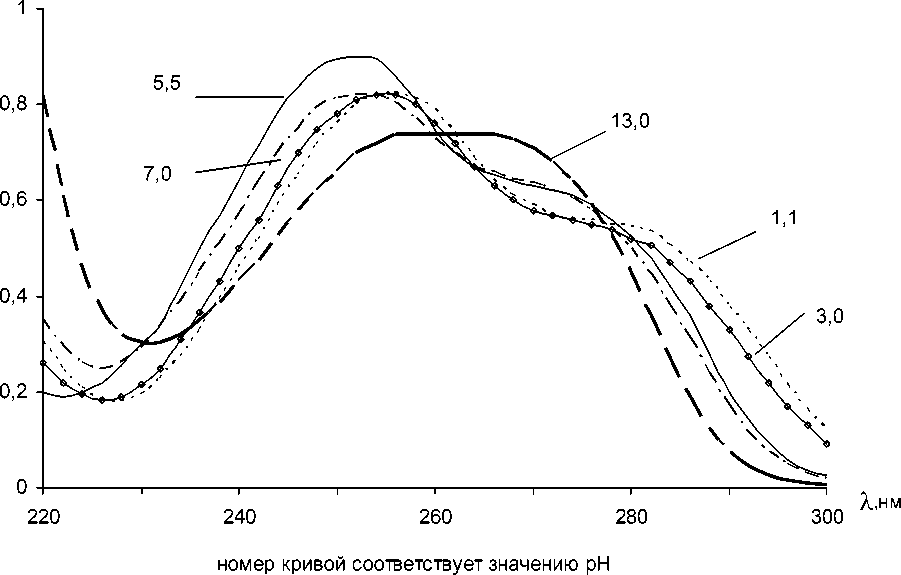
Рис. 1. УФ-спектр поглощения 0,0015% раствора ацикловира
Из приведенных экспериментальных данных видно, что при рН 1,1-3,0 спектр поглощения ацикловира характеризуется одной полосой поглощения с максимумом при длине волны 256±1нм. При увеличении рН от 5,5 до 7,0 происходит гипсохромный сдвиг максимума поглощения до 251 нм, а затем при рН 8,0-13,0 наблюдается постепенный батохромный сдвиг максимума и уширение полосы поглощения. Следует отметить, что при рН 1,1-3,0 спектр поглощения ацикловира характеризуется наличием «плеча» в области 274-277 нм, а при рН 5,5-7,0 – в области 265-275 нм.
Изучение стабильности растворов ацикловира (рис. 2) показало, что наиболее устойчив раствор ацикловира с рН 13,0. Поэтому в качестве оптимального растворителя для спектрофотометрического определения ацикловира нами выбран 0,1М раствор гидроксида натрия (рН 13,0).
Методом наименьших квадратов было рассчитано уравнение градуировочного графика ацикловира при оптимальных условиях (растворитель – 0,1М раствор гидроксида натрия, λ max =261 нм): А=(0,038±0,001)С, S A =0,014 (А – оптическая плотность, С – концентрация, мкг/мл).
Аналитическая длина волны ацикловира (261 нм) входит в интервал, оптимальный для феррицианида калия (255-267 нм) [4]. Следует отметить, что у феррицианида калия и ацикловира совпадают максимумы поглощения, и они имеют общий оптимальный растворитель – 0,1М раствор гидроксида натрия. Следовательно, можно предположить, что погрешность анализа ацикловира при отмеченных выше оптимальных условиях не будет превышать допустимую.
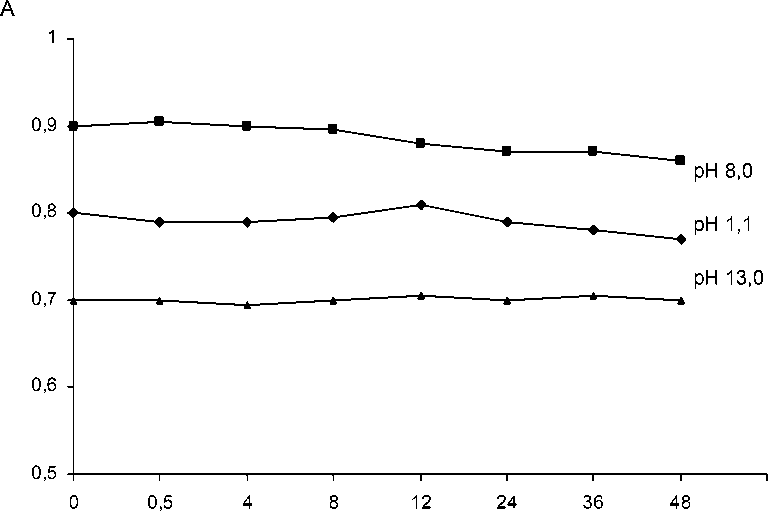
Рис. 2. Зависимость оптической плотности растворов ацикловира от времени хранения
время, ч
В связи с тем, что удельные показатели поглощения ацикловира и феррицианида калия не совпадают, необходимо рассчитать коэффициент пересчета [3]. Результаты экспериментальных исследований по определению коэффициента пересчета ацикловира по феррицианиду калия представлены в табл. 1.
Таблица 1 Результаты определения коэффициента пересчета для спектрофотометрического анализа ацикловира по внешнему образцу сравнения феррицианиду калия
|
а ос |
А ос |
1% 1 см ос |
а вос |
А вос |
1% 1 см вос |
К пер |
Метрологические характеристики (n=10, Р=95%) |
|
0,0932 |
0,4535 |
486,59 |
0,1447 |
0,5735 |
39,63 |
0,0815 |
К =0,0813 |
|
0,1025 |
0,4921 |
480,10 |
0,1447 |
0,5638 |
38,96 |
0,0812 |
S2=0,0000001 |
|
0,0992 |
0,4763 |
480,14 |
0,1403 |
0,5452 |
38,86 |
0,0809 |
S=0,0003 |
|
0,1021 |
0,5017 |
491,38 |
0,1381 |
0,5528 |
40,03 |
0,0815 |
S х =0,0001 |
|
0,1019 |
0,4935 |
484,30 |
0,1340 |
0,5302 |
39,57 |
0,0817 |
Δ Х =0,0002 |
|
0,1011 |
0,4881 |
482,79 |
0,1395 |
0,5452 |
39,08 |
0,0810 |
Е%=0,24 |
|
0,1003 |
0,4841 |
482,65 |
0,1365 |
0,5361 |
39,27 |
0,0814 |
S r =0,003 |
|
0,1020 |
0,4962 |
486,47 |
0,1451 |
0,5751 |
39,63 |
0,0815 |
|
|
0,0981 |
0,4711 |
480,22 |
0,1407 |
0,5467 |
38,86 |
0,0809 |
|
|
0,0926 |
0,4559 |
492,33 |
0,1385 |
0,5544 |
40,03 |
0,0813 |
Разработанные условия спектрофотометрического определения ацикловира позволили предложить методику количественного определения ацикловира в субстации.
Методика количественного определения ацикловира в субстанции по феррицианиду калия либо по рабочему стандартному образцу (РСО) ацикловира: точную массу препарата (0,1000 г) помещают в мерную колбу вместимостью 100 мл, растворяют в 20 мл воды, доводят объем раствора водой до метки и перемешивают. 1 мл полученного раствора помещают в мерную колбу вместимостью 100 мл, доводят объем раствора до метки 0,1М раствором гидроксида натрия и перемешивают. Измеряют оптическую плотность испытуемого раствора на спектрофотометре при длине волны 261 нм в кювете с длиной рабочего слоя 10 мм. В качестве раствора сравнения применяют 0,1М раствор гидроксида натрия. Параллельно измеряют оптическую плотность раствора внешнего образца сравнения феррицианида калия либо РСО ацикловира.
Методика приготовления раствора внешнего образца сравнения феррицианида калия : точную массу феррицианида калия (0,1400 г) помещают в мерную колбу вместимостью 100 мл, растворяют в 20 мл 0,1М раствора гидроксида натрия, доводят объем раствора этим же растворителем до метки и перемешивают. 5 мл полученного раствора помещают в мерную колбу вместимостью 50 мл, доводят объем раствора 0,1М раствором гидроксида натрия до метки и перемешивают.
Методика приготовления РСО ацикловира аналогична методике приготовления анализируемого образца ацикловира. Результаты количественного определения ацикловира в субстанции представлены в таблице 2.
Таблица 2 Результаты спектрофотометрического определения ацикловира по внешнему образцу сравнения феррицианиду калия и по РСО ацикловира
|
№ серии |
Образцы сравнения |
Метрологические характеристики (n=10, P=95%) |
||||||
|
Х |
S 2 |
S |
S х |
Δ Х |
Е% |
S r |
||
|
031002 |
феррицианид калия |
99,81 |
0,2525 |
0,5025 |
0,1899 |
0,47 |
0,47 |
0,005 |
|
ацикловир |
99,73 |
0,2486 |
0,4986 |
0,1884 |
0,46 |
0,46 |
0,005 |
|
|
051202 |
феррицианид калия |
99,76 |
0,1697 |
0,4120 |
0,1557 |
0,38 |
0,38 |
0,004 |
|
ацикловир |
99,83 |
0,2678 |
0,5175 |
0,1956 |
0,48 |
0,48 |
0,005 |
|
|
010103 |
феррицианид калия |
99,87 |
0,2714 |
0,5210 |
0,1969 |
0,48 |
0,48 |
0,005 |
|
ацикловир |
99,89 |
0,2174 |
0,4662 |
0,1762 |
0,43 |
0,43 |
0,005 |
|
Анализ приведенных результатов показывает, что при спектрофотометрическом определении ацикловира по внешнему образцу сравнения феррицианиду калия и по РСО ацикловира получены сопоставимые результаты. Относительная погрешность определения не превышает 0,48%. Методика спектрофотометрического определения с использованием внешнего образца сравнения характеризуется хорошей воспроизводимостью (S r не превышает 0,005) [5]. Проведена сравнительная оценка разработанной методики с методикой нормативного документа, которая показала преимущества методики спектрофотометрического определения по внешнему образцу сравнения: доступность, экс-прессность, высокая воспроизводимость, отсутствие высокотоксичных реактивов.


