Разработка ПЦР-тест системы для выявления вируса картофеля Y
Автор: Бессолицына Е.А., Тулинов А.Г., Новоселова Н.В., Харина А.В.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Растениеводство
Статья в выпуске: 7 (65), 2023 года.
Бесплатный доступ
Вирус картофеля Y поражает растения картофеля, нанося серьезный урон сельскому хозяйству за счет снижения урожайности данной культуры. Поэтому существует необходимость выявления данного возбудителя. Вирусы картофеля РНК-содержащие, поэтому могут быть использованы иммунологические методы или ПЦР, совмещенный с обратной транскрипцией. В ходе данной работы была разработана основа для ПЦР-тест системы для выявления вируса картофеля Y. Подобраны праймеры для реакции обратной транскрипции и последующей ПЦР, рассчитаны температуры отжига и размер амплифицируемого фрагмента. Проверены праймеры и условия реакции на растительном материале. Получены ПЦР-продукты рассчитанного размера. Определение их нуклеотидной последовательности подтвердило выявление генетического материала вируса картофеля Y. Таким образом, данная ПЦР-тест система может быть использована для выявления вируса картофеля Y.
Картофель, диагностика заболеваний, вирус y, праймеры, пцр-диагностика, пцр-тест система, обратная транскрипция
Короткий адрес: https://sciup.org/149144400
IDR: 149144400 | УДК: 578.85/.86 | DOI: 10.19110/1994-5655-2023-7-5-11
Development of a PCR test system for the detection of potato virus Y
Potato virus Y infects potato plants and causes serious damage to agriculture by reducing the yield of this crop. Therefore, there is a need to identify this pathogen. Potato viruses contain RNA, so immunological methods or PCR combined with reverse transcription can be used. The aim of this work was to develop a PCR test system for the detection of Potato virus Y. Primers for the reverse transcription reaction and subsequent PCR were found. Annealing temperatures and size of the amplified fragment were calculated. Primers and reaction conditions on plant material were tested. PCR products of the calculated size were obtained. The determination of their nucleotide sequence confirmed the identification of the genetic material of Potato virus Y. Thus, this PCR test system can be used to detect Potato virus Y.
Текст научной статьи Разработка ПЦР-тест системы для выявления вируса картофеля Y
В настоящее время известно 52 вида вирусов, поражающих картофель [1]. В Российской Федерации (далее – РФ) пять наиболее опасных видов: вирус картофеля Y (PVY), вирус картофеля X (PVX), вирус скручивания листьев (PLRV) и вироид веретеновидности клубней (PSTVd). Менее опасными, но при этом увеличивающими потери урожая при совместном заражении с другими вирусами, являются вирусы картофеля М и S (PVM и PVS соответственно) [2].
Вирус картофеля Y вызывает серьезные потери урожая картофеля (до 30 % и более в зависимости от времени воздействия, типа вируса, устойчивости сорта растения-хозя- ина), причем он поражает не только картофель, но и другие сельскохозяйственные культуры как в РФ, так и в других регионах планеты. Все эти факторы делают вирус картофеля Y экономически важным фитопатогеном [3, 4].
Вирус картофеля Y относится к роду Potyvirus, семейству Potiviridae. Вирусные частицы нитевидные, размер составляет 730×11 нм, осаждаются как единый компонент с коэффициентом седиментации около 150S [5]. Геном представлен одноцепочечной позитивной молекулой РНК, длина которой составляет 9.7 тыс. нуклеотидов, 5’-конец РНК ковалентно соединен 5’-концевым терминальным белком (Vpg), на 3’-конце располагается полиА-тракт [6]. Молекула РНК содержит 10 открытых рамок считывания, транслируемых одним полибелком [7].
Вирус картофеля Y передается при контакте поврежденных клубней, а также через семена. Другим агентом распространения вируса являются тли [8].
Симптомы заражения вирусом картофеля Y вариабельные и зависят от таких факторов, как штамм вируса, сорт и условия выращивания растения-хозяина. Может развиваться резкий некроз вдоль жилок, вплоть до полного отмирания листьев. Некроз может быть мозаичным, и сопровождаться морщинистостью листьев, которая может проявляться и без некротических изменений [9].
Множественность путей распространения вируса, вариабельность симптомов выявляют необходимость разработки достаточно быстрого, точного, чувствительного метода для выявления вируса как в организме растения-хозяина, так и в организмах переносчиков.
В настоящее время обычно используется метод имму-ноферментного анализа (далее – ИФА) – это высокоточный и высокочувствительный метод, но он достаточно дорог, и для него может быть использован только свежий материал [10]. Второй метод, активно используемый для выявления возбудителей заболеваний, – метод ПЦР, но его классический вариант нельзя применять, так как матрицей для ПЦР является молекула ДНК, а вирус картофеля Y (PVY) РНК-содержащий. Но существует модификация метода ПЦР – обратная транскрипция ПЦР (далее – ОТ-ПЦР), которая позволяет выявлять РНК различных возбудителей [там же]. Метод ОТ-ПЦР по себестоимости сопоставим с иммуноферментным анализом, но позволяет работать не только со свежим, но и фиксированным материалом.
Цель данной работы – разработка ПЦР-тест системы для выявления вируса картофеля Y в растительном ма- териале. Разработка включает в себя подбор структуры праймеров, условий реакции ОТ-ПЦР, анализ размера амплифицируе-
мого фрагмента, воспроизведение ОТ-ПЦР на растительном материале, определение нуклеотидной последовательности полу- ченного фрагмента, что является подтверждением того факта, что данная ПЦР-тест система выявляет именно наличие РНК вируса картофеля Y.
Материалы и методы
Последовательности геномов вируса картофеля Y (PVY) были скопированы из базы данных Genome, Nucleotide (www. . Названия последовательностей и их паспортные номера представлены в табл. 1.
Данные последовательности были проанализированы в программе AliBee - Multiple alignment Release 3.0 на сайте В выявленных консервативных участках отби- рали фрагменты 20–25 нуклеотидов, начинающиеся и заканчивающиеся на гуанин или цитозин (предполагаемые праймеры, представленные в табл. 2). Далее для праймеров проводился расчет температуры отжига по формуле:
Тотжига = (2×(количество аденина + тимина) + (1) 4×(количество гуанина + циозина)) – 5 .
Также в программе Nucleotide blast ( gov) проверялась уникальность праймеров и присваивался номер от 0 – последовательность не выявляется в нужных видах и генах, до 10 – последовательность выявляется только в геноме вируса и больше нигде.
Из табл. 1 были выбраны два уникальных праймера (уровень уникальности – от 8 и выше) с одинаковыми температурами отжига (допускаются различия температуры отжига до 2 оС), которые были синтезированы в фирме Синтол.
В качестве источника нуклеиновых кислот использовались пазушные почки клубня картофеля и покровная ткань вокруг них. Суммарные нуклеиновые кислоты выделялись с помощью модификации гуанидин-изотиоцианатного метода [11].
Реакцию обратной транскрипции проводили следующим образом: 50 нг РНК растворяли в 4 мкл воды, добавляли по 1 мкл обратного праймера в концентрации 40 рМ/мкл, прогревали при 95 оС 5 мин, затем добавляли 1 мкл 10Х буфера для обратной транскрипции, 1 мкл смеси dNTPs (концентрация 4 мкМ), 1 мкл обратной транскриптазы MMLV (15 е.а./мкл) (Сибэнзим) и деионизированную воду до 10 мкл. Полученную смесь инкубировали при 37 оС 1 ч 10 мин. Затем переосаждали и вносили на реакцию ПЦР: 2 мкл раствора матрицы после обратной транскрипции, 1 мкл буфера для ПЦР с 1.5 мМ MgCl2, 0.5 мкл смеси dNTPs
Таблица 1
Названия изолятов вируса картофеля Y (PVY) и их идентификационные номера в базе данных Genome, Nucleotide
Table 1
Names of Potato virus Y (PVY) isolates and their identification numbers in the database Genome, Nucleotide
|
№ |
Название |
Идентификационный номер |
|
1 |
Potato virus Y isolate May4B, complete genome |
MK563993 |
|
2 |
Potato virus Y isolate Egypt35 polyprotein gene, complete |
KY863551 |
|
3 |
Potato virus Y isolate Egypt7 polyprotein gene, complete cds |
KY863549 |
|
4 |
Potato virus Y isolate Egypt11 polyprotein gene, complete cds |
KY863548 |
|
5 |
Potato virus Y isolate VarB, complete genome |
KT290512 |
|
6 |
Potato virus Y isolate VarA, complete genome |
KT290511 |
|
7 |
Potato virus Y isolate GF_YL20, complete genome |
KJ634023 |
|
8 |
Potato virus Y genomic RNA, complete genome, isolate: T13 |
AB714135 |
|
9 |
Potato virus Y isolate WWA150131_G4_8, complete genome |
MT200673 |
|
10 |
Potato virus Y isolate MT12_Oth288, complete genome |
MT200671 |
|
11 |
Potato virus Y isolate BL2, complete genome |
MT200669 |
|
12 |
Potato virus Y strain N, complete genome |
MT350290 |
|
13 |
Potato virus Y strain O, complete genome |
MT350288 |
|
14 |
Potato virus Y isolate P097, complete genome |
MT264732 |
|
15 |
Potato virus Y isolate PVYO_R3S16L8, complete genome |
MK572844 |
|
16 |
Potato virus Y isolate PVYN_O_R3S2L8, complete genome |
MK572835 |
(концентрация 4 мкМ), по 1 мкл праймеров, концентрация каждого 10 рМ/мкл, 0.75 мкл Taq-полимеразы (5 ед.а./мкл) (Сибэнзим) и деионизированную воду до 10 мкл. Реакция ПЦР состоит из трех этапов 1-й и 3-й состоят из одного цикла, так как не требуется циклическое изменение температуры. Продукты реакции амплификации разделяли в 6 %-ной нативном полиакриламидном геле, который окрашивался бромистым этидием [там же].
ПЦР-продукты экстрагировали из геля [там же] и определяли нуклеотидную последовательность в фирме Евроген. Полученные результаты сравнивали в программе Nucleotide blast ( с уже имеющимися
Последовательности, использованные для праймеров, их положение в геноме, длина, температура отжига и степень уникальности
Table 2
Sequences used for primers, their position in the genome, length, annealing temperature and degree of uniqueness
|
№ |
Вирус |
Положение праймера |
Последовательность |
T, отжига , °С |
Уникальность 0–10 |
|
1 |
PVY |
2130 – 2157 |
GACATGTGTGTGCCAAAGCTTGGAACC |
59 |
8 |
|
2 |
PVY |
2140 – 2166 |
GTGCCAAAGCTTGGAACCTGGCCAAC |
60 |
7 |
|
3 |
PVY |
2220 – 2244 |
CATGATGCAGAACTGCCTAGAATA |
52 |
7 |
|
4 |
PVY |
2434 – 2457 |
ATATCACCTTTCAGAGAAGGAGG |
52 |
9 |
|
5 |
PVY |
2811 – 2835 |
GATGGTGTTGCAAGTTGTTAAGAA |
50 |
7 |
|
6 |
PVY |
2962 – 2983 |
GAAAAATTATCCGCAACATGG |
47 |
7 |
|
7 |
PVY |
3163 – 3189 |
AATATTTCATCCTTTTTCATTCGTAG |
48 |
7 |
|
8 |
PVY |
3683 – 3705 |
AGGGGAGCTGTTGGGTCTGGAA |
57 |
7 |
|
9 |
PVY |
4480 – 4503 |
GTTGATGGCAGAACAATGAAGCA |
52 |
7 |
|
10 |
PVY |
4948 – 4976 |
GATGGATCAATGCATCCTGTCATACATG |
56 |
7 |
|
11 |
PVY |
4959 – 4986 |
GCATCCTGTCATACATGACATTCTTAA |
53 |
7 |
|
12 |
PVY |
5323 – 5346 |
CAGAGCCAATTCAGAAGTCTCAT |
52 |
7 |
|
13 |
PVY |
5349 – 5377 |
GAAGGATGCTCAAGCATGTTTTCAATTG |
55 |
7 |
|
14 |
PVY |
5806 – 5833 |
GAATTCTTTGGATCTGCATACAGGAA |
53 |
7 |
|
15 |
PVY |
5857 – 5884 |
GTTGGTATGGGCAAGTCAAGCAGGAGG |
60 |
7 |
|
16 |
PVY |
6085 – 6111 |
TACTTCAGGAAAGATTGGTCTGACAA |
53 |
8 |
|
17 |
PVY |
7152 – 7175 |
TTCTTCAGGCCTTTGATGGATGC |
53 |
7 |
|
18 |
PVY |
7562 – 7586 |
GGACATTCACTGCTGCACCTTTAG |
55 |
7 |
|
19 |
PVY |
7804 – 7829 |
AGAAGCACATACATGGAAGATTGGG |
54 |
7 |
|
20 |
PVY |
7832 – 7857 |
TGGGGTTGCAAATGTTGCGCAATTT |
54 |
7 |
|
21 |
PVY |
7885 – 7908 |
TCAACTCCAGATGGAACAATTGT |
50 |
7 |
|
22 |
PVY |
8346 – 8374 |
CACCAAATCAGGAGATTCTACTCATGGT |
56 |
7 |
|
23 |
PVY |
8567 – 8591 |
ACACAATCGATGCAGGAGGAAGCA |
55 |
8 |
|
24 |
PVY |
8703 – 8730 |
GCTATCACGTCCAAAATGAGAATGCCC |
57 |
8 |
|
25 |
PVY |
8812 – 8839 |
GCAACTCAATCACAGTTTGATACGTGG |
56 |
7 |
|
26 |
PVY |
8900 – 8927 |
GGCTTATGGTTTGGTGCATTGAAAATG |
54 |
7 |
|
27 |
PVY |
8907 – 8935 |
GGTTTGGTGCATTGAAAATGGAACCTCG |
58 |
8 |
|
28 |
PVY |
8942 – 8969 |
CAACGGAGTTTGGGTTATGATGGATGG |
57 |
9 |
|
29 |
PVY |
8992 – 9019 |
TGAAACCAATCGTTGAGAATGCAAAAC |
53 |
8 |
|
30 |
PVY |
9025 – 9051 |
CTTAGGCAAATCATGGCACATTTCTC |
54 |
8 |
|
31 |
PVY |
9038 – 9065 |
TGGCACATTTCTCAGATGTTGCAGAAG |
56 |
8,5 |
|
32 |
PVY |
9051 – 9079 |
GATGTTGCAGAAGCGTATATAGAAATGC |
55 |
8 |
|
33 |
PVY |
9080 – 9108 |
GCAACAAAAAGGAACCATATATGCCACG |
56 |
8 |
|
34 |
PVY |
9094 – 9118 |
CCATATATGCCACGATATGGTTTA |
50 |
8 |
|
35 |
PVY |
9208 – 9231 |
CACATTCAAATGAAGGCCGCAGC |
55 |
8 |
|
36 |
PVY |
9272 – 9300 |
AACACAGAGAGGCACACCACCGAGGATG |
62 |
8 |
|
37 |
PVY |
9322 – 9351 |
TCTCCAAGTATGCATACTCTACTTGGAGT |
56 |
8,5 |
в них последовательностями генома различных изолятов вируса картофеля Y.
Результаты и их обсуждение
Вирус картофеля Y имеет белковый капсид, протеоме-ры которого могут быть использованы для детекции вируса в растительных тканях методом иммуноферментного анализа, однако этот метод достаточно дорог. Метод ПЦР дешевле, при этом имеет сопоставимые чувствительность и точность. Но геном вируса представлен молекулой РНК. Данная молекула не может быть матрицей для стандартного метода ПЦР. Поэтому был выбран метод обратной Таблица 2 транскрипции с последующей полимеразной цепной реакцией.
Для выявления РНК вируса PVY необходимо разработать праймеры. Для этого в базе данных ( gov) было выбрано 16 последовательностей полных геномов различных изолятов вируса картофеля Y. Последовательности полных геномов использовали для большей простоты выравнивания и получения максимального количества фрагментов последовательности РНК вируса, которые можно было бы использовать в качестве праймеров.
Названия изолятов и их номера в базе данных представлены в табл. 1.
Так как геном вируса представляет собой мРНК (+ цепь РНК), кодирующую один полибелок, который транслируется, а затем разрезается на отдельные субъединицы, выбор открытых рамок считывания, кодирующих отдельный белок, не производился, а анализу подвергались нуклеотидные последовательности всего генома.
Далее последовательности были проанализированы в программе AliBee - Multiple alignment Release 3.0 на сайте В результате сравнения последовательностей выявлены идентичные у всех исследованных изолятов участки геномов, в которых выбирали последовательности для будущих праймеров. Последовательности для праймеров должны быть длиной 20–25 нуклеотидов, начинаться и заканчиваться на гуанин или цитозин.
Затем с помощью формулы (1) были рассчитаны температуры отжига, а также посчитано количество нуклеотидов во всех фрагментах. Далее в программе Nucleotide blast ( проверяли уникальность праймеров. Для этого сравнивали исследуемую последовательность с уже имеющимися в базе. В зависимости от уникальности исследу- емым последовательностям присваивалось значение уникальности от 10 (обнаруживается только в геномах различных изолятов вируса картофеля Y) до 0 (не обнаруживается в геномах PVY, но выявляется в геномах других организмов).
Последовательности и их положение в геноме, температура отжига, количество нуклеотидов и его уникальность представлены в табл. 2.
Наибольшей степенью уникальности обладают фрагменты под №№ 28 (уникальность – 9), 31 и 37 (уникальность – 8.5), но у фрагмента № 28 температура отжига составила 57 °С. Фрагменты №№ 31 и 37 имеют одинаковую температуру отжига (56 °С). Поскольку в температурах отжига допускается различие до 2 °С, все три фрагмента могут быть использованы в качестве праймеров, но также необходимо учитывать размер ПЦР-продукта. Оптимальным для разделения с помощью гель-электрофореза в полиакриламидном геле являются фрагменты ДНК длиной от 150 до 300 пар нуклеотидов. Фрагменты №№ 28 и 31 будут образовывать ПЦР-продукт длиной 158 пар нуклеотидов, такая длина ближе к нижней границе оптимума. Пары фрагментов №№ 28/37 и №№ 31/37 будут образовывать фрагменты длиной 451 и 313 пар нуклеотидов. Соответственно, такие фрагменты длиннее оптимальных.
Поэтому были рассмотрены фрагменты с №№ 32 по 36, их уникальность составила 8. По температуре отжига совпал фрагмент № 33, у остальных температура отжига не совпадает больше допустимых различий. Определение длины ПЦР-продукта показало, что для пары №№ 33 и 37 она будет составлять 271 пару нуклеотидов, которая попадает в пределы оптимальных длин фрагмента.
Следует отметить, что фрагмент № 4 (уникальность – 9) не рассматривался в связи с далеким расположением от фрагмента № 28, с вероятностью не получить ампликон обычными методами и низкой уникальностью соседнерасположенных фрагментов.
Таким образом, последовательности №№ 33 и 37 были использованы для создания праймеров.
Как видно из результатов гель-электрофореза, положительный результат выявлен в образце № 1. В дорожке 1 видна единственная четкая полоса чуть ниже полосы маркера длиной 300 пар нуклеотидов. Также слабо светящаяся полоса на том же уровне присутствует в дорожке 6 (образец картофеля № 6). Наличие полос означает, что праймеры провзаимодействовали с матрицей, а размер полученного фрагмента ДНК соответствует ожидаемому. Эти факты позволяют предполагать, что в образцах картофеля №№ 1 и 6 присутствует РНК вируса PVY. Тогда как в других образцах вирус отсутствует. Отсутствие дополнительных полос на дорожках 1 и 6 указывает на то, что праймеры отжигаются только на одном участке в образце нуклеиновых кислот, что подтверждает высокую степень уникальности, которая была определена теоретически. Отсутствие одинаковых полос во всех образцах подтверждает отсутствие реакции праймеров с РНК хозяина, а также их уникальность.
Кроме того, задачей являлась оценка возможности использовать данные праймеры в существующих условиях реакции ПЦР для выявления вируса картофеля Y.
Так как положительный контроль – образец ткани картофеля, зараженного вирусом Y, отсутствовал, проверку того, что данный амплифицированный фрагмент и есть ДНК-копия генома вируса картофеля Y, проводили, определяя нуклеотидную последовательность полученного ПЦР-продукта.
Образец РНК № 1 использовали для получения ПЦР-про-дукта, который был очищен и отправлен на определение нуклеотидной последовательности в фирму Евроген.
Таблица 3
Последовательность праймеров для выявления вируса картофеля Y (PVY)
Table 3
Potato virus Y (PVY) primer sequence
|
Название праймера |
Последовательность праймера |
T, отжига , °С |
Размер ПЦР-продукта |
|
PVY 1 F |
5’ - GCAACAAAAAGGAACCATATATGCCACG - 3’ |
56 |
271 п.н. |
|
PVY 1 R |
5’ - ACTCCAAGTAGAGTATGCATACTTGGAGA - 3’ |
56 |
Название и последовательность, температура отжига праймеров представлены в табл. 3, а также предполагаемый размер ПЦР-продукта, рассчитанный по последовательности генома вируса.
Праймеры после обработки были заказаны в фирме Синтол. Далее проводилась проверка работы праймеров в реальных условиях. Для анализа использованы образцы пазушных почек клубней картофеля, так как растущие ткани более пригодны для выделения нуклеиновых кислот как ткани с меньшим размером клеточных стенок и большим объемом генетического материала. Клубни были предоставлены с фермерского поля в Куменском районе Кировской области.
Выбрано восемь клубней с прорастающими пазушными почками, из которых брался материал для обратной транскрипции и ПЦР. Продукты реакции визуализировали методом электрофореза в нативном полиакриламидном геле. Полученный результат представлен на рис. 1.
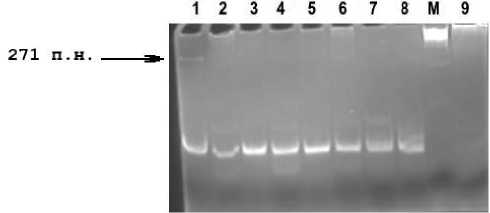
Рисунок 1. Гель-электрофорез в 6 %-ном нативном полиакриламидном геле, продуктов реакции ОТ-ПЦР на наличие вируса PVY. Дорожки 1–8 – реакции с образцами картофеля №№ 1–8; № 9 – отрицательный контроль; М – маркер длин фрагментов ДНК (Сибэнзим). Ожидаемый размер ПЦР-продукта PVY – 271 п.н.
Figure 1. Gel electrophoresis in 6 % native polyacrylamide gel of the RT-PCR reaction products for the presence of PVY. Lanes 1–8 – reactions with potato samples № 1 – № 8; № 9 – negative control; M – marker of DNA fragment lengths (Sibenzyme). The expected size of the PVY PCR product is 271 bp.
Получена следующая последовательность нуклеотидов: TGGCATTCTCATTTTGGACGTGATAGCTAAGCCTAAATATGCAA TGCAGGGATATTTACAATTTTTTATAAAAACACCCAGACCAAAACA AGTATCAACAGTCTGCTTCCTCCTGCATCGATTGTGTCA.
Она короче, чем размер ПЦР-продукта, так как секвенирование ПЦР-продуктов затруднено, поэтому в текстовый редактор переведен только тот участок, в котором были наиболее точные результаты капиллярного гель-электро-фореза.
Полученная последовательность проанализирована в Nucleotide blast (. Результаты представлены на рис. 2.
|
□ Potato virus Y strain 0 g ene for coat protein , partial cds |
PotatovirusYstralnO |
60,2 |
60.2 |
23% |
6e-05 |
100.00% |
799 |
10340445.1 |
|
Q Potato virus Y isolate PVY-CJ ooly protein ч епе , complete cds |
Potato virus Y |
60.2 |
60,2 |
23% |
6e-05 |
100.00% |
9614 |
KY6Q0342 1 |
|
Q Potato virus y isolate WG015 2Ю polv protein g ene , complete cds |
Potato virus Y |
60.2 |
60.2 |
23% |
6^05 |
100.00% |
9653 |
MF624291 1 |
|
Q Potato virus Y Is ola te WQQ15 204 RBteoteln gens. ЕОПЩе cd s |
Potato Y lrys Y |
Ы) 7 |
fin 2 |
23% |
Re-QR |
100,00% |
U64II |
MF624290 I |
|
Q Potato virus Y isolate WGO1S 201 p olv protein g ene, complete cds |
Potato virus Y |
fifi 9 |
60 2 |
93% |
Кя-Пб |
100,00% |
9633 |
MF624289.1 |
|
Q Potato virus Y Isolate Qth2016 153 polv protein g ene , complete cds |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
9655 |
MF624268.1 |
|
Q Potato virus Y isolate Yunnan 1 coat protein g ene , partial cds |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
801 |
KJ513434.1 |
|
Q Potato virus Y Isolate Guizhou 2 coat protein g ene , partial cds |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
801 |
KJ513425.1 |
|
Q Potato virus Y Isolate Gulzhou_1 coat protein g ene , partial cds |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
801 |
KJ513423.1 |
|
Q Potato virus Y isolate WI120018. complete g enome |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
9609 |
KY848028.1 |
|
Q Potato virus Y isolate WA316. complete g enome |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
9571 |
KY848025.1 |
|
Q Potato virus Y isolate SU2 . ,complete g enome |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
9655 |
К Y848024.1 |
|
Pvlutu Virus V isulsle ND 100040 uvmuleto ueriuiue |
Potato virus Y |
100.00% |
К Y847992.1 |
|||||
|
0 Potato virus Y isolate ID26 . complete genome |
Potato virus Y |
en 9 |
60 7 |
93% |
Ra-ПП |
100.00% |
germ |
KYM7955.1 |
|
Q Potato virus Y isolate 1021 . complete g enome |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
9676 |
К Y64 7954,1 |
|
Q Potato virus Y isolate ID13_6l0Brw . complete genome Q Potato virus Y Isolate ID1280, complete genome |
Potato virus Y Potato virus Y |
60.2 |
бе-05 |
100.00% 100.00% |
9605 |
KY847953.1 KY847951.1 |
||
|
Q Potato virus Y Isolate Xch-Wh nonfuncbOnal PIPO and nonfunctional polyprotein genes, complete segue.. |
. Potato virus Y |
tie-OD |
100.00% |
I ( Л.1- J ] |
||||
|
Q Potato virus Y Isolate ZLT-2012H Y coat protein mRNA , partial cds |
Potato virus Y |
60.2 |
602 |
23% |
6e-05 |
100.00% |
801 |
KU893142.1 |
|
Я Potato virus Y strain PVY-NE11 polvprotein gene, complete cds |
Potato virus Y |
fin 9 |
fifl 7 |
93% |
Rn.nh |
100.00% |
дЛЗЙ |
KP793716.1 |
|
Q Potato virus Y Isolate 1021 coat protein g ene , partial cds |
Potato virus Y |
60.2 |
60.2 |
23% |
6e-05 |
100.00% |
801 |
KJ741190.1 |
|
Я Potato virus Y Isolate CN:XT27:16 coat protein gene, partial cds |
Potato virus Y |
60.2 |
60 2 |
23% |
6e-05 |
100.00% |
801 |
MH054516.1 |
Рисунок 2. Результаты проверки нуклеотидной последовательности в Nucleotide blast ( gov).
Figure 2. Results of verification of the nucleotide sequence in Nucleotide blast (. 1
Как видно из результатов сравнения последовательности с последовательностями из базы данных генов в Nucleotide blast (, исследуемая последовательность на 100 % совпадает с последовательностью генома вируса картофеля Y (PVY). Соответственно, данная пара праймеров в выбранных условиях обеспечивает амплификацию с матрицы РНК PVY и может быть использована как пара праймеров для ПЦР-тест системы для выявления вируса картофеля Y.
Данная система апробирована с использованием материалов, предоставленных Институтом агробиотехнологий ФИЦ Коми НЦ УрО РАН (Республика Коми, г. Сыктывкар). Проанализировано 48 клубней картофеля по окончании периода зимней лежкости в хранилище Института. Клубни отобраны от 16 селекционных сортообразцов питомников предварительного, основного и конкурсного испытаний по три клубня от каждого номера. В данном случае повторность не учитывалась, так как клубни были выкопаны с разных участков полей и не могли быть перезаражены через насекомых или какие-либо микромеханические повреждения. Поэтому можно было анализировать клубни как отдельных представителей, возможно, зараженные патогеном. Из 48 образцов зараженными оказались восемь, т.е. процент общей зараженности составил 16.7 %. Только в одном сортообразце отмечено заражение двух клубней из трех, в остальных же случаях заражен был только один клубень из трех. Можно предположить, что, с одной стороны, это показывает, что механические микроповреждения, получаемые клубнями в ходе уборки копателем и контактом с его рабочим органом, обеспечивают непосредственно перенос патогена, так как сами клубни не контактировали и находились на разных участках полей, а с другой – заражение произошло в ходе контакта уже непосредственно во время закладки в лечебный период и при последующем зимнем хранении. Таким образом, данная аналитическая система требует дальнейшей проверки с подбором материала.
Заключение
Разработана ПЦР-тест система для выявления генетического материала вируса картофеля Y. По результату анализа генома подобраны праймеры, апробированные в условиях реакции. Таким образом, праймеры PVY 1 F и PVY 1 R готовы для разработки тест-системы для выявления материала вируса PVY. Так же были подобраны условия реакции, и за счет определения нуклеотидной последовательности подтверждена достоверность реакции.
Список литературы Разработка ПЦР-тест системы для выявления вируса картофеля Y
- Kreuze, J. F. Viral diseases in potato / J. F. Kreuze, J. A. C. Souza-Dias, A. Jeevalatha, A. R. Figueira, J. P. T. Valkonen, R. A. C. Jones // The Potato Crop. – Cham: Springer, 2020. – P. 389–429.
- Рогозина, Е. В. Широко распространенные и потенциально опасные для Российского агропроизводства возбудители вирусных болезней картофеля / Е. В. Рогозина, Н. В. Мироненко, О. С. Афанасенко, Ю. Мацухито // Вестник защиты растений. – 2016. – № 4 (90). – С. 24–33.
- Kerlan, C. Potato virus Y. – URL: https://dpvweb.net/dpv/showdpv/?dpvno=414.
- Lacomme, C. General characteristics of potato virus Y (PVY) and its impact on potato production: an overview / C. Lacomme, L. Glais, D. Bellstedt, B. Dupuis, A. Karasev, E. Jacquot // Potato virus Y: biodiversity, pathogenicity, epidemiology and management. – Cham: Springer, 2017. – P. 1–19.
- Baunoch, D.A. Potato virus Y helper component is associated with amorphous inclusions / D.A. Baunoch, P. Das, V. Hari // Journal of General Virology. – 1990. – Vol. 71(10). – P. 2479–2482. doi:10.1099/0022-1317-71-10-2479.
- Chung, Betty Y.-W. An overlapping essential gene in the Potyviridae / Betty Y.-W. Chung, W. Allen Miller, John F. Atkins, Andrew E. Firth // PNAS. – 2008. – Vol. 105(15). – P. 5897–5902. doi:10.1073/pnas.0800468105.
- Kneller, E.L. Cap-independent translation of plant viral RNAs / E.L. Kneller, A.M. Rakotondrafara, W.A. Miller // Virus Research. – 2006. – Vol. 119(1). – P. 63–75. doi: 10.1016/j.virusres.2005.10.010.
- Сухорученко, Г. И. Система интегрированной защиты репродукционного семенного картофеля от комплекса вредных организмов в Северо-Западном регионе Российской Федерации / Г. И. Сухорученко, Г. П. Иванова, С. А. Волгарев. – Санкт-Петербург: Пушкин, 2016. – 64 с.
- Galvino-Costa, S. B. F. Molecular and serological typing of potato virus Y isolates from Brazil reveals a diverse set of recombinant strains / S. B. F. Galvino-Costa, A. R. Figueira, F. A. C. Rabelo-Filho, F. H. R. Moraes, O. V. Nikolaeva, A. V. Karasev // Plant Disease. – 2012. – Vol. 96(10). – P. 1451–1458. doi: 10.1094/PDIS-02-12-0163-RE.
- Onozuka, N. One-step real-time multiplex reverse transcription- polymerase chain reaction assay with melt curve analysis for detection of potato leafroll virus, potato virus S, potato virus X, and potato virus Y / N. Onozuka, T. Ohki, N. Oka, T. Maoka // Virology Journal. – 2021. – Vol. 18. – № 131. doi: 10.1186/s12985-021-01591-3.
- Sambrook, J. Molecular cloning: a laboratory manual / J. Sambrook, T. Fritch, T. Maniatis. – New York: Cold Spring Harbor Laboratory Press, 1989. – 1659 p.


