Разработка радиационно-эпидемиологических критериев эффективности скрининговых программ рака лёгкого с применением компьютерной томографии для населения России
Автор: Кащеев В.В., Меняйло А.Н., Пряхин Е.А., Туманов К.А.
Рубрика: Научные статьи
Статья в выпуске: 4 т.26, 2017 года.
Бесплатный доступ
В работе предложен радиационно-эпидемиологический способ оценки эффективности скрининговых программ рака лёгкого с применением компьютерной томографии (КТ) для населения России. С использованием моделей риска МКРЗ (Публикация 103) и НКДАР ООН 2006, а также российских данных об онкологической заболеваемости, выполнен прогноз потерянных лет здоровой жизни в популяции, связанный с заболеваемостью раком лёгкого и с воздействием ионизирующего излучения на пациентов в результате многократного прохождения процедур компьютерной томографии. Показано, что для женщин, не имеющих дополнительных факторов риска заболеваемости раком лёгкого, проведение скрининговых обследований с применением низкодозной КТ нецелесообразно, т.к. во всём диапазоне возрастов радиационный вред превышает пользу от ожидаемого эффекта. С другой стороны, для мужчин радиационный вред меньше или сопоставим с пользой, только для лиц, включённых в скрининговое исследование после 50 лет. При начале скрининговых обследований в более раннем возрасте польза ощутима только до 70-75 лет, а при дожитии до более старших возрастов накопленный радиационный ущерб превышает ожидаемую пользу ранней диагностики. Полученные в исследовании результаты могут иметь первостепенное значение для принятия управленческих решений при оптимизации комплекса профилактических мероприятий в целях снижения онкологической смертности в России с учётом возможных финансово-экономических ограничений.
Радиация, онкология, риск, рак лёгкого, скрининг, медицинское облучение, компьютерная томография, потерянные годы жизни, сохранённые годы жизни, избыточный абсолютный риск
Короткий адрес: https://sciup.org/170170318
IDR: 170170318 | DOI: 10.21870/0131-3878-2017-26-4-22-32
Development of radiation epidemiological efficiency criteria for ct-based lung cancer screening program for russian population
Radiation epidemiological approach to assess efficiency of CT-based lung cancer screening program for Russian population is considered in the article. The number of years of healthy life lost in future due to the lung cancer and multiple CT scans was calculated with ICRP 103 and UNSCEAR 2006 risk models and national data on cancer incidence in Russia. We have found that lung cancer screening with low-dose CT in women of any ages free of additional risk factors of lung cancer does not make any sense, because the harm from radiation exceeds the benefit of the screening or the harm and benefit are commensurable. On the other hand, the benefit from СT scans prevails the harm or benfit and harm are comparable in men older than 50 years. If men are involved in the lung cancer screening program at younger ages the benefit of the screening prevails the harm until their age of 70-75 years, in older ages cumulative radiation associated harm exceeds expected benefit of CT scans performed at early ages. Results of the study can be of high priority for making managerial decisions on optimization of preventive measures towards lowering cancer mortality in Russia with account of financial and economical restraints.
Текст научной статьи Разработка радиационно-эпидемиологических критериев эффективности скрининговых программ рака лёгкого с применением компьютерной томографии для населения России
Настоящая научная работа продолжила начатые ранее коллективом учёных Национального радиационно-эпидемиологического регистра (НРЭР) исследования [1-5], направленные на решение фундаментально-прикладной проблемы современной радиационной эпидемиологии – разработку методов оценки возможного радиационного ущерба пациентов при прохождении медицинских диагностических процедур с применением компьютерной томографии (КТ).
На сегодняшний день рак лёгкого (трахеи, бронхи, лёгкое) занимает одно из лидирующих мест в общей структуре заболеваемости злокачественными новообразованиями (ЗНО) в России (на третьем месте в общей структуре онкологических заболеваний (10,2%) и на первом (17,8%) среди злокачественных опухолей у мужчин) [6]. Общеизвестно, одним из основных показателей, определяющих прогноз онкологического заболевания, является степень распространённости опухолевого процесса на момент диагностики. Для рака лёгкого доля больных с опухолевым процессом I-II стадии составляет всего 28,7% [7]. Одним из основных критериев оценки диагностического компонента помощи онкологическим больным является показатель запущенности. В 2016 г. в России у 40,9% больных заболевание раком лёгкого диагностировано с запущенным опухолевым процессом (IV стадия). Данный показатель имеет региональную зависимость и сильно варьируется с административно-территориальным делением РФ. В свою
Кащеев В.В.* – зав. лаб., к.б.н.; Меняйло А.Н. – ст. научн. сотр., к.б.н.; Пряхин Е.А. – научн. сотр.; Туманов К.А. – зав. лаб., к.б.н. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
очередь, эффективным средством ранней диагностики рака лёгкого может являться скрининг с применением компьютерной томографии.
Основные критерии, которые должны быть соблюдены перед проведением скрининга, чётко определены уже много лет назад. Они имеют фундаментальное значение для обеспечения целостности процесса скрининга в любой стране [8]. В настоящей работе для разработки радиационно-эпидемиологических критериев эффективности скрининговых программ рака лёгкого с применением компьютерной томографии рассматривались два основополагающих требования: скрининговый метод ранней диагностики должен приносить пользу (как правило, увеличивать продолжительность жизни) лицам, у которых диагностировано данное заболевание, и не представлять какой-либо опасности для обследуемого здорового населения.
Вопрос сопоставления пользы и вреда при применении современной КТ является наиболее актуальным и сложным, т.к. пациент может подвергаться достаточно высоким дозам облучения. С другой стороны, КТ является эффективным методом выявления рака лёгкого на начальных стадиях опухолевого процесса [9].
Модель оценки радиационного риска и потерянных лет жизни
На сегодняшний день вопросу разработки способов оценки и прогноза вреда здоровью человека в результате воздействия на его организм ионизирующего излучения уделяется всё больше внимания. Так, в последние годы математические представления для прогноза и оценки радиационных рисков были опубликованы следующими организациями: Международная комиссия по радиологической защите (МКРЗ), Национальный комитет ООН по действию атомной радиации (НКДАР ООН) и Всемирная организация здравоохранения (ВОЗ). Основной количественной мерой вреда здоровью при прохождении скрининговых исследований с применением КТ могут являться оценка годового избыточного абсолютного риска (EAR) онкологической заболеваемости, вызванной облучением, и количество потерянных лет здоровой жизни в результате облучения (YLL). В настоящем исследовании были использованы модели радиационных рисков Публикации 103 МКРЗ и НКДАР ООН 2006.
Важно отметить, что при исследовании лёгких с применением КТ облучение тела пациента происходит неравномерно и облучению подвергаются прилегающие органы и ткани. Таким образом, модели оценки радиационных рисков при КТ должны учитывать дозы облучения всех органов и тканей, находящихся под риском.
Под избыточным абсолютным риском заболеваемости (EAR) раком или смертности от рака понимается приращение соответствующего фонового показателя λ 0 после воздействия радиации (1):
EAR = λ - λ . (1)
Кроме избыточного абсолютного риска в радиационной эпидемиологии применяется понятие избыточного относительного риска (ERR). Связь между этими двумя рисками представлена в (2).
EAR = ERR ⋅ λ . (2)
Модель МКРЗ [10] избыточного абсолютного риска (аддитивная модель) заболеваемости солидным раком после однократного облучения представлена в формуле (3), а модель МКРЗ избыточного относительного риска после однократного облучения (мультипликативная модель) заболеваемости раком представлена в формуле (4).
, x « EAR ( c ) , / \x0.1'( g - 30 )
— - — МКРЗ ( .X . n ( X a a I I , Y EAR ( c ) 1
EAR однокр . ( s - c - g - a - d ) = d ' P ear ( s - c ) ' ^ —J '^ 1 + 100---J - (3)
, x « ERR ( c ) , / lx«.1'( g - 30 )
МКРЗ \ a a I I Y ( c ) 1
ERR однокр . ( S - c - g - a - d ) = d • P eRR ( s - c )'!7Q ! •[ 1 + 100----J . (4)
Здесь s – пол, c – локализация опухоли, g – возраст при облучении, a – возраст, на который рассчитывается риск (возраст дожития), d - доза облучения, p EAR , « EAR , y EAR - параметры аддитивной модели, p ERR , « ERR , y ERR - параметры мультипликативной модели. Значения этих параметров представлены в табл. 1.
Латентный период для солидных раков в модели МКРЗ, как и в модели НКДАР ООН [11] T LS равен 10-ти годам. То есть, в течение 10 лет после облучения избыточные риски, как по мультипликативной, так и по аддитивной моделям, принимаются равными нулю. Другими сло-
МКРЗ МКРЗ вами: EAR и ERR равны 0, если a < g + T,_ . однокр . однокр . " , « LS
Таблица 1
Параметры моделей риска заболеваемости для различных локализаций солидных ЗНО, модели МКРЗ [10]
|
Локализация опухоли |
Пол |
P err , Гр 1 |
Y ERR |
« ERR |
P ear , 10 -4 хГр-1 |
Y EAR |
« EAR |
|
Пищевод |
Муж |
0,40 |
-17 |
-1,65 |
0,48 |
64 |
2,38 |
|
Жен |
0,65 |
0,66 |
|||||
|
Желудок |
Муж |
0,23 |
-17 |
-1,65 |
6,63 |
-24 |
2,38 |
|
Жен |
0,38 |
9,18 |
|||||
|
Толстая кишка |
Муж |
0,68 |
-17 |
-1,65 |
5,76 |
-24 |
2,38 |
|
Жен |
0,33 |
2,40 |
|||||
|
Печень |
Муж |
0,25 |
-17 |
-1,65 |
4,18 |
-24 |
2,38 |
|
Жен |
0,40 |
1,30 |
|||||
|
Лёгкое |
Муж |
0,29 |
+17 |
-1,65 |
6,47 |
1 |
4,25 |
|
Жен |
1,36 |
8,97 |
|||||
|
Молочная железа |
Жен |
0,87 |
0 |
-2,26 |
10,9 |
-39 |
3,5* |
|
Яичник |
Жен |
0,32 |
-17 |
-1,65 |
1,47 |
-24 |
2,38 |
|
Мочевой пузырь |
Муж |
0,67 |
-17 |
-1,65 |
2,00 |
-11 |
6,39 |
|
Жен |
1,10 |
2,77 |
|||||
|
Щитовидная железа |
Муж |
0,53 |
-56 |
0,00 |
0,69 |
-24 |
0,01 |
|
Жен |
1,05 |
2,33 |
|||||
|
Остальные солидные |
Муж |
0,22 |
-34 |
-1,65 |
7,55 |
-24 |
2,38 |
|
Жен |
0,17 |
10,45 |
* Для рака молочной железы « ear =1 при возрасте дожития большем 50 лет.
В итоге для вычисления избыточного абсолютного риска заболеваемости солидными ЗНО после однократного облучения согласно модели МКРЗ нужно учесть взвешивание мультипликативной и аддитивной моделей и связь (2) между избыточным относительным и абсолютным риском (5).
сол • / ^ \ О заб V \ ^Г1Г1 МКРЗ /
EAR однокр • ( S - с - g - a - d )= Р ( c ) • ^ 0 ( S - a - c ) ' ERR однокр • ( S - c - g - a - d ) +
. (5)
+ ( 1 - р ( с )) • EAR Мн3 • ( s - c - g - a - d )
Здесь p равно 0,0 для молочной железы и костного мозга (лейкозы), 1 – для щитовидной железы и кожи, 0,3 – для лёгкого и 0,5 – для всех остальных локализаций.
Вычисление EAR заболеваемости лейкозами после однократного облучения производится по формуле (6).
EAR ОДНйокр . ( s , g , a , d ) = в ( s , g ) • d - ( 1 + 0,79 • d ) • exp [ « ( s , g И a - g - 25 )] • (6)
Здесь, так же как и в случае с риском для солидных типов рака, s – пол, g – возраст при облучении, a – возраст, на который рассчитывается риск, d – доза однократного облучения в Гр, в и a — параметры модели избыточного абсолютно риска заболеваемости лейкозами. Их значения, зависящие от возраста на момент облучения, приведены в табл. 2.
Латентный период для заболеваемости лейкозами T L L равен 2 годам и:
EAR олНОкр . ( s , g, a, d ) = 0 , если a < g + T ll •
EAF^eHBKI,(s,c,g,a,d)=
облучения требуется провести суммирование EAR
заб .
однокр
по возрастам на момент облучения с
Таблица 2
Параметры модели для вычисления избыточного абсолютного риска заболеваемости лейкозами после однократного облучения
n
EAR заб ' ( s , с , а , g 1 ,..., g n , d 1 ,..., d n ) = £ EAR оао „ p . ( s , c , g , ., a , d , ) , (8)
i = 1
Здесь n – количество облучений, g ,..., g – возраста на момент облучения, d ,..., d – соответствующие дозы облучения, полученные органом или тканью c . В совокупности g ,..., g , d ,..., d определяют дозовую историю облучения для данного органа или ткани.
Итоговое значение избыточного абсолютного риска от заболеваемости всеми типами рака получается путём суммирования EAR заб . по всем локализациям из табл. 1 плюс лейкозы:
EAR ( s , a , g 1 ,..., g n , d 1 ,..., d n ) = £ EAR ( s , c , a , g 1 ,..., g n , d 1 ,..., d n ) , (9)
все раки c
Вычисление ожидаемого числа потерь лет здоровой жизни (YLL) основано на описании аналогичной величины потерь лет жизни, представленной в отчёте НКДАР ООН 2006.
Величина потерянных лет здоровой жизни в целом от всех онкологических заболеваний после многократного облучения вычисляется по формуле ниже:
a
YLL ( s , e , a , g ...... gn , d ...... d n ) = £ [ S ( s , e , a ) - Sdose ( s , e , a , g ...... g n , d ...... d n )] , (10)
a = e
Здесь e – текущий возраст человека, в котором он жив.
S в (10) – это функция здорового дожития – величина, характеризующая вероятность для человека пола s и возраста e дожить до возраста a и не заболеть при этом раком. Она вычисляется по следующей формуле:
a — 1 Г
S ( s , e , a ) = exp
- i X бщ . смерт . ( s , k ) [ аб . ( s , k , c ) - 2с мерт . ( s , k , c ) ] l
“ e L “ J a > e
При этом в возрасте e и ранее, естественно, функция дожития по определению принимается равной единице, то есть S ( s , e , a ) = 1 , a < e .
Здесь Ло6щ . смерт . ( s , k ) - показатель общей фоновой смертности в год от всех причин для пола s в возрасте k .
S dose в (10) – функция здорового дожития, учитывающая также увеличение смертности за счёт радиационного облучения. Она вычисляется аналогично функции здорового дожития (11), но к показателю общей смертности добавляется избыточный абсолютный риск (EAR) заболеваемости в совокупности от всех онкологических заболеваний после многократных облучений:
Г
S dose ( s ’ e ’ a ’ 9 ......
g n , d ...... d n ) = exp
a -1
-I k = e
"X 0 6щ'смерт ■ ( s , k )+ ^ [ ^ 0 a6. ( s , k , c ) - Л 0 мерт
c
. ( s , k , c ) ] + 1
+ EAR за6. ( s , a , g ,,.
все раки 1
,..., g n , d 1 ,...,
d n )
a > e
Далее рассмотрим оценку потери лет здоровой жизни от рака лёгкого.
Функция здорового дожития для рака лёгкого вычисляется по формуле (13):
a - 1
s лёгкие ( s , e , a ) = exp - I U 06 щ .“е р т. ( s , k ) + x 0 а6 . ( s , k , c = лёгкие ) - Л 0 мерт . ( s , k , c = лёгкие ) !
L “ e L JJ
|
a > e |
(13) |
Среднее оставшееся время здоровой жизни (без рака) от заданного возраста e вычисляется по формуле (14):
a
L ( s , e ) = У S . ( s , e , a ) . (14)
лёгкие , лёгкие , , a = e
Ожидаемая потеря лет жизни от заболевания раком лёгких без скрининга вычисляется по формуле (15):
без скрининга , . „ без скрининга ™ _ заб , „ . , ,
YLL лёгкие ( s ’ e ) = P mrt 'Е 5 лёгкие ( s ’ e ’ 3 ' Х 0 ( s ’ 3 ’ c = лёгкие Г L лёгкие ( s ’ 3 )
а = e
Здесь P без скрининга – спонтанная вероятность умереть от рака лёгкого на первом году жизни в случае отсутствия скрининга.
Ожидаемая потеря лет жизни от заболевания раком лёгких при скрининге без учёта облучения вычисляется по формуле (16):
max со скринингом без облуч . , х со скринингом „_ , х -ас , х / \
YLL лёгкие ( S ’ 3 ) = P mrt £ 5 лёгкие ( » ’ 3’3 ) * ^ ё^ » ’ ^ , С = лёгкие )■ L лёгкие ( S , 3 )
а = e
Здесь P со скринингом – спонтанная (не связанная с радиацией) вероятность умереть от рака лёгкого на первом году жизни в случае проведения скрининговых исследований.
Итоговое значение ожидаемого числа потерь лет здоровой жизни с учётом облучения при скрининге будет вычисляться по (17):
со скринингом со скринингом без облуч . /\
YLL = YLL + YLL (s, e, а, g,,..., g , d,,..., d ), лёгкие лёгкие \ ’ ’ ’ 1 ’ ’ n n ’ 1’’ n / ,x / где YLL определяется облучением на компьютерном томографе, а дозовая история вычисляется согласно методике оценки органных доз на основе значений величины Dose Length Product (DLP) - мера поглощённой дозы за все КТ исследование [3], при условии, что DLP=200 (мГрхсм) два раза в год и DLP=1000 (мГрхсм) раз в три года.
Радиационно-эпидемиологические критерии эффективности скрининговых программ рака лёгкого
В настоящем исследовании разработка радиационно-эпидемиологических критериев эффективности скрининговых программ рака лёгкого с применением компьютерной томографии базировалась на сравнении потерянных лет жизни в популяции. Ожидаемая потеря лет жизни в популяции от заболевания раком лёгких без проведения дополнительно КТ скрининга ( YLL без скрининга ) вычислялась по формуле (15). Полученная величина сравнивалась со значением ожидаемого числа потерь лет здоровой жизни с учётом облучения, при прохождении КТ скрининга, рассчитанным согласно (17).
По данным официальной статистики в России летальность от рака лёгкого на первом году с момента установки диагноза составляет 50% [7]. В то же время годичная выживаемость при выявлении рака лёгкого на I стадии достигает 80% [7]. Предположение, что двукратное ежегодное скрининговое обследование с применением низкодозной КТ (DLP<100 мГр х см) с последующим третьим углублённым (при необходимости) исследованием (DLP<1000 мГр х см) позволит выявлять все раки на первой стадии [9] и будет достаточным для снижения годовой смертности на 30% ( P surv – P mrt ). Данное предположение было взято за основу ограничения годового радиационного риска при многократной КТ в течение всей жизни.
Следовательно, для оценки потерянных лет жизни в выражениях (15) и (17) следует ис-без скрининга со скринингом пользовать значения P =0,5 и P =1–0,8=0,2 соответственно. mrt , mrt , ,
На рис. 1 и 2 (для мужчин и женщин соответственно) представлена зависимость прогноза числа потерянных лет здоровой жизни от достигнутого возраста в результате спонтанной заболеваемости раком лёгкого ( YLL без скрининга ) и связанная с прохождением скрининговых обсле дований YLL со скринингом , рассчитанная на основе величины пожизненного атрибутивного риска. Величина YLL со скринингом была рассчитана для 4 сценариев ежегодных скрининговых КТ обследований в зависимости от возраста начала их проведения – с 20, 30, 40 и 50 лет.
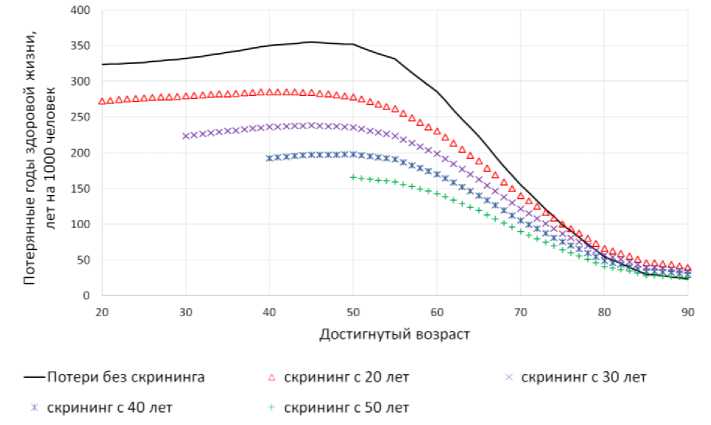
Рис. 1. Зависимость прогноза числа потерянных лет здоровой жизни мужчин от достигнутого возраста в результате спонтанной заболеваемости раком лёгкого и связанная с прохождением скрининговых обследований.
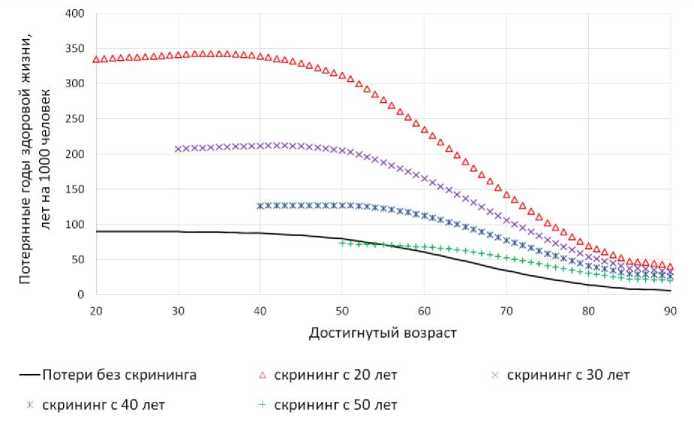
Рис. 2. Зависимость прогноза числа потерянных лет здоровой жизни женщин от достигнутого возраста в результате спонтанной заболеваемости раком лёгкого и связанная с прохождением скрининговых обследований.
Как видно из рисунков, для женщин, не имеющих дополнительных факторов риска заболеваемости раком лёгкого, проведение скрининговых обследований с применением низкодоз-ной КТ нецелесообразно, т.к. во всём диапазоне возрастов радиационный вред превышает со скринингом без скрининга пользу от ожидаемого эффекта, т.к. YLL > YLL для соответствующих достигнутых возрастов. Более сложная зависимость выявлена для мужчин. Радиационный вред меньше или сопоставим с пользой только для мужчин, включённых в скрининговое исследование после 50 лет. При начале скрининговых обследований в более раннем возрасте польза ощутима только до 70-75 лет, а при дожитии до более старших возрастов накопленный радиационный ущерб превышает ожидаемую пользу ранней диагностики.
Таким образом, в результате проведённого исследования предложены половозрастные критерии эффективности скрининговых программ рака лёгкого с применением компьютерной томографии для населения России.
В то же время, полученные результаты подтверждают необходимость проведения дополнительных исследований эффективности скрининговых программ рака лёгкого с применением низкодозной КТ для критических групп населения Российской Федерации:
-
1) лица, подвергающиеся воздействию техногенных факторов риска (радиоактивное облучение, контакт с асбестом, радоном, мышьяком, никелем, кадмием, хромом, хлорметиловым эфиром и др., загрязнение атмосферы);
-
2) курильщики;
-
3) лица с хроническими заболеваниями лёгких;
-
4) мужчины старше 50 лет;
-
5) лица с генетической предрасположенностью (наследственность).
Список литературы Разработка радиационно-эпидемиологических критериев эффективности скрининговых программ рака лёгкого с применением компьютерной томографии для населения России
- Ivanov V.K., Tsyb A.F., Mettler F.A., Menyaylo A.N., Kashcheev V.V. Methodology for estimating cancer risks of diagnostic medical exposure: with an example of the risks associated with computed tomography//Health Phys. 2012. V. 103, N 6. P. 732-739 DOI: 10.1097/HP.0b013e31825c179f
- Ivanov V.K., Kashcheev V.V., Chekin S.Yu., Menyaylo A.N., Pryakhin E.A., Tsyb A.F., Mettler F.A. Estimating the lifetime risk of cancer associated with multiple CT scans//J. Radiol. Prot. 2014. V. 34, N 4. P. 825-841 DOI: 10.1088/0952-4746/34/4/825
- Kashcheev V.V., Pryakhin E.A., Menyaylo A.N., Chekin S.Yu., Ivanov V.K. Comparing risk estimates following diagnostic CT radiation exposures employing different methodological approaches//Health Phys. 2014. V. 106, N 6. P. 806-811 DOI: 10.1097/HP.0000000000000096
- Кащеев В.В., Пряхин Е.А., Меняйло А.Н., Чекин С.Ю., Иванов В.К. Расчёт эквивалентных доз в отдельных органах и тканях и величины пожизненного радиационного риска развития рака при проведении типовых обследований с использованием компьютерной томографии//Радиация и риск. 2013. Т. 22, № 3. С. 8-20.
- Пряхин Е.А., Кащеев В.В., Меняйло А.Н., Иванов В.К. Оценка радиационных рисков при однократном прохождении ПЭТ/КТ-сканирования//Радиация и риск. 2017. Т. 26, № 2. С. 41-48.
- Злокачественные новообразования в России в 2015 году (заболеваемость и смертность)/Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена -филиал ФГБУ «НМИРЦ» Минздрава России, 2017. 250 с.
- Состояние онкологической помощи населению России в 2016 году/Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: МНИОИ им. П.А. Герцена -филиал ФГБУ «НМИРЦ» Минздрава России, 2017. 236 с.
- Holland W.W., Stewart S., Masseria C. Policy brief: screening in Europe. Copenhagen: European Observatory on Health Systems and Policies, 2006. 72 p.
- Ma J., Ward E.M., Smith R., Jemal A. Annual number of lung Cancer deaths potentially avertable by screening in the United States//Cancer. 2013. V. 119, N 7. P. 1381-1385 DOI: 10.1002/cncr.27813
- The 2007 Recommendations of the International Commission on Radiological Protection. ICRP Publication 103//Ann. ICRP. 2007. V. 37, N 2-4. Elsevier, 2007. 332 p.
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR). Sources and effects of ionizing radiation. UNSCEAR 2006 Report Vol. I, Annex A: Epidemiological studies of radiation and cancer. New York: United Nation, 2008.


