Разработка способа контроля органических примесей при очистке сточных вод
Автор: Мастюкова Т.В., Кривцова А.И.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 1 (75), 2018 года.
Бесплатный доступ
Изучена электрическая проводимость водных растворов поверхностно-активных веществ (ПАВ) разной природы в зависимости от концентрации электролитов в растворе, с целью контроля содержания вредных примесей органической природы в минерализованных водах кондуктометрическим методом. Установлено, что с увеличением концентрации ПАВ удельная электрическая проводимость снижалась, однако характер изменения в растворах низкомолекулярных и коллоидных ПАВ различный. В случае низкомолекулярных ПАВ зависимость имеет линейный вид, например, для раствора бутанола при ионной силе хлорида калия 2 моль/м3 по уравнению: y = -0,0604x + 0,5085, а для растворов коллоидных ПАВ – экстремальный, проходящий через минимум. Увеличение ионной силы среды для растворов ПАВ ионогенного (олеата натрия) и неионогенного типа (неонол АФ 9–10), приводит к уменьшению минимума на концентрационной кривой электрической проводимости. Установлено понижение значения критической концентрации мицеллообразования (ККМ) для олеата натрия от 1,1 10-3 моль/дм3, до 0,4?10-3 моль/дм3 при концентрации хлорида калия в растворе 2 моль/м3, и ККМ = 0,1 10-3 моль/дм3 при ионной силе раствора 10 моль/м3. В случае неонола АФ 9–10 (ККМ = 1,24?10-4 моль/дм3) увеличение концентрации электролита, например КCl от 2 до 75 моль/м3 в растворе не смещает точку ККМ во всем диапазоне ионной силы среды. Итак, экстремальный характер зависимости изотерм проводимости растворов коллоидных ПАВ в области низких ионных сил раствора, может послужить аналитическим сигналом для выявления примесей амфифильной природы и возможности прогнозирования общей минерализации воды сложного состава.
Растворы электролитов, электропроводимость, кондуктометрия, коллоидные пав, неионогенные пав, ионогенные пав, неонол аф 9-10, олеат натрия, мицеллы, мицеллообразование
Короткий адрес: https://sciup.org/140229964
IDR: 140229964 | DOI: 10.20914/2310-1202-2018-1-228-232
Development of methods for controlling organic impurities in wastewater treatment
Electrical conductivity was studied aqueous solutions of surface-active substances (surfactants) different nature depending on the concentration of electrolytes in solution, in order to control the content of harmful impurities of organic nature in mineralized waters conductometric method. It has been established that the specific electric conductivity decreased with increasing surfactant concentration, however, the nature of the changes in solutions of low-molecular and colloidal surfactants is different. In the case of low-molecular surfactants, the dependence has a linear form, for example, for a solution of butanol with an ionic potassium chloride force of 2 mol / m3, according to the equation: y = -0,0604x + 0,5085, and for solutions of colloidal surfactants – extremal, passing through a minimum. An increase in the ionic strength of the medium for solutions of surfactant ionogenic (sodium oleate) and nonionic type (neonol AF 9–10) leads to a decrease in the minimum on the concentration curve of electrical conductivity. A decrease in the value of the critical micelle concentration (CMC) for sodium oleate from 1.1 10-3 mol / dm3, up to 0.4 · 10-3 mol / dm3 at a concentration of potassium chloride in a solution of 2 mol / m3, and CMC = 0, 1 10-3 mol / dm3 at an ionic strength of the solution of 10 mol / m3. In the case of neonol AF 9–10 (CMC = 1.24 ? 10-4 mol / dm3), an increase in the electrolyte concentration, for example KCl from 2 to 75 mol / m3 in the solution, does not shift the CMC point in the entire ionic strength range of the medium. Thus, the extreme character of the dependence of the conductivity isotherms of colloidal surfactants in the region of low ionic strengths of the solution, can serve as an analytical signal for the detection of impurities of the amphiphilic nature and the possibility of predicting the overall mineralization of complex water.
Текст научной статьи Разработка способа контроля органических примесей при очистке сточных вод
При рассмотрении вопросов, связанных с загрязнением окружающей среды, наиболее актуальной проблемой является контроль химических загрязнителей, как в природных водоемах, так и в сточных водах различных производств [1-3]. При выборе метода контроля, одной из сложных задач является определение
загрязнителей органической природы, например, синтетических поверхностно-активных веществ (ПАВ). В настоящее время одним из широко применяемых методов физико-химического анализа природных вод является кондуктометрия [4]. Простота и мобильность данного метода позволяет в течении минуты определить электрическую проводимость анализируемого
объекта, а затем по результатам определить примерную минерализацию воды. Особенно это важно для осуществления непрерывного контроля загрязнения сточных вод отходами органической природы.
Известно, что кондуктометрия рассматривается как один из наиболее чувствительных методов, применяемых при изучении мицеллярных систем [5]. В основе такого подхода учитывается аддитивный вклад в электропроводность свободных противоионов, поверхностно-активных ионов, а также мицелл как макроионов. Измерение концентрационной зависимости электрической проводимости растворов ионогенных ПАВ, является наиболее распространенным способом определения критической концентрации мицеллообразования (ККМ), степени связывания противоионов мицеллами и чисел агрегации последних [6–11].
В этой связи в задачу настоящих исследований входило изучение влияния низкомолекулярных и коллоидных поверхностно-активных веществ на электрическую проводимость раствора сильного электролита с целью выявления возможности прогнозирования общей минерализации воды сложного состава.
Материалы и методы исследования
В качестве объектов исследования использовали водные растворы электролитов хлорида калия и сульфата цинка, ионная сила которых менялась от 2 до 75 (моль/м3), содержащие примеси (загрязнители) амфифильных соединений: н-бутанол, олеат натрия, неонол. Выбор органических соединений основан на отличительной способности указанных веществ к мицеллобра-зованию, диссоциации в растворе, где их ионы имеют различную подвижность и соответственно электрическую проводимость.
Олеат натрия, натриевая соль олеиновой кислоты (NaC 18 H 33 O 2 ), анионное ПАВ, критическая концентрация мицеллообразования которого 1,1×10-3 моль/дм3при 25 °С, является полиэлектролитом.
Оксиэтилированный моноалкилфенол (неонол АФ 9–10) на основе триммеров пропилена является высокоэффективным неионогенным поверхностно-активным веществом (НПАВ), критическая концентрация мицеллообразования, которого 1,24×10-4 моль/дм3.
Бутанол – является представителем одноатомных спиртов, обладает поверхностной активностью и не способен к агрегации. В отличие от метанола, этанола и пропанола только умеренно растворяется в воде – 7,6 г на 100 г. воды.
Значение ККМ для олеата натрия и неонола определяли по изотермам поверхностного натяжения, которое измеряли методом наибольшего давления в пузырьке, на лабораторной установке [12]. Для олеата натрия ККМ составила 1,3×10-3 моль/дм3, а для неонола АФ 9-10 – 1,28×10-4 моль/дм3, при температуре 18 ± 2 °С, что согласуется со справочными данными.
Модельные растворы электролитов готовились таким образом, что концентрация ПАВ в них менялась в пределах допустимой концентрации от 0 до 3 (моль/м3).
Электрическую проводимость растворов измеряли на кондуктометре марки Hanna Instruments 2314 (Германия).
Полученные результаты и их обсуждение
В результате проведенных исследований были получены изотермы электрической проводимости эталонных растворов электролитов КСl, ZnSO 4 и растворов, содержащих различные добавки ПАВ при температуре 18 ± 2 °С. Удельная электрическая проводимость модельного раствора хлорида калия и сульфата цинка с увеличением концентрации увеличивается линейно в соответствии с уравнением: y = 0,170x + 0,484 для KCl и y = 0,010x + 0,058 для ZnSO 4 .
Введение в раствор электролита приведенных выше поверхностно-активных веществ снижает удельную электропроводность раствора (рисунок 1) вследствие изменения диэлектрической проницаемости последнего, уменьшения степени диссоциации электролита и снижения в системе количества растворителя (воды) вследствие увеличения гидратации ионов ПАВ.
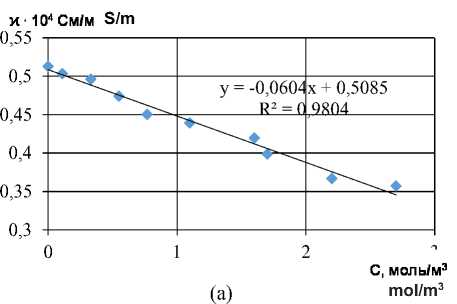
Вид кондуктометрических кривых зависит от природы ПАВ. При увеличении концентрации бутанола удельная электрическая проводимость убывает линейно во всем диапазоне изменения ионной силы электролита в растворе, ниже приведен пример зависимости при концентрации хлорида калия 2 моль/м3 (рисунок 1, a ). Замечено, что с повышением ионной силы среды наблюдается увеличение углового коэффициента зависимости, для раствора с ионной силой 75 моль/м3 уравнение имеет вид: y = -0,438x + 13,161.
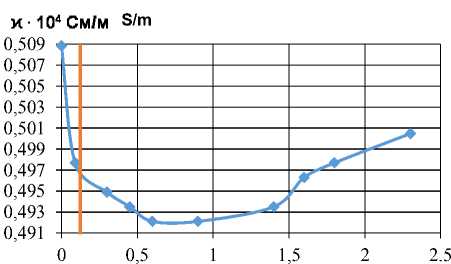
Для растворов олеата натрия и неонола в области низких концентраций КCl (от 1 до 10 моль/м3) наблюдается нелинейное изменение удельной электрической проводимости, понижение, а затем повышение (рисунок 1, b, c ), точка перегиба находится в области ККМ. Причем увеличение концентрации хлорида калия в растворе минимизирует этот эффект. При увеличении концентрации электролита больше 10 моль/м3 характер зависимости стремится к линейному виду, например, при ионной силе хлорида калия 60 моль/м3 уравнение зависимости для неонола: y = -0,275x + 10,39, а для олеата натрия: y = -0,441x + 10,56.
х-101, См/м S/m
|
0,525 я 0,52 0,515 0,51 |
|||||
|
0,5 0,495 |
|||||
|
0 |
0,5 1 (b) |
1,5 2 С,моль/м3 mol/m3 |
|||
(c)
С, МОЛЬ/М3 mol/m3
Рисунок 1. Изотерма электрической проводимости раствора KCl с ионной силой 2 моль/м3 в зависимости от концентрации н-бутанола (a), олеата натрия (b), неонола (c) при температуре 18 ± 2 °С
Figure 1. The isotherm of the electrical conductivity of the KCl solution with an ionic strength of 2 mol / m3, depending on the concentration of n-butanol (a), sodium oleate (b), neonol (c) at 18 ± 2 °С
Введение электролита в раствор ионогенного ПАВ вызывает два эффекта приводящих к снижению ККМ.
Во-первых, электролит частично дегидратирует полярные группы ионов ПАВ, так как он связывает воду за счет гидратации своих ионов. Уменьшение гидратации ионов ПАВ повышает их способность к ассоциации.
Во-вторых, добавленный электролит уменьшает эффективную степень ионизации поверхностно-активного вещества. Кроме того, снижение степени диссоциации поверхностноактивного электролита дополнительно гидро-фобизирует ПАВ, так как недиссоциированные полярные группы менее гидрофильны, чем ионы [10, 13].
В растворе неионогенных ПАВ мицелло-образование не связано с электрическим взаимодействием благодаря электронейтральности мицеллообразующихся частиц. Введение электролитов практически не изменяет молекулярного состояния таких растворов. Понижение ККМ неионогенных ПАВ происходит лишь вследствие эффекта дегидратации макромолекулы [14].
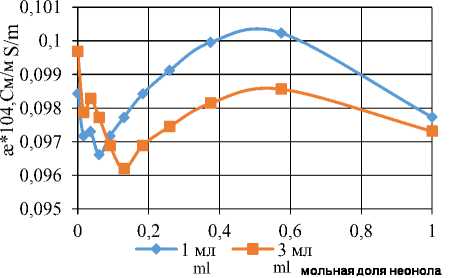
Контроль вредных примесей в сточных водах происходит в виде анализа многокомпонентной системы. Присутствие в анализируемой пробе смеси ПАВ разной природы, может влиять на точку перегиба кондуктометрической кривой. В этой связи были получены изотермы проводимости растворов электролитов (хлорида калия, сульфата цинка) в зависимости от концентрации олеата натрия и неонола, при разном их соотношении. В работе была выбрана область концентраций ПАВ в растворе электролита близкая ККМ олеата натрия и неонола. Для этого в раствор электролита с заданной ионной силой вводили определенный объем бинарной смеси ПАВ, в которой мольная доля каждого менялась от 0 до 1. На рисунке 2, приведен пример изотерм электрической проводимости раствора ZnSO 4 в зависимости от мольной доли ПАВ в бинарной смеси.
mole fraction of neonol
Рисунок 2. Изотерма электрической проводимости раствора ZnSO 4 в зависимости от мольной доли неонола и олеата натрия с ионной силой электролита 5 моль/м3 при температуре 18 ± 2 °С Figure2.The isotherm of the electrical conductivity of a solution of ZnSO 4 depending on the mole fraction of neonol and sodium oleate with an ionic strength of the electrolyte of 5 mol/m3 at a temperature of 18 ± 2 °C
Состав бинарной смеси влияет на ККМ раствора ПАВ и точку перегиба кривой, на изотерме (рисунок 2) точке перегиба соответствуем ККМ = 0,49×10-4 моль/дм3. Увеличение ионной силы среды незначительно влияет на точку перегиба кривой. Тогда как увеличение объема ПАВ в анализируемом растворе
Список литературы Разработка способа контроля органических примесей при очистке сточных вод
- Jiang J. Q. The role of coagulation in water treatment//Current Opinion in Chemical Engineering. 2015. V. 8. P. 36-44.
- Zaza S. et al. Recent advances in the separation and determination of impurities in pharmaceutical products//Instrumentation Science & Technology. 2015. V. 43. №. 2. P. 182-196.
- Jamaly S., Giwa A., Hasan S. W. Recent improvements in oily wastewater treatment: progress, challenges, and future opportunities//Journal of Environmental Sciences. 2015. V. 37. P. 15-30.
- Чудакова О.Г., Бескровный Д.В. Анализ и оценка сточных вод пивоваренного производства//Вестник Казанского технологического университета. 2015. Т. 18. № 16. С. 293-295.
- Сепченко Г.Б., Пикула Н.П., Дубова Н.М., Щукина Т.И. и др. Элетрохимический контроль качества вод (обзор)//Известия Томского политехнического университета. Инжиниринг георесурсов. 2009. Т. 314. № 3. С. 59-70.
- Холмберг К, Йенссон Б., Кронберг Б. и др. Поверхностно-активные вещества и полимеры в водных растворах. М.: БИНОМ. Лаборатория знаний, 2007. 528 с.
- Shinoda K., Nakagawa T., Tamamushi B. I. Colloidal surfactants: some physicochemical properties. Volume 12. Elsevier, 2016.
- Hao T. Exploring the charging mechanisms in non-aqueous multiphase surfactant solutions, emulsions and colloidal systems via conductivity behaviors predicted with eyring's rate process theory//Physical Chemistry Chemical Physics. 2016. V. 18. №. 1. P. 476-491.
- Nabi A. et al. Study of interaction between cationic surfactant (CTAB) and paracetamol by electrical conductivity, tensiometric and spectroscopic methods//Journal of Molecular Liquids. 2018. V. 256. P. 100-107.
- Щукин Е.Д., Перцов А.В., Амелина Е.А. Коллоидная химия. М.: Юрайт, 2012. 444.
- Фролов Ю.Г. Курс коллоидной химии. Поверхностные явления и дисперсные системы. М.: ИД Альянс, 2009.
- Корниенко Т.С., Гаршина С.И., Мастюкова Т.В. и др. Лабораторный практикум по коллоидной химии. Воронеж, ВГТА, 2001. 76 c.
- Алейнер Г.С., Усьяров О.Г. Электропроводность мицеллярных растворов ионных ПАВ и поверхностная проводимость мицелл//Коллоидный журнал. 2010. Т. 72. № 5. С. 580-586.
- Тихова А.А., Глухарева Н.А., Колесникова Е.Н. Изучение агрегации в водных растворах оксиэтилированных неионогенных поверхностно-активных веществ методом динамического светорассеяния//Научные ведомости. Серия Естественные науки. 2010. T. 13. № 21. С. 127-130.
- Вережников В.Н., Гермашева И.И., Крысин М.Ю. Коллоидная химия поверхностно-активных веществ. СПб.: Издательство «Лань», 2015. 304 с.


