Разработка стратегии оптимизации фармакотерапии на основании «ивабрадинового теста»
Автор: Толкачев Б.Е., Магницкая О.В., Смирнова Л.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Фармакология токсикология
Статья в выпуске: 1 (49), 2016 года.
Бесплатный доступ
В рамках исследования была проведена оценка информативности новой фенотипической пробы в реальной клинической практике. Основываясь на полученных данных, было сделано заключение, что ивабрадин может использоваться в качестве перспективного маркерного субстрата у пациентов с измененной активностью СYP3A4. Кроме того, определяемой по моче метаболический индекс «N-десметиливабрадин/ивабрадин» применим как биомаркер для оптимизации фармакотерапии.
Персонализированная медицина, ивабрадин, фенотипирование, сyp3a4, ферменты метаболизма лс, хроматография
Короткий адрес: https://sciup.org/142149163
IDR: 142149163 | УДК: 615.1:54
The use of ivabradine for pharmacotherapy optimization
Evaluation of newly developed phenotyping probe in clinical practice was performed. Based on the results obtained, conclusion can be made, that ivabradine could be exploited as promising marker substrate in patients with compromised activity of CYP3A4 isoenzyme. It is also worth noting that metabolic «N-demethylivabradine/ivabradine» ratio could serve as a biomarker for pharmacotherapy optimization.
Текст научной статьи Разработка стратегии оптимизации фармакотерапии на основании «ивабрадинового теста»
Разработка эффективных подходов к персонализации фармакотерапии является в настоящее время одним из приоритетных направлений клинико-фармакологических исследований [1, 2]. К числу таких подходов можно отнести фенотипирование ферментов метаболизма, которое заключается в оценке их активности in vivo с использованием различных маркёрных субстратов [3, 6].
В связи с этим было проведено пилотное исследование возможности использования ивабра-дина в качестве маркерного субстрата для оценки активности изофермента СYP3A4 у пациентов, принимающих в составе плановой терапии индукторы и ингибиторы данной изоформы, а также дальнейшей разработки неинвазивного скринингового теста как основы для новой стратегии оптимизации режима дозирования препаратов.
ЦЕЛЬ РАБОТЫ
Подтвердить информативность «ивабради-нового теста» в реальной клинической практике и возможность его использования в качестве основы для разработки алгоритма коррекции фармакотерапии у пациентов с измененной активностью изофермента CYP3A4 в условиях полипрагмазии.
МЕТОДИКА ИССЛЕДОВАНИЯ
В исследовании принимали участие две группы пациентов, находящиеся на лечении в НУЗ «Отделенческая клиническая больница на ст. Вол-гоград-1 ОАО ”РЖД“» и подписавшие информированное согласие на участие в исследовании.
Пациенты обеих групп принимали в составе плановой фармакотерапии препараты, влияющие на активность изофермента CYP3A4. Первую из них составили пациенты с обострением язвенной болезни, которым в составе плановой эрадикационной терапии был назначен кларитромицин – антибиотик из группы макролидов, в дозе 1 000 мг/сут. Вторая группа состояла из пациентов неврологического отделения, которым в связи с нейропатическими болями был назначен карбамазепин – индуктор CYP3A4, в дозе 400 мг/сут.
Данные препараты оказываются способными влиять на плазменные концентрации совместно с назначаемыми препаратами, что приводит к увеличению риска нежелательных лекарственных реакций либо снижению эффективности терапии [4, 8].
Фармакотерапия кларитромицином и карбамазепином назначалась пациентам лечащим врачом в плановом порядке.
Для оценки активности изофермента CYP3A4, включенным в исследование пациентам однократно назначался ивабрадин (Кораксан®, Servier, Франция) в дозе 10 мг в 2000. После этого в моче, собранной за 12 ч, определяли содержание ивабрадина и его N-деметилированного метаболита.
Количественный анализ концентраций искомых субстанций в моче пациентов был проведен с использованием валидированного метода ВЭЖХ с флуоресцентной детекцией [3, 5].
Метаболическое отношение в моче, собранной за 12 ч после однократного приема ивабрадина, рассчитывалось по отношению кумулятивной экскреции (CE) N-десметил-ивабрадина к ивабрадину, равной произведению концентрации вещества (С) на объем мочи (V):
_ CE0-124N-IVB ^1ХМОча
^М)-12ч IVB
Cn-IVBXVo-124
CivbXVq-124
Пробы мочи анализировали в обеих группах исходно и через 7 суток в группе 1 или 14 суток в группе 2 (рис. 1).
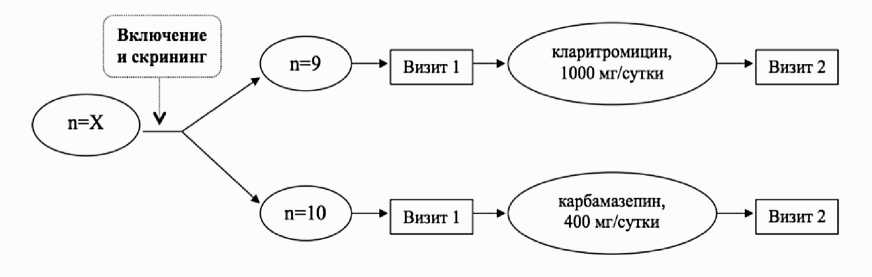
Рис. 1. Дизайн изучения активности изофермента CYP3A4 у пациентов на фоне приема индукторов либо ингибиторов
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
Результаты определения кумулятивной экскреции ивабрадина и его метаболита с мочой, собранной в течение 12 часов после однократного приема 10 мг препарата Кораксан® пациентами исходно и спустя 7 дней приема кларитромицина в дозе 1 000 мг/сут., представлены в табл. 1.
В результате было установлено, что кумулятивная экскреция ивабрадина в группе пациентов, получающих кларитромицин, повысилась на 8,5 %, в то время как экскреция N-десметиливабрадина снизилась на 38,2 %.
Для оценки активности CYP3A4 исходно и после курсового приема кларитромицина рассчитывалось метаболическое отношение кумулятивной экскреции N-десметиливабрадина и ивабрадина с мочой (табл. 2).
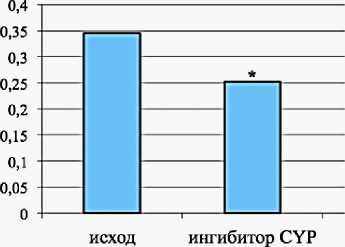
Достоверное уменьшение метаболического отношения в моче на 26,9 % подтвердило ожидаемое ингибирование CYP3A4 на фоне приема кларитромицина (рис. 2 а ).
В группе пациентов, получающих карбамазепин, были зафиксированы обратные изменения: 12-часовая экскреция с мочой ивабрадина увеличилась на 17 %, а метаболита – повысилась на 87,1 % (табл. 3).
Для оценки активности CYP3A4 исходно и после курсового приема карбамазепина также рассчитывалось метаболическое отношение кумулятивной экскреции N-десметиливабрадина и ивабрадина с мочой (табл. 4).
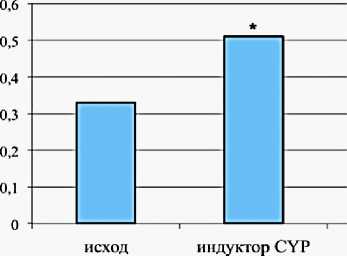
На фоне приема карбамазепина было зафиксировано достоверное увеличение на 54,2 % определяемого по моче метаболического отношения, что указывает на развитие индукции изофермента СYP3A4 (рис. 2 б ).
Таблица 1
Кумулятивная экскреция с мочой и метаболическое отношение ивабрадина и N-десметиливабрадина пациентов исходно и на фоне приема ингибитора CYP3A4 [Me (LQ; UQ)]
|
Кумулятивная экскреция |
Визит 1 |
Визит 2 (ингибитор CYP3A4) |
|
CE IVB , мкг |
163,21 (116,53; 211,89) |
177,19 (156,88; 222,47) |
|
CE N-IVB , мкг |
59,15 (39,66; 70,29) |
36,52 (30,84; 53,51) |
Таблица 2
Метаболические отношения, рассчитанные по моче пациентов исходно и на фоне приема ингибитора CYP3A4 [Me (LQ; UQ)]
|
Метаболическое отношение |
Визит 1 |
Визит 2 (ингибитор CYP3A4) |
р* |
|
MR моча |
0,3450 (0,32; 0,361) |
0,2520 (0,1905; 0,2575) |
0,008 |
Таблица 3
Кумулятивная экскреция с мочой и метаболическое отношение ивабрадина и N-десметиливабрадина у пациентов исходно и на фоне приема индуктора изофермента CYP3A4 [Me (LQ; UQ)]
|
Кумулятивная экскреция |
Визит 1 |
Визит 2 (индуктор CYP3A4) |
|
CE IVB , мкг |
198,54 (131,77; 312,45) |
232,41 (180,01; 274,15) |
|
CE N-IVB , мкг |
65,6 (48,61; 90,34) |
122,75 (93,16; 136,83) |
Таблица 4
Метаболические отношения, рассчитанные по моче пациентов исходно и на фоне приема индуктора CYP3A4 [Me (LQ; UQ)]
|
Метаболическое отношение |
Визит 1 |
Визит 2 (индуктор CYP3A4) |
р* |
|
MR моча |
0,3295 (0,2865; 0,3733) |
0,5080 (0,4450; 0,5455) |
0,005 |
Примечание: *р – критерий Вилкоксона.
ЗА4
ЗА4
б
Рис. 2. Метаболические отношения, определенные в моче пациентов исходно и после курсового приема ингибитора ( а ) и индуктора ( б ) CYP3A4 (*р < 0,05; критерий Вилкоксона)
ЗАКЛЮЧЕНИЕ
Таким образом, фенотипирование CYP3A4 с использованием «ивабрадинового теста» позволяет проводить мониторинг изменения активности данного изофермента у пациентов, получающих его индукторы, либо ингибиторы в составе плановой фармакотерапии.
Метаболическое отношение может служить достоверным показателем активности фермента CYP3A4 и использоваться для разработки протокола оптимизации фармакотерапии у пациентов на фоне полипрагмазии.
Список литературы Разработка стратегии оптимизации фармакотерапии на основании «ивабрадинового теста»
- От прикладных фармакокинетических исследований -к внедрению персонализированной фармакотерапии в реальную клиническую практику/Н. Г. Филиппенко, O. В. Поветкин, Г. O. Маль и др.//Биомедицина. -2010. -№ 3. -O. 158-160.
- Оценка активности изофермента цитохрома Р450 3a4 (CYP3A4) как реальная возможность персонализации фармакотерапии/В. Г. Кукес, Д. А. Сычев, Г. В. Раменская и др.//Врач. -2008. -№ 3. -С. 13-18.
- Сравнительная оценка методов определения метаболического коэффициента N-десметиливабрадин/ивабрадин в плазме и моче/В. И. Петров, О. В. Магницкая, Б. Е. Толкачёв и др.//Вестник ВолгГМУ. -2013. -№ 3 (47). -С. 33-34.
- CYP3A4 substrate selection and substitution in the prediction of potential drug-drug interactions/A. Galetin, K. Ito, D. Hallifax, et al.//J. Pharmacol. Exp. Ther. -2005. -№ 314. -P. 180-190.
- Determination of ivabradine and its N-demethylated metabolite in human plasma and urine, and in rat and dog plasma by a validated high-performance liquid chromatographic method with fluorescence detection/P. Klippert, J. P. Jeanniot, S. Polvé, et al.//J. Chromatogr. B Biomed. Sci. Appl. -1998. -№ 20 (719). -P. 125-133.
- Kivisto K. T., Kroemer H. K. Use of probe drugs as predictors of drug metabolism in humans//J. Clin. Pharmacol. -1997. -№ 37. -P. 40-48.
- Oral administration of a low dose of midazolam (75 microg) as an in vivo probe for CYP3A activity/C. B. Eap, T. Buclin, G. Cucchia, et al.//Eur. J. Clin Pharmacol. -2004. -№ 60. -P. 237-246.
- Zaigler M., Tantcheva-Poor I., Fuhr U. Problems and perspectives of phenotyping drug-metabolizing enzymes in man//Int. J. Clin. Pharmacol. Ther. -2000. -№ 37. -P. 1-9.


