Разработка удобной процедуры синтеза циклических непептидных аналогов ингибитора ВИЧ-1 протеазы и моделирование их свойств
Автор: Винюков А.В., Стариков А.С.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Химические науки
Статья в выпуске: 4-2 (43), 2020 года.
Бесплатный доступ
Разработка методик получения новых физиологически активных веществ является одним из самых важных направлений для современной органической химии. Бис(α-аминоалкил) фосфиновые кислоты симметричного строения, как известно, являются эффективными ингибиторами ВИЧ-1 протеазы, а также промежуточными продуктами для получения ряда непептидных аналогов ингибитора ВИЧ-1 протеазы циклического строения. Ранее нами был описан ряд процедур синтеза N-защищенных бис(α-аминоалкил) фосфиновых кислот путем двойного амидоалкилирования гидрофосфорильных соединений. Кроме того, циклизация свободных бис(α-аминоалкил) фосфиновых кислот позволила нам получить ряд непептидных циклических аналогов ингибитора ВИЧ-1 протеазы. Настоящая работа посвящена использованию бис(α-аминоалкил)фосфиновых кислот как «строительные блоки» в комбинации со «структурным имитатором воды» для образования мощных непептидных ингибиторов протеазы ВИЧ. Кроме того, нами был проведен предсказательный анализ полученных веществ на предмет физиологической активности и токсичности.
Ингибиторы вич-1 протеазы, амидоалкилирование гидрофосфорильных соединений, фосфиновые кислоты, двойное амаидоалкилирование, непептидные аналоги ингибитора вич-1 протеазы
Короткий адрес: https://sciup.org/170187555
IDR: 170187555 | DOI: 10.24411/2500-1000-2020-10349
Development of a convenient procedure for the synthesis of cyclic non-peptide analogues of the HIV-1 protease inhibitor and modeling their properties
The development of methods for obtaining new physiologically active substances is one of the most important areas for modern organic chemistry. Bis (α-aminoalkyl) phosphinic acids of the symmetric structure are known to be effective HIV-1 protease inhibitors, as well as intermediate products for the preparation of some non-peptide analogs of the HIV-1 protease inhibitor of the cyclic structure. We previously described a series of procedures for the synthesis of N-protected bis (α-aminoalkyl) phosphinic acids by double amino alkylation of hydrophosphoryl compounds. Also, the cyclization of free bis (α-aminoalkyl) phosphinic acids allowed us to obtain several non-peptide cyclic analogs of the HIV-1 protease inhibitor. The present work is devoted to the use of bis (α-aminoalkyl) phosphinic acids as “building blocks” in combination with a “structural water mimic” for the formation of potent non-peptide HIV protease inhibitors. Also, we conducted a predictive analysis of the obtained substances for physiological activity and toxicity.
Текст научной статьи Разработка удобной процедуры синтеза циклических непептидных аналогов ингибитора ВИЧ-1 протеазы и моделирование их свойств
На данный момент известно целый ряд известных ингибиторов ВИЧ-1 протеазы (индинавир, саквинавир), используемых при терапии ВИЧ. И все они обладают побочными эффектами и подходят далеко не во всех случаях. Механизм их действия заключается во встраивании в активный участок фермента, препятствуя тем самым расщеплению полипротеина Gag-Pol на отдельные белки и последующему созреванию вирусных частиц, которые становятся не способными заражать новые клетки. Ранее было обнаружено, что фос- финовые кислотные изостеры гексапептидов являются мощными ингибиторами протеазы ВИЧ [1-4].
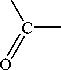
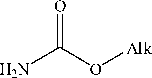
Существует достаточное количество методов получения симметричных бис(а-аминоалкил)фосфиновых кислот [5-7]. Ранее нами была предложена трехкомпонентная процедура амидоалкилирования гипофосфористой кислоты с получением N-защищенных бис(а-аминоалкил)фосфиновых кислот симметричного строения (рис. 1) [8-9].
OH
HPH
O
1 equiv
H
2 equiv
2 equiv
-
1. TSA
-
2. H2O
Ac 2 O
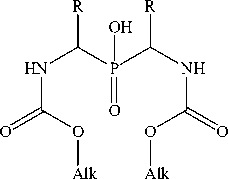
R= Me, Et, i-Pr, i-Bu, sec-Bu, Ph Alk = Me, Et, Bn
Рис. 1. Трехкомпонентное «двойное» амидоалкилирование гипофосфористой кислоты
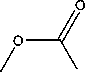
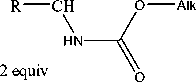
Кроме того, при использовании в качестве исходного реагента алкилиденби-скарбаматов в двухкомпонентной реакции амидоалкилирования гипофосфористой кислоты с последующей обработкой реак- ционной смеси соответствющим спиртом, удалось получить P, N-защищенные бис(α-аминоалкил)фосфиновые кислоты симметричного строения (рис. 2) [9].
OH
HPH
O
1 equiv
Alk NH
-
1. TSA
-
2. EtOH
Ac 2 O
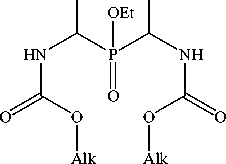
R= Me, Et, i-Pr, i-Bu, sec-Bu, Ph Alk = Me, Et, Bn
Рис. 2. Двухкомпонентное «двойное» амидоалкилирование гипофосфористой кислоты
В настоящей работе полученные и описанные ранее метиловые эфиры бис(α-амино)фосфиновых кислот 1 подвергали взаимодействию с карбонилдиимидазолом с получением циклических мочевин 2 I (рис. 3), затем N-алкилировали в присутствии NaH в среде ДМСО II. Далее эфир фосфиновой кислоты расщепляется с помощью HBr в уксусной кислоте с получением свободных кислот 4 III (рис. 3). Для синтеза N-(4-гидроксиметил) бензилзаме-щенных соединений 3 проводили алкилирование в присутствии 4-(4-метоксифеноксиметил) бензилбромида II. Бензиловый эфир 3 также разрушался при обработке HBr III, поэтому полученный бромид был превращен в соответствующий гидроксид 5 путем обработки CaCO3 в смеси диоксан/вода IV (рис. 3).
Далее нами был проведено прогнозирование биологической активности полученных циклических аналогов ингибитора ВИЧ-1 протеазы 5 (рис. 3) программой
PASS (“Prediction of Activity Spectra for Substances”), разработанной в Институте биомедицинской химии им. В.Н. Орехови-ча РАМН (табл. 1). Результаты прогноза биологической активности представлены в виде спектра биологической активности, включающих список активностей и вероятностей: Ра - «быть активным», Рi -«быть неактивным. В качестве контрольного вещества выступили бензил-замещенные молекулы (R = CH2Ph), которые были ранее синтезированы, испытаны и показали антивирусную активность. Было обнаружено, что в ряде полученных циклических аналогов ингибитора ВИЧ-1 протеазы у большинства полученных соединений присутствует достаточно большая вероятность проявить ВИЧ-антивирусную активность. Что в свою очередь делает их перспективными для дальнейших исследований их реальной физиологической активности.
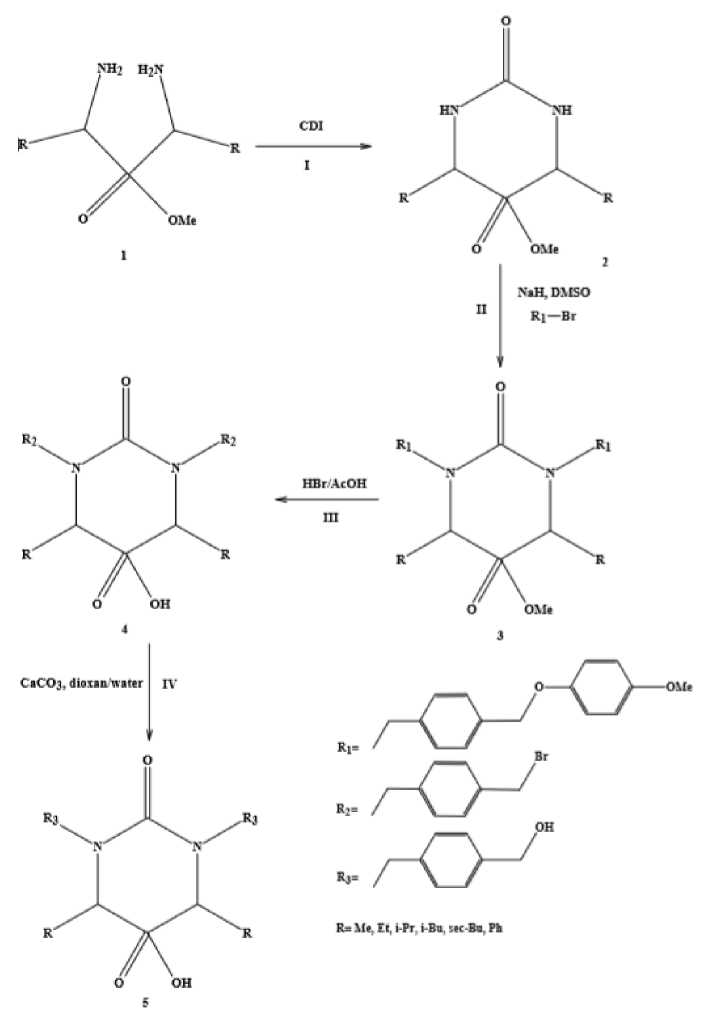
Рис. 3. Получение фосфиновых циклических непептидных аналогов ингибиторов ВИЧ-1 протеазы
Таблица 1. Прогнозирование биологической активности полученных циклических аналогов ингибитора ВИЧ-1 протеазы программой PASS
|
R |
Pa(Antiviral HIV) |
Pi(Antiviral HIV) |
|
Bn |
0.957 |
0.002 |
|
Me |
0.843 |
0.003 |
|
Et |
0.838 |
0.003 |
|
i-Pr |
0.812 |
0.003 |
|
sec-Bu |
0.781 |
0.003 |
|
Ph |
- |
- |
Bспользование программы GUSAR
(«General Unrestricted Structure-Activity Re- lationships») дало возможность оценить уровень острой токсичности для крыс
(LD50 мг/кг) полученных соединений. Для оценки острой токсичности для описания структур химических соединений в программе используются дескрипторы многоуровневых атомных окрестностей (MNA – Multilevel Neighborhoods of Atoms) и количественных атомных окрестностей (QNA – Quantitative Neighborhoods of Atoms). В GUSAR для построения моделей используется алгоритм самосогласованной регрессии (SCR). Так как большая часть перпаратов против ВИЧ принимаются перорально, то в качестве критерия будут рас- сматриваться только пероральная и внутривенная острые токсичности (рис. 4).
Согласно классификации острой токсичности Организации экономического сотрудничества и развития (OECD) все соединения являются малотоксичными (5 и 4 классом токсичности), за исключением контрольного бензил-замещенного, который обладает 3 классом токсичности. Что в свою очередь также указывает на перспективность дальнейших исследований полученных соединений на предмет их непосредственного применения при терапии ВИЧ.
oral, logLD50(mmol/kg)
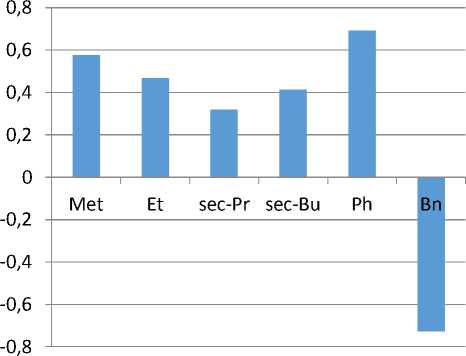
■ oral, logLD50(mmol/kg)
Рис. 4. Уровени острой токсичности при пероральном введении для крыс (LD50 ммоль/кг)
полученных соединений
Таким образом, важным результатом данного является получение ряда новых ранее неописанных фосфиновых соединений циклической структуры, являющихся структурными аналогами ингибитора ВИЧ-1 протеазы. Кроме того, моделирование физиологической активности позволи- ло сделать вывод об перспективности дальнейшего изучения полученных веществ. Данные и результаты, полученные в ходе настоящего исследования, могут быть использованы в изучении и терапии ВИЧ.
Список литературы Разработка удобной процедуры синтеза циклических непептидных аналогов ингибитора ВИЧ-1 протеазы и моделирование их свойств
- D. Grobelny, E.M. Wondrak, R.E. Galardy, S. Oroszlan, B&hem. Biophys. Res. Commun. 169 (1990) 1111.
- K.-H. Budt, A. Peyman, EP 0435059,199O; K.-H. Budt, J. Knolle, C. Meichsner. D. Ruppert, B. Stowasser, I. Winkler, A. Paessens, J. Hansen, EP 0428849A2 1990.
- J. Erickson, D.J. Neidhart, J. VanDrie, D.J. Kempf. X.C. Wang, D.W. Norbeck, J.J. Plattner, J.W. Rittenhouse, M. Turon, N. Wideburg, W. E. Kohlbrenner, R. Simmer, R. Helfrich, D.A. Paul Knigge, Science 249 (1990) 527.
- D.J. Kempf, D.W. Norbeck, L. Codacovi, X.C. Wang, W.E. Kohlbrenner, N.E. Wideburg, D.A. Paul, M.F. Knigge, S. Vasavonda, A. Craig-Kennard, A. Saldivar, W. Rosenbxocok Jr., J.J. Peyman, A. C2-symmetric phosphinic acid inhibitors of HIV protease / A. Peyman, K.-H. Budt, J. Spanig, B.Stowasser, D. Ruppert // Tetrahedron Lett. - 1992, -33, - 4549.
- Maier, L. Organic phosphorus compounds: LXXI. Preparation, properties, and structure of bis(aminomethyl)phosphinic acid, (H2NCH2)2P(O)OH / L. Maier // Journal of Organometallic Chemistry. -1979, -V. 178, -P. 157-169.
- Peyman, A. Inhibition of human immunodeficiency virus-1 protease by a C2-symmetrical phosphinic acid amide / A. Peyman, K. Wagner, K-H. Budt, J. Spanig, D. Ruppert, C. Meichsner, A. Paessens // Bioorg. Med. Chem. Lett. - 1994, - 4, - 1191.
- Tyka, R. Synthese symmetrischer und asymmetrischer a,a'-bis(aminoalkyl)phosphinsauren des typs NH2CHR1(NH2CHR2)P(O)OH(R1 = Ph; R2 = Ph, Me) / R. Tyka, G. Hagales, R. Boetzel // Phosphorus, Sulfur, and Silicon. -1991. -Vol. 62. -Р.75-81.
- Vinyukov A.V. An efficient one-pot synthesis of bis(a-aminoalkyl)phosphinic acids, phosphorus-isosteric analogues of HIV protease inhibitors / A.V. Vinyukov, A.V. Borodachev, A.S. Starikov, A.V. Afanasyev, M.E. Dmitriev, B.V. Lednev, V.V. Ragulin // Mendeleev Commun. -2018, -V.28, -P. 1-2.
- Винюков А.В. Получение непептидных аналогов ингибитора вич-1 протеазы и моделирование их физиологической активности / А.В. Винюков, А.С. Стариков // Химия, физика, биология, математика: теоретические и прикладные исследования: сб. ст. по материалам XXXIII Международной научно-практической конференции "Химия, физика, биология, математика: теоретические и прикладные исследования". - № 2 (23). - М., Изд. "Интернаука", 2020.


