Разработки южного научного центра ран в области криоконсервации репродуктивных клеток рыб
Автор: Белая Мария Михайловна, Красильникова Александра Андриановна, Пономарева Елена Николаевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Общая биология
Статья в выпуске: 5-2 т.20, 2018 года.
Бесплатный доступ
В статье рассматриваются вопросы низкотемпературного консервирования репродуктивных клеток рыб сотрудниками Южного научного центра Российской академии наук. Отмечено, что удалось усовершенствовать методику замораживания спермы рыб, которая показывает стабильно высокие результаты по выживаемости и активности дефростированных сперматозоидов (80-90 %). При хранении образцов репродуктивных клеток в жидком азоте, их качество не изменяется на протяжении долгого времени. На основании проведенных исследований создан криобанк генетического материала рыб.
Биоразнообразие, криоконсервация, репродуктивные клетки, редкие и исчезающие виды рыб, криобанк
Короткий адрес: https://sciup.org/148314065
IDR: 148314065 | УДК: 576.371
The developments of southern scientific center of the Russian academy of sciences in the field of cryopreservation of reproductive cells of fish
In the article the questions of low-temperature conservation of reproductive cells of fish by employees of Southern scientific center of the Russian academy of Sciences are considered. It was noted that it was possible to improve the method of freezing fish sperm, which shows consistently high results on the survival and activity of defrosted sperm (80-90 %). During the storage of samples of reproductive cells in liquid nitrogen the quality of them does not change for a long time. On the base of conducted researches a cryobank of the genetic material of fish was created.
Текст научной статьи Разработки южного научного центра ран в области криоконсервации репродуктивных клеток рыб
Работы выполнены в рамках реализации Гранта Президента РФ для государственной поддержки молодых российских ученых МК-159.2017.11 и ГЗ ЮНЦ РАН «Оценка современного состояния, анализ процессов формирования водных биоресурсов южных морей России в условиях антропогенного стресса и разработка научных основ технологии реставрации ихтиофауны, сохранения и восстановления хозяйственно ценных видов рыб»,
№ госрегистрации 01201354245» c использованием
Биоресурсной коллекции редких и исчезающих видов рыб ЮНЦ РАН № 73602.
Сохранение биоразнообразия естественных популяций рыб является неотъемлемой частью современной науки. В условиях катастрофического снижения численности большого количества ценных промысловых рыб в последние годы, а также в связи с нарушением видового и популяционного баланса, этот вопрос становится особенно актуальным.
В настоящее время гидрология ряда рек изменена настолько, что многие виды рыб не имеют возможности воспроизводства естественным путем [1].
Для сохранения и восполнения численности отдельных популяций рыб разработаны биотехнологии искусственного воспроизводства на различных рыбоводных предприятиях. В их основу положены принципы содержания и использования производителей из маточных стад, содержащихся на предприятии, что, в свою оче-
редь, ограничивает число особей, скрещивающихся между собой, и приводит впоследствии к инбридингу. Кроме того, в формировании маточных стад на рыбоводных заводах, особенно осетровых, отсутствуют какие-либо принципы и, зачастую, оно носит стихийный характер, что связано с нехваткой производителей.
Все это отражается на качестве (физиологическая, генетическая полноценность) молоди, выпускаемой с рыбоводных заводов [2-5]. Отмечено, что выпуск «заводской» молоди осетровых в водоемы увеличивает долю гетерозигот в популяции, а это приводит к сокращению численности и постепенной деградации потомства [6-9].
Криоконсервация остается одним из наиболее привлекательных и быстроразвивающихся направлений сохранения редких исчезающих видов. Наличие в криобанке генетически репрезентативных коллекций геномов рыб и маточных стад на рыбоводных заводах позволяет с максимальным эффектом сохранить генетическое разнообразие ценных промысловых объектов [10].
В настоящее время имеются данные о сохранении живых органелл, клеток, тканей, органов и целых организмов при сверхнизких температурах в течение длительного периода времени. Криоконсервацию широко используют для хранения спермы и эмбрионов млекопитающих, но исследований по криосохранению клеток морских гидробионтов немного.
Полученные результаты по дефростирован-ной сперме, а также по оплодотворяемости ею икры различных видов рыб нестабильны и варьируют в широких пределах (10-90 %). Тем не менее, для сохранения редких и исчезающих видов существующие методы криоконсервации их спермы пригодны для замораживания биоматериала, хранения в коллекционных банках и восстановления гидробионтов.
Однако проблема создания криотехнологий для больших объемов спермы, необходимых для формирования производственных криобанков, внедрения криотехнологий в производство решается очень медленно. Можно повысить эффективность существующей системы селекционно-племенных хозяйств и рыбоводных заводов, если использовать криотехнологии в процессе воспроизводства промысловых и заводских популяций.
Вопросами сохранения редких и исчезающих видов рыб методами низкотемпературного консервирования занимаются ученые Южного научного центра Российской академии наук (ЮНЦ РАН) с 2004 г. Разработки и достижения подтверждены патентами, ноу-хау, публикациями в ведущих российских и зарубежных изданиях [10-29].
До настоящего времени нет универсальной методики криоконсервации репродуктивных клеток рыб, что связано с их видоспецифич-ностью, обусловленной различным строением спермиев и яйцеклеток у разных видов рыб.
Способы криоконсервации различаются обычно: по составу основного криозащитного раствора и наличию дополнительных компонентов (сахара, белки, яичный желток, липиды); по скоростям охлаждения; используемому криопротектору; объему замораживаемого материала [30, 31].
Считается, что существенную роль в криоповреждении могут играть кристаллы льда, формирующиеся при замерзании криозащит-ных растворов.
Образование кристаллов льда наряду с другими негативными факторами (осмотический шок, латеральная диффузия липидов и белков, рекристаллизация при оттаивании, токсичность растворов криопротекторов) значительно снижает выживаемость клеток после процедуры замораживания-оттаивания при криоконсервации живых клеток и, в частности, сперматозоидов [32].
При поиске эффективных криозащитных составов надо учитывать не только размер и периметр кристаллов льда, образующихся при замерзании криозащитного раствора, но и форму кристаллов. Наиболее эффективны криозащит-ные растворы, при замерзании которых образуются кристаллы округлой формы, или наблюдается картина, близкая к стеклованию [33].
Сотрудниками ЮНЦ РАН разработаны оптимальные составы криосред для осетровых, карповых, белорыбицы [16, 17, 20, 22], обеспечивающие высокий уровень выживаемости дефро-стированных сперматозоидов (60-85 %) [34].
При охлаждении клеток важно избежать образования внутриклеточного льда или минимизировать процесс. При быстром замораживании (выше 100 °C/мин) внутриклеточная вода не успевает выйти из клеток, переохлаждается, что приводит к образованию кристаллов льда внутри клеток [35]. При медленном замораживании (менее 0,1 °C/мин) клетки теряют много воды, а это ведет к сжатию и лизису клеток. Поэтому для успешной криоконсервации необходим баланс между двумя негативными факторами: образованием внутриклеточного льда и осмотическими эффектами [36].
По результатам работ сотрудников ЮНЦ РАН определены оптимальные скорости замораживания для разных видов рыб. Так установлено, что для русского осетра оптимальная скорость замораживания 3 °C/мин [17], для белорыбицы – сверхскоростное замораживание на тефлоновой пластине [20], для карповых – ступенчатый режим замораживания (6 ºС/мин в течение 6 минут, 10 ºС/мин, в течение 4 минут, затем погружение в жидкий азот) [14, 37, 38, 39].
Для улучшения проникновения криораствора в клетки научные сотрудники ЮНЦ РАН разработали методику электростимуляции спермы рыб перед эквилибрацией. Так, установлено, что при воздействии прямоугольного низкочастотного сигнала на семенную жидкость, увеличивается процент живых клеток после дефростации [10, 15, 17-19].
Однако все криопротекторы оказывают токсическое воздействие на сперму рыб при длительном контакте [34, 40-43]. После размораживания часто отмечаются живые сперматозоиды, которым не хватает энергии для активации движения. Также установлено, что дефростирован-ные спермии начинают двигаться не сразу после активации водой, а спустя некоторое время [44]. Для снижения негативного влияния криопротекторов создан метод выведения токсических веществ из репродуктивных клеток [10, 17, 21].
На основе проведенных исследований сотрудниками ЮНЦ РАН усовершенствована технология криоконсервации спермы рыб (Рис. 1) [10, 17].
Из рисунка 1 видно, что качество дефрости-рованной спермы, замороженной по усовершенствованной схеме, значительно выше, чем по традиционной схеме. Сперму такого высокого качества целесообразно использовать для оплодотворения икры, а также для формирования криобанка.
Применение электростимуляции и выведения криопротектора из половых клеток после

Разбавление спермы криозащитной средой
Разбавление спермы криозащитной средой
Эквилибрация
Эл ектро стимуляция
Замораживание
Эквилибрация
Дефростирование
Замораживание
Выживаемость
50 – 60 %
Дефростирование
Выведение протектора раствором NaCl
+
Эл ектростимуляция
Выживаемость
80 – 90 %
Рис. 1. Качество спермы рыб в процессе криоконсервации с использованием усовершенствованной схемы дефростации увеличивает репродуктивные качества спермы рыб. Каждое из новых звеньев процесса криоконсервации способствует улучшению качества спермы, однако применение их в совокупности дает наилучший эффект (Рис. 2).
Однако активность и время жизни сперматозоидов являются субъективными показателями качества. Наиболее убедительными тестами успешности криоконсервации служат оплодотворение размороженными сперматозоидами и последующий анализ полученных эмбрионов.
Сначала проводят оплодотворение икры в лабораторных условиях в небольших количествах, а затем в производственных условиях на крупных партиях икры.
В лабораторных условиях получены стабильно высокие показатели оплодотворения икры дефростированной спермой осетровых рыб – 80-90 %. Показатели оплодотворения икры тех же партий нативной спермой в условиях рыбоводного завода составили 70-75 %.
Это объясняется тем, что для каждой партии спермы свойственна гетерогенность структуры. Наиболее активные спермии, способные к высокому проценту оплодотворения составляют, как правило, 25%; 60% партии – сперма среднего качества, спермии которой способны к оплодотворению, и третья составляющая 15% – нежизнеспособная сперма [45].
В процессе низкотемпературного консервирования в первую очередь гибели подвержены слабые спермии, после дефростации живыми остаются более сильные, способные к высокому уровню оплодотворения спермии. Таким образом, криоконсервация может служить способом получения элитных сперматозоидов, дающих мощное, физиологически полноценное потомство.
Это подтверждается исследованиями по оплодотворению икры в условиях рыбоводных заводов, проведенными с использованием деф-ростированной спермы русского осетра и белорыбицы [10, 20]. Отмечено, что полученное потомство по морфометрическим и физиологическим показателям не уступает нативному, а зачастую и превосходит его [10, 26, 28].
На основе усовершенствованной методики низкотемпературного консервирования половых клеток рыб начато формирование криобанка-репродуктора, основной целью которого является сохранение генетического разнообразия рыб и обеспечение рыбоводных предприятий репродуктивными клетками в необходимом количестве.
Криобанк ежегодно пополняется образцами спермы различных видов рыб. В настоящее время на долгосрочное хранение заложено более 12 л спермы ценных видов рыб (русский осетр, белуга, севрюга, стерлядь, веслонос, шип, белорыбица).
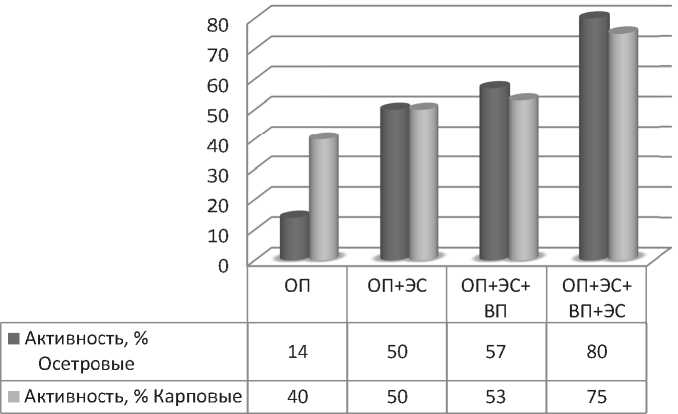
A
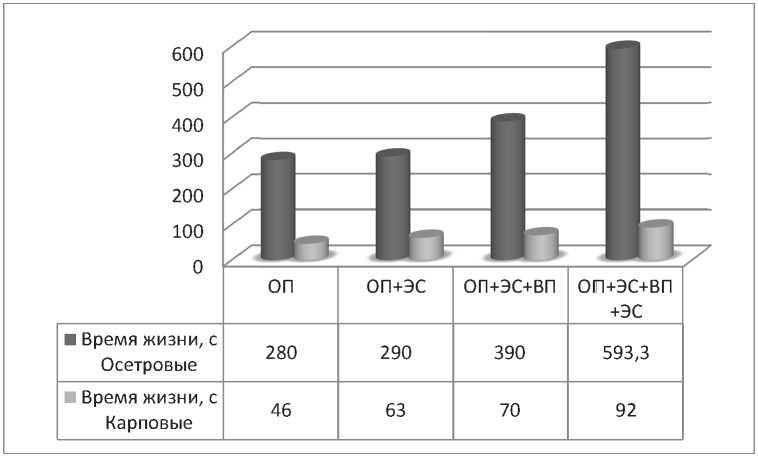
Б
Рис. 2. Изменение качества дефростированной спермы при использовании разных способов криоконсервации: А – активность дефростированной спермы, с; Б – время жизни спермиев, с;
ОП – применение оптимальных протекторов, ЭС – электростимуляция, ВП – выведение протектора из клеток
Ведется систематическая проверка качества спермы, хранящейся в криобанке. Установлено, что за это время сперма не утрачивает оплодотворяющей способности (Табл. 1).
Полученные данные сопоставимы с теоретическими расчетами времени хранения спермы, при котором не изменяется качество спермы. По мнению некоторых авторов [32] хранить образцы спермы можно сотни лет без утраты их функций.
Также сотрудники ЮНЦ РАН проводят исследования по замораживанию яйцеклеток рыб. Получены стабильные результаты по сохранению целостности оболочек икры после дефростации, а также проведены работы по оплодотворению дефростированной икры спермой [46, 47].
Сохранение репродуктивных клеток в криобанке позволяет получать необходимое количество дефростированных половых продуктов рыб в любое удобное время вне зависимости от внешних факторов. Получение свежей (нативной) спермы и икры может растягиваться на неопределенное время из-за долгого созревания производителей, также есть риск, что сперма или икра будет низкого качества или не будет получена вовсе. Криоконсервированную сперму
Таблица 1. Качество спермы стерляди после долгосрочного хранения в жидком азоте
|
Срок хранения, год |
Активность дефростированной спермы, % |
Процент оплодотворения |
|
1 |
92±2,3 |
67±3,3 |
|
2 |
90±2,0 |
69±2,7 |
|
3 |
90±1,9 |
70±2,8 |
|
4 |
90±1,8 |
67±1,9 |
|
5 |
90±2,4 |
69±2,2 |
|
6 |
90±2,1 |
70±1,7 |
можно хранить десятилетиями в жидком азоте без изменения репродуктивных показателей, в то время как нативная сохраняет свои качества в течение 3-4 суток. Ежегодное пополнение и обновление коллекции образцов репродуктивных клеток позволяет расширить генофонд воспроизводимых видов рыб; дает возможность выбора половых клеток с высокими репродуктивными качествами для проведения селекционных работ и товарного выращивания рыб.
Список литературы Разработки южного научного центра ран в области криоконсервации репродуктивных клеток рыб
- Подушка, С.Б. Кризис заводского воспроизводства в России и возможные пути его преодоления / С.Б. Подушка // Научно-технический бюллетень лаборатории ихтиологии ИНЭНКО. - 2007. № 12. - С. 5-15.
- Алтухов, Ю.П. Генетика популяций и сохранение биоразнообразия / Ю.П. Алтухов // Соросовский общеобразовательный журнал, 1995. № 1. - С. 32-43.
- Алтухов, Ю.П. Перепроизводство молоди рыбоводными заводами как причина деградации волжского стада русского осетра / Ю.П. Алтухов, А.Н. Евсюков // ДАН СССР. - 2001. - Т. 380, № 2. - С. 273-275.
- Рябова, Г.Д. О возможном влиянии рыбоводства на генетические и биологические характеристики севрюги / Г.Д. Рябова, М.В. Офицеров, В.О. Климонов // Состояние и перспективы научно-практических разработок в области марикультуры России. - М.: ВНИРО, 1996. - С. 269-274.
- Рябова, Г.Д. Влияние рыбоводства на генотипические и фенотипические характеристики волжской поздней яровой севрюги / Г.Д. Рябова, В.О. Климонов, К.И. Афанасьев // Аквакультура осетровых рыб: достижения и перспективы развития. - М.: ВНИРО, 2006. - С. 213-216.


