Развитие отечественного рынка постгеномных технологий
Автор: Кривенко Антон Николаевич, Федорончук Тамара Васильевна, Чойнзонов Евгений Лхамацыренович, Иванов Роман Алексеевич, Гришин Дмитрий Викторович, Лисица Андрей Валерьевич, Кайшева Анна Леонидовна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Передовая статья
Статья в выпуске: 6 т.17, 2018 года.
Бесплатный доступ
Выполнен анализ рынков и секторов экономики, развитие которых обеспечивается реализацией приоритета 20в «Переход к персонализированной медицине, высокотехнологичному здравоохранению и технологиям здоровьесбережения» в области постгеномных технологий, перечня ключевых технологий, включая редактирование генома и молекулярное профилирование, на основе анализа больших данных с учетом рассмотрения ключевых российских и зарубежных стратегических и прогнозных документов, прогнозов крупных корпораций и консалтинговых агентств, новостных и научных открытых российских и зарубежных ресурсов. Выполненный анализ позволил заключить, что рынок постгеномных технологий в России активно развивается. Сегменты рынка демонстрируют высокие темпы роста, следуя в русле мировых тенденций. Государственные институты развития приняли ряд программ, ориентированные на поддержку и развитие сектора практического внедрения постгеномных технологий. Политика Правительства Российской Федерации, направленная на импортозамещение зарубежных лекарств и изделий медицинского назначения, позволила создать полный цикл отечественного производства таргетных препаратов для персонализированной терапии злокачественных новообразований.
Постгеномные технологии, онкология, таргетные препараты, рынок, биотехнологии, зеленые технологии, белые технологии, красные технологии, персонализированная медицина, нанобиотехнологии, молекулярное профилирование
Короткий адрес: https://sciup.org/140254228
IDR: 140254228 | УДК: 575.113:577.21:615.2:614.2:338.2:616.04-08 | DOI: 10.21294/1814-4861-2018-17-6-7-14
Development of Russian market for postgenome technologies
We performed the analysis of the markets and sectors of the economy, the development of which is ensured by the implementation of the priority 20v «The transition to personalized medicine, high-tech health care and health protection technologies» in the field of post-genomic technologies, including genome editing and molecular profiling, based on the analysis of big data, considering the key Russian and foreign strategic and forecast documents, forecasts of large corporations and consulting agencies, news and scientific open Russian and foreign resources. The analysis showed the active development of the market for post-genomic technologies in Russia. Market segments demonstrated high growth rates, following in line with global trends. State institutions had adopted a number of programs aimed at supporting and developing the sector of practical implementation of post-genomic technologies. The policy of the Government of the Russian Federation, aimed at importing foreign drugs and medical products, created a full cycle of domestic production of targeted drugs for personalized therapy of malignant tumors.
Текст научной статьи Развитие отечественного рынка постгеномных технологий
Успешное завершение международного проекта «Геном человека» кардинальным образом изменило направление развития современной медицины, в том числе парадигму сегодняшней онкологии, и еще большие изменения можно предвидеть в ближайшем будущем. Приоритетной задачей современной медицины является внедрение новых технологий в повседневную практику [1].
Постгеномные технологии (ПГТ) опираются на знания о геномах живых организмов. К ним относят генетическое редактирование и молекулярное профилирование, включая эпигеномику, транскриптомику, протеомику, метиломику, метаболомику, интерактомику [2, 3]. Потенциал ПГТ сложно переоценить, поскольку его реализация обеспечит очередной технологический скачок и ознаменует переход к медицине нового типа. С практической точки зрения это означает радикальное улучшение диагностики, переход к персонализированной и превентивной медицине, создание новых лекарств, а также применение принципиально иных методов лечения [4, 5].
Постгеномные технологии являются сквозными технологиями и помимо медицины способны обеспечить научно-технологический прорыв в вопросах селекции новых и совершенствовании существующих сортов растений, пород животных, промышленной биотехнологии и проч. В 2017 г. Институт биомедицинской химии им. В.Н. Оре-ховича (ИБМХ) совместно с Европейской проте-омной ассоциацией (EuPA) организовали международную научную конференцию «Клиническая протеомика. Постгеномная медицина» (г. Москва). В рамках мероприятия проводилось обсуждение достижений геномных и постгеномных технологий, примеров их коммерциализации в области персонализированной медицины и нутрициологии, спортивной медицины и wellness-индустрии . Стоит отметить, что для постгеномной медицины не подходят шаблоны, используемые в ходе эпидемиологических исследований. Показателем эффективности применения постгеномных технологий в профилактической медицине является способность конкретного организма долговременно выдерживать воздействие определенного сочетания неблагоприятных факторов без запуска компенсаторных механизмов [6].
Гармонично развиваются в постгеномной эре технологии генетического редактирования (РГ). Сегодня в ряде стран технологии РГ из научноисследовательских лабораторий переходят в клиническую практику [7, 8]. Разрабатываются принципиально новые методы для лечения и ис- правления генетических нарушений у человека в любом возрасте [9].
Таким образом, постгеномные технологии в настоящее время являются магистральными направлениями приоритета, определённого пунктом 20в «Переход к персонализированной медицине, высокотехнологичному здравоохранению и технологиям здоровьесбережения, в том числе за счет рационального применения лекарственных препаратов (прежде всего антибактериальных)» Стратегии научно-технологического развития Российской Федерации (Указ Президента РФ от 01.12.2016, № 642).
Влияние постгеномных технологийна приоритетные рынки
За последнее десятилетие разработаны достаточно эффективные лабораторные технологии направленного редактирования геномов, которые лежат в основе получения клеточных линий, микроорганизмов, растений и животных с заданными свойствами. Активно разрабатываются методы прижизненного редактирования генома человека для лечения онкологических, орфанных, неинфекционных заболеваний. Помимо РГ, постгеномные технологии обеспечат переход от симптоматической медицины к превентивной и профилактической. Молекулярное профилирование, изучение взаимодействий молекулярных профилей человека обеспечивают исследователя важнейшей информацией об ассоциации биомакромолекул с (пато)физиологическим состоянием человека [10, 11].
Согласно отчету консалтинговой компании Grand View Research, объем мирового рынка биотехнологий на начало 2017 г. оценивался в 369,6 млрд долл. США. Ожидается, что к 2025 г. рынок биотехнологий достигнет 727,1 млрд долл. США, обеспечивая ежегодный рост на 7,4 % [12].
Ключевыми сегментами рынка в среднесрочной перспективе до 2025 г. станут регенеративная, персонализированная и диагностическая медицина, включая молекулярное профилирование. Компа- нии, специализирующиеся на развитии методов регенеративной терапии и синтетической биологии, обеспечат рост сектора до 2025 г.
Сегментирование рынка биотехнологий по ключевым технологиям включает секвенирование ДНК, нанобиотехнологии, тканевую инженерию и регенерацию, ферментацию, клеточные технологии и др. В свою очередь, сегментирование по отраслям биотехнологий определяется медициной и здоровьесбережением, сельским хозяйством и продуктами питания, сохранением природных ресурсов и окружающей средой и др. (рис. 1). Профили сегментов биотехнологий глобального и отечественного рынка очень схожи. Так, ожидается, что флагманы развития биотехнологий, в первую очередь «белые» промышленные биотехнологии и биоэнергетика, сельское хозяйство и продукты питания («зеленые» технологии), медицина и здоровьесбережение («красные» технологии), в среднесрочной перспективе сохранят свои лидирующие позиции [13] (Фарма-2020 – Программа Министерства промышленности и торговли развития поддержки фармацевтической отрасли до 2020 г.). Однако не меньшие темпы развития в России до 2020 г. получат сегменты биоэнергетики и аквапромышленности.
Основными рынками «красных» биотехнологий в области ПГТ являются:
– таргетная, иммунная и генная терапии злокачественных новообразований;
– генотерапевтические лекарственные препараты для лечения наследственных заболеваний;
– подходы к профилактике заболеваний, повышению продолжительности и качества жизни, основанные на использовании информации о геноме человека;
– омиксные методы диагностики для персонализации терапии тяжелых заболеваний, в том числе онкологических (таблица).
Рынки «белых» биотехнологий в области ПГТ:
– симбиотические растительно-микробные системы;
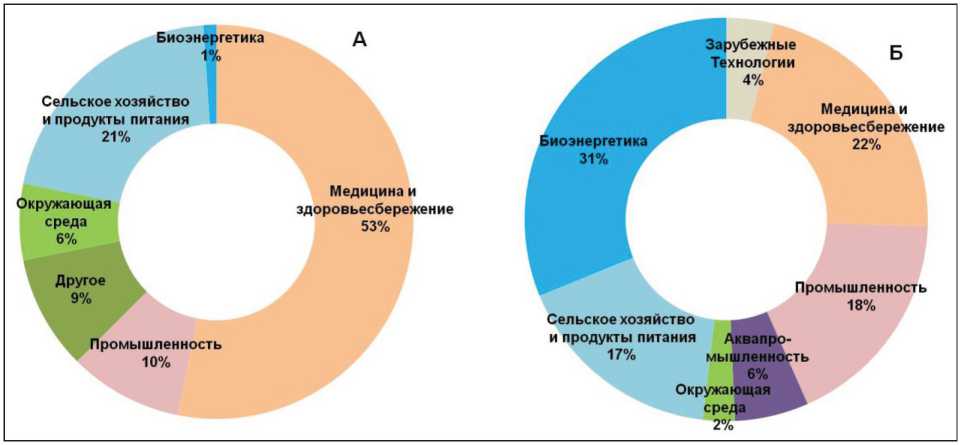
Рис. 1. Распределение мирового рынка (А) и отечественного (Б) между основными отраслями биотехнологий
таблица оценка степени влияния постгеномных технологий на приоритетные рынки
Постгеномные технологии
|
Рынки/Продукты |
Геномная |
Редактирование/ |
Клеточная инженерия тка- |
Метаинженерия |
Омикс- |
|
селекция |
изменение |
ней/органов/ |
микроорганизмов |
оцифровка |
|
|
генома |
эмбрионов |
и консорциумов |
организмов |
|
Терапия злокачественных образований, вирусных и бактериальных инфекций |
0 |
5 |
2 |
3 |
5 |
|
Излечение наследственных заболеваний (снижение степени инвалидизации) |
5 |
5 |
4 |
1 |
0 |
|
Синтетические/природные биоактивные соединения (фармсубстанции) Высокопродуктивные растения, устойчивые |
0 |
3 |
2 |
0 |
0 |
|
к воздействию фитопатогенов, гербицидов, пониженным температурам Сельскохозяйственно-ценные животные и |
4 |
5 |
3 |
2 |
1 |
|
аквакультуры, устойчивые к наиболее распространённым массовым заболеваниям Симбиотические микробные системы |
5 |
4 |
2 |
2 |
5 |
|
(биопродуценты, удобрения и источник систем редактирования) |
5 |
0 |
4 |
5 |
4 |
|
Возобновляемые ресурсы, плантации |
5 |
5 |
1 |
5 |
3 |
|
Переработка отходов и биоремедиация 5 4 Примечание: оценка по 5-балльной шкале, где 5 – максимальное влияние, 1 – |
2 минимальное влияние. |
1 |
2 |
||
– добыча и переработка полезных ископаемых, основанных на управлении микробиомами;
– «коррекция» микробиома как метод терапии заболеваний;
– переработка отходов и биоремедиация, основанные на использовании управляемых микробных консорциумов (таблица).
И, наконец, к «зеленым» биотехнологиям в области ПГТ относятся:
– выращивание высокопродуктивных растений, устойчивых к воздействию фитопатогенов и гербицидов;
– селекция животных, устойчивых к наиболее распространённым массовым заболеваниям;
– получение новых пород животных с помощью технологии геномной оценки племенной ценности эмбрионов;
– выращивание аквакультур с улучшенными потребительскими свойствами (таблица).
В географическом разрезе в настоящее время отрасль биотехнологий наиболее развита в США, на долю которой приходится около 40 % объема мирового рынка. США являются крупнейшим мировым поставщиком и потребителем биотехнологий по всем направлениям, в этой отрасли заняты более 1300 компаний. В Европе крупнейшими игроками этой отрасли являются: Великобритания, на долю которой приходится около половины всех венчурных инвестиций в биотехнологии; Германия со вторым после США биофармрынком; Франция, которая обладает значительным потенциалом в области биореакторов и агробиотехнологий; а также Бельгия и Дания. Однако ожидается, что наиболее быстрорастущими биотехнологическими рынками в ближайшие несколько лет станут страны Азиатско-Тихоокеанского региона, а именно Китай и Индия, обладающие огромным потенциалом развития отрасли. В России успешно реализуется госпрограмма «Фарма-2020», финансирование которой за последние 8 лет превысило 50 млрд руб. Программа предусматривает развитие сегментов медицины и здоровьесбережения, увеличение количества инновационных медико-биологических и фармкомпаний. Уже сегодня в России насчитывается 18 кластеров биотехнологической, фармацевтической и медицинской промышленности. Объем фармацевтического рынка, по данным исследовательского центра IPT Group, в 2016 г. составил 1,2 трлн рублей [14].
Развитие отечественного рынкатаргетных препаратов для онкологии
Отечественный фармацевтический рынок является одним из самых быстрорастущих в мире [15]. Согласно последнему докладу «Focus on Russia» от Global Data, правительственные регуляторные инициативы улучшают основные рыночные показатели и способствуют развитию внутреннего фармрынка, который определяется коммерческим рынком и государственными закупками. Коммерческий рынок доминирует, на его долю приходится 73 % общей стоимости и 85 % объема. Однако внутренняя продукция коммерческого рынка в 2015 г. составляла лишь треть, или 6,05 млрд долл. США. Государственная фармацевтическая программа «Фарма-2020» в России в первую оче- редь направлена на импортозамещение и развитие отечественного производства фармацевтических и медицинских препаратов, изделий медицинского назначения. В ответ на инициативу «Фарма-2020» фармацевтические гиганты Novartis, Takeda, Teva, Novo Nordisk организуют производственные мощности на территории России. В свою очередь, Pfizer и Bayer подписали соглашения о партнерстве с отечественными производителями [15].
Как уже говорилось выше, правительство России активно внедряет политику импортозамещения в более чем 20 секторах биотехнологий, включая фармацевтику, нацеленную к 2020 г. на практически полную замену зарубежных препаратов и изделий медицинского назначения. В августе 2017 г. Российская государственная корпорация «Ростех» и фармацевтическая компания «Марафон Групп» объявили о слиянии. После слияния фармацевтическая дочка «Нацимбио» будет ориентирована на создание национального фармацевтического сектора и производство инновационных отечественных лекарственных препаратов. Сегодня «Марафон Групп» производит около 350 лекарств и медицинских продуктов и работает в направлении обеспечения национального суверенитета в производстве и поставке лекарственных препаратов и изделий медицинского назначения, отсутствие производства которых на территории России представляет угрозу национальной безопасности в области здравоохранения. Рынок медицинских изделий в России в 2016 г. оценивался в 6,7 млрд долл. США [15]. Основными факторами роста этого сегмента является повышение продолжительности жизни населения и связанный с этим спрос на продукты и услуги здравоохранения, а также популяризация в обществе концепции здоровьесбережения и превентивной медицины.
Второй крупной инициативой правительства стало внедрение Комплексной программы развития биотехнологии в Российской Федерации на период до 2020 г. Целью инициативы является выход России на лидирующие позиции в области биомедицины, агробиотехнологий, промышленной биотехнологии и биоэнергетики. Ожидаемыми результатами реализации Программы станут увеличение на порядок потребления биотехнологической продукции на внутреннем рынке, импортозамеще-ние и выход производства биотехнологической продукции в объеме 1 % ВВП к 2020 г.
Сейчас уже очевидно достижение предела эффективности традиционной медицины (рис. 2). Так, структура основных причин смертности на протяжении последних 50 лет практически постоянна во всем мире. По сравнению с Россией в развитых странах с высокой долей пожилого населения лидирующей причиной смертности также является болезнь Альцгеймера [16]. Многолетнее сохранение структуры топ-10 наиболее опасных заболеваний, включая злокачественные новообразования, свидетельствует о том, что традиционная медицинская модель неэффективна как в России, так и за рубежом (рис. 2).
По данным Федеральной службы государственной статистики, в России болезни системы кровообращения и онкологические заболевания являются главными причинами летальных исходов в 50 % и 17 % случаев соответственно. Как уже отмечалось, такая структура смертности по заболеваниям остается однородной на протяжении многих десятилетий.
По данным ВОЗ (2017), объемы неинфекционных заболеваний (НИЗ) также растут. Являясь системными болезнями, НИЗ наиболее характерны для развитых стран, где продолжительность жизни высока. Так, в мире 46 млн человек болеют деменцией, и каждые 20 лет их число будет возрастать вдвое [17]. Неинфекционные заболевания являются дорогими недугами. Ежегодно на борьбу с онкологическими заболеваниями страны мира тратят около 895 млрд долл., нейродегенеративными заболеваниями – 818 млрд долл., и сердечно-сосудистыми – 753 млрд долл. [18]. Средства направлены на медицинскую помощь и социальные выплаты, в них оценены потери от снижения ожидаемой производительности труда. Расходы на лечение НИЗ воз-
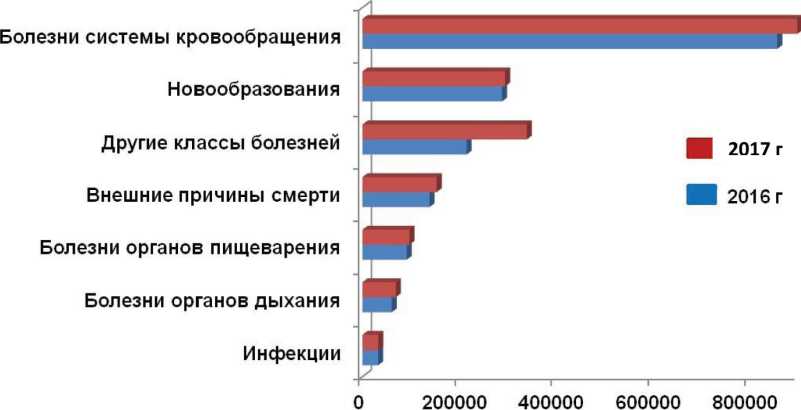
Число смертельных случаев
Рис. 2. Сравнение основных причин смерти в России в 2016 и 2017 гг. по данным Федеральной службы государственной статистики
растают с каждой стадией заболевания, поскольку траты на лечение рака I–II стадий в 2,5 раза ниже, чем расходы на лечение злокачественных новообразований III–IV стадий [19].
В целом фармацевтическая и медицинская промышленность во многом зависят от иностранных производителей активных фармацевтических субстанций, сырья и оборудования. Однако ситуация несколько отличается в отношении биотехнологических препаратов. В отличие от дженериков, или воспроизведенных лекарственных препаратов, субстанции которых получают методами химического синтеза, организация полного цикла производства биологических препаратов обладает экономическими преимуществами. В силу того, что свойства биологических лекарственных препаратов во многом определяются технологией их производства, безопасность и эффективность каждого воспроизведенного биологического лекарственного препарата (биоаналога) должна быть доказана в дорогостоящих сравнительных клинических исследованиях. Технологиями промышленного производства субстанций биотехнологических препаратов в мире владеет относительно небольшое число компаний, что вместе со значительной себестоимостью обусловливает их высокую цену. Необходимость существенных инвестиций в вывод биоаналога на рынок диктует целесообразность дополнительных инвестиций в собственное производство субстанции для контроля над себестоимостью и обеспечения высокой рентабельности. Поэтому локальное производство биологических лекарственных препаратов стало наиболее успешным примером реализации программы «Фарма-2020». Бенефициарами стали «Ф-Синтез», «Р-Фарм», МБЦ «Генериум», «Биокад» и другие. За время действия программы доля российских производителей на рынке выросла до 27 %. Освоен промышленный выпуск более 80 % из перечня жизненно необходимых и важнейших лекарственных препаратов.
Так, компанией «Биокад» разработаны, зарегистрированы и выпущены на рынки Российской Федерации и других стран биоаналоги трех препаратов для лечения онкологических заболеваний – Ацеллбия (ритуксимаб), Гертикад (трастузумаб) и Авегра (бевацизумаб). Данные препараты до 2014 г. были лидерами по объемам затрат государственного бюджета на противоопухолевые лекарственные средства; высокая стоимость оригинальных лекарственных препаратов обусловливала их малодоступность для российских больных.
Однако стоит отметить, что зачастую затрудняет коммерциализацию инновационных препаратов продолжительность цикла от фундаментального открытия до выведения препарата на рынок, который занимает около 15 лет. При этом 90 % лекарственных кандидатов не доходят до последней стадии клинических испытаний. В связи с этим фармкомпании опасаются финансировать такие проекты. С целью снижения затрат и сроков разработки ведущие мировые фармацевтические компании плотно взаимодействуют с университетами и частными исследовательскими лабораториями, которые разрабатывают для них новые кандидатные маркеры и сопровождают процесс доклинических и клинических испытаний.
С целью стимулирования разработки оригинальных лекарственных препаратов Министерство промышленности и торговли России в 2015 г. начало предоставлять субсидии на разработку улучшенных аналогов первых в классе лекарственных препаратов. Создание следующих в классе лекарственных препаратов, действующих на клинически валидированную мишень, сопряжено со значительно меньшими рисками неудачи доклинических и клинических исследований.
Создание биоаналогов и следующих в классе препаратов способно обеспечить устойчивый фундамент для развития биотехнологической промышленности. Однако с точки зрения выхода на рынки высокоразвитых стран наибольшие перспективы имеет разработка первых в классе препаратов с потенциально прорывной эффективностью. При этом вероятность достижения успеха в опережающей разработке максимальна в случае использования относительно недавно появившихся платформенных технологических решений. Примером такой платформенной технологии, находящейся в мире в процессе активного совершенствования, является генетическое редактирование. Особенно большие перспективы здесь открываются в связи с развитием технологии CRISPR/Cas9, позволяющей с высокой точностью редактировать или заменять гены, ответственные за проявление наследственных генетических заболеваний.
Заключение
Рынок биотехнологий в России развивается бурными темпами, однако значительно отстает от показателей западных стран. На государственном уровне был принят ряд программ, поддерживающих развитие биотехнологий в различных отраслях. Важная роль в развитии отрасли отводится Технологическим платформам «Медицина будущего», «Биотех 2030», «Биоэнергетика», а также национальным технологическим инициативам «ХелсНет» и «ФудНет». Акцентированы национальные технологические инициативы на импортозамещение. При поддержке программы «Фарма-2020» создаются аналоги зарубежных и оригинальных препаратов, прежде всего, лекарственные средства таргетной терапии злокачественных новообразований.
По предварительным оценкам, к 2030 г. будут достигнуты следующие экономические эффекты от развития ПГТ:
– развитие внутреннего рынка Российской Федерации (до 34 млрд долл. к 2035 г.), рост экс- портного потенциала за счёт выхода российских поставщиков продукции и услуг на международную арену (до 150 млрд. долл. к 2035 г.);
– увеличение доли компаний из РФ на мировом рынке – до 15 % в странах БРИКС и до 10 % в остальном мире;
– рост конкурентоспособности отечественного сельского хозяйства на внутреннем и мировом рынке и достижение к 2035 г. доли экспорта отечественных сельскохозяйственных культур и продукции племенного и товарного животноводства в общем объеме российского производства
Список литературы Развитие отечественного рынка постгеномных технологий
- Арчаков А.И. Постгеномные технологии и молекулярная медицина. Вестник российской академии наук. 2004; 74 (5): 423-428. [Archakov A.I. Postgenomic technology and molecular medicine. Bulletin of the Russian Academy of Sciences. 2004; 74 (5): 423-428. (in Russian)].
- Bai J.P.F., Melas I.N., Hur J., Guo E. Advances in omics for informed pharmaceutical research and development in the era of systems medicine. Expert Opin Drug Discov. 2018 Jan; 13 (1): 1-4. DOI: 10.1080/17460441.2018.1394839
- Crouser E.D., Fingerlin T.E., Yang I.V., Maier L.A., Nana-Sinkam P., Collman R.G., Kaminski N. Application of ‘Omics’ and Systems Biology to Sarcoidosis Research. Ann Am Thorac Soc. 2017 Dec; 14 (Supplement_6): S445-S451. DOI: 10.1513/AnnalsATS.201707-567OT
- Cheng T., Zhan X. Pattern recognition for predictive, preventive, and personalized medicine in cancer. EPMA J. 2017 Mar 9; 8 (1): 51-60. DOI: 10.1007/s13167-017-0083-9
- Дедов И.И., Тюльпаков А.Н., Чехонин В.П., Баклаушев В.П., Арчаков А.И., Мошковский С.А. Персонализированная медицина: современное состояние и перспективы. Вестник Российской академии медицинских наук. 2012; 67 (12): 4-12. [Dedov I.I., Tulipakov A.N., Chekhonin V.P., Baklaushev V.P., Archakov A.I., Moshkovsky S.A. Personalized medicine: current state and prospects. Bulletin of the Russian Academy of Medical Sciences. 2012; 67 (12): 412. (in Russian)].


