Реабилитация и качество жизни пациентов после онкологического эндопротезирования костей верхней конечности
Автор: Елхов Д.О., Бухаров А.В., Ерин Д.А., Державин В.А., Филоненко Е.В., Алиев М.Д., Каприн А.Д.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 3 т.23, 2024 года.
Бесплатный доступ
Среди современных методов хирургического лечения при опухолевом поражении костей верхней конечности наиболее популярным является эндопротезирование. Однако следует отметить, что функциональные результаты онкологического эндопротезирования костей верхней конечности далеко не всегда удовлетворяют больных и часто приводят к нарушению трудоспособности пациентов, а зачастую и к инвалидизации. Необходимость улучшения функциональных результатов определяет актуальность, научно-практическую и социально-экономическую значимость проблемы. Цель исследования - оценить влияние комплекса реабилитационных мероприятий на качество жизни пациентов после проведения хирургического лечения опухолей костей верхней конечности с эндопротезированием. материал и методы. Представлен анализ данных лечения и реабилитации 146 пациентов, из них 88 (60 %) мужчин и 58 (40 %) женщин. Средний возраст - 47 лет (интервал 19-75 лет). Опухолевое поражение у 98 (67 %) больных локализовалось в проксимальном отделе плечевой кости, у 18 (12 %) - в диафизе, у 16 (11 %) - в костях, составляющих локтевой сустав, у 14 (9,6 %) - в дистальном отделе лучевой кости.
Опухолевое поражение костей, плечевая кость, локтевой сустав, лучезапястный сустав, онкоортопедия, органосохранные операции, эндопротезирование, периоперационная реабилитация
Короткий адрес: https://sciup.org/140305920
IDR: 140305920 | УДК: 617.57-006-089.28 | DOI: 10.21294/1814-4861-2024-23-3-15-31
Rehabilitation and quality of life of patients after arthroplasty for malignant bone tumors of the upper limb
Arthroplasty is the most widely used surgical technique for bone tumors of the upper limbs. However, it should be noted that the functional outcomes after endoprosthetic reconstruction for malignant bone tumors of the upper limb does not always satisfy patients and often lead to impaired working capacity of patients, and their disability. The need to improve functional outcomes determines the practical and socio-economic significance of the research. The purpose of the study was to evaluate the impact of a complex of rehabilitation measures on the quality of life of patients after surgery with endoprosthetic reconstruction for malignant bone tumors of the upper limb. Material and Methods. The treatment and rehabilitation outcomes in 146 patients were analyzed. There were 88 (60 %) men and 58 (40 %) women with an average age of 47 years (range, 19-75 years). The tumor was localized in the proximal humerus in 98 (67 %) patients, in the diaphysis in 18 (12 %), in bones that make up the elbow joint in 16 (11 %) and in the distal radius in 14 (9.6 %) patients.
Текст научной статьи Реабилитация и качество жизни пациентов после онкологического эндопротезирования костей верхней конечности
Совершенствование системной лекарственной терапии является основным фактором, способствующим увеличению выживаемости онкологических пациентов с первичным и вторичным поражением костей верхних конечностей. Вместе с тем, объем и техника операции находятся в процессе постоянных изменений [1, 2]. Ампутационная хирургия была долгое время основным методом лечения опухолевого поражения костной системы. Современные технологии расширили показания для органосохраняющих методов лечения. Онкоорто-педические операции с сохранением конечности улучшают качество жизни, обеспечивают функциональность организма и сокращают реабилитационный период после операции [3]. Согласно современным исследованиям, при злокачественном поражении длинных трубчатых костей и крупных суставов в 90 % случаев возможно применение органосохраняющего хирургического лечения – онкологического эндопротезирования [4].
В связи с расширением показаний к органосохраняющим операциям, применением новых методов лечения, а также совершенствованием металлоконструкций появилась возможность улучшения качества жизни пациентов, что достигается с помощью различных реабилитационных мероприятий [5–7]. Методики реабилитационных мероприятий у онкологических пациентов должны иметь прецизионный и комплексный подход. Комплексная адекватная реабилитация повышает качество жизни пациента и значительно улучшает результаты лечения [8, 9]. Так, V.G. Marchese et al. [10] исследовали функциональные результаты, качество жизни и объем движений в суставах после органосохраняющих операций в онкологической ортопедии. Они обнаружили взаимосвязь между ограничением движений в оперированных суставах, функциональными показателями и качеством жизни. До 51,8 % пациентов не могут полностью вернуться к нормальной жизни из-за нарушений двигательной функции [11]. Исследование R. Na-garajan et al. [12] на примере больных с остеосаркомой показало, что эти нарушения могут сохраняться длительное время, 29,1 % пациентов спустя многие годы страдают от функциональных нару- шений, 22,1 % больных испытывают хронический болевой синдром. При этом ранняя комплексная периоперационная реабилитация может решить эти проблемы. Операции на суставах существенно влияют на паттерны движений мышц и непосредственно двигательную функцию, что необходимо учитывать при физической реабилитации [13].
Реабилитация пациентов с двигательными нарушениями вследствие онкоортопедических операций остается одной из наиболее актуальных проблем современной онкореабилитации. Одной из новых тенденций является применение инновационных металлоконструкций после обширных резекций, что позволяет восстановить функциональность поврежденного участка тела и улучшить качество жизни. В международной практике травматологии и ортопедии широко распространены протоколы реабилитации, которые определяют последовательность мероприятий, направленных на восстановление физической активности и функциональности конечностей после травмы или операции. Они включают в себя физическую терапию, лечебную гимнастику, массаж и другие методы, способствующие быстрому восстановлению. В онкоортопедии тактика реабилитации отличается от стандартных протоколов. При лечении онкологических заболеваний, требующих обширных хирургических вмешательств, необходимо учитывать особенности пациентов, такие как состояние иммунной системы, распространенность опухолевого процесса и дополнительные факторы риска. Поэтому реабилитация в данной области требует индивидуального подхода и тщательного планирования [8].
Цель исследования – оценить влияние комплекса реабилитационных мероприятий на качество жизни пациентов после хирургического лечения опухолей костей верхней конечности с эндопротезированием.
Материал и методы
В исследование вошло 146 пациентов, из них 88 (60 %) мужчин и 58 (40 %) женщин. Средний возраст – 47 лет (интервал 19–75 лет). Опухолевое поражение у 98 (67 %) пациентов локализовалось в проксимальном отделе плечевой кости, у 18 (12 %) – в диафизе, у 16 (11 %) – в костях, составляющих локтевой сустав, у 14 (9,6 %) – в дистальном отделе лучевой кости. Патологические переломы (ПП) наблюдались у 83 (57 %) пациентов, а их угроза (УПП) – у 29 (20 %). Распределение по гистологической структуре опухолевых образований: метастатическое поражение костей было у 91 (62 %) пациента, остеосаркома – у 22 (15 %), хондросаркома – у 16 (12 %), гигантоклеточная опухоль – у 10 (7 %), синовиальная саркома, недифференцированная саркома – у 6 (4 %), десмопластическая фиброма – у 1 больного.
Критерием включения в исследование была медиана наблюдения, установленная следующим образом: срок, включающий периоперационные мероприятия в течение 1 мес после хирургического лечения. Критерии исключения: осложнения, потребовавшие выполнения калечащих операций в срок до 1 мес, несчастные случаи. Группа сравнения была ретроспективной до начала применения предложенной методики реабилитации на базе отделения онкоортопедии МНИОИ им. П.А. Герцена.
С целью улучшения функциональных результатов эндопротезирования при опухолевом поражении верхней конечности нами разработана программа периоперационной реабилитации, которая проводилась 80 (55 %) пациентам с января 2013 г. по октябрь 2023 г.
В дооперационном периоде вне зависимости от локализации опухолевого процесса в программу реабилитации входили: психологическая подготовка пациента, обучение приемам вертикали-зации и использованию средств иммобилизации совместно с врачом-реабилитологом, обучение правильному глубокому грудному и диафрагмальному дыханию во время дыхательной гимнастики, проведение комплекса физических упражнений, направленных на укрепление мышц пояса верхних конечностей.
Все пациенты были полностью проинформированы о предстоящей операции и ограничениях, которые им предстоит соблюдать до и после вмешательства, чтобы они могли принять осознанное решение и быть готовыми к предстоящим изменениям. Знакомили и разъясняли нашу методику реабилитации, которая включает в себя физические упражнения, направленные на облегчение ранней активизации после операции.
Послеоперационные мероприятия с 0-х сут после вмешательства операции включали адекватное обезболивание, в том числе с использованием габа-пентиноидов для купирования послеоперационных болей и профилактики хронического болевого синдрома, дыхательную гимнастику, использование средств иммобилизации конечности (абсолютная/ относительная), правильное позиционирование конечности, вертикализацию пациента.
В раннем послеоперационном периоде с 1-х сут проводили абсолютную иммобилизацию конечности: совместно с инструктором по ЛФК комплекс упражнений на неоперированную верхнюю конечность, комплекс изометрических упражнений на оперированную конечность, активные движения в суставах, свободных от иммобилизации, сегментарный массаж верхних конечностей, за исключением послеоперационной области. Со 2-х сут после операции начиналась активизация пациента, в зависимости от состояния костной ткани, метода фиксации эндопротеза, уровень осевой нагрузки на оперированную конечность определялся, согласно «Программе активизации», для каждой анатомической области верхней конечности.
Средства и методы реабилитации выбираются с учетом расположения опухоли, объема вмешательства и сроков после операции, общего состояния пациента. С 0-х сут после операции начинался реабилитационный комплекс, пассивные упражнения для разработки оперированной конечности – на 3–7-е сут. Оценка функциональных результатов у группы пациентов с эндопротезированием суставов и костей верхней конечности проводилась на 30-е сут после операции, при этом использовалась международная шкала MSTS (Musculoskeletal Tumor Society Score) [14].
Резекция проксимального отдела плечевой кости с эндопротезированием плечевого сустава выполнена 98 пациентам, из них резекция проксимального отдела плечевой кости с обратным (реверсивным) эндопротезированием плечевого сустава (рис. 1б) осуществлена 52 (53 %) больным, анатомические эндопротезы (рис. 1а) установлены 46 (47 %) пациентам. Периоперационная реабилитация проведена 60 пациентам по следующей методике: абсолютная иммобилизация верхней конечности с использованием повязки-косынки с клиновидной подушкой, которая установлена в подмышечной впадине, или специального фиксирующего ортеза. После рентгенологического исследования на 2–3-е сут после операции переход в период относительной иммобилиза- ции осуществлялся с применением следующих реабилитационных мероприятий: изометрических упражнений на мышцы оперированной конечности; выполнения пассивных упражнений – аккуратные качательные движения в плече, придание плечу различных положений для расслабления мускулатуры (с помощью методиста по лечебной физкультуре или здоровой руки). На 4–7-е сут после эндопротезирования плечевого сустава разрешалось выполнение активных движений с поддержкой здоровой верхней конечностью. С 7–10-х сут после операции – выполнение активных движений с небольшой нагрузкой (до 3 кг). Следует отметить особенности реабилитации в зависимости от объема хирургического лечения – при резекции вращательной манжеты плеча, дельтовидной мышцы плеча сроки начала ряда реабилитационных мероприятий увеличивались: выполнение активных движений с помощью поддержки здоровой верхней конечностью начиналось на 10–14-е сут после операции, выполнение активных движений с небольшой нагрузкой (до 3 кг) – с 14–18-х сут. Также данной категории пациентов рекомендовалось носить косыночную повязку или плечевой ортез на протяжении 3–4 нед.
Резекция диафиза плечевой кости с эндопротезированием выполнена 18 пациентам (рис. 2). Программа периоперационной реабилитации
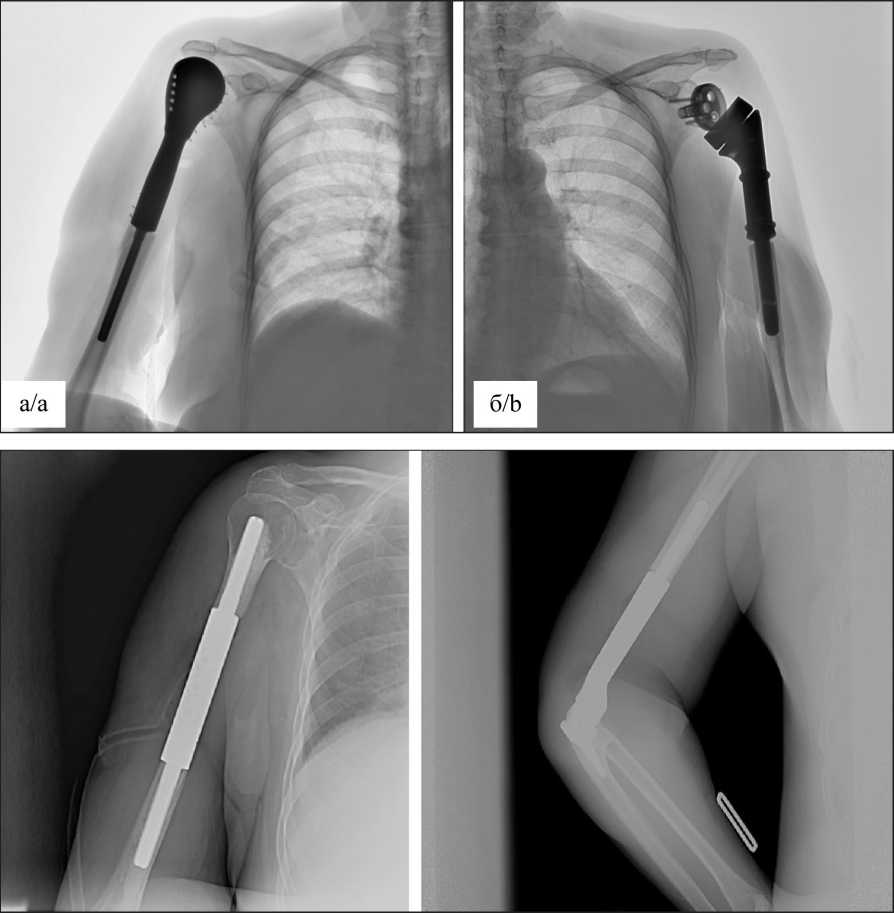
Рис. 1. Рентгенограмма плечевого сустава: а – анатомический эндопротез; б – обратный (реверсивный). Примечание: снимки выполнены авторами Fig. 1. X-ray of the shoulder joint: a – anatomical endoprosthesis;
b – reverse. Note: created by the authors
Рис. 2. Рентгенограммы в передней проекции плечевой кости после эндопротезирования диафиза. Примечание: снимки выполнены авторами Fig. 2. X-rays in the anterior projection of the humerus after diaphysis replacement. Note: created by the authors
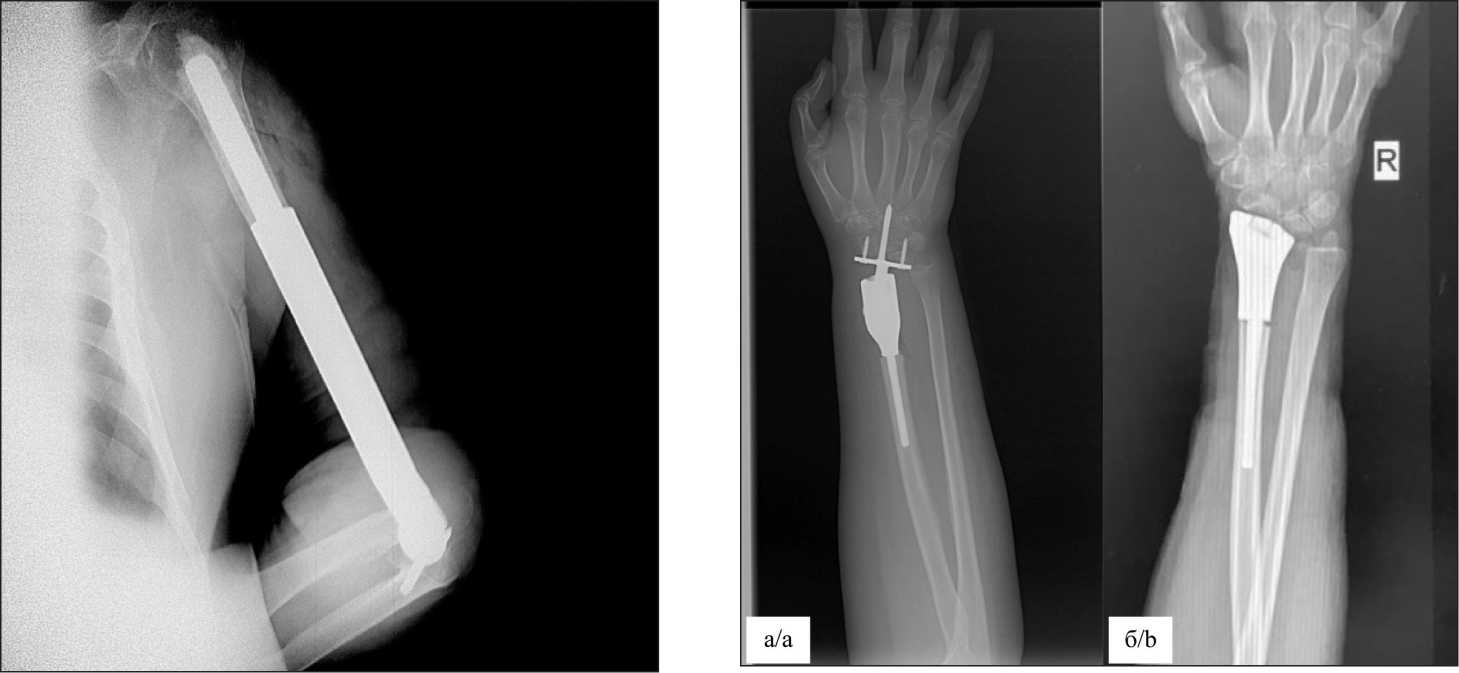
Рис. 3. Рентгенограммы локтевого сустава после резекции дистального отдела плечевой кости с эндопротезированием локтевого сустава. Примечание: снимок выполнен авторами Fig. 3. X-rays of the elbow joint after resection of the distal humerus with elbow arthroplasty. Note: created by the authors
Рис. 4. Рентгенограмма лучезапястного сустава: а – связанный тип эндопротеза; б – несвязанный тип эндопротеза. Примечание: снимки выполнены авторами Fig. 4. X-ray of the wrist joint: a – associated type of endoprosthesis; b – unrelated type of endoprosthesis.
Note: created by the authors проведена 8 пациентам по следующей программе: с 0-х суток послеоперационного периода проводились реабилитационные мероприятия: абсолютная иммобилизация верхней конечности с использованием повязки-косынки с клиновидной подушкой, установленной в подмышечной впадине, или специального фиксирующего ортеза; на 2–3-е сут после операции переход в период относительной иммобилизации, включающий изометрические упражнения на мышцы оперированной конечности; на 3–4-е сут после эндопротезирования – выполнение активных движений с поддержкой здоровой верхней конечностью с небольшой нагрузкой (до 3 кг); на 5–7-е сут – выполнение активных движений без поддержки здоровой верхней конечностью. Ношение косыночной повязки или плечевого ортеза рекомендовалось в течение 2 нед после операции.
Резекция дистального отдела плечевой кости/ резекция проксимального отдела локтевой кости с эндопротезированием локтевого сустава (рис. 3) выполнена 16 пациентам. Периоперационная реабилитация проведена 7 пациентам по следующей методике: с 0-х сут послеоперационного периода проводились реабилитационные мероприятия: абсолютная иммобилизация верхней конечности с использованием повязки-косынки или специального фиксирующего ортеза; на 2-й день после операции – переход в период относительной иммобилизации. Использование для облегчения (помощи) упражнений здоровой верхней конечности. При выполнении упражнений, направленных на разработку локтевого сустава после онкологического эндопротезирования, важно учитывать осевую нагрузку. Для обеспечения хороших функциональных результатов рекомендовалось начинать с облегченных исходных положений, обеспечивая амплитуду движений в пределах легкого и безболезненного растяжения мышц. Это помогало постепенно адаптировать оперированную конечность к физическим нагрузкам. Ротационные движения могут быть включены в программу упражнений уже на 5–7-е сут после эндопротезирования. Сгибание в локтевом суставе рекомендуется начинать на 7-й день после операции с амплитудой в 10–20° из фиксированного положения 90°. Максимальный угол разгибания в локтевом суставе через 4–6 нед до 150–180°.
Резекция дистального отдела лучевой кости с эндопротезированием лучезапястного сустава выполнена 14 пациентам, из них резекция дистального отдела лучевой кости со связанным типом эндопротеза лучезапястного сустава (рис. 4а) осуществлена 6 (43 %) больным, несвязанный тип эндопротеза (рис. 4б) установлен 8 (57 %) пациентам.
Программа периоперационной реабилитации проведена 5 пациентам. При связанном типе эндопротеза она осуществлялась по следующей методике: Абсолютная иммобилизация лучезапястного сустава специальным фиксирующим ортезом или лонгетой проводилась в течение 3–4 дней. После контрольного рентгенологического исследования на 5–7-е сут после операции переходили в период относительной иммобилизации. Этот период включает выполнение активных и пассивных движений для кисти оперированной конечности, а также массаж проксимальных отделов руки для восстановления подвижности и функциональности кисти. На
7–10-е сут после операции пациенту разрешалось выполнять активные движения с небольшой нагрузкой (до 1 кг). Это позволяет укрепить мышцы и восстановить силу кисти, лучезапястного сустава. Кроме того, на этом этапе начинается тренировка координации и адаптации к бытовым действиям. На 10–14-е сут после операции заканчивался период иммобилизации сустава, начиналось постепенное увеличение амплитуды активных и пассивных движений в оперированном сегменте.
При несвязанном типе эндопротеза абсолютная иммобилизация лучезапястного сустава специально фиксирующим ортезом или лонгетой проводилась на протяжении 10–14 дней. После контрольного рентгенологического исследования на 11–15-е сут после операции переходили к относительной иммобилизации, для восстановления подвижности и функциональности кисти начиналось выполнение активных и пассивных движений для кисти оперированной конечности совместно с массажем проксимальных отделов руки. На 21-е сут после операции разрешалось выполнять активные движения с нагрузкой до 1 кг. На 30-е сут после операции заканчивался период иммобилизации сустава, постепенно увеличивалась амплитуда активных и пассивных движений в оперированном сегменте, увеличивалась сила кисти, начиналась тренировка координации, адаптация к бытовым действиям.
Статистическая обработка данных проводилась с использованием пакетов программного обеспечения Statsoft Statistica Professional 13, R v. 4.0.2 и Microsoft Excel 2016. Для выявления межгрупповых различий использовались критерий U Манна–Уитни (для выборок >30) и критерий Стьюдента для малых выборок. Расчеты дополнены ящичковыми диаграммами для визуализации средних сравниваемых групп.
Результаты
При оценке функциональных результатов после резекции проксимального отдела плечевой кости с эндопротезированием у 98 пациентов отмечается корреляция улучшения функциональных результатов по шкале MSTS с видом использованного эндопротеза и объемом резекции (табл. 1). При этом установлено, что при применении эндопротеза обратного типа в большинстве случаев отмечается улучшение функциональных результатов. Такая же тенденция отмечалась и в зависимости от объема резекции и методик реабилитационного подхода. Комплекс хирургических и реабилитационных подходов рассматривался в отдельных подгруппах для более достоверной оценки их влияния на функциональные результаты после эндопротезирования плечевого сустава.
При изолированной оценке эффективности реабилитационных подходов показатель функциональных результатов составляет 72,3 % по шкале MSTS против 69,7 % без использования разработанной периоперационной реабилитации (табл. 2, рис. 5). При анализе функциональных результатов по шкале MSTS после резекции проксимального отдела плечевой кости в зависимости от типа эндопротезирования установлено, что у 52 пациентов, которым проведено хирургическое лечение с обратным (реверсивным) эндопротезированием плечевого сустава, отмечается незначительное улучшение функциональных результатов по сравнению с 46 больными после анатомического эндопротезирования – 72 и 70,5 % по шкале MSTS (табл. 3, рис. 6). Данные шкалы MSTS не имели значимых различий при сравнении следующих групп: новый и старый комплекс реабилитации, обратный и анатомический эндопротез (p>0,05, U-критерий Манна–Уитни). Однако стоит отметить, что ряд параметров используемых шкал относится к субъективным ощущениям пациента и как следствие может приводить к статистической недостоверности изменения параметров.
При анализе функциональных результатов по шкале MSTS у пациентов после резекции прок-
Таблица 1/table 1
Оценка функциональных результатов у пациентов после резекции проксимального отдела плечевой кости с эндопротезированием (по шкале Msts)
evaluation of functional outcomes in patients after resection of the proximal humerus with endoprosthetics (according to the Msts scale)
|
ГТ п т.т э тт я r<-/ Д ttnhntf1 |
Количество пациентов/ |
Функциональные результаты/ |
|
Признак/Attribute |
Number of patients (n=98) |
Functional results, (MSTS) |
|
Вид эндопротеза/ |
Обратный/Reverse |
52 % |
72,0 % |
|
Type of endoprosthesis |
Анатомический/Anatomic |
46 % |
70,5 % |
|
Объем резекции/ Resection volume |
Резекция вращательной манжеты, дельтовидной мышцы/ Muscle resection |
64 % |
64,4 % |
|
Без резекции/Non resection |
34 % |
84,3 % |
|
|
Реабилитация/ |
Новый комплекс/New complex |
60 % |
72,3 % |
|
Rehabilitation |
Старый комплекс/Old complex |
38 % |
69,7 % |
Примечание: таблица составлена авторами.
Note: created by the authors.
Таблица 2/table 2
Функциональные результаты у пациентов после резекции проксимального отдела плечевой кости в группе реабилитация (по шкале Msts)
Functional outcomes in patients after resection of the proximal humerus in the rehabilitation group (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Новый комплекс/ New complex |
Старый комплекс/ Old complex |
|
|
Среднее/Average |
72,27 |
69,71 |
|
ДИ 95 %/CI 95 % |
68,93 |
64,89 |
|
ДИ 95 %/CI 95 % |
75,60 |
74,53 |
|
Медиана/Median |
74 |
66 |
|
Минимум/Minimum |
48 |
50 |
|
Максимум/Maximum |
94 |
94 |
|
25 квартиль/25th quartile |
60 |
56 |
|
75 квартиль/75th quartile |
84 |
84 |
|
Разброс/Scatter |
46 |
44 |
|
Стандартное отклонение/ Standard deviation |
12,90 |
14,68 |
|
Межгрупповые различия/ Between-group difference |
0,3478 (U-критерий Манна–Уитни)/ (Mann–Whitney U test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
Реабилитация/Rehabilitation
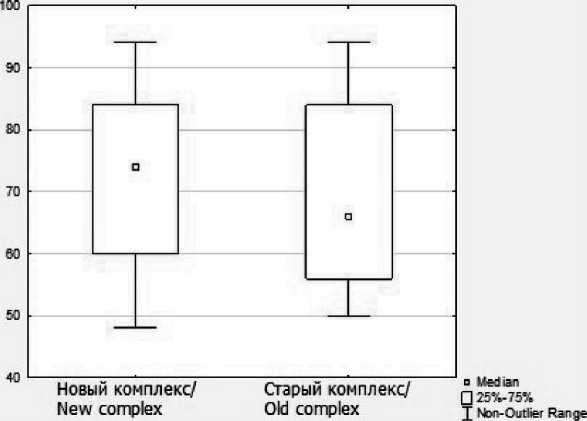
Рис. 5. Диаграмма размаха группы реабилитации. Примечание: диаграмма выполнена авторами Fig. 5. Rehabilitation group scope diagram. Note: created by the authors симального отдела плечевой кости в зависимости от объема резекции мышц отмечались значимые отличия при межгрупповом сравнении в группах с резекцией мышц и без резекции (p<0,05, критерий Манна–Уитни). Средние значения показателей шкалы MSTS составили 84,26 ± 6,91 (диапазон от 62 до 94) в группе без резекции мышц, с резекцией – 64,38 ± 10,97 (диапазон от 48 до 88) (табл. 4, рис. 7).
Таблица 3/table 3
Функциональные результаты у пациентов после резекции проксимального отдела плечевой кости в группе сравнения по типу эндопротеза (по шкале Msts)
Functional outcomes in patients after resection of the proximal humerus in the com parison group by type of endoprosthesis (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Обратный/ Reverse |
Анатомический/ Anatomic |
|
|
Среднее/Average |
71,98 |
70,48 |
|
ДИ 95 %/CI 95 % |
68,24 |
66,35 |
|
ДИ 95 %/CI 95 % |
75,72 |
74,61 |
|
Медиана/Median |
74 |
70 |
|
Минимум/Minimum |
50 |
48 |
|
Максимум/Maximum |
94 |
94 |
|
25 квартиль/25th quartile |
60 |
56 |
|
75 квартиль/75th quartile |
84 |
84 |
|
Разброс/Scatter |
44 |
46 |
|
Стандартное отклонение/ |
13,42 |
13,90 |
|
Standard deviation |
||
|
Межгрупповые различия/ Between-group difference |
0,6100 (U-критерий Манна–Уитни)/ (Mann–Whitney U test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
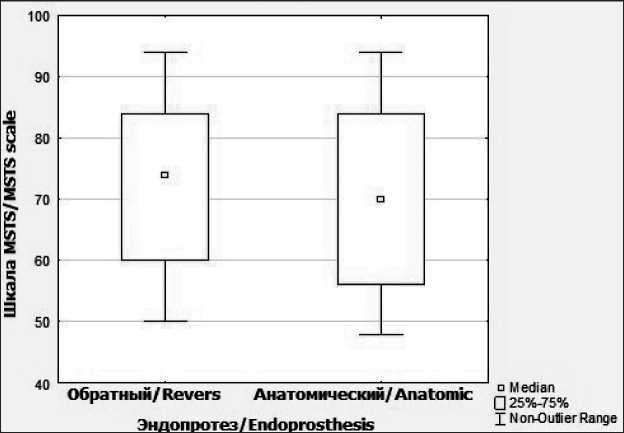
Рис. 6. Диаграмма размаха группы «тип эндопротеза». Примечание: диаграмма выполнена авторами
Fig. 6. Range diagram for a group of endoprosthesis types. Note: created by the authors
У 34 пациентов с эндопротезированием плечевого сустава без резекции вращательной манжеты плеча, дельтовидной мышцы получены отличные функциональные результаты (84,2 % по шкале MSTS), что положительно повлияло на качество жизни. У 64 пациентов с резекцией вращательной манжеты плеча, дельтовидной мышцы через 1 мес после операции функциональные результаты были хуже и составили 64,4 % по шкале MSTS.
Таблица 4/table 4
Функциональные результаты у пациентов после резекции проксимального отдела плечевой кости в группе сравнения по объему резекции мышц (по шкале Msts)
Functional outcomes in patients after resection of the proximal humerus in the comparison group based on the volume of muscle resection (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale Без резекции/ С резекцией/ Non resection Resection |
|
|
Среднее/Average |
84,26 |
64,38 |
|
ДИ 95 %/CI 95 % |
81,85 |
61,63 |
|
ДИ 95 %/CI 95 % |
86,67 |
67,12 |
|
Медиана/Median |
84 |
62 |
|
Минимум/Minimum |
62 |
48 |
|
Максимум/Maximum |
94 |
88 |
|
25 квартиль/25th quartile |
80 |
55 |
|
75 квартиль/75th quartile |
90 |
73 |
|
Разброс/Scatter |
32 |
40 |
|
Стандартное отклонение/ Standard deviation |
6,91 |
10,97 |
|
Межгрупповые различия/ Between-group difference |
0,0000 (U-критерий Манна–Уитни)/ (Mann–Whitney U test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
При анализе функциональных результатов у 18 пациентов после резекции диафиза плечевой кости с эндопротезированием оценивались параметры объема резекции и реабилитационного подхода (табл. 5–6, рис. 8). Цифровые значения оценок по шкале MSTS при оперативном вмешательстве на диафизе соответствовали нормальному распределению (p>0,05, S-W). Данные шкалы MSTS не имели значимых различий при операциях с и без резекции мышц (p>0,05, t-тест, критерий Стьюдента) (табл. 7, рис. 9). Отмечались значимые отличия данных шкалы MSTS при межгрупповом сравнении в группах с применением старого и нового комплексов реабилитации (p<0,05, t-тест,
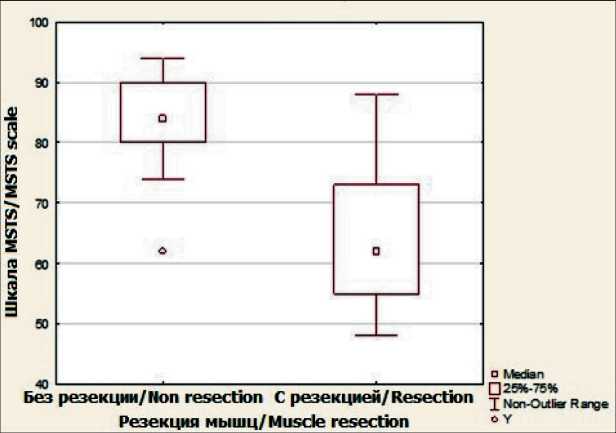
Риc. 7. Диаграмма размаха группы резекции мышц (Шкала МSTS). Примечание: диаграмма выполнена авторами Fig. 7. Мuscle Resection Band Span Сhart (МSTS Scale).
Note: created by the authors
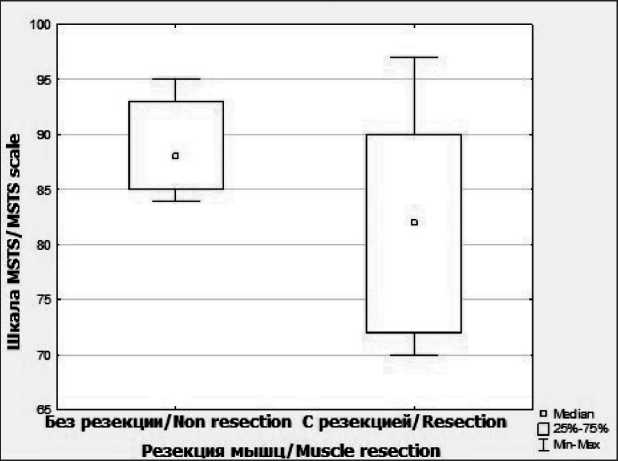
Риc. 8. Диаграмма размаха группы резекции мышц. Примечание: диаграмма выполнена авторами Fig. 8. Diagram of the range of the muscle resection group. Note: created by the authors
Таблица 5/table 5
Оценка функциональных результатов у пациентов после резекции диафиза плечевой кости с эндопротезированием (по шкале Msts)
evaluation of functional results in patients after resection of the humeral shaft with endoprosthetics (according to the Msts scale)
|
Признак/Attribute |
Количество пациентов/ Number of patients (n=18) |
Функциональные результаты/ Functional results |
|
|
Объем резекции/ Resection volume |
Резекция двуглавой, трехглавой, плечевой мышц/Muscle resection |
10 |
81,9 % |
|
Без резекции/Non resection |
8 |
88,9 % |
|
|
Реабилитация/ |
Новый комплекс/New complex |
8 |
91,8 % |
|
Rehabilitation |
Старый комплекс/Old complex |
10 |
79,6 % |
Примечание: таблица составлена авторами.
Note: created by the authors.
Таблица 6/table 6
Функциональные результаты у пациентов после резекции диафиза плечевой кости с эндопротезированием в группе сравнения по объему резекции мышц (по шкале Msts) Functional results in patients after resection of the humeral diaphysis with endoprosthetics in the comparison group based on the volume of muscle resection (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Без резекции/ Non resection |
С резекцией/ Resection |
|
|
Среднее/Average |
88,88 |
81,90 |
|
ДИ 95 %/CI 95 % |
85,26 |
74,89 |
|
ДИ 95 %/CI 95 % |
92,49 |
88,91 |
|
Медиана/Median |
88 |
82 |
|
Минимум/Minimum |
84 |
70 |
|
Максимум/Maximum |
95 |
97 |
|
25 квартиль/25th quartile |
85 |
72 |
|
75 квартиль/75th quartile |
93 |
90 |
|
Разброс/Scatter |
11 |
27 |
|
Стандартное отклонение/ Standard deviation |
4,32 |
9,80 |
|
Межгрупповые различия/ Between-group difference |
0,0808 (t-тест, критерий Стьюдента)/ (t-test, Student's test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
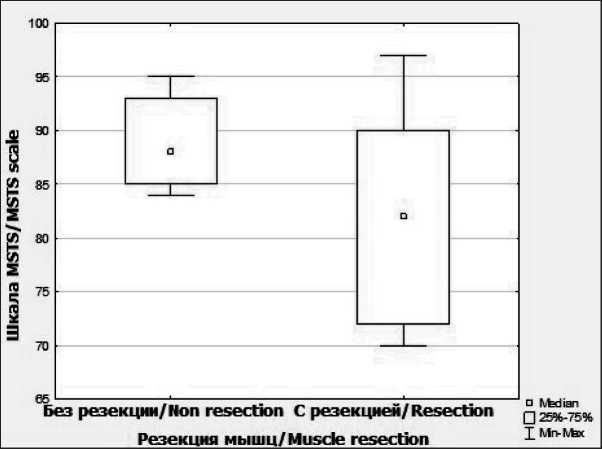
Рис. 9. Диаграмма размаха группы «методики реабилитации». Примечание: диаграмма выполнена авторами
Fig. 9. Diagram of the scope of the group of rehabilitation techniques. Note: created by the authors критерий Стьюдента). Средние значения показателей шкалы MSTS составили 91,75 ± 3,65 (диапазон от 86 до 97) при использовании нового комплекса реабилитации, старого комплекса – 79,60 ± 7,17 (диапазон от 70 до 88).
При анализе результатов у пациентов после резекции диафиза плечевой кости с эндопротезированием установлено, что основными факторами, влияющими и на функциональные результаты,
Таблица 7/table 7
Функциональные результаты у пациентов после резекции диафиза плечевой кости с эндопротезированием в группе сравнения по методике реабилитации (по шкале Msts) Functional results in patients after resection of the humeral diaphysis with endoprosthetics in the comparison group according to the rehabilitation method (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Новый комплекс/ New complex |
Старый комплекс/ Old complex |
|
|
Среднее/Average |
91,75 |
79,6 |
|
ДИ 95 %/CI 95 % |
88,69 |
74,47 |
|
ДИ 95 %/CI 95 % |
94,81 |
84,73 |
|
Медиана/Median |
92 |
81 |
|
Минимум/Minimum |
86 |
70 |
|
Максимум/Maximum |
97 |
88 |
|
25 квартиль/25th quartile |
89 |
72 |
|
75 квартиль/75th quartile |
94,5 |
86 |
|
Разброс/Scatter |
11 |
18 |
|
Стандартное отклонение/ Standard deviation |
3,65 |
7,17 |
|
Межгрупповые различия/ Between-group difference |
0,0005 (t-тест, критерий Стьюдента)/ (t-test, Student's test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
являлись объем резекции мышц и реабилитационные мероприятия. Так, у 10 больных с резекцией диафиза плечевой кости без дополнительного иссечения мягких тканей получены отличные функциональные результаты – 88,9 % по шкале MSTS. У 8 пациентов с вовлечением в опухолевый процесс двуглавой и/или трехглавой и/или плечевой мышц с их резекцией функциональные результаты были хуже, составляя 81,9 % по шкале MSTS. Из 18 больных после эндопротезирования диафиза плечевой кости разработанный план реабилитационных мероприятий удалось реализовать у 8 пациентов, при этом получены отличные функциональные результаты – 91,8 % по шкале MSTS, у 10 больных без периоперационной реабилитации этот показатель составил 79,6 % по шкале MSTS. Таким образом, наиболее важным компонентом, влияющим на функциональные результаты у данной группы пациентов, является реализация реабилитационных мероприятий разработанной программы.
При оценке функциональных результатов при онкологическом эндопротезировании локтевого сустава так же, как и при эндопротезировании плечевой кости, сравнение проводилось в зависимости от типа резекции мышц и методик реабилитации (табл. 8, 9). Цифровые значения оценок по шкале MSTS при хирургическом вмешательстве на
Таблица 9/table 9
Функциональные результаты у пациентов после онкологического эндопротезирования локтевого сустава в группе сравнения по объему резекции мышц (по шкале Msts)
Functional results in patients after oncologic elbow arthroplasty in the comparison group based on the volume of muscle resection (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale Без резекции/ С резекцией/ Non resection Resection |
|
|
Среднее/Average |
72,10 |
79,33 |
|
ДИ 95 %/CI 95 % |
67,42 |
71,86 |
|
ДИ 95 %/CI 95 % |
76,78 |
86,80 |
|
Медиана/Median |
72 |
79 |
|
Минимум/Minimum |
62 |
70 |
|
Максимум/Maximum |
84 |
88 |
|
25 квартиль/25th quartile |
68 |
74 |
|
75 квартиль/75th quartile |
74 |
86 |
|
Разброс/Scatter |
22 |
18 |
|
Стандартное отклонение/ Standard deviation |
6,54 |
7,12 |
|
Межгрупповые различия/ Between-group difference |
0,0569 (t-тест, критерий Стьюдента)/ (t-test, Student's test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
Таблица 8/table 8
Оценка функциональных результатов у пациентов после онкологического эндопротезирования локтевого сустава (по шкале Msts)
evaluation of functional results in patients after oncologic elbow replacement (using the Msts scale)
|
Признак/Attribute |
Количество пациентов/ Number of patients (n=16) |
Функциональные результаты/ Functional results |
|
|
Объем резекции/ Resection volume |
Резекция разгибателей, трехглавой, плечевой мышц/ Muscle resection |
10 |
72,1 % |
|
Без резекции/Non resection |
6 |
79,3 % |
|
|
Реабилитация/ |
Новый комплекс/New complex |
7 |
80,9 % |
|
Rehabilitation |
Старый комплекс/Old complex |
9 |
70,1 % |
Примечание: таблица составлена авторами.
Note: created by the authors.
локтевом суставе соответствовали нормальному распределению (p>0,05 S-W) (рис. 10). При сравнении показателей шкалы MSTS в зависимости от резекции мышц значимые различия не выявлены (p=0,0569). У 10 пациентов с эндопротезированием локтевого сустава с объемом удаляемых разгибателей, трехглавой, плечевой мышц средние функциональные результаты составили 72,1 % по шкале MSTS. У 6 больных без резекции мышц этот показатель достигал более высоких значений – 79,3 % по шкале MSTS (табл. 10, рис. 11). Отмечались значимые отличия данных шкалы MSTS при межгрупповом сравнении в зависимости от применения старого и нового комплексов реа-
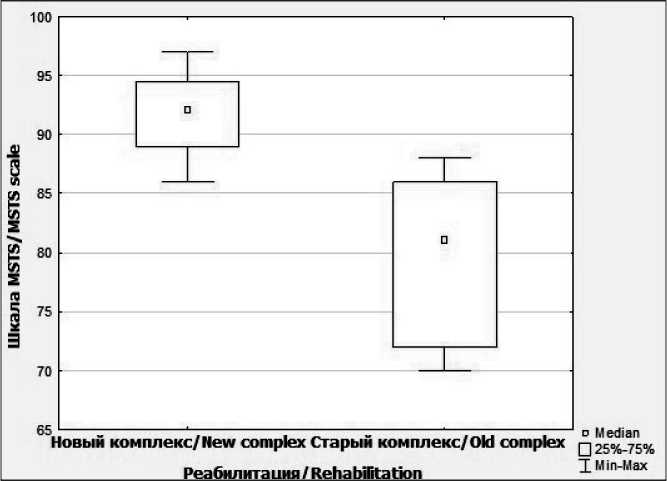
Рис. 10. Диаграмма размаха группы резекции мышц. Примечание: диаграмма выполнена авторами Fig. 10. Diagram of the range of the muscle resection group. Note: created by the authors билитации (p<0,05, t-тест, критерий Стьюдента). Средние значения показателей шкалы MSTS при использовании нового комплекса реабилитации составили 80,86 ± 5,98 (диапазон от 72 до 88), старого комплекса – 70,11 ± 4,54 (диапазон от 62 до 76). В группе эндопротезирования локтевого сустава, включенной в программу периоперационной реабилитации (n=7), удалось достичь более высоких (отличных) показателей функциональных результатов по сравнению с группой без реабилитации (n=9) – 80,9 vs 70,1 % по шкале MSTS. Ключевым показателем, влияющим на функциональные результаты после эндопротезирования локтевого сустава, также является проведение реабилитационных мероприятий.
При оценке функциональных результатов при онкологическом эндопротезировании лучезапястного сустава в зависимости от вида эндопротеза и методики реабилитации (табл. 11, 12, рис. 12) отмечались значимые отличия данных шкалы MSTS при межгрупповом сравнении в группах со связанным и несвязанным эндопротезом (p<0,05, t-тест, критерий Стьюдента). Средние значения
Таблица 10/table 10 Функциональные результаты у пациентов после онкологического эндопротезирования локтевого сустава в группе сравнения по объему реабилитационных методик
(по шкале Msts)
Functional results in patients after oncological endoprosthetics of the elbow joint in the comparison group in terms of the volume of rehabilitation techniques (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Новый комплекс/ New complex |
Старый комплекс/ Old complex |
|
|
Среднее/Average |
80,86 |
70,11 |
|
ДИ 95 %/CI 95 % |
75,32 |
66,62 |
|
ДИ 95 %/CI 95 % |
86,39 |
73,60 |
|
Медиана/Median |
82 |
70 |
|
Минимум/Minimum |
72 |
62 |
|
Максимум/Maximum |
88 |
76 |
|
25 квартиль/25th quartile |
74 |
68 |
|
75 квартиль/75th quartile |
86 |
74 |
|
Разброс/Scatter |
16 |
14 |
|
Стандартное отклонение/ Standard deviation |
5,98 |
4,54 |
|
Межгрупповые различия/ Between-group difference |
0,0011 (t-тест, критерий Стьюдента)/ (t-test, Student's test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
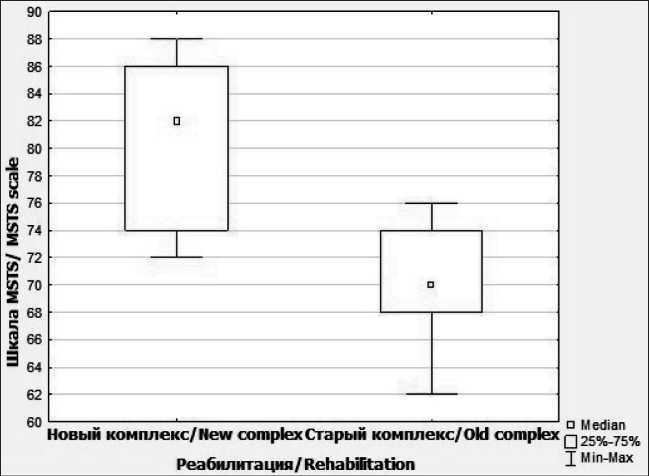
Рис. 11. Диаграмма размаха группы реабилитации. Примечание: диаграмма выполнена авторами Fig. 11. Rehabilitation group scope diagram.
Note: created by the authors
Таблица 11/table 11
Оценка функциональных результатов у пациентов после онкологического эндопротезирования лучезапястного сустава (по шкале Msts)
evaluation of functional results in patients after oncologic wrist replacement (using the Msts scale)
|
Количество пациентов/ |
Функциональные результаты/ |
|
|
ризнакttrute |
Number of patients (n=14) |
Functional results |
|
Вид эндопротеза/ Type of endoprosthesis |
Связанный тип/Connected |
6 |
88,7 % |
|
Несвязанный тип/Unconnected |
8 |
65,6 % |
|
|
Реабилитация/ |
Новый комплекс/New complex |
5 |
79,2 % |
|
Rehabilitation |
Старый комплекс/Old complex |
9 |
73,4 % |
Примечание: таблица составлена авторами.
Note: created by the authors.
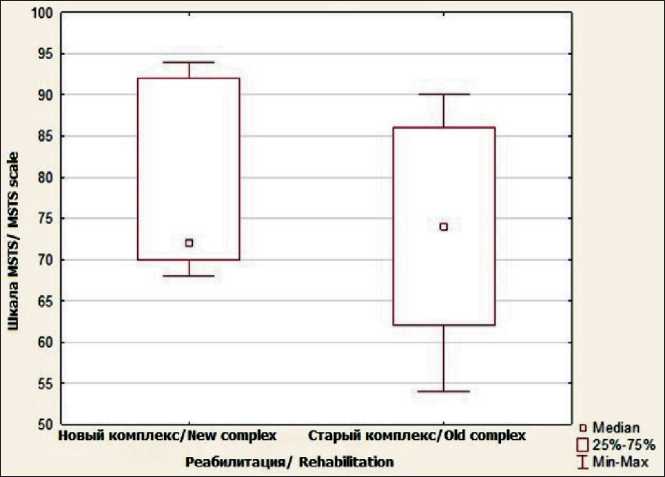
показателей шкалы MSTS в группе c несвязанным эндопротезом составили 65,63 ± 6,72 (диапазон от 54 до 74), со связанным эндопротезом – 88,67 ± 4,32 (диапазон от 82 до 94). У 6 пациентов, которым проведено замещение лучезапястного сустава связанным типом эндопротеза, отмечаются отличные функциональные результаты по сравнению с 8 больными, у которых использовались несвязанные эндопротезы, – 88,7 и 65,6 % по шкале MSTS (табл. 13, рис. 13). В группе пациентов с эндопротезированием лучезапястного сустава, вошедших в программу периоперационной реабилитации, показатель функциональных результатов составил 79,2 % по шкале MSTS vs 73,4 % без реабилитации. Несмотря на небольшое количество больных с эндопротезированием данной анатомической области, очевидно, что ключевым моментом, влияющим на функциональные результаты, является вид эндопротеза.
При оценке уровня послеоперационных осложнений при эндопротезировании костей верхней конечности, в том числе при использовании индивидуальных эндопротезов, изготовленных с помощью 3D-принтеринга, установлено, что осложнения возникли у 74 (50,7 %) больных (табл. 14, 15). Медиана срока наблюдений после эндопротезирования составила 12 мес, максимальный период наблюдения – 68 мес. Положительные результаты эндопротезирования наблюдались в 78,1 % случаев, неудовлетворительные функцио-
Таблица 12/table 12
Функциональные результаты у пациентов после резекции дистального отдела лучевой кости в группе сравнения по типу эндопротеза (по шкале Msts)
Functional results in patients after resection of the distal radius in the comparison group by type of endoprosthesis (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Несвязанный/ Unconnected |
Связанный/ Connected |
|
|
Среднее/Average |
65,63 |
88,67 |
|
ДИ 95 %/CI 95 % |
60,01 |
84,13 |
|
ДИ 95 %/CI 95 % |
71,24 |
93,20 |
|
Медиана/Median |
66,5 |
89 |
|
Минимум/Minimum |
54 |
82 |
|
Максимум/Maximum |
74 |
94 |
|
25 квартиль/25th quartile |
61 |
86 |
|
75 квартиль/75th quartile |
71 |
92 |
|
Разброс/Scatter |
20 |
12 |
|
Стандартное отклонение/ |
6,72 |
4,32 |
|
Standard deviation |
||
|
Межгрупповые различия/ Between-group difference |
0,0000 (t-тест, критерий Стьюдента)/ (t-test, Student's test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
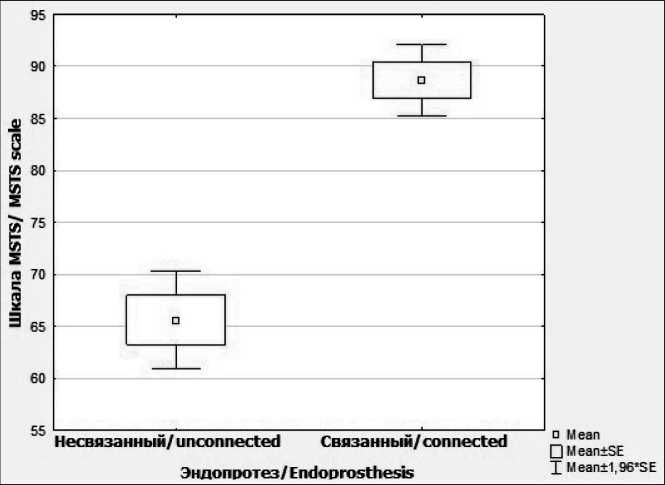
Рис. 12. Диаграмма размаха группы «тип эндопротеза». Примечание: диаграмма выполнена авторами
Fig. 12. Range diagram for a group of endoprosthesis types. Note: created by the authors нальные результаты (>60 % по шкале MSTS) – в 21,9 %.
Анализ результатов с использованием классификации Henderson показал, что наиболее распространенной анатомической локализацией с осложнениями после онкологического эндопротезирования является плечевой сустав, осложнения выявлены у 3 (3 %) пациентов, отмечен 1 (1 %) случай перипротезного перелома, 1 (1 %) – выви-
Таблица 13/table 13
Функциональные результаты у пациентов после резекции дистального отдела лучевой кости в группе сравнения по методике реабилитации (по шкале Msts)
Functional results in patients after resection of the distal radius in the group compared to the rehabilitation method (according to the Msts scale)
|
Показатели/ Parameteres |
Шкала MSTS/MSTS scale |
|
|
Новый комплекс/ New complex |
Старый комплекс/ Old complex |
|
|
Среднее/Average |
79,20 |
73,44 |
|
ДИ 95 %/CI 95 % |
63,44 |
63,00 |
|
ДИ 95 %/CI 95 % |
94,96 |
83,89 |
|
Медиана/Median |
72 |
74 |
|
Минимум/Minimum |
68 |
54 |
|
Максимум/Maximum |
94 |
90 |
|
25 квартиль/25th quartile |
70 |
62 |
|
75 квартиль/75th quartile |
92 |
86 |
|
Разброс/Scatter |
26 |
36 |
|
Стандартное отклонение/ Standard deviation |
12,70 |
13,59 |
|
Межгрупповые различия/ Between-group difference |
0,4529 (t-тест, критерий Стьюдента)/ (t-test, Student's test) |
|
Примечание: таблица составлена авторами.
Note: created by the authors.
Риc.13. Диаграмма размаха группы по реабилитационной методике. Примечание: диаграмма выполнена авторами Fig. 13. Diagram of the scope of the group of rehabilitation techniques. Note: created by the authors ха головки эндопротеза и 1 (1 %) – асептической нестабильности ножки диафизарного компонента эндопротеза. Эти осложнения потребовали повторных операций: 2 случая в объеме реэндопротезирования, 1 случай в объеме мышечной пластики.
На втором месте по частоте встречаемости осложнений – лучезапястный сустав. Инфекционные осложнения возникли у 1 (7,1 %) пациента и наблюдались в позднем послеоперационном
Таблица 14/table 14
Распределение осложнений после онкологического эндопротезирования по классификации Henderson classification of complications after oncological endoprosthetics according to the Henderson classification
|
Тип осложнения/ Type of complication |
Вид осложнения/ Class of complication |
Описание/Description |
|
Механические/Mechanical |
||
|
1 |
Повреждение мягких тканей/ Soft tissue damage |
Нестабильность и вывих, повреждения сухожилия, асептическое расхождение швов/Instability and dislocation, tendon damage, aseptic dehiscence |
|
2 |
Асептическая нестабильность/ Aseptic instability |
Клинические и рентгенологические признаки нестабильности/ Clinical and radiological signs of instability |
|
3 |
Структурные повреждения/ Structural damage |
Перипротезный перелом, поломка протеза, выраженный перипротезный остеопороз/ Periprosthetic fracture, prosthesis breakage, severe periprosthetic osteoporosis |
|
Немеханические/Non-mechanical |
||
|
4 |
Инфекция/Infection |
Инфекционные осложнения, требующие удаления импланта/ Infectious complications requiring implant removal |
|
5 |
Опухолевая прогрессия/ Tumor progression |
Локальный рецидив, в том числе с прогрессией заболевания/ Local relapse, including with disease progression |
Примечание: таблица составлена авторами.
Note: created by the authors.
Таблица 15/table 15
Оценка осложнений по классификации Henderson в зависимости от области операции (n=146) assessment of complications according to the Henderson classification depending on the area of surgery (n=146)
|
Тип осложнения/ Type of complication |
Вид осложнения/ Class of complication |
Плечевой сустав/ Shoulder (n=98) |
Диафиз плечевой кости/ Humeral diaphysis (n=18) |
Локтевой сустав/ Elbow (n=16) |
Лучезапястный сустав/ Radiocarpal joint (n=14) |
|
Механические/Mechanical |
|||||
|
1 |
Повреждение мягких тканей/ Soft tissue damage |
1 (1,0 %) |
– |
1 (6,3 %) |
1 (7,1 %) |
|
2 |
Асептическая нестабильность/ Aseptic instability |
1 (1,0 %) |
1 (5,6 %) |
– |
– |
|
3 |
Структурные повреждения/ Structural damage |
1 (1,0 %) |
– |
– |
– |
|
Немеханические/Non-mechanical |
|||||
|
4 |
Инфекция/Infection |
– |
– |
– |
1 (7,1 %) |
|
5 |
Опухолевая прогрессия/ Tumor progression |
– |
– |
– |
1 (7,1 %) |
|
Примечание: таблица составлена авторами. |
|||||
|
Note: created by the authors. |
|||||
периоде. Пациенту проведено двухэтапное хирургическое лечение: удаление эндопротеза, санация послеоперационной раны с установкой цементного спейсера с антибактериальной терапией, через 2 мес после полной санации мягких тканей, второй этап – реэндопротезирование. У 1 (7,1 %) пациента с впервые выявленной хондросаркомой дистального отдела лучевой кости через 22 мес после операции возник рецидив опухоли в ложе эндопротеза, по поводу чего выполнена ампутация верхней конечности. У одного больного через 4 мес после резекции дистального отдела лучевой кости с эндопротезированием лучезапястного сустава диагностирован вывих эндопротеза с формированием «косорукости», в связи с чем выполнена корригирующая остеотомия локтевой кости с металлостеосинтезом и артродезированием сустава.
У 1 (5,6 %) пациента после резекции диафиза плечевой кости с эндопротезированием спустя 8 мес после лечения возникло асептическое расшатывание дистальной ножки эндопротеза. Потребовалось повторное хирургическое вмешательство – замена стандартной интрамедуллярной ножки на ножку с якорной сцепкой. У 1 (6,3 %) пациента в раннем послеоперационном периоде после эндопротезирования локтевого сустава появился участок ишемии мягких тканей в виде локального некроза по краю послеоперационной раны, что потребовало некрэктомии мягких тканей с наложением вторичных швов. Данное осложнение купировано в полном объеме без дальнейшего развития ишемических изменений.
Суммарный показатель осложнений при онкологическом эндопротезировании костей верхней конечности составил 5,5 %. Несмотря на увеличение количества органосохраняющих операций и как следствие увеличение частоты их осложнений, на основании проведенного анализа становится очевидно, что прецизионное планирование хирургической тактики при эндопротезировании позволяет не только сохранить анатомическую целостность верхней конечности, но и значительно снизить, а в некоторых случаях исключить развитие послеоперационных осложнений. Свой вклад в снижение количества послеоперационных осложнений вносит междисциплинарный подход к тактике ведения данных пациентов, включающий тесное взаимодействие онкологов терапевтического и хирургического профиля, реабилитологов, что обеспечивает реализацию максимального объема профилактических мероприятий как на дооперационном этапе, так и в послеоперационном периоде.
Обсуждение
На улучшение функциональных результатов при онкологическом эндопротезировании костей верхней конечности влияют комплексная реабилитация и объем вмешательства. В литературе достаточно полно рассмотрена проблема оптимальности хирургического пособия как со стороны онкологических показателей, так и со стороны сохранности функции. Вопросы же относительно объема, сроков начала и длительности реабилитации остаются предметом дискуссий [15, 16]. Несмотря на тенденцию в современной онкоортопедии к формированию общих концепций реабилитации в зависимости от локализации поражения и объемов выполненных операций, необходим прецизионный подход к реабилитации пациента в зависимости от возраста и компенсаторных возможностей мышечных структур протезированной конечности [17]. В мировой литературе представлено не так много работ, посвященных реабилитации после эндопротезирования верхней конечности.
В нашем исследовании средние функциональные результаты при хирургическом лечении опухолевого поражения проксимального отдела плечевой кости составили 70 %, что соответствует показателям ведущих зарубежных клиник. Так, при использовании онкологических эндопротезов плечевого сустава среднее значение функциональных результатов по MSTS у разных авторов колеблется от 65 до 88 % [18–20].
A. MсGrath et al. оценивали результаты лечения 18 пациентов со злокачественными опухолями диафиза плечевой кости в объеме онкологического эндопротезирования [21], средние функциональные результаты составили 67 %. В нашем исследовании средний показатель функциональных результатов при онкологическом эндопротезировании диафиза плечевой кости по шкале MSTS составил 88 %.
При онкологическом эндопротезировании локтевого сустава у 36 пациентов R. Capanna et al. [22] приводят функциональные результаты, равные 76,2 %, что сопоставимо с показателями, полученными в нашем исследовании, в котором средний показатель функциональных результатов при аналогичном эндопротезировании составил 74 % по шкале MSTS.
H. Hatano et al. показали, что функциональный результат после резекции дистального отдела лучевой кости с эндопротезированием лучезапястного сустава у 2 больных составил 83 % [23]. K. Gokaraju et al. сообщают о сравнимых результатах после онкологического эндопротезирования лучезапястного сустава, при этом функциональный результат составил 70–83 % [24].
Нами проанализированы различные факторы, влияющие на функциональные результаты при онкологическом эндопротезировании длинных костей верхней конечности. При этом объем операции имел наиболее важное значение при локализации опухоли в проксимальном отделе плечевой кости. Проведение реабилитационных мероприятий послужило важнейшим компонентом, влияющим на функциональные результаты у пациентов после онкологического эндопротезирования диафиза плечевой кости, костей, составляющих локтевой сустав. При хирургическом лечении опухолей лучезапястного сустава наиболее значимым для достижения отличных функциональных результатов является тип эндопротезирования.
Реабилитация после хирургического лечения играет важную роль в обеспечении полноценного восстановления пациентов. Особенно актуальной является система реабилитационных мероприятий, проводимых как до, так и после онкологического эндопротезирования костей верхней конечности. Несмотря на это, в современной литературе отсутствуют работы, которые бы обобщали эти мероприятия на различных этапах лечения. Ряд авторов указывает на важность адекватной реабилитации, отечественные работы, посвященные ранней послеоперационной реабилитации, носят спорадический характер. В то же время зарубежные публикации, как правило, ориентированы на проведение реабилитации в специализированных центрах или на дому, а не в раннем послеоперационном периоде во время пребывания пациента в стационаре. Однако необходимость ранней послеоперационной реабилитации не следует недооценивать. Комплексная периоперационная реабилитация является неотъемлемой частью лечения после онкологического эндопротезирования костей верхней конечности.
Заключение
Реабилитационные мероприятия играют важную роль в поддержании оптимального качества жизни пациентов после хирургического лечения опухолевого поражения костей верхней конечности с эндопротезированием за счет улучшения функциональных результатов. Однако на данный момент не существует систематизированного подхода в реабилитации пациентов после онкологического эндопротезирования костей верхней конечности. Разработанная нами программа реабилитации
Список литературы Реабилитация и качество жизни пациентов после онкологического эндопротезирования костей верхней конечности
- Sostoyanie onkologicheskoi pomoshchi naseleniyu Rossii v 2019 godu. Pod red. A.D. Kaprina, V.V. Starinskogo, A.O. Shakhzadovoi. M., 2020. 239 s.
- Bukharov A.V., Derzhavin V.A., Yadrina A.V., Erin E.A., Elkhov D.O., Aliev M.D., Kaprin A.D. Khirurgicheskoe lechenie patsientov s metastazami v kosti. Klinicheskaya i eksperimental'naya khirurgiya. Zhurnal im. akademika B.V. Petrovskogo. 2022; 10(3): 100-7. https://doi.org/10.33029/2308-1198-2022-10-3-100-107.
- Aliev M.D. Onkoortopediya vchera, segodnya, zavtra. Vestnik Moskovskogo onkologicheskogo obshchestva. 2013; 5(598): 3-4.
- Bukharov A.V., Derzhavin V.A., Golubev P.V., Yadrina A.V. Lechenie patsientov s metastaticheskim porazheniem dlinnykh kostei. Khirurgiya. Zhurnal im. N.I. Pirogova. 2021; (5): 89-94. https://doi.org/10.17116/hirurgia202105189.
- Ehne J., Tsagozis P. Current concepts in the surgical treatment of skeletal metastases. World J Orthop. 2020; 11(7): 319-27. https://doi.org/10.5312/wjo.v11.i7.319.
- Hennessy D.W., Raskin K.A., Schwab J.H., Lozano-Calderón S.A. Endoprosthetic Reconstruction of the Upper Extremity in Oncologic Surgery. J Am Acad Orthop Surg. 2020; 28(8): 319-27. https://doi.org/10.5435/JAAOS-D-19-00219.
- Ivanov V.E., Kuril'chik A.A., Starodubtsev A.L., Zubarev A.L., Gumenetskaya Yu.V. Reabilitatsiya onkologicheskikh bol'nykh posle endoprotezirovaniya krupnykh sustavov. Tezisy pervogo mezhdunarodnogo foruma onkologii i radiologii. Moskva, 23-28 sentyabrya 2018 g. Issledovaniya i praktika v meditsine. 2018; 5(2s): 194.
- Stepanova A.M. Prakticheskie rekomendatsii po reabilitatsii onkoortopedicheskikh bol'nykh: obzor literatury. Fizicheskaya i reabilitatsionnaya meditsina, meditsinskaya reabilitatsiya. 2019; 3: 73-8. https://doi.org/10.36425/2658-6843-2019-3-73-78.
- Bukharov A.V., Filonenko E.V., Erin D.A., Derzhavin V.A., Yadrina A.V., Shatalov A.M., Elkhov D.O., Aliev M.D. Osobennosti rannei reabilitatsii onkologicheskikh patsientov posle rezektsii dlinnykh kostei nizhnei konechnosti s endoprotezirovaniem. Sibirskii onkologicheskii zhurnal. 2022; 21(5): 142-8. https://doi.org/10.21294/1814-4861-2022-21-5-142-148.
- Marchese V.G., Spearing E., Callaway L., Rai S.N., Zhang L., Hinds P.S., Carlson C.A., Neel M.D., Rao B.N., Ginsberg J. Relationships among range of motion, functional mobility, and quality of life in children and adolescents after limb-sparing surgery for lower-extremity sarcoma. Pediatr Phys Ther. 2006; 18(4): 238-44. https://doi.org/10.1097/01.pep.0000232620.42407.9f.
- Wampler M.A., Galantino M.L., Huang S., Gilchrist L.S., Marchese V.G., Morris G.S., Scalzitti D.A., Hudson M.M., Oeffinger K.C., Stovall M., Leisenring W.M., Armstrong G.T., Robison L.L., Ness K.K. Physical activity among adult survivors of childhood lower-extremity sarcoma. J Cancer Surviv. 2012; 6(1): 45-53. https://doi.org/10.1007/s11764-011-0187-5.
- Nagarajan R., Kamruzzaman A., Ness K.K., Marchese V.G., Sklar C., Mertens A., Yasui Y., Robison L.L., Marina N. Twenty years of follow-up of survivors of childhood osteosarcoma: a report from the Childhood Cancer Survivor Study. Cancer. 2011; 117(3): 625-34. https://doi.org/10.1002/cncr.25446.
- Elkhov D.O., Erin D.A., Bukharov A.V., Filonenko E.V., Derzhavin V.A., Yadrina A.V., Shatalov A.M. Funktsional'nye rezul'taty pri khirurgicheskom lechenii opukholevogo porazheniya proksimal'nogo otdela plechevoi kosti s endoprotezirovaniem. Sarkomy kostei, myagkikh tkanei i opukholi kozhi. 2022; 14(3): 20-5. https://doi.org/10.17650/2219-4614-2022-14-3-20-25.
- Enneking W.F., Dunham W., Gebhardt M.C., Malawar M., Pritchard D.J. A system for the functional evaluation of reconstructive procedures after surgical treatment of tumors of the musculoskeletal system. Clin Orthop Relat Res. 1993; (286): 241-6.
- Kaprin A.D., Aliev M.D., Filonenko E.V., Stepanova A.M., Bukharov A.V., Erin D.A. Effektivnost' rannei aktivizatsii bol'nykh posle onkoortopedicheskikh operatsii v ramkakh I etapa reabilitatsii. Fizicheskaya i reabilitatsionnaya meditsina, meditsinskaya reabilitatsiya. 2021; 3(2): 207-13. https://doi.org/10.36425/rehab70762.
- Grushina T.I., Teplyakov V.V. Fizioterapiya pri rannei reabilitatsii bol'nykh s kostnymi sarkomami posle endoprotezirovaniya krupnykh kostei i sustavov. Fizioterapiya, bal'neologiya i reabilitatsiya. 2018; 17(4): 192-8.
- Nelson C.M., Marchese V., Rock K., Henshaw R.M., Addison O Alterations in Muscle Architecture: A Review of the Relevance to Individuals After Limb Salvage Surgery for Bone Sarcoma. Front Pediatr. 2020; 8: 292. https://doi.org/10.3389/fped.2020.00292.
- Janssen S.J., van Rein E.A., Paulino Pereira N.R., Raskin K.A., Ferrone M.L., Hornicek F.J., Lozano-Calderon S.A., Schwab J.H. The Discrepancy between Patient and Clinician Reported Function in Extremity Bone Metastases. Sarcoma. 2016. https://doi.org/10.1155/2016/1014248.
- Guzik G. The Use of a Custom-made Prosthesis in the Treatment of Chondrosarcoma of Distal Radius. Ortop Traumatol Rehabil. 2016; 18(1): 65-72. https://doi.org/10.5604/15093492.1198866.
- Mikailov I.M., Grigor'ev P.V., Ptashnikov D.A., Maikov S.V. Rezul'taty endoprotezirovaniya plechevogo sustava u bol'nykh s novoobrazovaniyami proksimal'nogo otdela plechevoi kosti. Travmatologiya i ortopediya Rossii. 2014; 20(4): 27-35. https://doi.org/10.21823/2311-2905-2014-0-4-27-35.
- McGrath A., Sewell M.D., Hanna S.A., Pollock R.C., Skinner J.A., Cannon S.R., Briggs T.W. Custom endoprosthetic reconstruction for malignant bone disease in the humeral diaphysis. Acta Orthop Belg. 2011; 77(2): 171-9.
- Capanna R., Muratori F., Campo F.R., D’Arienzo A., Frenos F., Beltrami G., Scoccianti G., Cuomo P., Piccioli A., Müller D.A. Modular megaprosthesis reconstruction for oncological and non-oncological resection of the elbow joint. Injury. 2016; 47s4: 78-83. https://doi.org/10.1016/j.injury.2016.07.041.
- Hatano H., Morita T., Kobayashi H., Otsuka H. A ceramic prosthesis for the treatment of tumours of the distal radius. J Bone Joint Surg Br. 2006; 88(12): 1656-8. https://doi.org/10.1302/0301-620X.88B12.17989.
- Gokaraju K., Sri-Ram K., Donaldson J., Parratt M.T.R., Blunn G.W., Cannon S.R., Briggs T.W.R. Use of a distal radius endoprosthesis following resection of a bone tumor. Sarcoma. 2009. https://doi.org/10.1155/2009/938295.


