Реакционная способность анион-радикала нитросоединения при фотохимическом восстановлении
Автор: Владислав Вадимович Левин, Сергей Васильевич Зеленцов, Дмитрий Вадимович Овсянников
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
Анион-радикалы нитробензола и 4 нитрометилбензоата изучены современными методами квантовой химии: BP, MP2, HF (вычисления проводились в квантово-химической программе Orca 5.0.4). Изучены и проанализированы отечественные и зарубежные работы по тематике исследования, определены возможные механизмы реакций анион-радикала нитросоединения в различных условиях. Были вычислены геометрические параметры равновесной молекулы нитросоединения и её анион-радикала, установлено соответствие полученных данных с уже известными ранее. Моделировались реакционные схемы с нейтральными молекулами, такими, как диметилсульфид. Установлено, что в ходе реакции анион-радикал нитросоединения приводит к замедлению протекания реакции фотохимического восстановления, процесс отрыва атома водорода от субстрата не происходит. Рассмотрен перенос заряда с молекулы анион-радикала на диметилсульфид в реальном времени, в результате которого происходит перенос отрицательного заряда на молекулу диметилсульфида и переход анион-радикала нитросоединения в исходное состояние. Проанализировано поведение анион-радикала нитросоединения в реакциях с катионами – протонодонорными молекулами. Подробное изучение механизма возникновения и реакционной способности анион-радикалов нитросоединений позволит наиболее полно изучить реакции фотохимического восстановления нитросоединений.
Нитросоединение, анион-радикал, фотохимическая реакция, фотохимическое восстановление, возбуждённое состояние, синглетное состояние, триплетное состояние
Короткий адрес: https://sciup.org/147252525
IDR: 147252525 | УДК: 544.18 | DOI: 10.14529/chem250413
Reactivity of radical anions of nitro compounds during photochemical reduction
It is a well-known fact that photochemical reduction reactions of nitro compounds are used in many fields of science and industry. However, there are factors that inhibit or nullify the total reaction process. Such a role is attributed to radical anions. The radical anions of nitrobenzene and 4-nitromethylbenzoate were considered. These molecules were studied by modern methods of quantum chemistry: BP, MP2, HF, calculations were carried out in quantum chemical program Orca 5.0.4. Russian and foreign works on the subject of research were studied and analysed, possible mechanisms of radical anion reactions of nitro compounds under different conditions were suggested. Geometrical parameters of the equilibrium molecule of a nitro compound and its radical anion were calculated, the correlation of the obtained data with the previously known ones was established. Reaction schemes with neutral molecules such as dimethyl sulfide were modelled. It was found that during the reaction the radical anion of a nitro compound led to slowing down of the photochemical reduction reaction, the process of hydrogen atom detachment from the substrate did not occur. The charge transfer from the radical anion to the dimethyl sulfide molecule in real time was considered. It has been found that the negative charge transfer to the dimethyl sulfide molecule and transition of the radical anion of a nitro compound to the initial state really occurs. The behaviour of the radical anion of a nitro compound in reactions with cations – proton-donor molecules – has been analysed. The practical role of the radical anions is enormous; a detailed study of the mechanism of its occurrence and reactivity makes it possible to study the mechanisms of photochemical reduction of nitro compounds fully.
Текст научной статьи Реакционная способность анион-радикала нитросоединения при фотохимическом восстановлении
Реакции фотовосстановления нитросоединений привлекают большое внимание учёных всего мира последние несколько лет. Хорошо известно, что нитросоединения загрязняют сточные воды и задача их нейтрализации должна быть решена таким образом, чтобы не было необходимости создавать промышленные предприятия или модифицировать уже существующие. Одним из предложений по нейтрализации нитросоединений заключается в их фотохимическом восстановлении до аминов. Реакция фотовосстановления изучается давно, но из-за большого количества продуктов невозможно установить её механизм [1].
Исследователи из разных стран [2, 3] предлагали различные механизмы реакции взаимодействия света с нитрогруппой. Одним из наиболее сложных вопросов является роль анион-радикала в этом процессе. Его существование косвенно установлено методами ЭПР- и ИК-спектроскопии. Известно, что фотовосстановление протекает и в неполярных растворителях, таких как гексан [4]. Образование анион-радикалов в таком случае протекать не должно, а механизм реакции должен быть радикальным. Прояснить роль анион-радикала в механизме реакции может помочь квантовая химия и фотохимия.
Молекулы в возбуждённых состояниях могут вступать в различные окислительновосстановительные реакции, включающие несколько процессов: перенос электрона от окисляемой частицы к окислителю, перенос атома водорода к окислителю, присоединение кислорода к электронно-возбуждённой частице и т. д. [5]. Хорошим примером является фотохимическое восстановление нитробензола в изопропиловом спирте [6]. Данная молекула обладает высоким окислительным потенциалом и очень быстро восстанавливается до N-фенилгидроксиламина. Поэтому его не удаётся выделить в качестве промежуточного продукта восстановления, хотя данные электрохимического восстановления однозначно указывают на его образование. Дальнейшее восстановление нитрозосоединения до N-арилгидроксиламина включает две аналогичные стадии одноэлектронного восстановления до анион-радикала и далее – до дианиона нитрозосоединения, который при протонировании превращается в N-арилгидроксиламин [7]. В результате последующих темновых реакций окисления и конденсации с образующимся нитробензолом конечным продуктом является азоксибензол. Квантовые выходы данных реакций относительно низкие и составляют 0,001–0,2. Причиной служит конкуренция фотофизической дезактивации возбуждённого состояния молекул [8].
На примере фотохимического восстановления нитробензола был установлен общий механизм восстановления нитросоединений в присутствии протонодонорных молекул: возбуждение нитросоединения, интеркомбинационная конверсия, отрыв атома водорода от изопропилового спирта, последующая рекомбинация радикалов.
Совершенно иная картина наблюдается при фотохимическом восстановлении нитросоединений в присутствии аминов. Имеются данные, что фотовосстановление нитросоединений в присутствии аминов, в частности, диэтил- или триэтиламина протекает легче [9]. В работах Гёрне-ра [10] приведены экспериментальные данные, полученные при помощи УФ- и ИК-спектроскопии, а также метода ЭПР. Автор утверждает, что реакция протекает в две стадии, ани-он-радикал нитросоединения образуется и участвует в данной реакции. Было отмечено особое влияние кислорода в синглетном состоянии на течение реакции [11]. Таким образом, отмечается совершенно иной механизм фотовосстановления нитросоединений, в ходе которого образуется анион-радикал нитросоединения, как интермедиат, не приводящий к образованию целевого продукта. Данная молекула образуется в результате переноса электрона с донора на нитросоединение. Амин является отличным донором электронов и при отрыве электрона образуется катион-радикал, несущий положительный заряд [12].
Однако, ускорение реакции в присутствии ароматического амина нельзя связать только с электронным переходом. Известно [13], что атом водорода, присоединённый к α-атому углерода, во вторичных и третичных аминах очень подвижен, и отрывается нитросоединением в триплетном состоянии. Это приводит к тому, что помимо переноса электронной плотности наблюдается перенос атома водорода [14].
Особого внимания заслуживает роль анион-радикалов в реакции фотохимического восстановления нитросоединений [15]. Одной из сложностей исследования анион-радикалов является малое время их жизни, порядка 10–12–10–10 с. Их трудно зафиксировать и ещё труднее наблюдать. Другой проблемой является то, что высокореакционные участники обычно вступают не в одну реакцию, а несколько.
В связи с этим целью работы являлось изучение роли анион-радикалов в ходе реакции фотохимического восстановления нитросоединений. Были поставлены следующие задачи: во-первых, расчёт структуры нейтральной молекулы 4-нитрометилбензоата и его анион-радикала; во-вторых, моделирование реакционных схем анион-радикалов ароматических нитросоединений с нейтральными молекулами и донорами протонов и, в-третьих, рассмотрение процесса переноса в реальном времени от анион-радикала к молекуле субстрата.
Экспериментальная часть
В работе применяются методы квантовой химии. Для моделирования структурных и энергетических параметров используется метод функционала плотности (DFT).
В качестве обменно-коррекляционного функционала применялся BP-86. В качестве базисного набора был выбран базис Карлсруэ def2-SVP. Он является сферическим, обладает достаточным количеством поправок [16].
Так же проводилось моделирование эволюции электронной плотности в реальном времени с помощью программы NWChem.
Для работы использовалась квантово-химическая программа Orca версии 5.0.3. Программа распространяется на бесплатной основе (проприетарная лицензия). Визуализатором служила программа Avogadro. Она является свободным программным обеспечением.
Вычисления проводились на суперкомпьютере «Лобачевский».
Эволюция электронной плотности моделировалась в реальном времени методом функционала плотности. Для этого применялась программа NWChem версии 7.0.2. Она является свободным программным обеспечением. В качестве функционала был выбран B3LYP с базисным набором cc-pVDZ. Моделирование проводилось на промежутке 600 фс, шаг по времени выбран 0,1 фс. Эволюция электронной плотности моделировалась следующим образом: оптимизировался комплекс нитросоединения с молекулой субстрата. Далее формировались файлы с информацией об электронной плотности отдельных молекул. Молекула субстрата являлась синглетной, а анион-радикала дублетной с зарядом –1. Далее создавался файл общей электронной плотности и из исходной конфигурации решалось дифференциальное уравнение методом Магнуса. В выходном файле печатался заряд молекул на каждом шаге. В результате можно построить ломаную линию, соответствующую изменению заряда на одной из молекул с течением времени.
Моделирование в реальном времени не учитывает изменения структуры молекулы, но можно считать, что его не происходит, так как перенос электрона происходит за времена, существенно короче, чем частоты колебания атомов вдоль химических связей.
Обсуждение результатов
В ходе работы моделировались комплексы анион-радикалов нитросоединений, таких, как нитробензол и 4-нитрометилбензоат с диметилсульфидом, димети- и триметиламином как молекулами субстратов. В качестве основных характеристик комплексов рассматривались заряды на атомах, вычисленные по Малликену, длины связей и величины валентных углов.
Моделирование анион-радикала нитросоединения. Вначале провели моделирование нейтральной молекулы 4-нитрометилбензоата и её анион-радикала. Геометрические параметры изучались с использованием современных квантово-химических методов: HF, MP2, BP86.
Равновесная структура нейтральной молекулы 4-нитрометилбензоата представлена на рис. 1.
Значение геометрических параметров и малликеновские заряды на атомах в нейтральной молекуле 4-нитрометилбензоата представлены в табл. 1 и 2.
Таблица 1
Расчётные значения геометрических параметров нейтральной молекулы 4-нитрометилбензоата
|
Параметр |
Метод |
||
|
BP86 |
HF |
MP2 |
|
|
B (N 18 – O 19 ), Å |
1,232 |
1,212 |
1,227 |
|
B (N18 – O20), Å |
1,232 |
1,212 |
1,227 |
|
B (C 11 – N 18 ), Å |
1,491 |
1,467 |
1,476 |
|
A (O 19 – N 18 – O 12 ), ○ |
125,3 |
125,1 |
125,2 |
Данные табл. 1 указывают на то, что геометрические параметры нейтральной молекулы 4-нитрометилбензоата, предсказанные различными методами квантовой химии согласуются между собой. Данные об экспериментальном исследовании структуры 4-нитрометилбензоата отсутствуют, но в литературе имеются данные для нитрометана и ряда других нитроалканов [17]. Для этих молекул сходятся теоретические и экспериментальные данные. Различие по длинам связей не превышает 0,01 Å , по углам – 1○. Следовательно, можно утверждать, что и для данной молекулы расчётные данные будут находится в согласии с реальными.
Таблица 2
Малликеновские заряды на атомах в нейтральной молекуле 4-нитрометилбензоата
|
Атом |
Метод |
||
|
BP86 |
HF |
МР2 |
|
|
N 18 |
0,1876 |
0,3691 |
0,3195 |
|
O 19 |
–0,2079 |
–0,3457 |
–0,3280 |
|
O 20 |
–0,2066 |
–0,3441 |
–0,3668 |
|
C 11 |
0,1685 |
0,1123 |
0,1038 |
Данные по зарядам на атомах в молекуле 4-нитрометилбензоата, полученные в рамках различных вычислительных методов также согласуются друг с другом. Видно, что в молекуле 4-нитрометилбензоата отрицательный заряд в основном локализован на атомах кислорода О19 и О20. Наибольший положительный заряд по данным расчётных методов локализован на атоме азота нитрогруппы N 18 . На атоме углерода С 11 тоже имеется положительный заряд, но он невелик.
Следующим шагом стало моделирование анион-радикала 4-нитрометилбензоата. Структура данной молекулы представлена на рис. 2.
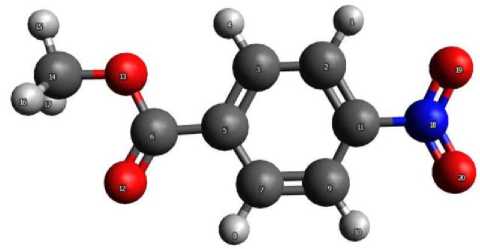
Рис. 1. Равновесная структура 4-нитрометилбензоата
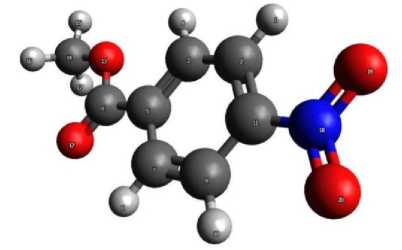
Рис. 2. Структура анион-радикала 4-нитрометилбензоата
Присоединение электрона к нейтральной молекуле приводит к образованию анион-радикала 4-нитрометилбензоата. Равновесная структура, геометрические параметры, малликеновские заряды и спиновая плотность на атомах в молекуле представлены в табл. 3 и 4.
Таблица 3
Расчётные значения геометрических параметров анион-радикала 4-нитрометилбензоата
|
Параметр |
Метод |
||
|
BP86 |
HF |
MP2 |
|
|
B (N 18 – O 19 ), Å |
1,268 |
1,253 |
1,261 |
|
B (N18 – O20), Å |
1,268 |
1,254 |
1,261 |
|
B (C 11 – N 18 ), Å |
1,422 |
1,363 |
1,409 |
|
A (O 19 – N 18 – O 12 ), ○ |
122,6 |
122,0 |
122,3 |
Данные табл. 3 показывают, что присоединение электрона к нейтральной молекуле с последующим образованием анион-радикала 4-нитрометилбензоата приводит к уменьшению длины связи С 11 – N 18 и угла O 19 – N 18 – O 20 в среднем на 0,087 Å и 3 ○ соответственно. Было обнаружено увеличение связей N 18 – O 19 и N 18 – O 20 в среднем на 0,553 Å и 0,564 Å соответственно. Геометрические параметры других связей и углов не изменяются. Из данных табл. 3 можно сделать вывод о том, что расчётные данные, полученные разными методами, хорошо соотносятся друг с другом.
Таблица 4
Малликеновские заряды и спиновая плотность на атомах в анион-радикале 4-нитрометилбензоата
|
Атом |
Метод |
||
|
BP86 |
HF |
МР2 |
|
|
N 18 |
0,1708 |
0,2859 |
0,3365 |
|
O 19 |
–0,3549 |
–0,5813 |
–0,6012 |
|
O 20 |
–0,3535 |
–0,5791 |
–0,6004 |
|
C 11 |
0,1287 |
0,0870 |
0,1010 |
Анализ результатов по малликеновским зарядам (табл. 4) на атомах показывает, что в анион-радикале 4-нитрометилбензоата локализация зарядов на атомах происходит в основном также, как в нейтральной молекуле, однако, отрицательные заряды, преимущественно локализованные на атомах кислорода О 19 и О 20 уменьшаются в среднем на 0,147 и 0,233 соответственно, а положительный заряд, локализованный на атоме азота нитрогруппы N 18 уменьшается в среднем на 0,1 по сравнению со значениями зарядов на атомах в случае нейтральной молекулы 4-нитрометилбензоата.
Моделирование реакционных схем анион-радикала 4-нитрометилбензоата с нейтральными молекулами. На рис. 3 изображён комплекс нитробензола с диметилсульфидом. Диметилсульфид ориентируется атомом водорода к атому кислорода нитрогруппы. Одним из возможных маршрутов реакции фотохимического восстановления является перенос водорода от субстрата к нитрогруппе [18]. Однако вычисления энергии связи кислород-водород полученного комплекса говорит о том, что этот механизм невозможен энергетически. Предположительно, в этом комплексе происходит перенос электрона от анион-радикала к субстрату. Таким образом, анион-радикал возвращается в исходное нитросоединение. Реакция фотовосстановления не протекает, продукт не образуется.
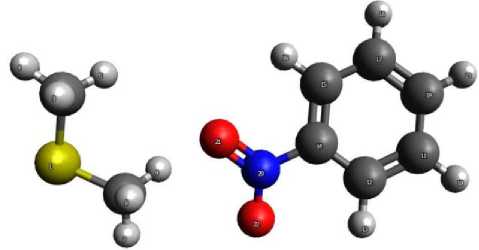
Рис. 4 и 5 представляют собой реакционные системы 4-нитрометилбензоата с диметил- и триметиламином.
Рис. 3. Реакционная схема нитробензола и диметилсульфида
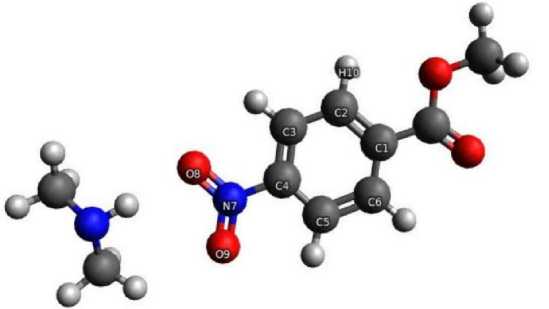
Рис. 4. Реакционная система 4-нитрометилбензоата с диметиламином
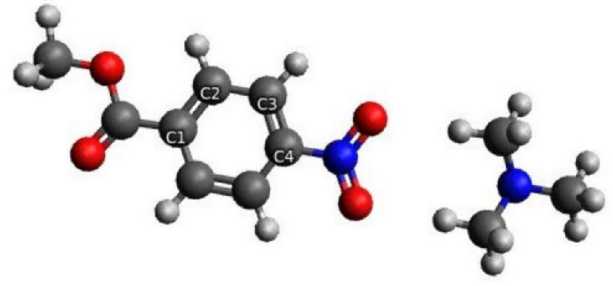
Рис. 5. Реакционная система 4-нитрометилбензоата с триметиламином
Были рассчитаны заряды на атомах в молекулах нитробензола и 4-нитрометилбензоата. Данные сведены в табл. 5 и 6.
Таблица 5
Малликеновские заряды в реакционной системе с 4-нитрометилбензоатом
|
Заряды, а.е. |
||||
|
R |
N 7 |
O 8 |
O 9 |
X |
|
SMe 2 |
0,1676 |
–0,3149 |
–0,3270 |
–0,1713 |
|
NHMe 2 |
0,1518 |
–0,3282 |
–0,3325 |
–0,2781 |
|
NMe 3 |
0,1579 |
–0,3293 |
–0,3386 |
–0,3470 |
|
X = S, N |
||||
Таблица 6
Малликеновские заряды в реакционной системе с нитробензолом
|
Заряды, а.е. |
||||
|
R |
N 7 |
O 8 |
O 9 |
X |
|
SMe 2 |
0,1700 |
–0,3575 |
–0,3684 |
–0,2105 |
|
NHMe 2 |
0,1579 |
–0,3293 |
–0,3389 |
–0,3470 |
|
NMe 3 |
0,1824 |
–0,3583 |
–0,3702 |
–0,2884 |
|
X = S, N |
||||
Также были проведены расчёты и оптимизация геометрических структур субстратов в реакционной схеме. Результаты представлены в табл. 7. Полученные расчётные данные хорошо иллюстрируют протекающий процесс. Видно, что отрицательные заряды на атомах кислорода увеличиваются в положительную сторону по сравнению с найденными выше до значений, соответствующих нейтральной молекуле реагента.
Таблица 7
Расчётные параметры геометрической структуры субстратов в различных реакционных схемах (длины связей в Å , углы в градусах)
|
Система |
В (NO) |
B (NO`) |
B (CH) |
B (OH) |
A (ONO`) |
|
PhNO2 + SMe2 |
1,264 |
1,258 |
1,188 |
2,656 |
123,5 |
|
4-НМБ + SMe 2 |
1,239 |
1,239 |
1,093 |
1,923 |
124,5 |
|
4-НМБ + NHMe 2 |
1,251 |
1,260 |
1,036* |
2,025 |
123 |
|
4-НМБ + NMe 3 |
1,254 |
1,255 |
1,110* |
2,340 |
123 |
|
Под * понимается длина связи N – H |
|||||
Положительные заряды, локализованные на атомах серы и азота субстратов, напротив, уменьшаются в отрицательную сторону. Хорошо характеризует протекающий процесс сведения о длинах связей в молекуле субстратов. Видно, что в молекуле анион-радикала нитросоединения длины связей не изменяются, связь, возникающая между кислородом нитрогруппы и атомом водорода субстрата согласно информации о длине, является водородной [19].
Согласно этим данным, можно предположить, что анион-радикал 4-нитрометилбензоата переходит в основное состояние, триплетное же состояние «гасится». В следствие этого процесса, квантовый выход реакции фотовосстановления сводится к нулю [20].
Моделирование реакционных схем анион-радикала нитросоединения с катионами. Были смоделированы реакции взаимодействия анион-радикала 4-нитрометилбензоата с катионами гидроксония и аммонния. Выдвинуто предположение, что в данном случае анион-радикал нитросоединения будет вести себя как типичный радикал, т. е. отрывать атом водорода от молекул субстрата, превращая их в нейтральные молекулы. Дальнейшее превращение полученного продукта описывается классическими случаями восстановления нитросоединения [21].
На рис. 6, 7 указаны реакционные схемы 4-нитрометилбензоата с катионом гидроксония и аммония.
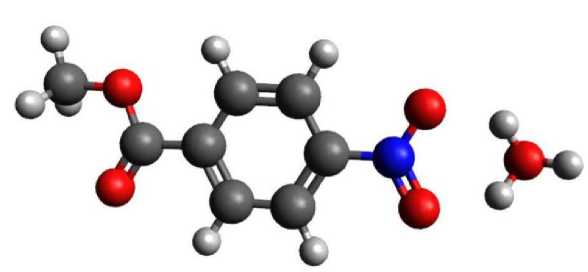
Рис. 6. Реакционная схема 4-нитрометилбензоата с катионом гидроксония
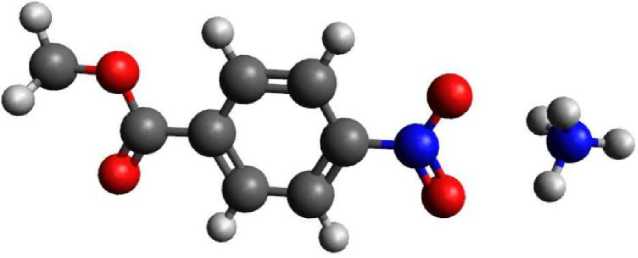
Рис. 7. Реакционная схема 4-нитрометилбензоата с катионом аммония
В результате моделирование реакции было выявлено, что анион-радикал 4-нитрометилбензоата отрывает атом водорода от катионов гидроксония и аммония. Это прекрасно характеризует его по свойствам как частицу с одним неспаренным электроном – т. е. свободного радикала [22]. Результаты взаимодействия представлены на рис. 8, 9.
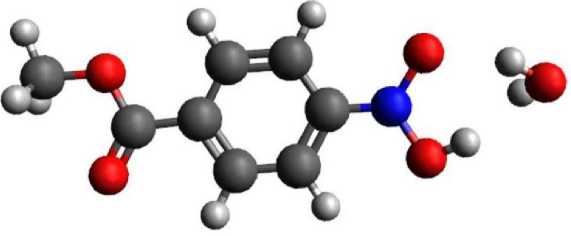
Рис. 8. Результат взаимодействия 4-нитрометилбензоата с катионом гидроксония
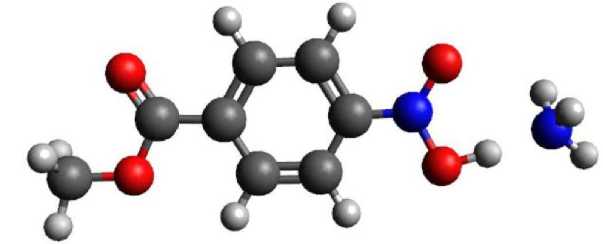
Рис. 9. Результат взаимодействия 4-нитрометилбензоата с катионом аммония
В ходе кантово-химических расчётов были рассчитаны длины связей между атомами кислорода и атомом азота нитрогруппы, между атомом кислорода нитрогруппы и атомом водорода, оторванным от катиона, угол в нитрогруппе. Также особое внимание уделялось распределению зарядов и спиновой плотности на соответствующих атомах. Результаты представлены в табл. 8–10.
Таблица 8
Геометрические параметры 4-нитрометилбензоата в результате реакции с катионами гидроксония и аммония (длины связей в Å , углы в градусах)
|
Параметр |
Значение |
|
Н 3 О+ |
|
|
B (O – H) |
0,975 |
|
B (N – O) |
1,385 |
|
B (N – O`) |
1,38 |
|
A (O` – N – O) |
113,1 |
|
NH 4 + |
|
|
B (O – H) |
0,972 |
|
B (N – O) |
1,383 |
|
B (N – O`) |
1,379 |
|
A (O` – N – O) |
112,6 |
Таблица 9
Малликеновские заряды в реакционной системе 4-нитрометилбензоата с катионами
|
Катион |
N |
O |
O` |
X |
|
H 3 O+ |
0,1410 |
–0,3501 |
–0,1972 |
0,1975 |
|
NH 4 + |
0,1491 |
–0,3032 |
–0,3380 |
–0,5943 |
|
X = H, N |
||||
Таблица 10
Распределение спиновой плотности в реакционной системе 4-нитрометилбензоата с катионами
|
Катион |
N |
O |
O` |
X |
|
H 3 O+ |
0,3860 |
0,3455 |
0,0705 |
–0,0007 |
|
NH 4 + |
0,2913 |
0,3091 |
0,0966 |
–0,0003 |
|
X = H, N |
||||
Из квантово-химических расчётов следует, что в результате отрыва атома водорода от молекулы катиона длины связей N-O и N-O' увеличиваются приблизительно на 0,1 А, угол O'-N-O уменьшается на 10 градусов. Длины связей O'-H равны 0,975 и 0,972 А, что говорит о протекании реакции. Об этом же также свидетельствуют данные о распределении зарядов и спиновой плотности. Заряд на атоме кислорода, присоединяющим атом водорода, увеличивается на 0,1408 по сравнению с другим атомом кислорода нитрогруппы, что связано с присоединением атома водорода, имеющего положительный заряд [23].
Исследование переноса заряда в реальном времени. Чтобы исследовать перенос заряда в реальном времени, был выполнен расчёт эволюции электронной плотности на атомах молекул субстрата. На рис. 10 и 11 изображено изменение заряда во времени.
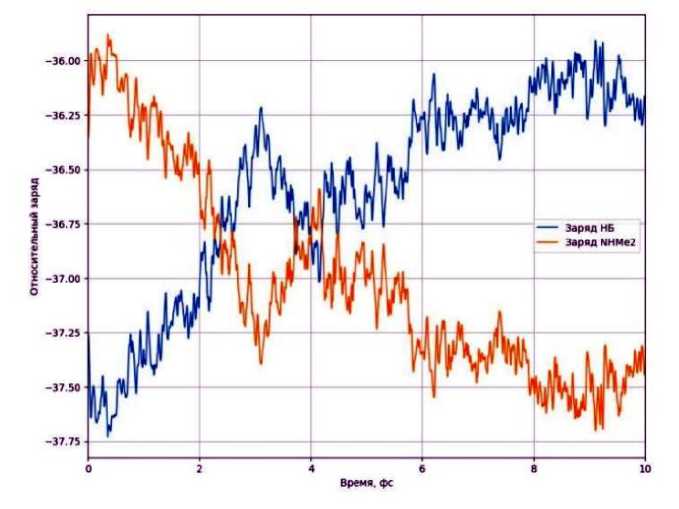
Рис. 10. Перенос заряда с молекулы нитробензола на диметиламин
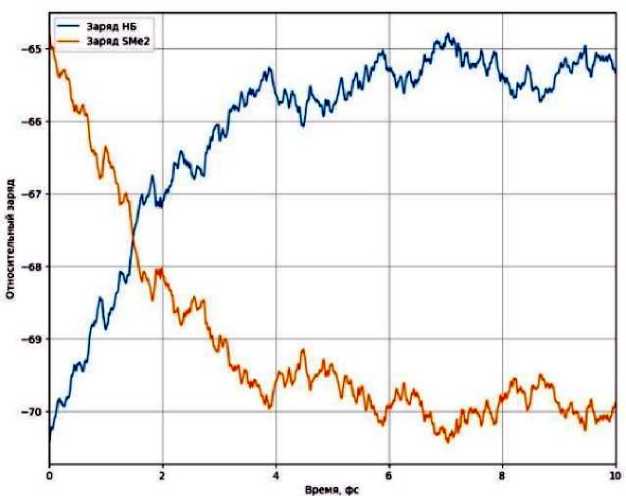
Рис. 11. Перенос заряда с молекулы нитробензола на диметилсульфид
Оно было получено время-разрешённым B3LYP/cc-pVDZ. Синяя линия соответствует суммарному относительному заряду на нитробензоле. Для удобства восприятия к зарядам на диметилсульфиде и диметиламине были прибавлены константы, чтобы графики находились на одном уровне. Поэтому ось зарядов отражает лишь качественный характер изменения. Из графика видно, что заряд на молекулах одновременно изменяется на одни и те же значения. Заряд нитробензола растёт, а диметилсульфида уменьшается. Это может говорить о том, что происходит процесс переноса заряда с одной молекулы на другую. Перенос происходит достаточно быстро – не более 10 фемтосекунд [24].
Заключение
Рассчитаны структуры нейтральной молекулы 4-нитрометилбензоата и его анион-радикала квантово-химическими методами. Проанализированы геометрические параметры данных молекул и сделаны выводы о том, что они находятся в хорошем соответствии с табличными данными. Смоделированы реакционные схемы анион-радикала нитробензола и 4-нитрометилбензоата с диметилсульфидом, диметил- и триметиламином, катионом аммония и гидроксония. В случае взаимодействия с нейтральной молекулой, анион-радикал нитросоединения приводит к замедлению протекания реакции фотохимического восстановления, процесс отрыва атома водорода от субстрата не происходит. В случае взаимодействия с протонодонорными молекулами происходит отрыв атома водорода от молекулы субстрата и присоединение его к атому кислорода нитрогруппы, что подтверждается распределением зарядов на атомах реагирующих молекул. Анион-радикал нитросоединения в данном случае выступает как типичный радикал. Также был рассмотрен перенос заряда с молекулы анион-радикала нитросоединения на молекулу диметилсуль-фида в реальном времени. Обнаружено, что действительно происходит перенос отрицательного заряда на молекулу диметилсульфида и переход анион-радикала нитросоединения в исходный нитробензол.


