Реактивация / обострение хронических вирусных гепатитов во время противоопухолевой терапии
Автор: Феоктистова П.С., Винницкая Е.В., Нурмухаметова Е.А., Тихонов И.Н.
Журнал: Злокачественные опухоли @malignanttumors
Статья в выпуске: 3S2-2 т.15, 2025 года.
Бесплатный доступ
Хронический вирусный гепатит, реактивация вирусного гепатита В, противоопухолевая химиотерапия, анти PD-L1 ингибиторы
Короткий адрес: https://sciup.org/140312996
IDR: 140312996 | DOI: 10.18027/2224-5057-2025-15-3s2-2-21
Текст статьи Реактивация / обострение хронических вирусных гепатитов во время противоопухолевой терапии
Значимость выделения группы пациентов с хроническим вирусным гепатитами, получающими противоопухолевое лечение, определяется как распространенностью заболевания, так и ухудшением прогноза лечения онкологических пациентов в случае реактивации вирусного гепатита. Во всем мире около 296 миллионов человек инфицированы вирусом гепатита В и 58 миллионов инфицированы вирусом гепатита С. До 8% (6–9 млн) людей являются бессимптомными носителями поверхностного антигена ВГВ (HBsAg+), а 1% — носителями антител к ВГС (anti-HCV+). Ежегодно регистрируется около 1,5 миллионов новых случаев ВГВ и ВГС. Около 1% пациентов имеют ко-инфекцию ВИЧ. Наиболее значимым с точки зрения прогноза является вирусный гепатит В, в первую очередь за счет рисков реактивации, препятствующих лечению основного заболевания или приводящих к декомпенсации функции печени.
-
1. ВИРУСНЫЙ ГЕПАТИТ В
1.1. Понятие хронического вирусного гепатита B, понятие реактивации ВГВ и обострения ВГВ
Хронический вирусный гепатит В: стадия инфекции ВГВ, при которой в крови пациентов в течение более чем 6 месяцев после острой инфекции определяется HBsAg. При этом в практике довольно часто встречаются пациенты, у которых в крови отсутствует HBsAg, но при этом обнаруживаются anti-HBc c/без anti-HBs. В общей популяции прогрессирование ХГВ у этих пациентов встречается крайне редко, но для иммунокомпрометированных лиц, в том числе получающих противоопухолевое лечение, такая картина представляет собой опасность в плане потенциальной реактивации ХГВ: при наличии anti-HBс вероятность реактивации ХГВ — 5%, а в отсутствии — у 14 % больных.
Понятие реактивации вирусного гепатита включает острое повышение уровня ДНК вируса гепатита B (ВГВ) и повышение активности аминотрансфераз (АЛТ и АСТ) в сыворотке крови. Необходимо отметить, что единое и общепризнанное определение реактивации вирусного гепатита отсутствует, можно выделить вирусологические и биохимические критерии реактивации ВГВ.
1.1.2. Вирусологические критерии
-
• Обнаружение ДНК ВГВ de novo у пациентов с ранее неопределяемой ДНК ВГВ (серореверсия)
-
• Увеличение ДНК ВГВ не менее чем на 1 log (10-кратное) МЕ/ мл
-
• Рост ДНК ВГВ выше условного порога (например, 20000 МЕ/мл) у пациентов с ухудшением биохимических показателей.
1.1.3. Биохимические критерии
-
• 2- или 3-кратное повышение АЛТ выше верхней границы нормы.
В соответствии с определением AASLD 2018 г., «ОБОСТРЕНИЕ ХГВ» — это повышение АЛТ > 3 норм или на 100 Е/л и нарастание уровня ДНК ВГВ.
Важно подчеркнуть, что понятия реактивации ВГВ-инфекции и понятия обострения ХГВ различаются, поскольку реактивацией можно назвать любое появление ДНК ВГВ в крови больных, у которых она исходно не обнаруживалась, а обострение обязательно предполагает повышение активности АЛТ. Так, по данным систематического обзора 14 исследований, у пациентов с HBsAg, находившихся на иммуносупрессивной терапии и не получавших противовирусного лечения, реактивация ВГВ-инфекции произошла у 39% больных, а обострение ХГВ —у 33%.
1.2. Инфекция ВГВ у пациентов с медикаментозной иммуносупрессией
Реактивация вирусного гепатита В — одно из самых тяжелых осложнений иммуносупрессивной терапии.
Чаще всего реактивацию могут вызывать препараты для биологической терапии, в частности, наибольший риск отмечен при применении ритуксимаба. Риск реактивации ХГВ выше у пациентов онкогематологическими заболеваниями — от 18% у пациентов с анти-HBc до 48% у пациентов с хроническим ВГВ.
У пациентов с солидными опухолями риск реактивации ВГВ относительно невысок: ~ 3% у анти-HBc-позитивных пациентов до 25% у пациентов с хроническим ВГВ. Несвоевременно начатая противовирусная терапия при реактивации ВГВ на фоне иммуносупрессиной противоопухолевой терапии может привести к летальному исходу или вынужденной отмене лечения.
Риск развития реактивации определяется серологическим статусом ВГВ, уровнем виремии и иммуносупрессивной активностью применяемых препаратов (таблицы 1, 2).
Таблица 1. Частота реактивации ВГВ инфекции в различных группах пациентов, получающих иммуносупрессивную/противоопухолевую терапию
Риск реактивации ВГВ
|
Тип лечения |
HBsAg (+), % |
HBsAg (–), HBcoreAg (+), % |
|
Трансплантация КМ, стволовых клеток |
32–50 |
до 50 |
|
Анти-CD20 (ритуксимаб) |
50 |
18 |
|
Анти-ФНО (инфликсимаб и др.) |
39 |
5 |
|
Трансплантация солидных органов |
50–90 |
0,9–5 |
|
Полихимиотерапия |
39–41 |
3 |
1.3. Оценка риска реактивации ВГВ
Клинические проявления реактивации вирусного гепатита В могут варьировать от клинически незначимых до фульминантных. В некоторых случаях реактивация вирусного гепатита В может протекать без повышения трансаминаз, оставаясь бессимптомной. По данным крупного исследования, обострение ХГВу пациентов, получающих иммуносупрессивную терапию привело к декомпенсации процесса у 13% и у 5,5% — к летальному исходу.
У пациентов с HBsAg в крови реактивация ВГВ может возникнуть при лечении невысокими дозами химиопрепаратов, в то время как пациентам без HBsAg (HBsAg-отрицательные, анти-HBcore положительные, с антителами к HBsAg или без них [анти-HBs]) это происходит при более высоких дозах иммунодепрессантов (табл. 2).
Таблица 2. Риск реактивации ВГВ инфекции, связанный с иммуносупрессивной терапией
|
Риск реактивации ВГВ |
HBsAg-негативных/ HBsAg-позитивных пациентов анти-HBcore-позитивных пациентов |
|
Высокий риск > 10% |
• Генно-инженерные биологи- Генно-инженерные биологические препараты ческие препараты (монокло- (моноклональные антитела), включая ритуксимаб, нальные антитела), включая офатумумаб, устекинумаб, натализумаб, алемтузу- ритуксимаб, офатумумаб, маб, ибритумомаб устекинумаб, натализумаб, алемтузумаб, ибритумомаб |
|
Риск реактивации ВГВ |
HBsAg-позитивных пациентов |
HBsAg-негативных/ анти-HBcore-позитивных пациентов |
|
||
|
Средний риск |
• Менее мощные ингибиторы |
• Умеренные (преднизолон 10–20 мг в день |
|
1–10% |
ФНО-α, (например, этанерцепт)
|
или эквивалент) или высокие (преднизо лон > 20 мг в день или эквивалент) дозы ГКС ежедневно в течение ≥ 4 недель
|
|
Низкий |
• Антиметаболиты, азатиоприн, |
• Антиметаболиты, азатиоприн, 6-меркаптопурин, |
|
риск < 1% |
6-меркаптопурин, метотрексат • Любая доза пероральных кортикостероидов ежедневно в течение < 1 недели или внутрисуставное введение кортикостероидов |
метотрексат
|
1.4. Рекомендации по обследованию пациентов перед началом терапии
-
• Всем пациентам перед назначением системной противоопухолевой терапии необходимо определить HBsAg, суммарные анти-HBcore и анти-HBs антитела.
-
• Пациенты с хроническим ВГВ (HBsAg+), получающие любую системную противоопухолевую терапию, должны получать профилактически противовирусные препараты, во время лечения и не менее 6–12 месяцев после завершения про-
- тивоопухолевой терапии. Общеизвестно, что предпочтительно использование нуклеозидных аналогов с высоким барьером к резистентности — энтекавира и тенофовира; ламивудин в этой ситуации не рекомендован к применению.
-
• Риск реактивации ВГВ у пациентов с HBsAg+ или HBsAg-/анти-HBcore + при применении только гормонотерапии низкий. В случае изменения режима лечения с добавлением к гормонотерапии противоопухолевых лекарственных агентов с иным механизмом действия необходимо рассмотреть вопросы профилактического лечения повторно.
-
• Пациентам, у которых в крови обнаружены анти-HBc + (с отрицательным или положительным анти-HBs) без HBsAg–, получающим противоопухолевую терапию, связанную с высоким риском реактивации ВГВ (например, ритуксимаб), следует начинать противовирусную профилактику в начале противоопухолевой терапии и продолжать её в течение как минимум 12 месяцев после прекращения противоопухолевого лечения. Вирусную нагрузку — ДНК HBV — необходимо оценить до начала лечения и контролировать каждые 6 месяцев во время противовирусной терапии. Пациенты с отрицательным результатом анти-HBs антител могут иметь более высокий риск реактивации ВГВ, чем пациенты с положительным результатом анти-HBs. Для этой категории больных можно предложить следующий подход: тщательный мониторинг HBsAg и ДНК HBV каждые 3 месяца с незамедлительным началом противовирусной терапией при самых ранних признаках реактивации ВГВ (появление HBsAg или ДНК ВГВ > 1000 МЕ/мл) и при условии, что есть возможность активного наблюдения во время противоопухолевой терапии и далее в течение 12 месяцев после последней её дозы. Это связано с тем, что отсроченная реактивация ВГВ может произойти спустя годы после прекращения противоопухолевой терапии. Если уровень ДНК ВНВ определяемый, но менее 1000 МЕ/мл, показано повторное тестирование с интервалом в месяц. Обострение гепатита проявляется повышением активности АЛТ и может возникать после прекращения противовирусной терапии. Таким образом, активность АЛТ следует контролировать регулярно и после завершения противовирусного лечения, как минимум, ежемесячно в течение первых 3 месяцев после прекращения противовирусной терапии и далее каждые 3 месяца в течение 1 года.
-
• Пациенты, у которых в крови обнаружены анти-HBc (с отрицательным или положительным анти-HBs) без HBsAg (HBsAg–), получающие противоопухолевую химиотерапию, которая несёт очевидно низкий риск реактивация ВГВ (например, схемы, которые не включают моноклональные антитела против CD20 или трансплантацию стволовых клеток), следует контролировать HBsAg статус и активность АЛТ каждые 3 месяца (с последующим определением вирусной нагрузки ДНК HBV в случае обострения гепатита). Начинать противовирусную терапию необходимо только если обнаружен HBsAg или вирусная нагрузка превышает 1000 МЕ/мл.
-
2. ХРОНИЧЕСКИЙ ВИРУСНЫЙ ГЕПАТИТ С
-
3. ПРИМЕНЕНИЕ АНТИ PD-L1 ИНГИБИТОРОВ
1.5. Мониторинг
Включает определение уровня аланинаминотрансферазы (АЛТ) и ДНК ВГВ исходно, перед началом противоопухолевой терапии, а также каждые 6 месяцев в ходе противовирусной терапии. Реактивация гепатита может возникать после прекращения противовирусной терапии. Таким образом, уровень АЛТ необходимо контролировать, по крайней мере, ежемесячно в течение первых 3 месяцев после прекращения противовирусной терапии и каждые 3 месяца — в течение 1 года. Важно учитывать, что после применения энтекавира реактивация после его прекращения происходит позже, чем при применении тенофовира. Поэтому активный мониторинг следует начинать спустя 3 месяца после окончания приема энтекавира. Пациентам настоятельно рекомендуется координировать лечение с врачом, имеющим опыт лечения ВГВ, особенно для наблюдения после отмены противовирусной терапии и оценки состояния печени для исключения цирроза или рака печени.
Понятия «реактивация вирусного гепатита С» (или обострение вирусного гепатита С), также как и «профилактическая противовирусная терапия» у пациентов с ВГС и онкологическим заболеванием не существует. Перед назначением противоопухолевой терапии наряду с маркерами ВГВ и ВИЧ-инфекции и печёночными биохимическими тестами следует исследовать суммарные антитела к ВГС (анти-HCV IgM + G). При положительном результате необходима консультация инфекциониста для решения вопроса противовирусной терапии. Она может применяться одновременно с иммуносупрессивными препаратами при условии лекарственной совместимости.
Механизм реактивации ВГВ, вызванный ингибиторам контрольных точек иммунного ответа (ИКТИО), до конца не ясен, однако, по данным исследований, препараты данной группы могут способствовать пролиферации Т-регуляторных клеток, нарушать иммунный гомеостаз или приводить к выходу в кровеносное русло ранее неактивных вирусов. Отсутствие противовирусной профилактики — важный фактор реактивации ВГВ. По данным некоторых исследований, частота реактивации составляет 5,3% у пациентов с HBsAg+. Однако, по данным других исследований частота реактивации ВГВ значимо ниже: у пациентов с HBsAg — 1 %, и вообще отсутствует у HBsAg–негативных пациентов, вне зависимости от статуса анти-HBcore.
Существуют данные, что ИКТИО потенциально обладают противовирусным ответом, снижая количество истощенных Т-клеток и повышая ответ вирус-специфических Т-кле-ток. Исследования демонстрируют устойчивый противовирусный ответ PD-L1 блокады при хроническом вирусном гепатите В. В пилотном исследовании cреди HBeAg-негативных пациентов блокада ИКТИО хорошо переносилась и приводила к снижению уровня HBsAg у большинства пациентов. Эти находки подтверждают данные исследования, которое показало снижение уровня HBsAg, особенно у больных с исходным уровнем HBsAg > 1000 МЕ/мл. Новые данные свидетельствуют о том, что ИКТИО могут играть роль в противовирусном ответе. Таким образом, риск реактивации ВГВ при терапии ИКТИО достоверно не установлен, и чётких рекомендаций по профилактике и мониторингу реактивации ВГВ нет.
Определить HBsAg и анти-HBc, anti-HBs до начала лечения
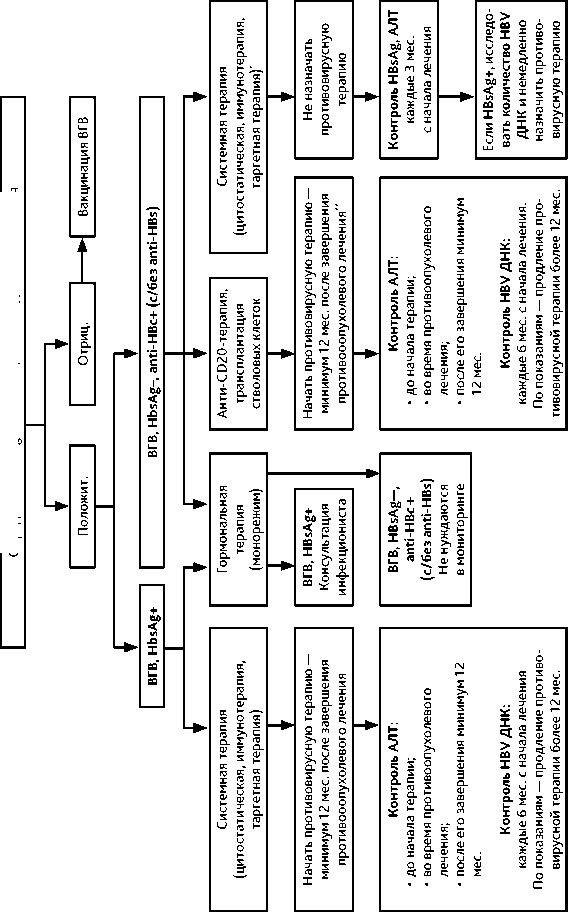
Рисунок 1. Алгоритм обследования, тактики лечения и мониторинга пациентов с ВГВ, получающих системную противоопухолевую терапию
|
том/vol. 15(3s2)2025
ЗЛОКАЧЕСТВЕННЫЕ
Malignant
Tumors
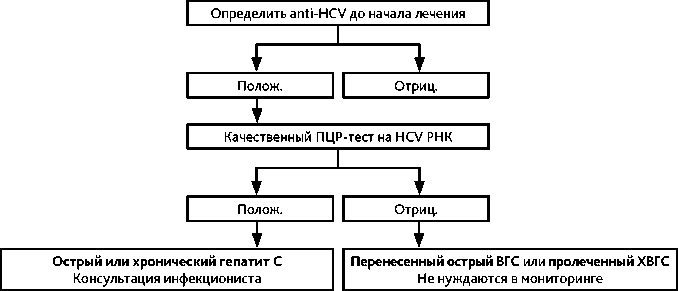
Рисунок 2. Алгоритм обследования и мониторинга пациентов с ВГC, получающих системную противоопухолевую терапию.
том/vol. 15(3s2)2025
|
ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ
Malignant Tumors


