Рецептор эпидермального фактора роста как мишень молекулярно-направленной терапии у непредлеченных пациентов с немелкоклеточным раком легкого
Автор: Сакаева Дина Дамировна, Гордиев Марат Гордиевич
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Фундаментальная онкология и экспериментальная медицина
Статья в выпуске: 3 (19), 2016 года.
Бесплатный доступ
Рецептор эпидермального фактора роста (EGFR) - один из наиболее важных и наиболее изученных сигнальных путей, регулирующий рост, выживаемость, пролиферативную активность и дифференцировку клеток у млекопитающих [1]. В тоже время EGFR и семейство белков - эпидермальных факторов роста, играют центральную роль в патогенезе и прогрессии различных видов опухолей [2]. В 80-х годах прошлого века была выдвинута гипотеза о том, что данный сигнальный путь может стать мишенью для лекарственной терапии [1]. В настоящее время существует 3 поколения ингибиторов тирозинкиназ (ИТК) EGFR. Препараты данного класса активно используются в клинической практике для лечения больных распространенным HMPJ1 с наличием мутации гена EGFR. Исследования этих препаратов продолжаются. В данном обзоре освещены возможности использования ИТК в 1-й линии терапии распространенного НМРЛ, а также в адъювантном режиме.
Egfr мутация, итк, нмрл
Короткий адрес: https://sciup.org/140222653
IDR: 140222653 | DOI: 10.18027/2224-5057-2016-3-11-17
Epidermal growth factor receptor as target of molecular-targeted therapy in patients with primary non-small cell lung cancer
Epidermal Grows factor receptor (EGFR) is one of the most significant and studied signaling pathway, regulating growth, survival, proliferation and differentiation of mamllian cells. At the same time EGFR and its protein family play a central role in pathogenesis and progression of different type of tumors. In the 80-s, it was proposed that this signaling pathway could be the target for the therapy. Today there are 3 generations of tyrosine kinase inhibitors (TKIs). This drug class is actively used in clinical practice for therapy of patients with EGFR mutation positive advanced non small cell lung cancer (NSCLC). Investigation of TKIs is continuing. In this review, the options of TKI use in the adjuvant setting and the 1st line treatment of advanced NSCLC are highlighted.
Текст научной статьи Рецептор эпидермального фактора роста как мишень молекулярно-направленной терапии у непредлеченных пациентов с немелкоклеточным раком легкого
Впервые кровоизлияние в опухоль гипофиза описал Baily в 1898 году [1].
По данным аутопсий, частота встречаемости микроаденом гипофиза у людей, не имевших характерного анамнеза,– 3–27%, по данным разных авторов. Макроаденомы встречаются у 0,3–0,5% «здоровых» людей [2–6].
Риск увеличения объема опухоли (не кровоизлияния) достигает 14% для микроаденом и 30% для макроаденом за 1,8–6,7 лет [7–9].
Размер половины макроаденом увеличивается в среднем на 10% за 32 месяца [10].
Риск кровоизлияния в опухоль гипофиза составляет от 0,4 до 7% за период от 2 до 6 лет [7, 11, 12] и может достигать 9,5% за 5 лет [10].
В 80% случаев кровоизлияние в аденому гипофиза – первое проявление заболевания [13, 14].
Риск кровоизлияния в опухоль гипофиза в 5,4 раза выше риска кровоизлияния в другую внутричерепную опухоль [15].
Существуют собственные «внутренние» опухолевые факторы, повышающие риск кровоизлияния. К ним относятся агрессивность роста опухоли и васкулопатия опухолевых сосудов [16–22]. Для опухолевых артерий характерно не- постоянство развития, неполноценность базальной мембраны, расширенные периваскулярные пространства, инфильтрированные плазматическими белками и эритроцитами [23].
МАТЕРИАЛЫ И МЕТОДЫ
Для проведения данного исследования мы проанализировали 97 случаев кровоизлияний в опухоли гипофиза, произошедшие в различные сроки (от первых суток до более 12 мес) до поступления пациента в наш стационар или до его амбулаторной консультации. То есть нам представилась возможность наблюдать результаты перенесенных кровоизлияний в различные сроки, исходно не участвуя в лечении пациента и принятии решений о выборе лечебной тактики. Необходимо принимать во внимание допущение, что нам удалось наблюдать «полный» спектр «острых» ситуаций и что число случаев, когда пациенты не переживают кровоизлияние без оказания помощи и соответственно не попадают в наше поле зрения, незначительно. То есть «истинная» ситуация статистически не отличается от полученных нами результатов.
Пациенты были распределены на несколько групп:
-
1) Пациенты, подвергшиеся только консервативному лечению (n=37)
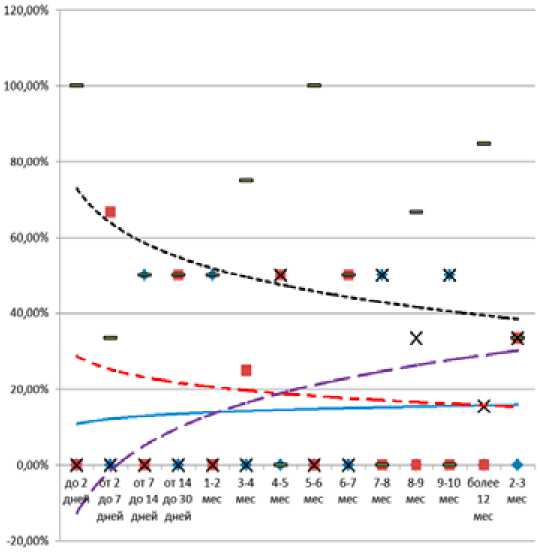
Рис. 1. Изменение зоны кровоизлияния в зависимости от его давности
-
♦ Хирурпезеское лечение бесструктурные ма<СЫ - бСССЗруКТурНЫВ массы
-
■ ХирурТИЧССКОС ЛСЧСННГ - ДИффуТНОС ПрОЛИЗЫ ЯЛ НЫР
-
— Хирургическое лечение - Лизированная Кровь
X Хирургичсоос лечение - прозрачная жидкое зь - прозрачная жидкость
— Логарифмическая (Хирургическое лечение • бесструктурные массы • 6rccipywiypwe массы)
-
— — Лагарифмичесиля (Хирурси^гскг* лечение ■ Диффузное пропип*ание)
-
- —• Логарифмическая (Хирургическое лечение • Лизированная кровь)
— - Логарифмическая (Хирургическое лечение • прозрачная жидкость -прозрачная жидкость)
-
2) Пациенты, подвергшиеся хирургическому лечению (n=45)
-
3) Пациенты с крупными постгеморрагическими кистами (n=15) составили группу «эксклюзивных» наблюдений, не подпадающих под общую статистику, но интересных в плане демонстрации вариантов кровоизлияний и течения заболевания.
Случаи острых кровоизлияний, когда пациент был доставлен в ИНХ и оперирован по срочным показаниям, оказались единичными. Группа пациентов, получавших консервативное лечение, была составлена из пациентов, перенесших острое кровоизлияние вне ИНХ и не поступивших в ИНХ в течение первого месяца. Лечение почти всех пациентов этой группы согласовывалось с авторами исследования в максимально близкие к моменту кровоизлияния сроки. В процессе проведения лечения оценивалась динамика состояния пациентов, и принималось решение о необходимости проведения хирургического лечения. Фактически эта группа пациентов была сформирована из пациентов, у которых после проведенного курса терапии отпала необходимость в хирургическом лечении. В группе пациентов, подвергшихся хирургическому лечению, собраны пациенты, оперированные в отделении транссфеноидальным доступом. Пациенты этой группы сопоставимы по основным показателям с пациентами группы «консервативного лечения».
За время сбора материала в отделении было выполнено всего несколько транскраниальных вмешательств по поводу опухолей, в строму которых произошло кровоизлияние. В основном это были гигантские опухоли. Они были включены в третью группу наблюдений.
Основные статистические закономерности кровоизлияний в опухоли гипофиза были установлены в ходе анализа первых двух групп пациентов. Данные о пациентах третьей группы были использованы для описания редко выявляющихся особенностей.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Морфологические особенности кровоизлияний
Тинкториальные свойства ткани аденомы гипофиза не зависят от ее гормональной активности. В нашей серии наблюдений 81% образцов опухоли имели эозинофильную окраску.
Макроскопически в первые дни очаг кровоизлияния представлен либо лизированной кровью, либо диффузным пропитыванием ткани опухоли. В дальнейшем содержимое очага кровоизлияния перерождается в бесструктурные массы или в кисту с прозрачной жидкостью. Некрозы в опухоли перестают выявляться после первого месяца от момента кровоизлияния в опухоль (рис. 1).
Микроскопическая картина трансформации очага кровоизлияния носит закономерный характер. К концу первого месяца после кровоизлияния некротическая ткань в очаге кровоизлияния начинает замещаться фиброзом, как результат развивающихся процессов регенерации и организации тканей в очаге. Также закономерным является отложение кристаллов холестерина и кальцинатов в очаге кровоизлияния, что является проявлением дегенерации тканей. Кристаллы холестерина были выявлены в одном наблюдении при давности кровоизлияния 1–2 мес, каль-цинаты – в двух наблюдениях при давности кровоизлияния более 12 мес.
Выявляющаяся лимфоидная инфильтрация и периваскулярные структуры, вероятно, носят случайный и вторичный характер, отражая непостоянно возникающую реакцию на кровоизлияние ткани, окружающей очаг. Лимфоидная инфильтрация в ткани опухоли была выявлена в одном наблюдении при давности кровоизлияния 4–5 мес, периваскулярные структуры – при давности кровоизлияния более 8 мес.
Ангиоматоз выявлялся в подавляющем числе наблюдений (73,33%). При этом не наблюдалось никакой разницы в его выявлении в зависимости от «свежести» кровоизлияния по данным морфологического исследования. Выявление признаков ангиоматоза в большинстве наблюдений позволяет предполагать, что его наличие является характерной особенностью (или предрасполагающим фактором) аденом, в строму которых происходят кровоизлияния. Не исключено, что в случаях, когда ангиоматоз не выявляется в ткани опухоли, это является проявлением трансформации сосудов после произошедшего в её строму кровоизлияния.
Малая частота выявления фактора роста эндотелия сосудов (VEGF) очевидно является подтверждением того, что развитие ангиоматоза в этой группе опухолей не обусловлено экспрессией VEGF в строме опухоли. В большинстве наблюдений – 15 (65,2%) экспрессия VEGF оказалась отрицательной. В 4 случаях (17,4%) она оказалась положительной и в 4 (17,4%) – сомнительной.
Отдельного обсуждения и изучения требует феномен значительной экспрессии VEGF в ткани аденогипофиза, прилегающего к опухоли, в строму которой происходит кровоизлияние. Не исключено, что именно это и есть основной стимул неоангиогенеза в опухоли.
Проведенное иммуногистохимическое исследование позволяет предположить, что предрасполагающим фактором к кровоизлиянию в опухоль гипофиза является умеренная пролиферативная активность (высокий уровень циклина D1 – белка, участвующего в регуляции клеточного цикла, и умеренно выраженная экспрессия EGFR – эпидермального фактора роста) на фоне активного неоангиогенеза. Повышение уровня циклина D1 и умеренно выраженная экспрессия EGFR, уровень Ki-67 <5%, являются проявлением умеренной пролиферативной активности аденом гипофиза.
В нашей серии ИГХ-наблюдений из 23 случаев экспрессия циклина D1 была выявлена в 21 наблюдении (91,3%). При этом митозы в клетках опухолей выявлялись только в 11 (24,4%) из 45 случаев. Экспрессия EGFR выявлялась в 12 случаях (52,2%) и в 3 случаях (13,0%) она оказалась сомнительной. Ki-67 в большинстве случаев не превышал 5%. Только в одном наблюдении его уровень составил 10%. Еще одним подтверждением склонности исследованных опухолей к пролиферации является отсутствие экспрессии p53 – маркера апоптоза. Среди удалённых опухолей, в строму которых произошло кровоизлияние, экспрессия p53 была выявлена только в 1 случае из 23 (4,3%). Мы столкнулись либо с истинным отсутствием маркера, либо с экспрессией мутированной формы белка, неспособной регулировать апоптоз и не определяющейся нашей тест-системой (рис. 2).
Плотность ткани опухоли при ее диффузном пропитывании кровью после произошедшего в неё кровоизлияния часто повышается. В первые дни после кровоизлияния плотность ряда опухолей оказывалась настолько высокой, что полное их удаление без риска повреждения капсулы и медиальных стенок кавернозных синусов представлялось невозможным. Доля плотных опухолей прогрессивно уменьшается по мере увеличения сроков давности кровоизлияния. Этот факт может быть использован для обоснования проведения отсроченной операции в случаях, когда зрительные и глазодвигательные функции нарушены незначительно.
ВЫВОДЫ
Установлены морфологические особенности опухолей, в строму которых происходят кровоизлияния. Эти особенности подтверждают одну из гипотез апоплексии аденом гипофиза, а также выявляют феномен повышенной секреции факторов неоангиогенеза в ткани аденогипофиза, прилегающей к аденоме. Экспрессия фактора роста эндотелия сосудов (VEGF) не в строме опухоли, а в окружающей её ткани аденогипофиза, требует дополнительного изучения. Возможно это один из предрасполагающих к кровоизлиянию факторов.
Крайне высокая плотность ткани имбирированной опухоли в первые дни после кровоизлияния делает её радикальное удаление без риска повреждения капсулы и медиальных стенок кавернозных синусов рискованным или невозможным, что является обоснованием отсроченной операции.
А
БВ
Г
Д
Е
Ж
З
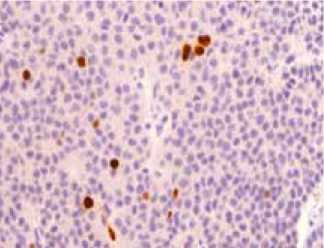
И
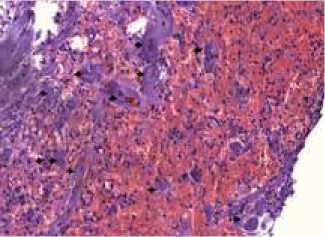
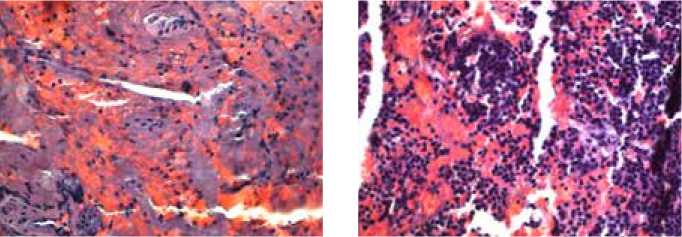
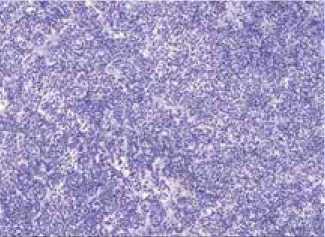
Рис. 2. Микроскопические особенности зоны кровоизлияния
А – Ангиоматоз в строме опухоли гипофиза. В строме опухоли наряду с множественными очагами кровоизлияния (красного цвета) стрелками указаны многочисленные разнокалиберные сосуды.
Б – Фиброз стромы опухоли.
В – Периваскулярные структуры в строме опухоли.
Г – Отсутствие экспрессии p53 в опухоли гипофиза. В микропрепарате не выявлено ни одной метки p53.
Д – Выраженная экспрессия циклина D1 в ткани опухоли. В строме опухоли (2) выявлено значительное накопление циклина D1, в отличие от ткани аденогипофиза (1), где выявлены единичные метки.
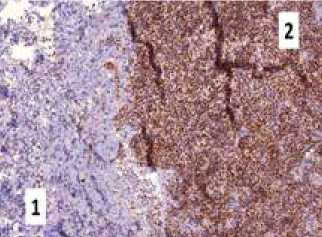
Е – Экспрессия EGFR в строме опухоли гипофиза. В строме опухоли (2) выявлена значительная экспрессия EGFR. В ткани аденогипофиза (1) экспрессия EGFR также выявлена, но менее выраженная. 3 – капсулы опухоли.
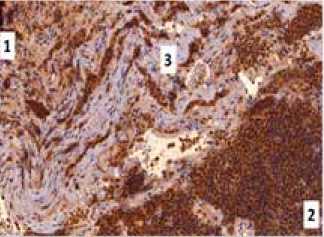
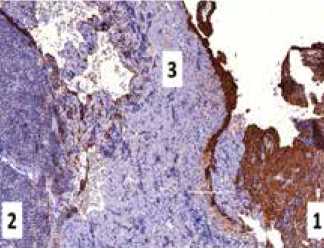
Ж, З – Экспрессия VEGF в аденогипофизе и строме опухоли гипофиза.
В ткани аденогипофиза (1) выявлена выраженная экспрессия VEGF. Его экспрессия выявлена в меньшем объеме в строме опухо ли (2), в основном в проекции вновь образованных сосудов (З). 3 – капсула опухоли.
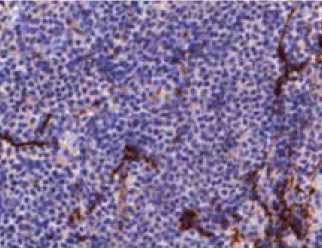
И – Индекс пролиферативной активности Ki-67. Уровень Ki-67–5% – подтверждение невысокой пролиферативной активности опухоли.
Список литературы Рецептор эпидермального фактора роста как мишень молекулярно-направленной терапии у непредлеченных пациентов с немелкоклеточным раком легкого
- D.S. Salomon, R. Brandt, F. Ciardiello, N. Normanno «Epidermal growth factor-related peptides and their receptors in human malignancies», Crit. Rev. Oncol. Hematol., 19 (1995), pp. 183-232.
- Oda K., Matsuoka Y., Funahashi A., Kitano FI. (2005). «A comprehensive pathway map of epidermal growth factor receptor signaling». Mol. Syst. Biol. 1 (1): 2005.0010.
- Gazdar A. F. et al. «Inhibition of EGFR Signaling: All Mutations Are Not Created Equal Trends» Mol Med 2004; 10:481-486.
- Sharma S. et al. «Epidermal growth factor receptor mutations in lung cancer». Nat Rev Cancer 2007; 7:169-81.
- B.M. Моисеенко, С. А. Проценко, И. И. Семенов. Современная Онкология № 1, том 12, 2010, 60-66.
- Практические рекомендации по лечению злокачественных опухолей. Портал Российского общества клинической онкологии rosoncoweb.ru , 06.06.16, URL: http://www.rosoncoweb.ru/standarts/RUSSC0/01.pdf
- M. Reck, S. Popat, N. Reinmuth, D. De Ruysscher, K. M. Kerr and S. Peters, «Metastatic non-small-cell lung cancer (NSCLC): ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up». Ann Oncol (2014) 25 (suppl 3): III27-III39.
- Masters et al. «Systemic Therapy for Stage IV Non-Small-Cell Lung Cancer: American Society of Clinical Oncology Clinical Practice Guideline Update». JCO August 31,2015,1-30.
- NCCN Guidelines. Портал национальной всеобщей онкологической сети nccn.org. [Электронный ресурс], 06.06.16, URL: http://www.nccn.org/professionals/physician_ gls/pdf/nscl.pdf NCCN Guidelines. Portal nacional'noj vseobshhej onkologicheskoj seti nccn.org. [Jelektronnyj resurs], 06.06.16, URL: http://www.nccn.org/professionals/physician_gls/pdf/ nscl.pdf
- Tony S. Mok, Yi-Long Wu, Sumitra Thongprasert, Chih-Hsin Yang, Da-Tong Chu, Nagahiro Saijo, et al. «Gefitinib or Carboplatin-Paclitaxel in Pulmonary Adenocarcinoma», N Engl J Med 2009; 361:947-957.
- Han J.Y., Park K., Kim S.W. et al. First-signal: first-line single-agent Iressa versus gemcitabine and cisplatin trial in never-smokers with adenocarcinoma of the lung. J Clin Oncol. 2012; 30:1122-8.
- Maemondo M., Inoue A., Kobayashi K. et al. Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR. N Engl J Med. 2010; 362:2380-8.
- Mitsudomi T., Morita S., Yatabe Y. et al. Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor (WTJOG 3405): an open label, randomised phase 3 trial. Lancet Oncol. 2010; 11:121-8.
- Zhou C., Wu Y. L., Chen G. et al. Erlotinib versus chemotherapy as first-line treatment for patients with advanced EGFR mutation-positive non-small-cell lung cancer (OPTIMAL, CTONG-0802): a multicentre, open-label, randomized, phase 3 study. Lancet Oncol. 2011; 12:735-42.
- Rosell R., Carcereny E., Gervais R. et al. Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer (EURTAC): a multicentre, open-label, randomized phase 3 trial. Lancet Oncol. 2012; 13:239-46.
- Cesare Gridelli, Fortunato Ciardiello, Ciro Gallo, Ronald Feld, Charles Butts et al. First-Line Erlotinib Followed Epidermal growth factor receptor as target of molecular-targeted therapy in patients with primary non-small cell lung cancer by Second-Line CisplatinGemcitabine Chemotherapy in Advanced Non-Small-Cell Lung Cancer: The TORCH Randomized Trial J Clinical Oncol. Vol 30 Num 242012:3002-3011.
- Lecia V. Sequist, James Chih-Hsin Yang, Nobuyuki Yamamoto, Kenneth O'Byrne et al. Phase III Study of Afatinib or Cisplatin Plus Pemetrexed in Patients With Metastatic Lung Adenocarcinoma With EGFR Mutations. J Clin Oncol 2013; Vol. 31 Num 27:3327-3334;
- Wu Y.L., Zhou C., Hu C.P. et al. Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations (LUX-Lung 6): an open-label, randomised phase 3 trial. Lancet Oncol. 2014; 15:213-222.
- Сервис Национального Института Здоровья США//Портал ClinicalTrials.gov , 20.10.15. URL: https://clinicaltrials.gov/ct2/results?term=chemotherapy+and+ TKI+NSCLC&Search=Search
- Wu Y. L., Lee J. S., Thongprasert S., Yu C. J., Zhang L., Ladrera G. et al. Intercalated combination of chemotherapy and erlotinib for patients with advanced stage non-small-cell lung cancer (FASTACT-2): a randomised, double-blind trial. Lancet Oncol. 2013 Jul; 14(8):777-86.
- Kanda S. et al. Phase II study of gefitinib and inserted cisplatin plus docetaxel as a first-line treatment for advanced nonsmall cell lung cancer haboring an epidermal growth factor receptor activating mutation. ASCO 2013, abs 8064 J Clin Oncol 31,2013 (suppl; abstr 8064).
- S. Sugawara, S. Oizumi, K. Minato et al. Randomized phase II study of concurrent versus sequential alternating gefitinib and chemotherapy in previously untreated non-small cell lung cancer with sensitive EGFR mutations: NEJ005/TCOG0902Ann Oncol (2015) 26 (5): 888-894.
- O.lshimoto, S. Oizumi, K. Minato et al. Randomized phase II study of concurrent versus sequential alternating gefitinib and chemotherapy in previously untreated non-small cell lung cancer (NSCLC) with sensitive EGFR mutations: NEJ005/TCOG0902. Annals of Oncology 25 (Supplement 4): iv426-iv470,2014.
- Ying Cheng, Haruyasu Murakami, Pan-ChyrYang, Jianxing He, Kazuhiko Nakagawa et al. Randomized Trial of Gefitinib with and without Pemetrexed as First-Line Therapy in East-Asian Patients with Advanced NS NSCLC with EGFR Mutations. Journal of Thoracic Oncology, Vol. 10, Sup 2,2015, S206 (ORAL 17.02).
- D’Angelo S.P. et al. Distinct Clinical Course of EGFR-Mutant Resected Lung Cancers J Thorac Oncol. 2012; 7:1815-1822.
- Karen Kelly, Nasser K. Altorki, Wilfried E. E. Eberhardt, Mary E. R. O’Brien et al. Adjuvant Erlotinib Versus Placebo in Patients With Stage IB-IIIA Non-Small-Cell Lung Cancer (RADIANT): A Randomized, Double-Blind, Phase III Trial. J Clin Oncol. V. 33, Num. 34,2015:1-8
- Сервис Национального Института Здоровья США//Портал ClinicalTrials.gov , 07.06.16. URL: https://clinicaltrials.gov/ct2/show/NCT02511106?term=ADAU RA&ran k=1
- Pasi A. Jänne, James Chih-Hsin Yang, Dong-Wan Kim, David Planchard, Yuichiro Ohe, Suresh S. et al. AZD9291 in EGFR Inhibitor-Resistant Non-Small-Cell Lung Cancer, N Engl J Med 2015; 372:1689-1699
- Catherine A. Eberlein, Daniel Stetson, Aleksandra A. Markovets, et al. Acquired Resistance to the Mutant-Selective EGFR Inhibitor AZD9291 Is Associated with Increased Dependence on RAS Signaling in Preclinical Models. Cancer Res; 75(12) June 15, 2015, 2489-2500


