Редкий случай эндокардита леффлера как проявление эозинофильного гранулематоза с полиангиитом
Автор: Скрябина Е.Н., Сафонова В.Н., Агарева Т.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Внутренние болезни
Статья в выпуске: 4 т.13, 2017 года.
Бесплатный доступ
Эозинофильный гранулематоз с полиангиитом (ЭГПА) является редким заболеванием, которое поражает мелкие и средние артерии различных органов и характеризуется наличием бронхиальной астмы, выраженной периферической эозинофилией крови. Поражение сердца отмечается в 20-50% случаев, является основной причиной смерти. В статье изложен случай ЭГПА у 43-летней женщины, имевшей эндокардит, ассоциированный с формированием тромба в левом желудочке, тромбоэмболическим синдромом и рецидивирующими инфарктами мозга. Представленный клинический случай показывает, что полное обследование сердца является чрезвычайно важным даже у больных с бессимптомным течением заболевания при подозрении на ЭГПА. Ранняя полная диагностика поражения сердца приводит к улучшению прогноза.
Диагностика, тромбоз, эндокардит леффлера, эозинофильный гранулематоз с полиангиитом
Короткий адрес: https://sciup.org/14918556
IDR: 14918556
A rare case of loeffler endocarditis associated with eosinophilic granulomatosis with polyangiitis
Eosinophilic granulomatosis with polyangiitis (EGPA) is a rare disease that affects small and medium-sized blood vessels of different organs, characterized by asthma, prominent peripheral blood eosinophilia. Cardiac involvement was reported in 20-50% and it is the major cause of mortality. A case of EGPA in a 43-year-old female, who had endocarditis, associated with thrombus formation in left ventricle, thromboembolic syndrome and recurrent stroke has been reported. The described case has showed that it is of crucial importance to perform the full cardiac imaging even in asymptomatic patients with suspected EGPA. The early identification of cardiac involvement may lead to better prognosis.
Текст научной статьи Редкий случай эндокардита леффлера как проявление эозинофильного гранулематоза с полиангиитом
1 Введение. Эозинофильный гранулематоз с полиангиитом (ЭГПА), или синдром Черджа — Стросса, — некротизирующий васкулит мелких и средних артерий, проявляющийся поражением различных органов в связи с развитием в них эозинофильных инфильтратов и часто сочетающийся с бронхиальной астмой (БА) и эозинофилией. Является редким системным васкулитом с распространенностью 7 случаев на 1 млн населения, однако в последнее время в мире отмечена тенденция к увеличению количества больных с данной патологией [1, 2]. Встречается в любом возрасте, но наиболее часто в возрасте от 35 до 45 лет [3–5].
В течении заболевания условно выделяют три основные фазы. В продромальный период, который длится до 30 лет, у больных имеются различные аллергические реакции, включающие ринит, полиноз и БА. Второй этап характеризуется эозинофилией крови и тканей. В этот период у больных нередко диагностируются синдром Леффлера, эозинофильная пневмония или эозинофильный гастрит. В третьей фазе в клинической картине болезни превалируют признаки системного васкулита [4, 5].
Эозинофильный васкулит с пристеночным эндокардитом впервые описан в 1936 г. W. Loeffler. В дальнейшем это заболевание встречалось в литературе под разными названиями: «фибропластический париетальный эндокардит с эозинофилией», «гиперэозинофильный синдром» и др. Оно характеризуется повреждающим действием эозинофилов на эндокард и сосуды. В результате инфильтрации эндокарда и миокарда [6] эозинофилами развивается фиброз эндокарда с рестриктивной кардиомиопатией. Поражение папиллярных мышц и хорд приводит к недостаточности митрального, а иногда и трехстворчатого клапана. Эндокардит осложняется образованием пристеночных тромбов с последующей тромбоэмболией. Исходом пристеночного эндокардита служит сердечная недостаточность, которая является наиболее частой причиной смерти [7].
Актуальность проблемы обусловлена высокой частотой поражения сердца (от 20 до 50%) [2, 8] и смертности (до 50%) [8] при ЭГПА, что делает необ-
ходимым поиск новых подходов к ранней диагностике данной патологии.
Цель: продемонстрировать тяжесть и неблагоприятный прогноз поражения сердца при ЭГПА, необходимость раннего полного применения визуализирующих методов обследования.
Клиническое наблюдение . Больная Ш. 43 лет с 2008 г. (37 лет) страдает БА, по поводу чего принимала сальбутамол периодически до 4–10 раз, преднизолон по 1–3 таблетки в сутки. С марта 2016 г. выявлены полипы носа, а также неоднократные обострения БА, которые купировались на фоне бронхолитической и противовоспалительной терапии (эуфилли-ном, преднизолоном; ингаляциями симбикорта, а впоследствии форадила комби и сальбутамола). Через месяц состояние ухудшилось, появились боли и припухание мелких суставов кистей и стоп, повышение температуры тела до 37,5°С без озноба.
К лету 2016 г. отмечено постепенное уменьшение явлений артрита кистей и стоп. В конце июля резко снизилось зрение обоих глаз, появились шаткость походки, посинение кончиков пальцев кистей и стоп, а также обострение БА. При КТ головного мозга обнаружены признаки дисциркуляторных изменений, данных за острое нарушение мозгового кровообращения (ОНМК) не получено. На фоне терапии пирацетамом, амброксолом, фуросемидом, инфузий с преднизолоном и эуфиллином неврологический дефицит, посинение пальцев кистей и стоп, обострение астмы купировались.
С октября 2016 г. больная отметила нарастание одышки смешанного характера при умеренной физической нагрузке, наросла бронхиальная обструкция, в связи с чем доза форадила комби увеличена с 200 до 400 мкг/сутки. Постепенно появились посинения пальцев кистей и стоп с формированием язвочек в области дистальных фаланг, периодически колющие боли в сердце, слабость и головокружение. При МРТ: картина мультифокального очагового и диффузного поражения головного мозга, возможно соответствующая системному сосудистому поражению (васкулит?), данных за ОНМК нет. В конце октября госпитализирована в ЦРБ по поводу постепенного нарастания отеков голеней до верхней трети, обострения БА. При КТ: лимфаденопатия средостения, двусторонний гидроторакс, гидроперикард, интерстициальные изменения в легких, правосторонняя пневмония с локализацией в S4-5-7 сегментах. В анализе плевральной жидкости: эритроциты 50-60%, лейкоциты 8-10%, нейтрофилы 2-4%, лимфоциты 4-6%, клетки мезотелия единичные, атипичные клетки не обнаружены. На ЭКГ: низкий вольтаж зубцов, ЧСС 120 в минуту, СРБ резко положительный. На фоне ноотропной, мочегонной, глюкокортикоидной терапии в/в и внутрь (преднизилоном 15 мг, дексаметазоном 8 мг в сутки), антибактериальной терапии (цефтриаксон 4,0/сут в/в) состояние больной продолжало ухудшаться: постепенно нарастала одышка смешанного характера, возникающая уже при минимальной физической нагрузке.
В ноябре 2016 г. в связи с нарастающим ухудшением состояния больная госпитализирована в ревматологическое отделение ГУЗ «Областная клиническая больница» (Саратов). У больной появились интенсивные боли преимущественно по передней поверхности левой голени, сопровождавшиеся выраженной гиперемией с синеватым оттенком и формированием нескольких булл различного размера с прозрачным содержимым желтоватого цвета. Наиболее крупная, содержащая до 200 мл жидкости, впоследствии вскрылась с образованием язвенного дефекта размерами 10х7 см. В легких на фоне жесткого дыхания определялись единичные рассеянные хрипы на выдохе, ЧДД 18–20 в 1 минуту. ЧСС 115 в 1 минуту, АД 120 и 80 мм рт.ст. Со стороны пищеварительной, мочевыводящей системы патологии не выявлено. Отмечено снижение мышечной силы в правых конечностях. При лабораторном исследовании: СРБ 10 мг/л (N<7 мг/л), лейкоцитоз 13,3х109/л (N 4,0–10,0х109/л) с палочкоядерным сдвигом и эозинофилией до 17% (N до 5%). В биохимическом анализе крови: мочевина 9,3 ммоль/л (N 2,5–8,3 ммоль/л), креатинин 103 мкмоль/л (N 44–124 мкмоль/л), глюкоза 7,1 ммоль/л (N 3,9–6,1 ммоль/л), общий билирубин 42,8 мкмоль/л (N 5–21,0 мкмоль/л) за счет обеих фракций, АСТ 16,6 Е/л (N до 40 Е/л), АЛТ 44,7 Е/л (N до 40 Е/л), ГГТП 87 Е/л (N 7,0–50,0 Е/л), КФК 63 Е/л (N 26–174 Е/л), КФК-МВ 10 Е/л (N до 24 Е/л), HbAlc 6,4 мг/л (N 4,0–6,0 мг/л). АТ к ВИЧ, АТ к ДНК, РФ, ВАКГ, АСЛ (О), АНЦА, АТ к фосфатидилсерину, кардиолипину, β2-гликопротеину I отсутствуют. Выявлено повышение уровня прокальцитонина: 8,8 нг/мл (N менее 0,1 нг/мл), при бактериологическом исследовании раневого отделяемого обнаружена Psedomonas aeruginosa. В ОАМ патологии не выявлено. Исследование ФВД: резкая рестрикция и тяжелая обструкция. ЭКГ: вольтаж зубцов снижен, синусовый ритм, неопределенное положение ЭОС, ЧСС 109 в минуту. Нарушена внутрижелудочковая проводимость. Гипертрофия миокарда левого желудочка. При ЭХОКГ: небольшое расширение полости правого предсердия (ПП), в верхушечной области левого желудочка (ЛЖ) визуализируется тромб диаметром 2,2х2,3 см, легочная гипертензия второй степени (СДЛА 55 мм рт.ст.), небольшое количество жидкости в полости перикарда. При УЗИ брюшной полости, почек патологии не выявлено. При КТ: участок пневмофиброза в средней доле правого легкого, лимфоаденопатия средостения, двусторонний гидроторакс (справа жидкость в большем количестве), жидкость в полости перикарда, признаки грыжи пищеводного отверстия диафрагмы. При МРТ: признаки множественных инфарктов мозга в бассейнах корковых ветвей левой и правой среднемозговых артерий (ЛСМА, ПСМА), хронической ишемии головного мозга (ХИГМ). Осмотры сосудистого и гнойного хирургов, невролога, окулиста, эндокринолога не выявили причин указанных симптомов.
С учетом наличия в анамнезе БА, эозинофилии, инфильтратов в легких высказано предположение о наличии ЭГПА. Однако отсутствие достаточного количества классификационных критериев позволило первоначально выставить диагноз: «Недифференцированный некротизирующий васкулит, подострое течение, высокая активность с поражением кожи, синдромом Рейно с критической ишемией (язвы кистей рук). Васкулит сосудов головного мозга. Последствия лакунарных инфарктов головного мозга в бассейнах ЛСМА, ПСМА неуточненного срока давности. Пирамидно-мозжечковый синдром. ХИГМ II ст. смешанного генеза. Тромб в полости левого желудочка. Относительная недостаточность митрального клапана II ст. Недостаточность трикуспидального клапана III ст. БА, среднетяжелое течение, обострение. Полисерозит (плеврит, перикардит). Легочная гипертензия II ст. Интерстициальное поражение легких, лимфоаде-нопатия средостения в анамнезе». Осложнения: «ДН II ст. Инфицированный дефект мягких тканей левой голени. Сахарный диабет, специфический тип (глюкокортикоидный), впервые выявленный».
В связи с наличием инфекции мягких тканей левой голени от проведения пульс-терапии (глюкокортикоидами и цитостатиками), от назначения цитостатиков внутрь решено было воздержаться. С учетом высокой активности васкулита, поражения сосудов головного мозга назначен преднизолон внутрь в дозе 40 мг/сутки на фоне терапии антибактериальными препаратами (в период госпитализации назначался цефтриаксон в/в; амбулаторно супракс внутрь). Применяли дезагреганты, антикоагулянты, диуретики, бронхолитические средства. Констатировано улучшение состояния: исчезновение кашля, значительное уменьшение одышки (проходит до 150 м) и отеков, уменьшение проявлений кожного васкулита.
В период после выписки приступов экспираторной одышки не возникало (ингаляционные препараты не принимала), исчезла синюшность и эпите-лизировались язвочки на кончиках пальцев кистей, уменьшились язвочки на стопах, раневой дефект кожи левой голени покрылся струпом, из-под которого отмечалось частое и обильное выделение жидкости сукровичного характера. С середины декабря 2016 г. появились дергающие боли в области данного дефекта, в связи с чем производилось введение обезболивающих препаратов, с этого же времени отметилась тенденция к нарастанию отеков, субфебрилитет (температура тела до 37,5°С с познабливанием).
В январе 2017 г. больная вновь госпитализирована в ревматологическое отделение ГУЗ «Областная клиническая больница» (Саратов) с ухудшением состояния в виде нарастания одышки смешанного характера, прогрессирования отеков до верхней трети голени, пастозности бедер, жжения в области подошвенной поверхности стоп. В ходе лабораторного обследования выявлено повышение острофазовых показателей: СОЭ 33 мм/ч (N 10–15 мм/ч), СРБ 27 мг/л (N<7 мг/л), лейкоцитоз 15,6х109/л (N 4,0–10,0х109/л) с палочкоядерным сдвигом, анемией (гемоглобин 79 г/л при N 115–160 г/л, эритроциты 3х1012/л при N 3,5–5,7х1012/л). В биохимическом анализе крови: мочевина 11 ммоль/л (N 2,5–8,3 ммоль/л), креатинин 102 мкмоль/л (N 44–124 мкмоль/л), общий билирубин 30 мкмоль/л (N 5–21,0 мкмоль/л) за счет прямого и непрямого билирубина, АСТ 15 Е/л (N до 40 Е/л), АЛТ 27 Е/л (N до 40 Е/л), ГГТП 321 Е/л (N 7,0–50,0 Е/л), КФК 75 Е/л (N 26–174 Е/л), КФК-МВ 11 Е/л (N до 24 Е/л), HbAlc 6,4 мг/л (N 4,0–6,0 мг/л). Изменения в моче отсутствовали, маркеры вирусных гепатитов не выявлены. При ЭХОКГ: отсутствует динамика в сравнении с предыдущим исследованием.
Постепенно состояние больной становится более тяжелым в связи с появлением вязкости речи, головной боли, резкой слабости (больная не может сидеть). При осмотре наблюдались дизартрия, ограничение объема движений в правых конечностях, отклонение языка в правую сторону, на вопросы отвечала не всегда адекватно. При МРТ: признаки повторного инфаркта головного мозга в бассейне ЛСМА, ПВМА, в остальном без динамики. Для уточнения характера поражения сердца как возможной причины повторных инфарктов головного мозга проведена чреспи- щеводная ЭХОКГ: выявлена облитерация верхушки сердца массивными неоднородными гипо- и гиперэхогенными образованиями, переходящими на среднюю часть полости ЛЖ до уровня сосочковых мышц. Хордальный аппарат и митральный клапан не изменены. От свободного края образований визуализировались множественные мелкие и крупные тромбы различных форм с высокоподвижными головками. Тромб максимального размера имел длину до 2,2 см (рис. 1, 2).
Проведенное обследование с выявлением необходимого количества классификационных критериев, а также других характерных для ЭГПА клинических признаков дали основание поставить диагноз:
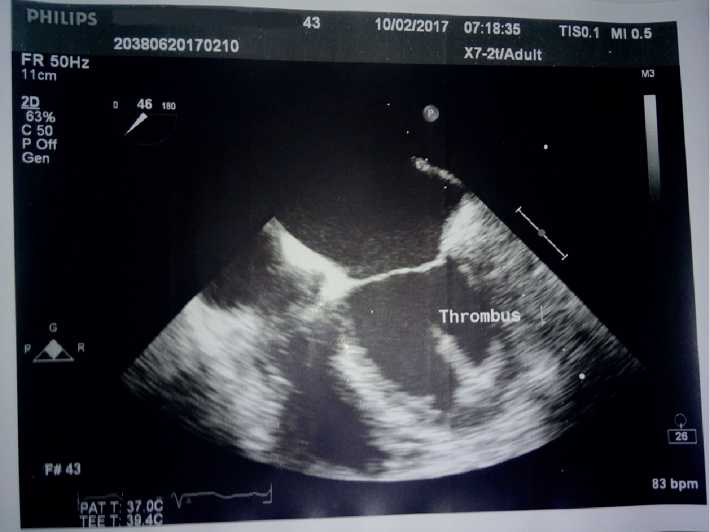
Рис. 1. Тромб размерами 2,2 см с высокоподвижной головкой в полости ЛЖ.
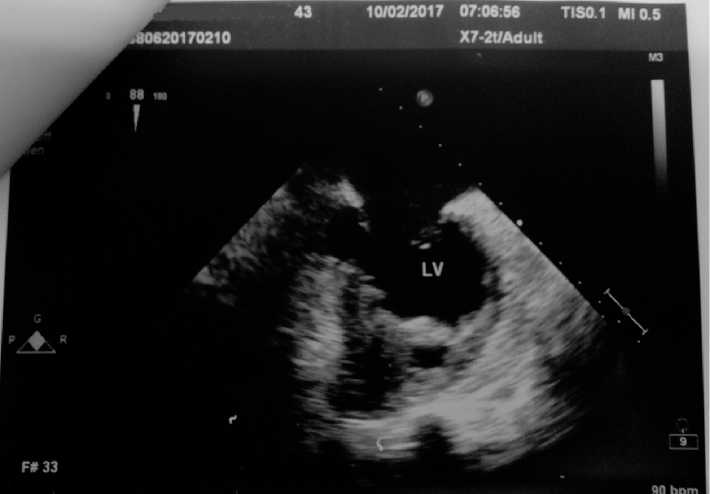
Рис. 2. Массивные неоднородные гипо- и гиперэхогенные образования, облитерирующие верхушку сердца полости ЛЖ.
«Эозинофильный гранулематоз с полиангиитом, АНЦА-отрицательный, хроническое течение, А III ст. Пристеночный фибропластический эндокардит Леффлера с развитием рестриктивной кардиомиопатии и формированием множественных мелких и крупных тромбов в полости ЛЖ. Относительная недостаточность митрального клапана II ст. Недостаточность трикуспидального клапана III ст. Легочная гипертензия II ст. Тромбоэмболический синдром: повторные инфаркты мозга в бассейнах ЛСМА, ПВМА. Последствия лакунарных инфарктов головного мозга в бассейне ЛСМА, ПВМА неуточненного срока давности. Полинейропатия. Бронхиальная астма, тяжелое течение, вне обострения. Лимфоаденопатия средостения. Анемия средней степени тяжести. Интерстициальное поражение легких с эозинофильной инфильтрацией S4-5-9, полисерозит (плеврит, перикардит), синдром Рейно, сетчатое ливедо, некротизирующий васкулит (язвы на кончиках пальцев кистей, стоп) в анамнезе». Осложнения: « ДН II ст. Н II Б (ФК III). Трофическая язва левой голени (инфицированная). Сахарный диабет, специфический тип (глюкокортикоидный), впервые выявленный. Стероидный остеопороз в стадии переломов, перелом Th 10 позвонка в январе 2017 г.».
В связи с наличием инфицированной язвы левой голени больной назначен цефтриаксон, затем, в связи с отсутствием эффекта, меронем. Пациентка получала преднизолон 40 мг/сут., прадаксу 300 мг/сут., мексидол 600 мг/сут. в/в, глицин 6 таб/сут., торасе-мид 10 мг/сут., верошпирон 150 мг/сут., карведилол 12,5 мг/сут., гликлазид МВ 30 мг/сут., сальбутамол по требованию. Трижды консультирована различными кардиохирургами, однако в оперативном лечении ей было отказано в связи с прогрессирующим течением заболевания, в частности патологии сердца, и высоким риском повторного тромбообразования в полости ЛЖ. На фоне проводимого лечения состояние больной значительно улучшилось: пациентка стала более активной, нормализовалась температура тела, исчезли отеки на нижних конечностях, уменьшилась одышка, начала эпителизироваться трофическая язва на левой голени. Пациентка выписана для продолжения лечения в ЦРБ по месту жительства. В марте 2017 г. получено сообщение от родственников о смерти больной.
Обсуждение клинического случая. Редкость ЭГПА и тяжелый прогноз при вовлечении в процесс сердца делают значимым анализ каждого клинического случая для выработки наиболее рациональных методов диагностики и лечения.
Возраст больной на момент постановки диагноза составил 43 года, что соответствует данным L. Qiao, D. Gao [9], выявивших заболевание у женщин в старшем возрасте (46, 67 лет) по сравнению с мужчинами (38, 10 лет). При первичном поступлении в стационар диагноз ЭГПА не был поставлен в связи с отсутствием необходимого количества классификационных критериев. К ним относятся: БА, эозинофилия >10%, нейропатия, рентгенологические признаки легочных инфильтратов, патология гайморовых пазух, экстра-васкулярная эозинофилия по данным биопсии [1]. У пациентки имелись только БА, эозинофилия (17%) и наличие легочного инфильтрата в анамнезе. При повторном поступлении присоединилась полинейропатия, что составило в сумме 4 критерия. Подтверждением диагноза служили дополнительно выявленные симптомы: синдром Рейно, сетчатое ливедо, некро- тизирующий васкулит, полисерозиты, полиартрит, эндокардит Леффлера.
В развитии заболевания выделяют три фазы, которые можно отметить и у нашей больной. Первая фаза, продолжительностью 6 лет, началась в 37-летнем возрасте с развития симптомов БА. Вторая фаза наступила в 43-летнем возрасте с появления инфильтратов в легких (октябрь 2016 г.) и характеризовалась быстрым переходом в третью фазу с присоединением признаков системного васкулита.
Особенностью заболевания у нашей больной явилось бессимптомное течение поражения сердца, что стало причиной поздней диагностики эндокардита Леффлера. Однако, как указывают некоторые авторы [2], даже при бессимптомном течении заболевания с подозрением на ЭГПА крайне важно выполнение полной визуализации сердца, которая может включать МРТ, КТ, чреспищеводную ЭХОКГ, коронарную ангиографию, цветную допплеровскую ультрасонографию, а в ряде случаев эндомиокардиальную биопсию. У нашей пациентки проведение трансторокальной ЭХОКГ оказалось недостаточно информативным, только выполнение чреспищеводной ЭХОКГ позволило выявить полную картину поражения ЛЖ.
Трудности диагностики на первоначальном этапе были обусловлены также АНЦА-негативным результатом анализа крови. Вместе с тем установлена определенная взаимосвязь между наличием АНЦА и особенностями патогенеза и клинической картины заболевания [5, 8, 9]. Для АНЦА-отрицательного варианта ЭГПА характерны полипоз слизистой оболочки носа, легочные инфильтраты, кардиомиопатия, полинейропатия. АНЦА-положительный вариант ЭГПА сопровождается, как правило, некротизирующим гломерулонефритом, пурпурой, легочным кровотечением, множественным мононевритом. У пациентки был симптомокомплекс, свойственный АНЦА-негативно-му варианту ЭГПА.
Как правило, ЭГПА быстро отвечает на иммуносупрессивную терапию, что обусловливает достаточно хороший прогноз. Глюкокортикоиды (ГК) являются первой линией терапии. В случае частых рецидивов или тяжелой формы некротизирующего васкулита в таких органах, как желудочно-кишечный тракт или сердце, рекомендуется применение циклофосфомида. У нашей больной течение заболевания осложнялось инфицированием крупной язвы (10х7 см) левой голени, что значительно ограничило возможности иммуносупрессивной терапии (ГК назначались в средних дозах, а от применения цитостатиков решено было воздержаться). Проведена массивная терапия антибактериальными препаратами, на фоне которой отмечалось улучшение состояния больной: стойкая нормализация температуры, появление начальных признаков эпителизации язвы.
Таким образом, основной причиной неблагоприятного исхода заболевания у нашей пациентки явилось поражение сердца; дополнительные факторы, отягчающие прогноз: присоединение инфекции и невозможность в связи с этим применения адекватной иммуносупрессивной терапии.
Заключение. Поражение сердца при ЭГПА является неблагоприятным прогностическим признаком. Применение полного объема визуализирующих методов обследования сердца позволяет обеспечить раннюю диагностику и адекватную терапию даже при бессимптомном течении ЭГПА. Важным фактором, отражающим участие сердца в патологическом процессе ЭГПА, является АНЦА-негативность.
Список литературы Редкий случай эндокардита леффлера как проявление эозинофильного гранулематоза с полиангиитом
- Системные васкулиты. В кн: Российские клинические рекомендации: Ревматология. М.: ГЭОТАР-Медиа, 2017; с. 180-204
- Francis W, Kuwari MAAEA, Ghareep A-N, et al. A Rare right ventricular involvement of eosinophilic granulomatosis demonstrated by cardiac MRI. Pol J Radiol2016; 81: 598-601
- Болезнь Чарга -Стросса. В кн: Клиническая ревматология. 2-е изд. СПб.: 000 «Издательство Фолиант», 2005; с. 325-327
- Синдром Чарга -Стросса: Васкулиты и васкулопа-тии. Ярославль: Верхняя Волга, 1999; с. 348-356
- Синдром Чарджа -Стросса. В кн: Ревматология: национальное руководство. М.: ГЭОТАР-Медиа, 2008; с. 554-557
- Beck KS, Jeong SY, Lee KY, et al. Native T1 mapping demonstrating apical thrombi in eosinophilic myocarditis associated with ChurgStrauss. Korean Circulation Journal 2016; 46 (6): 882-885
- Семенкова E.H. Системные васкулиты. M.: Медицина, 1988; 112 с.
- Jennette JC, Falk RJ, Bacon PA, et al. Revised International Chapel Hill Consensus Conference. Nomenclature of Vasculitides. Arthritis Rheum 2013; 65 (1): 1 -11
- Qiao L, Gao D. A case report and literature review of Churg -Strauss syndrome presenting with myocarditis. Medicine (Baltimore) 2016; 95 (51): e5080.


