Редкое клиническое наблюдение гипертрофической кардиомиопатии
Автор: Вахромеева М.Н., Соломанников В.М., Вахрамеева А.Ю., Сивохина Н.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 3-2 т.15, 2020 года.
Бесплатный доступ
Апикальная необструктивная гипертрофическая кардиомиопатия (синдром Yamaguchi) - это редкое наследственное заболевание, основным клиническим проявлением которого является перестройка миокарда левого желудочка, приводящая к выявляемому по данным ЭхоКГ, вентрикулографии и МРТ изменению его полости по типу «туз-пик». Данная патология была впервые описана H. Yamaguchi в 1979 году. Тем не менее, правильная дифференциальная диагностика болезней сердца на фоне этого синдрома представляет собой проблему для многих специалистов, что связано с малым количеством литературных данных, сложностью выбора адекватного метода диагностики. В данной работе мы рассматриваем пример диагностики ишемической болезни сердца у пациента с синдромом Yamaguchi при помощи однофотонной эмиссионной томографии миокарда. Мы приводим полученные нами изображения данной редкой патологии, снабженные подробными пояснениями и кратким обзором литературы, который позволил нам правильно интерпретировать полученные данные и снять диагноз ИБС, что кардинально изменило тактику ведения пациента.
Офэкт, гипертрофическая кардиомиопатя, синдром yamaguchi, эхокардиография
Короткий адрес: https://sciup.org/140260037
IDR: 140260037 | DOI: 10.25881/BPNMSC.2020.89.65.034
Cardiac spect in diagnosis of Yamaguchi syndrome
Apical non-obstructive hypertrophic cardiomyopathy also known as Yamaguchi syndrome is a rare inheritable disorder that affects the inner structure of myocardium of the left ventricle giving it a certain ace-of-spades appearance on ventriculograms, echocardiography and cardiac MRI. First described my H. Yamaguchi in 1979 this rare disorder is still a challenge for physicians around the world. Given that this condition might manifest in a number of clinical syndromes or simply coexist with other cardiac pathologies, single-photon emmition tomography seems like a viable option for differential diagnosis of coronary artery disease in this group of patients. Therefore we present a clinical observation of such a patient and a detailed illustrated description of all SPECT findings. Our case report is accompanied by a small review of literature on the matter, which, we hope, shall facilitate the work of future physicians that will have to work with patients with this rare and complex disorder.
Текст краткого сообщения Редкое клиническое наблюдение гипертрофической кардиомиопатии
Апикальная необструктивная гипертрофическая кардиомиопатия (ГКМП) или синдром Yamaguchi была впервые описана H. Yamaguchi et al. [1] в 1979 г. в качестве одного из подтипов ГКМП у 30 пациентов. Им же были впервые описаны ветрикулографические, электрокардиографические (ЭКГ) и эхокардиографические (ЭхоКГ) признаки данной патологии:
– систолическая вентрикулограмма/ ЭхоКГ картина, имеющая вид «туз-пик» в отсутствие признаков функциональной обструкции выносящего тракта левого желудочка (ЛЖ) и при-

знаков утолщения межжелудочковой перегородки (МЖП);
– наличие инвертированных зубцов Т большой амплитуды (более 1 мВ) в отведениях V4 и V5 на ЭКГ [2; 3].
Это редкое наследственное заболевание, выявляется у 25% пациентов с ГКМП в странах Азии и у 1–10% во всех остальных регионах мира на фоне общей распространенности всех наследственных форм ГКМП от 0,3 до 0,5 новых случаев в год на 100000 населения [4].
Первичная диагностика
Сложность диагностики этого синдрома обусловлена не сложными диагностическими критериями [5] или необходимостью применения дорогостоящих методов диагностики, а малой настороженностью специалистов практического здравоохранения и значительным количеством клинических вариантов течения, что часто приводит к отсроченной постановке диагноза. H. Patel et al. [3] посвятили оригинальную статью одному из таких случаев. Исходно изменения на ЭКГ были выявлены в ходе обследования терапевтом, к которому 83 летний мужчина обратился с целью подбора и коррекции терапии при артериальной гипертензии (АГ). Терапевт описал глубокие инвертированные зубцы Т в отведениях V4–V6 и назначил пациенту проведение ЭхоКГ. Тем не менее, на ЭхоКГ аномалия была пропущена. Пациент был дообследован лишь три года спустя, когда ему была выполнена ЭхоКГ с контрастом, на которой было отмечено типичное изменение полости ЛЖ по типу «туз-пик». После этого пациенту была проведена однофотонная эмиссионная компьютерная томография (ОФЭКТ) миокарда, из результатов которого авторы отмечают лишь повышенное накопление радиофармпрепарата в сегментах верхушки ЛЖ, и генетическое тестирование, показавшее наличие антисмысловой мутации Leu425Pro в гене ACTN2 [6; 7].
Однако большую сложность представляют случаи, когда диагноз должен быть поставлен быстро, например, в случае экстренной госпитализации пациента. Так, J. Morales et al. [8] описали случай диагностики синдрома Yamaguchi у 81-летнего пациента, поступившего в приемное отделение клиники с диагнозом острый коронарный синдром: инфаркт миокарда (ОКС: ИМ) с подъемом сегмента ST. На ЭКГ, снятой после поступления, авторы отметили наличие типичных инвертированных зубцов Т, на фоне которых в отведениях aVL, V1,
V3–V6 наблюдались изменения сегмента ST, исходно рассмотренные в качестве депрессии. Несмотря на низкие значения тропонина I (менее 0,016 нг/мл за весь период наблюдения), авторы обоснованно предпочли действовать по алгоритму ОКС и провели коронарную ангиографию (КАГ), в ходе которой гемодинамически значимые стенозы или окклюзии коронарных артерий (КА) выявлены не были, но было подтверждено наличие типичного изменения полости ЛЖ. Аналогичный случай был доложен в 2015 году C. Diaconu et al. [9].
Случай манифестации апикальной ГКМП в виде атриовентрикулярной узловой тахикардии по типу реентри был описан N. Candelario et al. [10] у 63 летнего мужчины. Типичные изменения в виде глубоких инвертированных зубцов Т в отведениях I, aVL и V4–V6 были описаны авторами на ЭКГ, полученной после проведения кардиоверсии. ЭхоКГ подтвердила диагноз. После чего пациенту была выполнена радиочастотная абляция (РЧА).
Дифференциальная диагностика ИБС и клинических проявлений синдрома Yamaguchi может вызывать значительные затруднения. Такой случай был доложен A. Abugroun et al. [11] на примере 58 летней пациентки, у которой были описаны типичные изменения на ЭКГ в отведениях II, III, aVF. До момента окончательной постановки диагноза пациентке многократно проводилась велоэргометрия. Лишь после госпитализации и получения подтверждения отсутствия гемодинамически значимого поражения КА, авторам удалось наглядно продемонстрировать отсутствие у данной пациентки морфологического субстрата ИБС и поставить окончательный диагноз, основанный на подтверждении типичной морфологии ЛЖ по данным ЭхоКГ. Аналогичный случай описан и отечественными авторами [12]. В этой ситуации дифференциальная диагностика потребовала нескольких повторных КАГ, в ходе которых была выполнена вентрикулография, подтвердившая наличие типичной морфологии ЛЖ на фоне классических изменений на ЭКГ.
Синдром Yagamuchi может сосуществовать с ИБС. Отечественные авторы Е.А. Ковалевская и др. [13] описали случай манифестации ИБС в форме стенокардии напряжения на фоне апикальной ГКМП у пациента 62 лет. Диагноз апикальной формы ГКМП был успешно поставлен пациенту после проведения КАГ при первой госпитализации. Одна- ко авторов насторожили изменения на ЭКГ при проведении нагрузочных тестов. Пациент был оставлен под наблюдением. В течение последующих 6 лет ему регулярно проводились нагрузочные тесты, были планово выполнены несколько КАГ, которые в итоге помогли заподозрить у пациента дебют ИБС и своевременно выполнить ЧКВ с баллонной ангиопластикой и имплантацией стента в переднюю межжелудочковую ветвь левой КА (ПМЖВ).
Апикальная форма ГКМП длительное время рассматривалась в качестве патологии с благоприятным прогнозом. Тем не менее, ряд ретроспективных исследований продемонстрировали, что данная группа пациентов больше расположена к возникновению определенных отсроченных сердечно — сосудистых осложнений, нежели общая популяция [14]. В качестве основных осложнений синдрома Yagamuchi на данный момент выделяют ОКС: ИМ, фибрилляцию предсердий (ФП). При этом у 33% пациентов могут наблюдаться желудочковые аритмии, верхушечный ИМ, тромбоз верхушки с последующий тромбоэмболией, ОКС: внезапная сердечная смерть (ВСС) [3]. ФП является наиболее частым осложнением и выявляется почти у 25% пациентов при длительном наблюдении [15]. При этом возникновение ФП у пациентов женского пола ассоциировано с наихудшим прогнозом течения заболевания [4]. Верхушечный ИМ миокарда с формированием аневризмы у пациентов с синдромом Yamaguchi также должен рассматриваться в качестве одного из маркеров неблагоприятного прогноза [14].
Клинический случай
Пациентка Л., 60 лет обратилась в ФГБУ «НМХЦ имени Н.И. Пирогова» Минздрава России для проведения ОФЭКТ с целью исключения ИБС на фоне ранее диагностированной апикальной необструктивной ГКМП (синдром Yamaguchi). Пациентка впервые обратилась к кардиологу в связи с наличием эпизодов сердцебиений. Семейный анамнез отягощен: отец и мать умерли в возрасте 70 и 77 лет вследствие ОНМК, у родной сестры 57 лет ЭКГ и ЭхоКГ признаки апикальной формы ГКМП. На момент исследования были предоставлены следующие данные дополнительных обследований:
-
1) ЭКГ: ритм синусовый, правильный, ЧСС 84/мин. Выраженная инверсия зубца Т в отведениях I, aVL, V3–V6. Индекс Соколова-Лайона = 36.
-
2) ЭхоКГ: МЖП в диастолу 1,1 см в базальном отделе, в верхушечном отделе до 1,8 см, индекс массы миокарда ЛЖ 108 г/кв.м. КДО 60 мл, КСО 24 мл, УО 36 мл, ФВ 60%. Выраженная гипертрофия верхушечных сегментов ЛЖ. Значительное расширение полости левого предсердия, выраженное уменьшение в размере полости ЛЖ, в систолу приобретающего конфигурацию «Туз-Пик». Диастолическая дисфункция ЛЖ по гипертрофическому типу. Зоны нарушения локальной сократимости не определяются.
-
3) Данные клинического и биохимического анализов крови: полученные измерения в пределах референсных значений.
-
4) Суточное мониторирование ЭКГ: основной ритм синусовый. Зарегистрировано два эпизода неустойчивой ЖТ (длительность по 5 сек), частая наджелудочковая экстрасистолия (4414/сут.), частая наджелудочковая тахикардия. Эпизоды удлинения интервала QT до 530 мсек.
-
5) УЗДГ брахиоцефальных артерий: атеросклеротические бляшки до 30% в устье внутренней сонной артерии.
На момент исследования пациентка активно жалоб не предъявляет. При подробном опросе упоминает, что ее периодически беспокоят эпизоды сердцебиений. Наличие иных болезней, в том числе хронических инфекционных, отрицает. Она также утверждает, что никогда не курила и регулярно не принимает никаких лекарственных препаратов. Краткий осмотр не выявил патологических изменений. Частота сердечных сокращений (ЧСС) на момент осмотра 80 ударов в минуту, артериальное давление (АД) — 112/86 мм рт. ст. Учитывая анамнестические данные и данные осмотра, индекс вероятности наличия ИБС Duke у данной пациентки составил менее 5%.
Перед выполнением ВЭМ пациентке была снята ЭКГ в покое (Рис. 1). На ЭКГ: ритм регулярный, синусовый, с частотой 85 в минуту, электрическая ось сердца не отклонена. Обращает на себя внимание наличие инвертированных зубцов Т в отведениях I, II, aVL, V2–V6, с наибольшей амплитудой в отведениях V4–V6 (отмечен0 стрелками), смена полярности зубца Т в отведении aVR.
Пациентке была выполнена ОФЭКТ миокарда. Исследование выполнялось по однодневному протоколу: физическая нагрузка (ВЭМ) — покой. Радиофармпрепарат (РФП) 99mТс-технетрил был введён на пике физической нагрузки, активностью
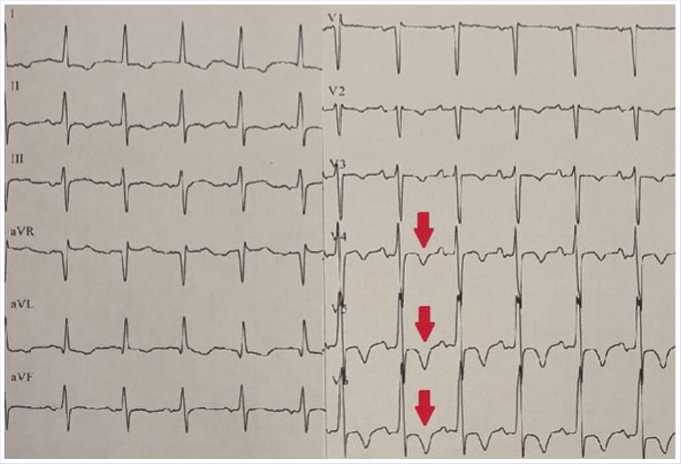
Рис. 1. ЭКГ в покое.

Рис. 2. Кривые сократимости и объемов ЛЖ в покое и при физической нагрузке (А).
370 МБк, и в покое — 740 МБк, внутривенно, болюсно. Повторное исследование в покое выполняли с интервалом в 3 часа после нагрузки. Регистрацию изображений начинали через 40 мин. после введения РФП.
Исследование проводили на двухдетекторной ротационной томографической гамма-камере «Discovery NM/CT 670» компании General Electric (США) с использованием параллельного коллиматора высокого разрешения. Регистрацию изображений проводили с синхронизацией записи по R-зубцу ЭКГ пациента.
Результаты нагрузочного теста: ВЭМ — 75 Вт, проба отрицательная, была прекращена при достижении субмаксимальной ЧСС. Во время исследования диагностически значимого смещения сегмента ST не регистрировалось. Нарушения ритма: на пике нагрузки частые наджелудочковые экстрасистолы, парные желудочковые экстрасистолы.
Полученные сцинтиграфические данные были обработаны на рабочей станции General Electric Xeleris 4.0. В ходе анализа были использованы программы QGS/QPS и Corridor 4DM.
Обработка проведена с использованием фильтра Butterworth с параметрами: critical frequency 0,52, power 5, ramp filter: quantitative.
Перед началом интерпретации карт перфузии в Corridor 4DM были построены кривые сократимости для различных отделов ЛЖ, а также кривые объемов ЛЖ в покое и при нагрузке (Рис. 2). Анализ кривых продемонстрировал сходные параметры систолического утолщения по всем отделам миокарда ЛЖ после нагрузки (А) с незначительным снижением выраженности систолического утолщения сегментов верхушки (APX, отмечены синим) в покое (Б) на фоне нормальной глобальной сократительной способности миокарда ЛЖ (В). Систолические сокра-
щение по всем сегментам миокарда ЛЖ было синхронным. Полученные графики по форме соответствовали таковым, получаемым при анализе изображений здоровых пациентов.
Дальнейший анализ сократимости и подвижности отделов ЛЖ был проведен в программе QGS/QPS (Рис. 3), которая наглядно продемонстрировала нарушения подвижности верхушки и верхушечных сегментов задней и задне-боковой стенок ЛЖ, МЖП (отмечены черным и темносиним цветами) в конечно-диастолическую фазу, как после нагрузки (А), так и в покое (Б).
Для более точной интерпретации нами были построены перфузионные полярные диагнраммы raw — накопления, которые позволяют оценить накопление РФП до обработки данных программой с целью оценки дефектов перфузии (Рис. 4). Вопреки нормальному паттерну накопления, который предполагает преимущественное накопление РФП боковой стенкой ЛЖ, максимальное накопление у данной пациентки, как при нагрузке (А), так и в покое (Б), также наблюдалось преимущественно в области верхушки и верхушечных сегментов задней и заднебоковой стенок ЛЖ, МЖП (более 80).
Распределение зон локальной гиперфиксации полностью соответствовало зонам, в которых мы ранее наблюдали сниженную подвижность (Рис. 3).
В заключение были построены и интерпретированы карты перфузии (Рис. 5), на которых наблюдались дефекты с практически полным отсутствием обратимости (значение параметра SDS = 1). Вполне очевидно, что наличие подобных дефектов перфузии у пациентки без анамнеза ОКС:ИМ, не может и не должно быть интерпретировано как рубцовое поражение, в то время как полное отсутствие обратимости в сочетании с нормальным региональным систолическим утолщением по всему миокарду ЛЖ снимает вопрос о наличии ишемии или рубцового поражения миокарда.
Приведенные изменения были интерпретированы нами как участки умеренного диффузного снижения перфузии относительного характера на фоне наличия выраженной апикальной ГКМП. Общая зона относительно гипоперфузии не превышала 7–10%.
После ОФЭКТ миокарда пациентке была выполнена ЭхоКГ на аппарате General Electric Vivid E9 (Рис. 6, А), подтвердившая наличие типичного для данной патологии изменения полости ЛЖ по типу «туз-пик» (Рис. 6, Б).
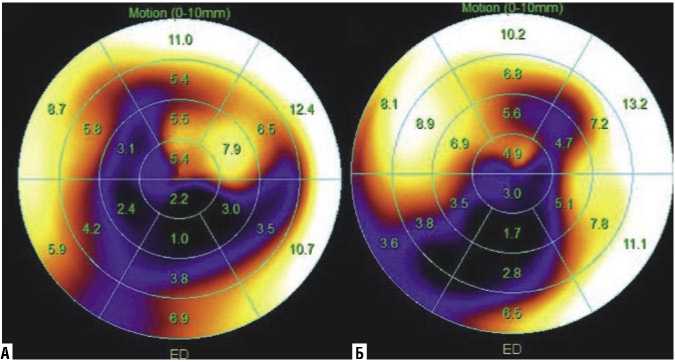
Рис. 3. Полярные карты подвижности отделов ЛЖ при нагрузке (А) и в покое (Б).
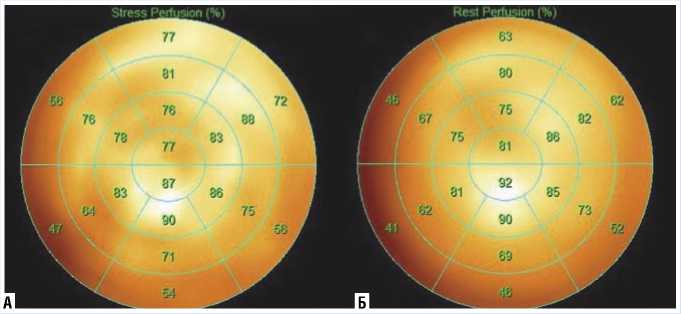
Рис. 4. Перфузионные полярные диаграммы с накоплением РФП при нагрузке (А) и в покое (Б).
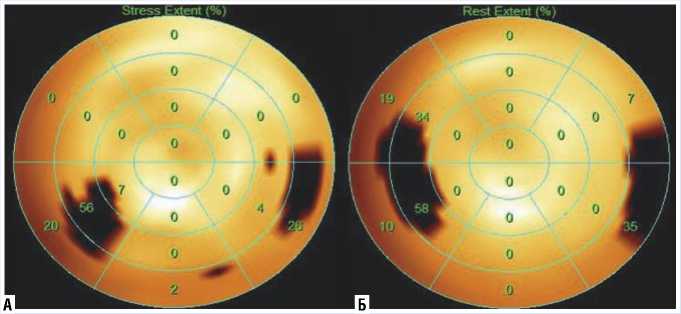
Рис. 5. Перфузионные полярные диаграммы с зонами гипоперфузии при нагрузке (А) и в покое (Б).
После проведённого обследования, данных за ИБС получено не было. Пациентке была скорректирована медикаментозная терапия — назначены антиарит-мические препараты и рекомендовано динамическое наблюдение.
Заключение
Применение ОФЭКТ миокарда в данной группе пациентов может являться мощным дополнительным методом для подтверждения или опровержения диагноза ИБС. В нашем наблюдении мы
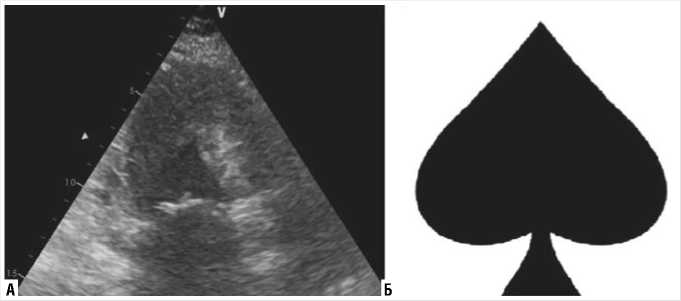
Рис. 6. ЭхоКГ типичных изменений ЛЖ в рамках синдрома Yamaguchi.
демонстрируем изменения, которые являются типичными для данной патологии у пациентов с низкой претестовой вероятностью наличия ИБС и могут быть использованы в качестве референсных в дальнейшей клинической практике.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Hypertrophic nonobstructive cardiomyopathy with giant negative T waves (apical hypertrophy): ventriculographic and echocardiographic features in 30 patients. Am J Cardiol . 1979;44(3):401–412. doi: 10.1016/0002-9149(79)90388-6.
Список литературы Редкое клиническое наблюдение гипертрофической кардиомиопатии
- Yamaguchi H, Takao I, Shinichiro N, et al. 6 Hypertrophic nonobstructive cardiomyopathy with giant negative T waves (apical hypertrophy): ventriculography and echocardiography features in 30 patients. Am J Cardiol. 1979;44(3):401-412. doi: 10.1016/0002- 79149(79)90388-6.
- Yamaguchi H, Nishiyama S, Nakanishi S, et al. Electrocardiographic, echocardiographic and ventriculographic characterization of hy-pertrophic non-obstructive cardiomyopathy. 8. Eur Heart J. 1983;4(1):105-119. doi: 10.1093/ eurheartj/4'Suppl_f'105'
- Patel H, KoKo NL, Kumar S, et al. "Acing" the hidden spade: review of diagnosis, follow-up, prognosis, and various associations of apical variant hypertrophic cardiomyopathy. Cureus. 2019;11 (1 ):5—10. doi: 10.7759/cureus.3979.
- Klarich KW, Attenhofer J, Christine H, et al. Risk of death in long-term follow-up of patients with apical hypertrophic cardiomyopa- 13. thy. Am J Cardiol. 2013;111(12):1784-1791. doi: 10.1016/j.amjcard.2013.02.040.
- Pillarisetti J, Gupta K. Giant inverted T waves in the emergency department: case report and review of differential diagnoses. J Electrocar-diol. 2010;43(1):40-42. doi: 10.1016/j.jelectro card.2009.08.048.
- Arad M, Penas-Lado M, Monserrat L, et al. Gene mutations in apical hypertrophic cardiomyopathy. Circulation. 2005;112(18):2805-2811. doi: 10.1161/CIRCULATI0NAHA.105.547 448. 14.
- Leaphart D, Waring A, Suranyi ,P et al. Call a spade a spade: missed diagnosis of apical hypertrophic cardiomyopathy. Am J Med Sci. 2019;358(4):299-303. doi 10.1016/ j.amjms.2019.07.002. 15.
- Morales J, Giraldo M. Case report: apical variant hypertrophic cardiomyopathy simulating an acute inferior myocardial infarction. J Electrocardiol. 2019;52:35-37. doi: 10.1016/ j.jelectrocard.2018.11.003.
- Diaconu CC, Dumitru N, Fruntelata AG, et al. Apical hypertrophic cardiomyopathy: the ace-of-spades as the disease card. Acta Cardiol. 2015;31(1):83-86. doi: 10.6515/ acs20140310c.
- Candelario N, Penalver J, Sen M. Yamaguchi syndrome presenting as atrioventricular nodal re-entrant tachycardia in an African-American patient. BMJ Case Rep. 2017;1(1):1-5. doi: 10.1136/bcr-2016-218051.
- Abugroun A, Ahmed F, Vilchez D, et al. Apical hypertrophic cardiomyopathy: a case report. Cardiol Res. 2017;8(5):265-268. doi: 10.14740/cr619w.
- Газизова Л.Ю., Валеев И.Г. Проблемы диагностики апикальной формы гипертрофической кардиомиопатии // Кардиология: Новости. Мнения. Обучение. — 2016. — T.8. — №1. — C. 29-34. [Gazizova LYu, Valeev IG. The problems of diagnosis of the apical form of hypertrophic cardiomyopathy. Cardiology: News, Opinions, Education. 2016;8(1):29-34. (In Russ).] doi: 10.15829/1560-4071-20189-48-53.
- Ковалевская Е.А., Крылова Н.С., Потешкина Н.Г., и др. Гипертрофическая кардиомиопа-тия в сочетании с ишемической болезнью сердца: 6-летняя история наблюдения // Российский кардиологический журнал. — 2018. — Т.1. — №9. — С. 48-53. [Kova-levskaya EA, Krylova NS, Poteshkina NG et al. Hypertrophic cardiomyopathy comorbid with coronary heart disease: 6 — year follow — up. Russian Journal of Cardiology. 2018;1(9):48-53. (In Russ).] doi: 10.15829/1560-40712018-9-48-53.
- Dahiya A, Thavendiranathan P, Thomas JD, et al. Apical hypertrophic cardiomyopa-thy with and without aneurysm. J Am Coll Cardiol. 2012;60(17):1709. doi: 10.1016/ j.jacc.2012.05.055.
- Lee SE, Park JK, Uhm JS, et al. Impact of atrial fibrillation on the clinical course of apical hypertrophic cardiomyopathy. Heart. 2017;10-3(19):1496-1501. doi: 10.1136/heartjnl-2016-310720.


