Регистр плутониевого пневмофиброза в когорте работников предприятия атомной промышленности ПО «Маяк»
Автор: Азизова Т.В., Мосеева М.Б., Григорьева Е.С., Жунтова Г.В., Банникова М.В., Сычугов Г.В., Казачков Е.Л.
Рубрика: Научные статьи
Статья в выпуске: 3 т.30, 2021 года.
Бесплатный доступ
В клиническом отделе ФГУП ЮУрИБФ ФМБА создан регистр плутониевого пневмофиброза (ППФ) в когорте работников первого российского предприятия атомной промышленности ПО «Маяк». Регистр включает 188 случаев ППФ: 117 (62,23%) у мужчин и 71 (37,77%) у женщин. В статье представлена структура и подробная описательная характеристика регистра. Показано, что частота ППФ не зависела от суммарной поглощённой в лёгких дозы внешнего гамма-излучения на дату установления диагноза. Напротив, частота ППФ зависела от суммарной поглощённой в лёгких дозы внутреннего альфа-излучения и статистически значимо возрастала с увеличением дозы внутреннего альфа-облучения. В статье обсуждаются перспективы использования регистра в будущих исследованиях.
Профессиональное облучение, внешнее гамма-облучение, внутреннее альфа-облучение, плутониевый пневмофиброз, когорта, по «маяк», регистр, зависимость, частота, перспективы использования
Короткий адрес: https://sciup.org/170179226
IDR: 170179226 | УДК: 616.24-004-02:546.799.4 | DOI: 10.21870/0131-3878-2021-30-3-56-67
Registry of plutonium-induced lung fibrosis in a cohort of nuclear workers of the Mayak production association
The registry of plutonium-induced lung fibrosis cases (PuLF) diagnosed in members of a cohort of the first Russian nuclear industry facility Mayak Production Association was established in the clinical department of the Southern Urals Biophysics Institute of the Federal Medical-Biological Agency (SUBI). The registry includes 188 plutonium-induced lung fibrosis diagnoses: 117 (62.23%) in males and 71 (37.77%) in females. This paper describes the structure and detailed characteristics of the registry. The number of PuLF cases was shown to have no association with cumulative lung absorbed dose from external gamma rays as of the date of diagnosis. On the contrary, the PuLF rate was shown to be associated with cumulative lung absorbed dose from incorporated alpha particles and to increase significantly with increasing dose from internal radiation exposure. This paper discusses potential applications of the registry to scientific investigations in the future.
Текст научной статьи Регистр плутониевого пневмофиброза в когорте работников предприятия атомной промышленности ПО «Маяк»
Известно, что после локального облучения грудной клетки при радиотерапии рака лёгкого, молочной железы, пищевода и злокачественных новообразований (ЗНО) лимфоидной и кроветворной тканей развивается острый радиационный пневмонит (ОРП). Спустя 6-24 месяца ОРП трансформируется в поздний постлучевой фиброз альвеолярных стенок, периальвеолярной ткани и других соединительно-тканных структур лёгкого [1]. Установлено, что основными факторами, определяющими развитие ОРП и пневмофиброза, являются суммарная поглощённая в лёгких доза излучения, объём облучённой ткани и временной фактор, связанный с пролиферацией альвеоцитов 2 типа и репарацией повреждений [2].
Описано несколько случаев ОРП, зарегистрированных у ликвидаторов последствий аварии на Чернобыльской атомной станции, подвергшихся острому облучению в суммарной дозе от 5,6 до 13,4 Гр [3]. Кроме этого, случаи плутониевого пневмофиброза (ППФ) были зарегистрированы в когорте работников производственного объединения (ПО) «Маяк» – предприятия атомной промышленности на Южном Урале вблизи Озёрска [4-6]. ПО «Маяк» введён в эксплуатацию в июне 1948 г., и включал комплекс промышленных реакторов, радиохимический завод, завод по производству оружейного плутония, а также ряд вспомогательных производств (завод водоподготовки, ремонтно-механический завод и др.). Первый случай ППФ установлен у работника плутониевого завода ПО «Маяк» в 1956 г. во время медицинского обследования на основе выраженных клинико-функциональных и рентгенологических изменений лёгких [4]. Лишь спустя несколько лет после установления первых клинических диагнозов была представлена экспериментальная модель ППФ [7]. Позднее подробно описана клиническая картина ППФ с характеристикой
Азизова Т.В.* – зам. директора, зав. клин. отд., к.м.н.; Мосеева М.Б. – науч. сотр.; Григорьева Е.С. – науч. сотр.; Жунтова Г.В. – вед. науч. сотр., к.м.н.; Банникова М.В. – мл. науч. сотр. ФГУП ЮУрИБФ ФМБА России. Сычугов Г.В. – доцент, к.м.н.; Казачков Е.Л. – зав. кафедрой, д.м.н., проф. ФГБОУ ВО ЮУГМУ Минздрава России.
рентгенологических и функциональных изменений в бронхолёгочной системе, критерии диагностики, клинические особенности, течение и исходы ППФ [8-10].
Регулярное медицинское наблюдение работников ПО «Маяк» (более 70 лет) с обязательными ежегодными комплексными обследованиями по стандартной программе позволило накопить первичные данные, которые были использованы при создании уникального регистра ППФ.
В настоящей статье представлена подробная характеристика регистра ППФ в когорте работников ПО «Маяк», подвергшихся внешнему гамма- и внутреннему альфа-излучению, и перспективы его использования.
Материал и методы
Как и в других исследованиях [11-13], когорта работников ПО «Маяк» включала 22377 человек (25,40% женщин), впервые нанятых на один из основных заводов (реакторы, радиохимический или плутониевый) в период 1948-1982 гг., независимо от пола, возраста, национальной принадлежности, профессии, продолжительности работы и других характеристик. В этой когорте уже на протяжении нескольких десятилетий изучаются неопухолевые [11-13] и опухолевые эффекты [14-16] и развивающиеся в разные сроки после профессионального облучения. Подробная характеристика изучаемой когорты работников ПО «Маяк» представлена в указанных и других многочисленных публикациях [11, 12, 17, 18].
Следует отметить, что период наблюдения за когортой начинался от даты найма на один из основных заводов и продолжался до первого из следующих событий: даты смерти; 31 декабря 2018 г. для живых работников, проживающих в Озёрске (резиденты); даты «последней медицинской информации» для работников-резидентов с неизвестным жизненным статусом и для работников, выехавших из Озёрска на другое постоянное место жительства (мигранты). Следует подчеркнуть, что медицинская и иная информация для работников регулярно обновлялась только за период проживания в Озёрске, т.к. доступ к медицинской информации после выезда работника из города был невозможен. В изучаемой когорте работников на конец периода наблюдения число мигрантов составило 9286 человек (41,50%), но преобладающее большинство из них выехали из Озёрска в период 1948-1968 гг. (91,10%).
К концу периода наблюдения жизненный статус известен для 21344 членов (95,34%) изучаемой когорты; из них 14351 человек (67,27%) умерли, 6983 человек (32,73%) живы (среди резидентов жизненный статус известен для 13081 человека, из которых 9091 человек (69,5%) умерли и 3990 человек (30,50%) живы).
Дозиметрическая система для изучаемой когорты работников ПО «Маяк» претерпела несколько существенных изменений и в настоящей работе была использована последняя улучшенная версия «Дозиметрической системы работников ПО «Маяк» - 2013» (ДСРМ-2013) [19]. Необходимо отметить, что работники реакторов в ходе своей профессиональной деятельности подвергались только внешнему, преимущественно гамма-излучению, а работники радиохимического и плутониевого заводов подвергались как внешнему облучению, так и воздействию альфа-активных аэрозолей трансурановых элементов. Оценки доз внешнего гамма-излучения доступны для всех работников ПО «Маяк»; в то время как оценки доз внутреннего альфа-облучения имеются только у 44,81% работников (от всех, кто потенциально мог подвергнуться воздействию альфа-активных аэрозолей), у которых измерена альфа-активность в биосубстратах (в основном, в образцах суточной мочи). Следует отметить, что 41,00% работников изучаемой когорты наняты на ПО «Маяк» до 1955 г., то есть в период наиболее неблагоприятных производственных условий, поэтому средние суммарные дозы профессионального облучения работников при сравнении с другими когортами работников существенно выше. Средняя (здесь, и далее ± стандартное отклонение, СО) суммарная поглощённая в лёгких доза внешнего гамма-излучения в изучаемой когорте работников составила 0,48±0,68 Гр у мужчин и 0,39±0,58 Гр у женщин. Среди работников, контролировавшихся на внутреннее облучение, средняя суммарная поглощённая в лёгких доза внутреннего альфа-излучения на конец периода наблюдения составила 0,18±0,53 Гр у мужчин и 0,31±1,39 Гр у женщин.
Регистр ППФ является структурной частью медико-дозиметрической базы данных «Клиника» [20, 21]. В структуру регистра ППФ входят следующие основные блоки персонифицированной информации: «Идентификационные и паспортные данные», «Медицинская история и жизненный статус», «Факторы риска», «Заболеваемость», «Клинические данные», «Дозиметрические данные», «Профессиональный маршрут», «Предыдущая профессиональная деятельность». Подробное описание первичных данных, содержащихся в основных блоках, и источники этой информации представлены ранее [20]. Источниками медицинской информации являлись архивные и текущие медицинские карты, истории болезней, протоколы аутопсии, акты судебномедицинской экспертизы, журналы регистрации результатов обследований, журналы скорой медицинской помощи и др.
Статистическая обработка первичных данных проведена с использованием стандартного пакета STATISTICA 10.0. Различия считали статистически значимыми при уровне значимости (p) ниже 0,05 [22].
Результаты
В изучаемой когорте работников в течение всего периода наблюдения зарегистрировано 188 случаев ППФ: 117 (62,23%) у мужчин и 71 (37,77%) у женщин.
К концу периода наблюдения жизненный статус известен у 97,87% работников с ППФ; из них 181 (98,37%) работника умерли, 3 (1,63%) – живы. Большинство (64,80%) работников с ППФ умерли в возрасте старше 60 лет. Средний возраст на момент смерти у мужчин составил 66,54±11,80 лет (диапазон 35,0-93,0) и у женщин – 64,61±15,34 (диапазон 34,0-94,0); а средний возраст на конец периода наблюдения – 83,00 и 90,00±4,24 лет (диапазон 83,0-93,0) соответственно. Следует отметить, что аутопсия была проведена у 57,00% умерших работников, и во всех случаях диагноз пневмофиброза, установленный при жизни, был подтверждён.
Распределение работников с ППФ в зависимости от возраста и пола на момент установления диагноза представлено в табл. 1. Половина случаев (50,54%) ППФ зарегистрирована у работников в возрасте моложе 40 лет; средний возраст на момент установления диагноза у мужчин – 42,69±8,17 лет и у женщин – 39,97±6,79 лет (табл. 1).
Таблица 1
Распределение работников с ППФ в зависимости от возраста и пола на момент установления диагноза
|
Возраст, лет |
Мужчины |
Женщины |
Оба пола |
|||
|
число |
% |
число |
% |
число |
% |
|
|
≤ 40 |
52 |
44,44 |
43 |
60,56 |
95 |
50,54 |
|
41-45 |
22 |
18,80 |
15 |
21,13 |
37 |
19,68 |
|
46-50 |
22 |
18,80 |
6 |
8,45 |
28 |
14,89 |
|
≥ 50 |
21 |
17,95 |
7 |
9,86 |
28 |
14,89 |
|
Всего |
117 |
100,00 |
71 |
100,00 |
188 |
100,00 |
Анализ структуры смертности (табл. 2) показал, что 56,91% работников с ППФ умерли от ЗНО, 25,97% – от болезней системы кровообращения. Следует отметить, что у 6 (3,31%) работников ППФ являлся основной причиной смерти. Среди умерших от ЗНО у 59 (57,28%) работников основной причиной смерти были ЗНО лёгкого, у 17 (16,50%) работников – ЗНО печени, и у 3 (2,91%) работников – ЗНО костей, т.е. 76,70% работников с ППФ, умерших от ЗНО, умерли от ЗНО органов основного депонирования плутония.
Таблица 2 Структура смертности в группе работников с ППФ
|
Класс МКБ-9 |
Название класса |
Мужчины |
Женщины |
Оба пола |
|||
|
число |
% |
число |
% |
число |
% |
||
|
I |
Инфекционные и паразитарные |
0 |
0,00 |
1 |
1,49 |
1 |
0,55 |
|
II |
Новообразования, из них: |
66 |
57,89 |
37 |
55,22 |
103 |
56,91 |
|
ЗНО лёгкого |
43 |
37,72 |
16 |
23,88 |
59 |
32,60 |
|
|
ЗНО печени |
5 |
4,39 |
12 |
17,91 |
17 |
9,39 |
|
|
ЗНО костей |
1 |
0,88 |
2 |
2,99 |
3 |
1,66 |
|
|
III |
Эндокринные расстройства, нарушения обмена и иммунитета |
1 |
0,88 |
0 |
0,00 |
1 |
0,55 |
|
IV |
Болезни крови и кроветворных органов |
0 |
0,00 |
0 |
0,00 |
0 |
0,00 |
|
V |
Психические расстройства |
2 |
1,75 |
0 |
0,00 |
2 |
1,10 |
|
VI |
Болезни нервной системы и органов чувств |
0 |
0,00 |
0 |
0,00 |
0 |
0,00 |
|
VII |
Болезни системы кровообращения |
29 |
25,44 |
18 |
26,87 |
47 |
25,97 |
|
VIII |
Болезни органов дыхания |
5 |
4,38 |
1 |
1,49 |
6 |
3,32 |
|
IX |
Болезни органов пищеварения |
1 |
0,88 |
3 |
4,48 |
4 |
2,21 |
|
X |
Болезни мочеполовой системы |
1 |
0,88 |
0 |
0,00 |
1 |
0,55 |
|
XVI |
Симптомы, признаки и неточно обозначенные состояния |
4 |
3,51 |
1 |
1,49 |
5 |
2,76 |
|
XVII |
Травмы и отравления |
5 |
4,39 |
6 |
8,96 |
11 |
6,08 |
|
из них 990.33-990.36 |
2 |
1,75 |
4 |
5,97 |
6 |
3,31 |
|
|
Всего |
114 |
100,00 |
67 |
100,00 |
181 |
100,00 |
|
Следует подчеркнуть, что преобладающее большинство (93,62%) работников с ППФ были наняты на ПО «Маяк» в 1948-1954 гг. Средний возраст начала работы в условиях контакта с альфа-активными аэрозолями у мужчин составил 28,38±7,17 лет (диапазон 18,0-50,0), у женщин – 26,79±5,09 лет (диапазон 20,0-46,0). У преобладающего большинства (81,70%) работников продолжительность работы в контакте с альфа-активными аэрозолями до момента установления диагноза ППФ составляла более 10 лет (в среднем 18,42±7,84 лет у работников радиохимического завода и 13,78±5,12 лет у работников плутониевого завода). В то время как средняя продолжительность работы до начальных клинических проявлений ППФ была в 3,5 раза меньше.
Распределение работников с ППФ в зависимости от суммарной поглощённой в лёгких дозы внешнего гамма- и внутреннего альфа-излучения на дату установления диагноза ППФ представлено в табл. 3 и 4.
Таблица 3
Распределение работников с ППФ в зависимости от суммарной поглощённой в лёгких дозы внешнего гамма-излучения на момент установления диагноза ППФ
|
Суммарная поглощённая в лёгких доза внешнего гамма-излучения, Гр |
Мужчины |
Женщины |
Оба пола |
|||
|
число |
% |
число |
% |
число |
% |
|
|
0,0-0,25 |
16 |
13,68 |
10 |
14,08 |
26 |
13,83 |
|
0,26-0,50 |
14 |
11,97 |
9 |
12,68 |
23 |
12,23 |
|
0,51-0,75 |
17 |
14,53 |
9 |
12,68 |
26 |
13,83 |
|
0,76-1,00 |
16 |
13,67 |
11 |
15,49 |
27 |
14,36 |
|
1,01-2,00 |
36 |
30,77 |
23 |
32,39 |
59 |
31,38 |
|
2,01-3,00 |
15 |
12,82 |
8 |
11,27 |
23 |
12,23 |
|
> 3,00 |
3 |
2,56 |
1 |
1,41 |
4 |
2,14 |
|
Всего |
117 |
100,00 |
71 |
100,00 |
188 |
100,00 |
Таблица 4
Распределение работников с ППФ в зависимости от суммарной поглощённой в лёгких и альвеолярно-интерстициальном отделе дозы внутреннего альфа-излучения от инкорпорированного плутония на момент установления диагноза ППФ
|
Доза, Гр |
Мужчины |
Женщины |
Оба пола |
|||
|
число |
% |
число |
% |
число |
% |
|
|
Распределение работников с ППФ в зависимости от суммарной поглощённой |
||||||
|
в лёгких дозы альфа-излучения, Гр |
||||||
|
Не измерена |
31 |
26,50 |
9 |
12,66 |
40 |
21,29 |
|
0-0,25 |
1 |
0,85 |
1 |
1,41 |
2 |
1,06 |
|
0,26-0,50 |
7 |
5,98 |
6 |
8,45 |
13 |
6,91 |
|
0,51-1,00 |
23 |
19,66 |
8 |
11,27 |
31 |
16,49 |
|
1,01-3,00 |
46 |
39,32 |
16 |
22,54 |
62 |
32,98 |
|
3,01-6,00 |
9 |
7,69 |
16 |
22,54 |
25 |
13,30 |
|
6,01-12,00 |
0 |
0,00 |
13 |
18,31 |
13 |
6,91 |
|
> 12,01 |
0 |
0,00 |
2 |
2,82 |
2 |
1,06 |
|
Итого |
117 |
100,00 |
71 |
100,00 |
188 |
100,00 |
|
Распределение работников с ППФ в зависимости от суммарной поглощённой |
||||||
|
в альвеолярно-интерстициальном отделе дозы альфа-излучения, Гр |
||||||
|
Не измерена |
32 |
27,34 |
9 |
12,67 |
41 |
21,81 |
|
0-0,25 |
1 |
0,85 |
0 |
0,00 |
1 |
0,53 |
|
0,26-0,50 |
2 |
1,71 |
3 |
4,23 |
5 |
2,66 |
|
0,51-1,00 |
10 |
8,55 |
4 |
5,63 |
14 |
7,45 |
|
1,01-3,00 |
40 |
34,19 |
14 |
19,72 |
54 |
28,72 |
|
3,01-6,00 |
23 |
19,66 |
12 |
16,90 |
35 |
18,62 |
|
6,01-12,00 |
10 |
8,55 |
13 |
18,31 |
23 |
12,23 |
|
12,01-24,00 |
0 |
0,00 |
13 |
18,31 |
13 |
6,91 |
|
> 24,00 |
0 |
0,00 |
3 |
4,23 |
3 |
1,60 |
|
Итого |
117 |
100,00 |
71 |
100,00 |
188 |
100,00 |
Средняя суммарная поглощённая в лёгких доза внешнего гамма-излучения у мужчин составила 0,84±1,15 Гр, у женщин – 2,79±3,83 Гр; средняя суммарная поглощённая в лёгких доза внутреннего альфа-излучения – 1,64±1,22 Гр и 3,99±3,59 Гр, а поглощённая в альвеолярно-интерстициальном (АИ) отделе лёгкого – 3,21±2,82 Гр и 8,24±8,40 Гр соответственно.
Как показал анализ, частота ППФ не зависела от суммарной поглощённой в лёгких дозы внешнего гамма-излучения на дату установления диагноза (рис. 1а). Напротив, частота ППФ зависела от суммарной поглощённой в лёгких дозы внутреннего альфа-излучения и статистически значимо возрастала с увеличением дозы альфа-облучения (рис. 1б и 1в).
а) 100
60 с с
40 го т
0 0-0,10 0,11-0,25 0,26-0,50 0,51-0,75 0,76-1,00 1,01-2,00 2,01-3,00 >3,00
Суммарная поглощённая в лёгких доза внешнего гамма-излучения на конец периода наблюдения, Гр
Рис. 1. Частота ППФ в изучаемой когорте работников в зависимости от суммарной поглощённой в лёгких дозы внешнего гамма-излучения (а) и суммарной поглощённой в лёгких (б) и АИ отделе (в) дозы внутреннего альфа-излучения от инкорпорированного плутония.
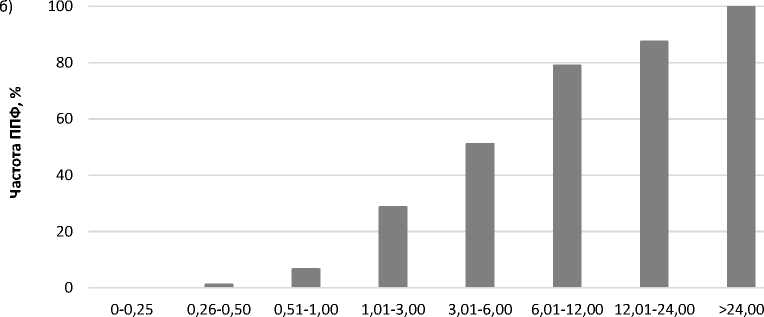
Суммарная поглощённая в лёгких доза внутреннего альфа-излучения от инкорпорированного плутония, Гр
в) 100
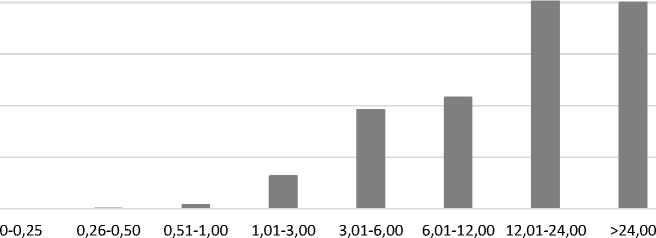
Суммарная поглощённая в АИ отделе лёгких доза внутреннего альфа-излучения от инкорпорированного плутония, Гр
Рис. 1 (продолжение). Частота ППФ в изучаемой когорте работников в зависимости от суммарной поглощённой в лёгких дозы внешнего гамма-излучения (а) и суммарной поглощённой в лёгких (б) и АИ отделе (в) дозы внутреннего альфа-излучения от инкорпорированного плутония.
Обсуждение
ПО «Маяк» – крупное предприятие атомной промышленности – включал в себя комплекс промышленных реакторов для наработки плутония, радиохимический завод для выделения плутония из облучённого в реакторе сырья, плутониевый завод для получения чистого металлического плутония для изготовления ядерных зарядов, а также вспомогательные производства [23, 24]. Несовершенство оборудования и технологического процесса, низкая степень механизации и автоматизации производства в первые годы эксплуатации приводили к высокому содержанию альфа-активных аэрозолей в воздухе рабочих помещений. В связи с тем, что до 1957 г. работники ПО «Маяк» не применяли индивидуальные средства защиты органов дыхания, альфа-активные аэрозоли преимущественно ингаляционным путём попадали в организм в больших количествах и накапливались в органах основного депонирования (лёгкие, печень, скелет). Внутреннее альфа-облучение в дозах, многократно превышавших допустимые дозы, приводило к развитию ППФ у работников радиохимического и плутониевого заводов ПО «Маяк» [6, 10, 25].
Диагноз ППФ у работников ПО «Маяк» был установлен на основании клинической картины заболевания, физикального и рентгенологического обследования лёгких (обзорная рентгенография в двух проекциях с крупнофокусной рентгенографией верхушек и I-II межреберий), лабораторных исследований и исследования функции внешнего дыхания (жизненная ёмкость лёгких, мощность вдоха и выдоха, диффузионная способность лёгких, коэффициент сопротивления дыханию и др.). Следует напомнить, что, к сожалению, в период установления диагнозов ППФ у работников ПО «Маяк» (1956-1968 гг.) отсутствовала возможность использовать такие методы диагностики как компьютерная томография, ядерно-магниторезонансная томография, волоконно-оптическая бронхоскопия и др.
Анализ показал, что частота ППФ в когорте работников ПО «Маяк» значимо возрастала с увеличением суммарной поглощённой в лёгких (и в АИ отделе) дозы внутреннего альфа-излучения от инкорпорированного 239Pu, и не зависела от дозы внешнего гамма-излучения. Полученные результаты хорошо согласуются с результатами экспериментальных исследований на животных, свидетельствующих о том, что частота фиброза и степень его тяжести у крыс [10] и собак [26], подвергшихся воздействию альфа-активных аэрозолей, возрастала с увеличением суммарной поглощённой в лёгких дозы внутреннего альфа-излучения как при однократном, так и при хроническом ингаляционном поступлении. Ретроспективное исследование, проведённое среди работников завода по производству ядерного оружия «Рокки Флэтс» (США), выявило повышенный риск пневмофиброза при облучении лёгких в дозе более 10 Зв [27]. Исследуемая группа состояла из 326 работников, подвергшихся внутреннему альфа-излучению в суммарной поглощённой в лёгких дозе от 0 до 28 Зв, и 194 необлучённых работников. Сравнивая степень интерстициальных нарушений в лёгких на рентгенограммах грудной клетки, авторы пришли к выводу, что облучение лёгких в дозе 10 Зв и более приводило к 5,3-кратному увеличению риска (95% ДИ: 1,2-23,4) развития нарушений, характерных для лёгочного фиброза, при сравнении с необлучёнными работниками с учётом влияния мешающих факторов (возраст, курение и воздействие асбеста).
Как было показано ранее, ППФ является детерминированным эффектом (реакцией ткани лёгкого на альфа-излучение), характеризующимся дозовым порогом и увеличением частоты, распространённости и выраженности склеротических изменений, и как следствие, степени тяжести реакции с увеличением дозы облучения [10, 28, 29]. Однако, до сих пор не уточнены зависимости доза-эффект и дозовый порог для развития ППФ с учётом нерадиационных факторов, способствующих развитию пневмофиброза (статус и индекс курения, наличие сопутствующих заболеваний лёгких, и, в первую очередь, хронического бронхита, контакт с другими фиброгенными частицами и др.).
Созданный регистр ППФ в когорте работников ПО «Маяк» с полной и качественной демографической, медицинской и дозиметрической информацией позволит в будущем проанализировать и уточнить зависимости доза-эффект и мощность дозы-эффект с учётом нерадиационных факторов; определить латентный период, риск и дозовый порог для развития ППФ. Следует отметить, что одним из главных преимуществ изучаемой когорты является наличие биологических образцов для 30,00% её членов, в том числе для 72 (38,30%) работников с установленным диагнозом ППФ. Наличие биологических образцов ткани лёгкого позволит изучить морфологические и другие характеристики ППФ; определить маркеры ППФ, а также лучше понять механизмы развития ЗНО лёгкого у работников, подвергшихся внутреннему альфа-излучению, и разработать биологическую модель развития радиационно-индуцированного ЗНО лёгкого.
Заключение
Создан регистр плутониевого пневмофиброза в когорте работников первого российского ядерного предприятия ПО «Маяк». Регистр включает 188 случаев ППФ: 117 (62,23%) у мужчин и 71 (37,77%) у женщин. Полные и качественные первичные медицинские и дозиметрические данные на всех работников с ППФ, наличие биологических образцов ткани лёгкого для 38,30% случаев позволят в будущем уточнить латентный период, риск и дозовый порог развития ППФ, лучше понять механизмы развития ЗНО лёгкого у работников, подвергшихся внутреннему альфа-излучению.
Список литературы Регистр плутониевого пневмофиброза в когорте работников предприятия атомной промышленности ПО «Маяк»
- McDonald S., Rubin P., Phillips T.L., Marks L.B. Injury to the lung from cancer therapy: clinical syndromes, measurable endpoints, and potential scoring systems //Int. J. Radiat. Oncol. Biol. Phys. 1995. V. 31, N 5. P. 1187-1203.
- Bentzen S.M., Skoczylas J.Z., Bernier J. Quantitative clinical radiobiology of early and late lung reactions //Int. J. Radiat. Biol. 2000. V. 76, N 4. P. 453-462.
- Баранов А.Е., Гейл Р.П., Гуськова А.К. Трансплантация костного мозга после облучения у пострадавших при аварии на Чернобыльской АЭС //Гематология и трансфузиология. 1989. № 34. С. 3-16.
- Волкова Л.Г. Пневмосклероз как исход лучевой болезни, вызванной интоксикацией плутония //Бюл. рад. мед. 1961. № 2. С. 82-91.
- Мишачев А.А. К вопросу о профессиональном пневмосклерозе у работников предприятия по переработке плутония-239 //Бюл. рад. мед. 1962. № 4а. С. 97-100.
- Кошурникова Н.А., Аристов В.П., Лембрг В.К., Нифатов А.П., Терновский И.А., Хохряков В.Ф. Некоторые отдалённые последствия поражения плутонием-239 у людей //Бюл. рад. мед. 1978. № 4. С. 53-59.
- Булдаков Л.А., Любчанский Э.Р., Москалев Ю.И., Нифатов А.П. Проблемы токсикологии плутония. М: Атомиздат, 1969. 368 с.
- Никитин В.П. Рентгендиагностика профессионального плутониевого пневмосклероза //Бюл. рад. мед. 1976. № 1. С. 26-30.
- Окладникова Н.Д., Кудрявцева Т.И., Беляева З.Д. Плутониевый пневмосклероз, итоги многолетнего медицинского наблюдения //Вопросы радиационной безопасности. 2002. № 1. С. 42-49.
- Плутоний. Радиационная безопасность /под ред. Л.А. Ильина. М.: Изд. АТ, 2005. 416 с.
- Azizova T.V., Grigorieva E.S., Hunter N., Pikulina M.V., Moseeva M.B. Risk of mortality from circulatory diseases in Mayak workers cohort following occupational radiation exposure //J. Radiol. Protect. 2015. V. 35, N 3. P. 517-538.
- Azizova T.V., Grigoryeva E.S., Haylock R.G.E., PikulinaM.V., Moseeva M.B. Ischaemic heart disease incidence and mortality in an extended cohort of Mayak workers first employed in 1948-1982 //Br. J. Radiol. 2015. V. 88, N 1054. P. 20150169.
- Azizova T.V., Zhuntova G.V., Haylock R.G.E., Grigoryeva E.S., Moseeva M.B., Pikulina M.V., Belyaeva Z.D., Bragin E.V. Chronic bronchitis in the extended Mayak worker cohort: workers first employed between 1948-1982 //Occup. Environ. Med. 2017. V. 74, N 2. P. 105-113.
- Shilnikova N.S., Preston D.L., Ron E., Gilbert E.S., Vassilenko E.K., Romanov S.A., Kuznetsova I.S., Sokolnikov M.E., Okatenko P.V., Kreslov V.V., Koshurnikova N.A. Cancer mortality risk among workers at the Mayak nuclear complex //Radiat. Res. 2003. V. 159, N 6. P. 787-798.
- Hunter N., Kuznetsova I.S., Labutina E.V., Harrison J.D. Solid cancer incidence other than lung, liver and bone in Mayak workers: 1948-2004 //Br. J. Cancer. 2013. V. 109, N 7. P. 1989-1996.
- Azizova T.V., Bannikova M.V., Grigoryeva E.S., Rybkina V.L. Risk of malignant skin neoplasms in a cohort of workers occupationally exposed to ionizing radiation at low dose rates //PLoS One. 2018. V. 13, N 10. P. e0205060.
- Azizova T.V., Bannikova M.V., Grigorieva E.S., Bagaeva Ya.P., Azizova E.V. Risk of lower extremity arterial disease in a cohort of workers occupationally exposed to ionizing radiation over a prolonged period //Radiat. Environ. Biophys. 2016. V. 55, N 2. P. 147-159.
- Azizova T.V., Bragin E.V., Hamada N., Bannikova M.V. Risk of cataract incidence in a cohort of Mayak PA workers following chronic occupational radiation exposure //PLoS One. 2016. V. 11, N 10. P. e0164357.
- Napier B.A. The Mayak worker dosimetry system (MWDS-2013): an introduction to the documentation //Radiat. Protect. Dosim. 2017. V. 176, N 1-2. P. 6-9.
- Azizova T.V., Day R.D., Wald N., Muirhead C.R., O'Hagan J.A., Sumina M.V., Belyaeva Z.D., Druzhinina M.B., Teplyakov I.I., Semenikhina N.G., Stetsenko L.A., Grigoryeva E.S., Krupenina L.N., Vlasenko E.V. The "Clinic" medical-dosimetric database of Mayak production association workers: structure, characteristics and prospects of utilization //Health Phys. 2008. V. 94, N 5. P. 449-458.
- Азизова Т.В., Сумина М.В., Беляева З.Д., Григорьева Е.С., Дружинина М.Б., Тепляков И.И. Регистр плутониевого пневмосклероза //Вопросы радиационной безопасности. 2009. № 2. С. 45-54.
- Zar J.H. Biostatistical analysis. New Jersey: Prentice Hall, 1999. 620 p.
- Третьяков Ф.Д. Характеристика радиационной обстановки на плутониевом производстве ПО «Маяк» в разные периоды его деятельности //Источники и эффекты облучения работников ПО «Маяк» и населения, проживающего в зоне влияния предприятия. Часть 1 /под ред. С.А. Романова, М.Ф. Киселева. Челябинск: Челябинский дом печати, 2009. С. 4-50.
- Третьяков Ф.Д., Романов С.А. Характеристика радиационной обстановки на первом радиохимическом заводе ПО «Маяк» //Источники и эффекты облучения работников ПО «Маяк» и населения, проживающего в зоне влияния предприятия. Часть 2 /под ред. М.Ф. Киселева, С.А. Романова. Челябинск: Челябинский дом печати, 2010. С. 8-34.
- Хохряков В.Ф., Меньших З.С., Мигунова Н.И. О вероятности возникновения пневмосклероза и рака лёгких у персонала, подвергавшегося ингаляции аэрозолями плутония //Бюл. рад. мед. 1978. № 4. C. 72-75.
- Park J.F., Watson C.R., Buschbom R.L., Dagle G.E., Strom D.J., Weller R.E. Biological effects of inhaled 239PuO2 in beagles //Radiat. Res. 2012. V. 178, N 5. P. 447-467.
- Newman L.S., Mroz M.M., Ruttenber A.J. Lung fibrosis in plutonium workers //Radiat. Res. 2005. V. 164, N 2. P. 123-131.
- Гуськова А.К., Байсоголов Г.Д. Лучевая болезнь человека. М.: Медицина, 1971. 384 c.
- ICRP, 2012. ICRP statement on tissue reactions and early and late effects of radiation in normal tissues and organs - threshold doses for tissue reactions in a radiation protection context. ICRP Publication 118 //Ann. ICRP. 2012. V. 41, N 1-2. P. 1-322.


