Реканализация подкожной вены голени после клеевой облитерации на фоне пожизненной антикоагулянтной терапии
Автор: Ширинбек О., Мнацаканян Г.В., Одинокова С.Н.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4 т.19, 2024 года.
Бесплатный доступ
Цианоакрилатная клеевая облитерация (ЦКО) на протяжении более десятилетия успешно используется у пациентов с варикозной болезнью нижних конечностей (ВБНК). Преимуществом метода являются отсутствие необходимости тумесцентной анестезии и послеоперационной компрессии. В клиническом наблюдении продемонстрирован опыт ЦКО варикозных вен у пациентки, находящейся на пожизненной антикоагулянтной терапии варфарином. За период наблюдения в послеоперационном периоде в течение 1, 3, 6 и 12 месяцев была отмечена стойкая целевая окклюзия подкожной венозной магистрали. Однако при контрольном осмотре через 36 месяцев была отмечена значимая реканализация одной из двух сафенных вен.
Цианоакрилатная клеевая облитерация, варикозная болезнь, антикоагулянтная терапия, реканализация, варфарин
Короткий адрес: https://sciup.org/140308708
IDR: 140308708 | DOI: 10.25881/20728255_2024_19_4_152
A case of vein recanalization after glue ablation on a patient receiving permanent antithrombotic therapy
Cyanoacrylate adhesive closure (CAC) of varicose veins of the lower limbs has been in practical use for more than a decade. The main advantages of CAC are avoidance of tumescent anesthesia and post-interventional compression. In this clinical report we illustrate a case of glue ablation in a patient receiving life-long antithrombotic therapy (warfarin). The follow-up on 1, 3, 6 and 12 months post-procedure has shown occlusion of the target saphenous veins. However, following 36 months post intervention, recanalization of one of the two previously occluded veins has been detected.
Текст научной статьи Реканализация подкожной вены голени после клеевой облитерации на фоне пожизненной антикоагулянтной терапии
За последние два десятилетия в хирургии ВБНК за счет внедрения ряда новых технологий удалось добиться значительного прогресса [1]. По мере развития и внедрения методов эндовенозной облитерации варикозных вен проведение самой процедуры стало доступным практически для каждого пациента в условиях инфильтрационной (тумесцентной) анестезии [2] или даже без нее [3; 4]. Данные способы лечения пациентов с ВБНК представляют собой не менее эффективную альтернативу комбинированной фле-бэктомии [5; 6], являются для оператора технически несложными, воспроизводимыми, демонстрируют малые риски повреждения кожи и кожных ветвей периферических нервов и, в целом, являются безопасными и для пациента [7–9]. В до-эндовенозную эпоху, когда флебология не рассматривалась без применения скальпеля и анестезиологического пособия, пациенты, длительно или на постоянной основе получающие антикоагулянтную терапию, представляли собой задачу, решение которой представляло собой большую проблему как для хирурга, так и для анестезиолога. Да и в целом хирургическое вмешательство как таковое для данной группы больных всегда связано с интра- и послеоперационными рисками геморрагических осложнений, что актуально и в настоящее время в рамках амбулаторной и большой хирургии, что требующее персонализированного подхода к каждому подобному пациенту. Однако на результат эндовенозной термооблитерации несостоятельных магистральных подкожных не может повлиять антикоагулянтная терапия. Причиной этому является деструкция венозной стенки на физико-химическом уровне и смена белковых молекул конфигурации, и как результат, своей структуры [10–12].
Сравнительно недавно были внедрены в практику новые методы нетермической эндовенозной облитерации варикозных вен, не требующие проведения тумесцентной анестезии [13–15]. При анализе отечественных источников литературы по данному вопросу мы не встретили сообщений, в которых бы описывался опыт применения цианоакрилатной клеевой облитерации (ЦКО) у пациентов с целевой гипокоагуляцией. В этой связи мы хотели бы представить первый в России подобный опыт с описанием результатов отдаленного наблюдения.
Пациентка Р., 74 лет, 22.09.2020 г. обратилась с жалобами на потемнение кожи правой ноги, расширенные вены в обеих ногах; на чувство тяжести, отека голеней. Кроме того, больная жаловалась на снижение памяти, нарушение ходьбы, шаткость и неуверенность походки, периодическое повышение АД, а также учащенное мочеиспускание с резями и подтекание мочи при напряжении. Со слов пациентки жалобы со стороны нижних конечностей присутствовали на протяжении длительного времени.
Из анамнеза известно, что пациентка находится под наблюдением кардиолога по поводу хронической ревматической болезни сердца с формированием комбинированного митрально-аортального порока. В 1997 г. пациентке выполнено хирургическое вмешательство в объеме протезирования аортального и митрального клапанов протезами Carbomedics в условиях искусственного кровообращения, непрямой фармакохолодовой кардиоплегии и гипотермии. В послеоперационном периоде у пациентки развилась фибрилляция предсердий, в дальнейшем некупируемая ни электрической, ни фармакологической кардиоверсией, ФК III по EHRA. Пациентке была назначена постоянная антикоагулянтная терапия препаратом «Варфарин» с целевыми значениями МНО в диапазоне 2,5–3,5. Имеет место также нарушение

ритма сердца по типу желудочковой экстрасистолии (ФК 4а по Lown-Wolff), хроническая сердечная недостаточность, функциональный класс III по NYHA, гипертоническая болезнь III ст., 3 ст., риск сердечно-сосудистых осложнений 4, риск геморрагических осложнений по шкале CHA2DS2VASc 5 баллов.
Пациентка также наблюдается у невролога по поводу хронической ишемии головного мозга на фоне атеросклероза, вестибуло-базиллярной недостаточности, болезни Паркинсона (гиперкинетическая форма), астено-невротических реакций. Также известно, что пациентка страдает сахарным диабетом II типа с 2016 г., хроническим циститом, старческой катарактой справа, артифакией слева.
Объективный статус: общее состояние относительно удовлетворительное, сознание ясное, положение тела активное, телосложение нормостеническое. Пастозность голеней с обеих сторон.
Неврологический статус: скованность движений, с трудом начинает ходьбу и с трудом останавливается. Ги-помимия. В позе Ромберга покачивается. Постуральная неустойчивость. Пальценосовую пробу выполняет неуверенно с 2-х сторон. Пяточно-коленную пробу выполняет неуверенно.
Органы дыхания: грудная клетка обычной формы, активно участвует в акте дыхания. Аускультативно дыхание в легких везикулярное, проводится во все отделы. Хрипов отсутствуют. ЧДД 20 в мин.
Сердечно-сосудистая система: ау-скультативно тоны сердца приглушены, аритмичные. На верхушке сердца выслушивается короткий систолический шум с иррадиацией в область основания сердца и левую подмышечную область. АД 135/65 мм рт. ст. ЧСС 80 уд/мин. Пульс 72 уд/мин. Дефицит пульса 8 уд/мин. Пульсация брюшного отдела аорты в области эпигастрия удовлетворительная.
Органы пищеварения: без изменений.
Status localis: имеются варикозно-расширенные притоки бассейнов большой подкожной вены (БПВ) обеих нижних конечностей и малой подкожной вены (МПВ) справа. Множество ретикулярных вен и телангиэктазий на обеих нижних конечностях. Симптомы Мозеса и Хоманса отрицательны. Гиперпигментация нижней трети голеней. В проекции магистральных артерий нижних конечностей пульсация удовлетворительного наполнения. Термоасимметрии нет.
По данным ЭхоКГ (от августа 2020 г.): ФВ 63%, аортальный градиент 34 мм рт. ст., скорость 2,9 м/с, аортальная регургитация I ст.; митральный градиент 19 мм рт. ст., скорость 2,1 м/с, трикуспит-дальная регургитация II ст., регургитация на ЛС I ст. Систолическое давление в ЛА 52 мм рт. ст.
По данным ультразвукового ду-плескного сканирования (УЗДС) вен нижних конечностей (от августа 2020 г.): признаки клапанной недостаточности са-фено-феморальных соустий (СФС) с обеих сторон, клапанной несостоятельности и расширения БПВ справа с сегментарным рефлюксом в пределах голени; признаки клапанной несостоятельности и расширения БПВ слева с тотальным рефлюксом; по передне-медиальной, заднемедиальной поверхности левого бедра на уровне средней и нижней третей, медиальной поверхности обеих голеней на уровне нижней, средней и верхней третей множественные притоки БПВ с патологическим рефлюксом; признаки несостоятельности сафено-поплитеального соустья (СПС) с обеих сторон; тотальная клапанная несостоятельность МПВ справа; признаки расширения перфорантных вен обеих голеней до 4 мм с признаками клапанной недостаточности.
В амбулаторных условиях 26.09.2020 г. пациентке выполнена клеевая облитерация БПВ слева и МПВ справа по методике VenaSeal.
Описание операции
В положении пациентки на животе, в асептических условиях после двухкратной обработки операционного поля спиртовым раствором под местной анестезией раствором лидокаина 2%-1.0 мл выполнена пункция и канюляция МПВ у нижней границы рефлюкса в нижней трети голени справа у латеральной лодыжки. По стандартной методике выполнена катетеризация ствола МПВ. По протоколу VenaSeal набрано в шприц 3.0 мл цианоакрилатного адгезива. Шприц присоединён к пистолету-дозатору, клей введен в доставочный катетер. Последний установлен на расстоянии 5 см от устья СПС. Зона СПС пережата ультразвуковым датчиком. По-сегментарно выполнено введение клея в ствол МПВ с последующей мануальной компрессией. Израсходовано 1.0 мл адгезива. Наложены стрипы, асептическая наклейка на место венозного доступа. При эхо-контроле, МПВ справа на всем протяжении не сдавливается. В положении больной на спине, после обработки операционного поля спиртовым раствором дважды под местной анестезией раствором лидокаина 2%-1.0 мл выполнена пункция и канюляция БПВ (s-тип) у нижней границы рефлюкса в верхней трети бедра слева. По стандартной методике выполнена катетеризация ствола БПВ. По технологии VenaSeal, набрано в шприц 3.0 мл цианокрилатного адгезива. Шприц присоединён к пистолету-дозатору, клей введен в доставочный катетер. Последний по интродьюсеру установлен на расстоянии 5 см от устья СФС. Зона СФС пережата ультразвуковым датчиком. Посегментарно выполнено введение в ствол БПВ клея с последующей мануальной компрессией. Израсходовано 0.5 мл клея. Наложены стрипы, асептическая наклейка на место венозного доступа. При эхо-контроле, БПВ слева не сдавливается. Системных осложнений, связанных с процедурой, не наблюдалось. Пациентка немедленно активизирована.
При контрольном осмотре на 3-и сутки после вмешательства: жалоб нет, состояние удовлетворительное. Местный статус: кожные покровы нижних конечностей без признаков воспаления, единичный экхимоз на голени справа. На контрольной и УЗДС вен нижних конечностей вен — окклюзия просветов БПВ слева и МПВ справа, культя БПВ 0,5 см, зона СФС слева и СПС справа – без особенностей.
В отдаленном послеоперационном периоде пациентка к флебологу не обращалась до августа 2023 г. При этом предъявляет жалобы на расширение вен левой нижней конечности, чувство тяжести и отечности в левой ноге. Данные жалобы пациентка, со слов, отмечает на протяжении последних 6 месяцев. При местном осмотре имеется картина варикозного синдрома в бассейнах передней окружающей бедро вены слева и МПВ справа (Рис. 1).
При УЗДС вен нижних конечностей признаки клапанной недостаточности БПВ слева с рефлюксом в бассейн передней окружающей бедро вены; признаки полной реканализации с картиной пристеночно расположенных «цианоакрилатных бляшек» в стволе БПВ слева от области СФС и на всем протяжении ранее выполненной облитерации (Рис. 2); признаки тотальной клапанной недостаточности МПВ слева и БПВ справа; картина полной целевой окклюзии МПВ справа.
Ситуация расценена как рецидив варикоза в бассейне БПВ слева и прогрессирование заболевания в бассейнах БПВ справа и МПВ слева. Было принято

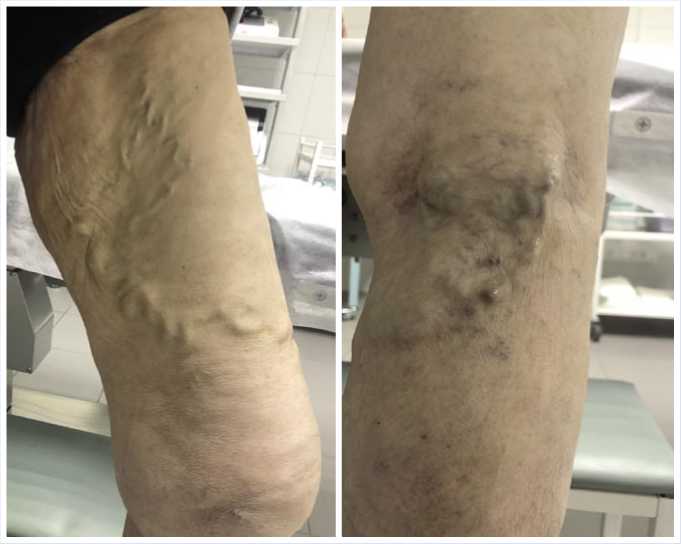
Рис. 1. Фото нижних конечностей с варикозом бассейна БПВ слева и МПВ справа.
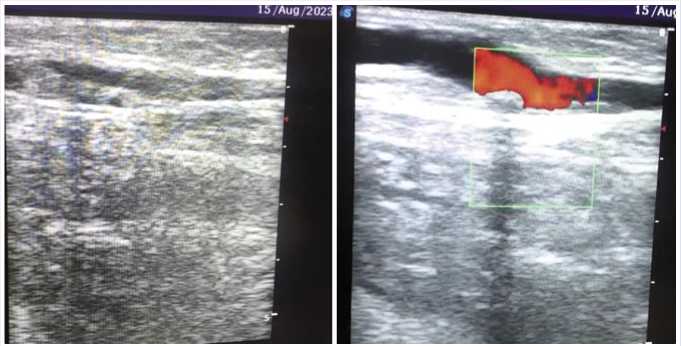
Рис. 2. Фото эхо-картины реканализации ствола БПВ слева.
решение о повторной клеевой облитерации БПВ слева, облитерации БПВ справа и МПВ слева.
Обсуждение
Согласно ряду исследований применение клеевых технологий устранения рефлюкса в отдаленном периоде демонстрирует высокую эффективность, сопоставимую с термооблитерацией несостоятельных магистральных подкожных вен. В частности, в своем систематическом обзоре литературы Dimech A.P и соавт. [16] на примере 2910 пациентов, из которых большей части выполнена ЦКО (n = 1981), а остальным – термиче- ская облитерация, сообщают результаты двухлетней целевой окклюзии, которая составила 93,7, 90,9 и 91,5% для ЦКО, радиочастотной и лазерной облитерации, соответственно.
За время регистрации в РФ метода VenaSeal для клеевой облитерации магистральных подкожных вен в отечественной литературе не было сообщений о результатах применения данной технологии у пациентов с гипокоагуляционным статусом. Обратившись к зарубежным источникам, мы обнаружили, что данная проблема достаточно подробно описана в контексте различных показаний для применения антикоагулянтов. В част- ности, в случае применения пероральных антикоагулянтов (ПОАК) по поводу эндовенозного клей-индуцированного тромбоза (EGIT), Pappas J.N. et al. [17] сделан вывод о том, что при определенных стадиях данного послеоперационного осложнения ПОАК не оказывает существенного влияния на ретракцию клеевого субстрата облитерированной вены [18]. Тем не менее, применение ПОАК в случае EGIT представляется целесообразным в качестве профилактики тромботической адгезии на клеевой субстрат после ЦКО [19]. Но данная проблема является предметом отдельного обсуждения и отдельной публикации. По теме же применения в качестве антикоагулянтной терапии препарата кумаринового ряда нами обнаружены единичные сообщения, в частности Lane T.R. et al. [20] описывают пожизненное применение варфарина пациенткой по поводу постоянной формы фибрилляции предсердий, на фоне чего проводилась клеевая облитерация БПВ. Несмотря на отсутствие предписания по данной методике использования послеоперационной компрессии, пациентке было предложено использования компрессионного трикотажа 2 класса. На контрольном осмотре через 8 недель была зарегистрирована окклюзия БПВ от уровня 2 см от СФС до дистальной точки пункции вены. Пациентка отметила регресс веноспецифической симптоматики и выраженности визуального проявления варикозного синдрома. Во время 6-месячного планового контрольного осмотра, включающий УЗДС, выявлена полная реканализация БПВ, за исключением единичного сегмента длиной в 2 см. При этом пациенткой не было отмечено появление новых или повторное проявление старых варикозных вен на оперированной нижней конечности, тем не менее предъявлялись жалобы на ощущение отечности и объективный асимметричный отек в области голени. Таким образом, можно заключить, что, несмотря на прогрессирование симптомов ХВН и несостоятельность БПВ, варикозный синдром у данной пациентки отсутствовал. В последующем авторами сообщения было принято решение о проведении стволовой пенной склеротерапии.
Необходимо подчеркнуть, что процесс цианоакрилатной окклюзии сам по себе не имеет ничего общего с реакциями коагуляционного каскада. Данное обстоятельство является поводом для возникновения закономерного вопроса в этом отношении. Если полимеризация адгезива в просвете сосуда — это

не продукт коагуляционного механизма, почему антикоагулянтный препарат обладает свойством лизиса молекул цианоакрилата. На этот закономерный и крайне любопытный вопрос должны пролить свет дальнейшие исследования в данной области.
Заключение
При внедрении в практику клеевой облитерации необходимость послеоперационного контроля должна быть неотъемлемой частью протокола наблюдения, в особенности, когда проводится антикоагулянтная терапия по любым релевантным показаниям. Дальнейшие исследования в этом аспекте могут прояснить роль антикоагуляции как предиктора реканализации вен.
Список литературы Реканализация подкожной вены голени после клеевой облитерации на фоне пожизненной антикоагулянтной терапии
- Lane TR, Pandey VA, Davies AH. Superficial venous disease treatment--is there still a role for open surgery in 2011? Acta Chir Belg. 2011; 111(3): 125-9. doi: 10.1080/00015458. 2011.11680722.
- Бокерия Л.А., Михайличенко М.В., Прядко С.И., Париков М.А., Коваленко В.И. Хирургическое лечение больных с варикозной болезнью нижних конечностей. Эволюция проблемы – прошлое и настоящее // Анналы хирургии. – 2014. – №4. – С.5-12.
- Ontario Health (Quality). Nonthermal Endovenous Procedures for Varicose Veins: A Health Technology Assessment. Ont Health Technol Assess Ser. 2021; 21(8): 1-188.
- Ширинбек О., Одинокова С.Н. Цианоакрилатная клеевая облитерация подкожных вен // Флебология. – 2021. – №15(4). – С.297 303. doi: 10.17116/flebo202115041297.
- Ширинбек О. Справочник хирурга-флеболога. – М.: ГЭОТАР-Медиа, 2024. – 144 с.
- Ширинбек О., Мнацаканян Г.В., Одинокова С.Н. Цианоакрилатная клеевая облитерация варикозных вен в реальной клинической практике: двухлетние результаты лечения // Амбулаторная хирургия. – 2022. – №19(1). – С.132-139. doi: 10.21518/1995-1477-2022-19-1-132-139.
- Gao RD, Qian SY, Wang HH, Liu YS, Ren SY. Strategies and challenges in treatment of varicose veins and venous insufficiency. World Journal of Clinical Cases. 2022; 10(18): 5946-5956. doi: 10.12998/wjcc.v10.i18.5946.
- Paravastu SCV, Horne M, Dodd PDF. Endovenous ablation therapy (laser or radiofrequency) or foam sclerotherapy versus conventional surgical repair for short saphenous varicose veins. Cochrane Library. 2016; 2016(11). doi: 10.1002/14651858.cd010878.pub2.
- Ширинбек О., Мнацаканян Г.В., Одинокова С.Н. Нежелательные явления и осложнения после цианоакрилатной клеевой облитерации варикозных вен // Ангиология и сосудистая хирургия. – 2023. – №29(1). – С.59-66. doi: 10.33029/ 1027-6661-2023-29-1-59-66.
- Sharifi M, Mehdipour M, Bay C, Emrani F, Sharifi J. Effect of anticoagulation on endothermal ablation of the great saphenous vein. J Vasc Surg. 2011; 53(1): 147-9. doi: 10.1016/j.jvs. 2010.07.062.
- Delaney CL, Russell DA, Iannos J, Spark JI. Is endovenous laser ablation possible while taking warfarin? Phlebology. 2012; 27(5): 231-4. doi: 10.1258/phleb.2011.011031.
- Gabriel V, Jimenez JC, Alktaifi A, et al. Success of endovenous saphenous and perforator ablation in patients with symptomatic venous insufficiency receiving long-term warfarin therapy. Ann Vasc Surg. 2012; 26(5): 607-11. doi: 10.1016/j.avsg.2011.10.019.
- Almeida JI, Javier JJ, Mackay EG, Bautista C, Proebstle T. Cyanoacrylate glue great saphenous vein ablation: preliminary 180-day follow-up of a first-in-man feasibility study of a no-compression-no-local-anesthesia technique. J Vasc Surg. 2012; 55: 297.
- Elias S, Raines JK. Mechanochemical tumescentless endovenous ablation: final results of the initial clinical trial. Phlebology. 2011; 27(2): 67-72. doi: 10.1258/phleb.2011.010100.
- Ширинбек О., Одинокова С.Н. Цианоакрилатная клеевая облитерация подкожных вен // Флебология. – 2021. – №15(4). –С.297 303. doi: 10.17116/flebo202115041297.
- Ширинбек О. Клеевая облитерация магистральных подкожных вен: руководство для врачей. М.: ГЭОТАР-Медиа, 2022. doi: 10.33029/9704-7103-6-KOV-2022-1-48.
- Shirinbek O. Cyanoacrylate adhesive closure of refluxing saphenous veins. M.: GEOTAR-Media, 2023. doi: 10.33029/9704-7103-6-KOV-2022-1-48.
- Dimech AP, Cassar K. Efficacy of Cyanoacrylate Glue Ablation of Primary Truncal Varicose Veins Compared to Existing Endovenous Techniques: A Systematic Review of the Literature. Surg J (N Y). 2020; 6(2): 77-86. doi: 10.1055/s-0040-1708866.
- Pappas JN, Pappas PJ, Lakhanpal S, Kennedy R, Soto T. Natural history and role of anticoagulation in the management of endovenous glue-induced thrombus. J Vasc Surg Venous Lymphat Disord. 2023; 11(5): 938-945. doi:.1016/j.jvsv.2023.03.021.
- Cho S, Gibson K, Lee SH, Kim SY, Joh JH. Incidence, classification, and risk factors of endovenous glue-induced thrombosis after cyanoacrylate closure of the incompetent saphenous vein. J Vasc Surg Venous Lymphat Disord. 2020; 8(6): 991-998. doi: 10.1016/j. jvsv.2020.01.009.
- Sermsathanasawadi N, Pruekprasert K, Prapassaro T, et al. Thrombus extension after cyanoacrylate closure of incompetent saphenous veins. Int Angiol. 2022; 41(2): 143-148. doi: 10.23736/S0392-9590.22.04768-X.
- Lane TR, Kelleher D, Moore HM, Franklin IJ, Davies AH. Cyanoacrylate glue for the treatment of great saphenous vein incompetence in the anticoagulated patient. J Vasc Surg Venous Lymphat Disord. 2013; 1(3): 298-300. doi: 10.1016/j.jvsv.2012.09.007.


