Ремоделирование компонентов аэрогематического барьера легких в условиях высокогорья
Автор: Матвиенко Виктор Васильевич, Абдумаликова Инобат Абдусаттаровна, Шидаков Юсуф Хаджи-Махмудович, Маргарян Артур Ванушович, Захарчук Ольга Викторовна, Истомина Ольга Фридриховна, Шидин Владимир Александрович, Тулекеев Тохтогазы Иманалиевич
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Биологические науки
Статья в выпуске: 1, 2023 года.
Бесплатный доступ
Цель. Изучить структурные и ультраструктурные изменения на уровне аэрогематического барьера (АГБ) у крыс в разные сроки адаптации к высокогорной гипоксии. Материалы и методы. Эксперименты проведены на 60 половозрелых беспородных лабораторных крысах-самцах массой 140-160 г в условиях высокогорья (3200 м над ур. м.). Использованы гистологический метод окраски гематоксилин-эозином по Майеру, трансмиссионная и растровая электронная микроскопия на 7, 15 и 30-е сут пребывания животных в горах. Статистическая обработка материала проведена с помощью прикладных программ Statistica 6.0 (США) и StatTech v. 2.8.4 (Россия) с использованием критерия достоверности Стьюдента. Различия считали статистически значимыми при p
Высокогорная гипоксия, сурфактант, аэрогематический барьер, межальвеолярная перегородка, базальная мембрана
Короткий адрес: https://sciup.org/14127216
IDR: 14127216 | УДК: 611.24-911.7 | DOI: 10.34014/2227-1848-2023-1-114-124
Remodeling of the aero-hematic lung barrier components under high altitudes
The aim of the study is to examine structural and ultrastructural aero-hematic barrier (AHB) changes in rats during adaptation to high-altitude hypoxia. Materials and Methods. The experiments were carried out on 60 sexually mature outbred laboratory male rats weighing 140-160 g at high altitude (3200 m above sea level). The authors followed Mayer's hematoxylin and eosin staining protocol, and used transmission and scanning electron microscopy on the 7th, 15th and 30th days of the animals' life in the mountains. Statistical data processing was carried out using Statistica 6.0 (USA) and StatTech v. 2.8.4 (Russia) and Student's t-test. Differences were considered statistically significant at p
Текст научной статьи Ремоделирование компонентов аэрогематического барьера легких в условиях высокогорья
Введение. Ключевым фактором, оказывающим влияние на организм в течение всего периода пребывания человека и животных в высокогорье, является гипоксия, действующая на организм в комплексе с другими составляющими высокогорной среды обитания [1–3]. В процессе адаптации к условиям высокогорья на фоне гипоксии важную роль играет респираторный отдел легких [4, 5]. Вследствие это- го вполне обоснован интерес к морфологическому и морфометрическому изучению органов дыхания на горных высотах, особенно роли аэрогематического барьера (АГБ) легких и неразрывному единству дыхания, кровообращения и нейрогуморального регулирования обеспечения организма кислородом [6, 7].
Результаты исследования АГБ в условиях экспериментальных моделей гипоксии далеки от оригинальных данных, полученных в высокогорье. Экспериментальные данные порой несопоставимы с методами исследования, что не дает возможности составить единое представление о механизмах реакции АГБ на отдельные виды гипоксии [8–10]. При этом особого внимания заслуживает исследование характера этих реакций и структурных изменений АГБ в зависимости от длительности гипоксического воздействия [11, 12].
Цель исследования. Изучить структурные и ультраструктурные изменения в легких на уровне аэрогематического барьера у крыс в разные сроки адаптации к высокогорью.
Материалы и методы. Эксперименты проведены на половозрелых беспородных лабораторных крысах-самцах массой 140–160 г. Первая группа животных (20 крыс) – контрольная, вторая (60 крыс) – опытная. Вторая группа животных была транспортирована на высокогорную базу пер. Туя-Ашу (3200 м над ур. м.). Животные содержались в клетках по 20 крыс в условиях вивария при температуре 21–22 °С. Содержание животных и эвтаназия были реализованы в соответствии с принципами биоэтики, изложенными в Международных рекомендациях по проведению медико-биологических исследований с использованием животных (Хельсинки, 1985). Эксперименты на животных проведены в соответствии с принципами, изложенными в Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других целей (Страсбург, 1986), и Приказе Минздрава России № 199 от 01.04.2016 «Об утверждении правил надлежащей лабораторной практики».
На 7, 15 и 30-е сут адаптации к условиям высокогорья под общим внутрибрюшинным наркозом Thiopentalum-natrium животных выводили из эксперимента, извлекали кусочки легких и фиксировали в 10 % растворе нейтрального формалина на фосфатном буфере (рН 7,2). Далее проводили по спиртам возрастающей концентрации (50, 70, 80, 90, 96, 100 %), заливали в парафин и приготовляли срезы толщиной 7–8 мкм на микротоме «Биолам». Срезы окрашивали по общепринятой методике гематоксилин-эозином по Майеру и по Ван-Гизону и заключали в канадский баль- зам под покровным стеклом. Для проведения обзорной световой микроскопии и морфометрического исследования производили микрофотосъемку случайных полей зрения гистологических препаратов цифровой камерой OLYMPUS XC30 на базе микроскопа OLYMPUS СX41 (Япония) при увеличении окуляра SWH ×10 и объектива UPLanFL ×40 (не менее 10 полей зрения в каждом гистологическом срезе). Для морфометрического анализа данных использовали компьютерные программы анализа изображений Image Scope Color и OLYMPUS Сell Sens (Япония). Статистическую обработку полученных данных проводили c использованием пакета прикладных программ Statistica 6.0 (США).
Для электронно-микроскопического изучения структуры клетки кусочки легочной ткани 1×1 мм фиксировали в 2,5 % растворе глутарового альдегида, дофиксировали в 1 % растворе четырехокиси осмия, контрастировали в 1 % растворе уранилацетата и цитрата свинца по Рейнолдсу, заливали в эпоновые смеси из аралдитов 964 и 812. Электронномикроскопические исследования биопрепаратов легочной ткани проводили в Тюменском научном центре Сибирского отделения Российской академии наук. Ультратонкие срезы толщиной 250 нм готовили на ультрамикротоме LEICA EM UC7 (США). Микрофотосъемку производили на трансмиссионном электронном микроскопе JEM-1011 (Япония). Для сканирующей электронной микроскопии готовили сколы легочной ткани в жидком азоте и напыляли коллоидным золотом в вакуумной установке HI CUDE (ФРГ). Объекты изучали под растровым микроскопом HITACI (Япония). Статистическую обработку осуществляли с помощью пакета МS Excel 2007 и пакета прикладных программ Statistica 6.0 с использованием критерия достоверности Стьюдента. Различия считали статистически значимыми при p<0,05.
Результаты и обсуждение. В табл. 1 отражены сведения о количественных изменениях толщины цитоплазматических отростков (ЦО) альвеолоцитов 1-го типа (А I типа), эн-дотелиоцитов, базальных мембран (БМ), суммарной толщины АГБ и межальвеолярных перегородок (МАП).
Таблица 1
Table 1
Морфометрия основных компонентов АГБ в процессе адаптации к условиям высокогорья, мкм, М±m
Morphometry of basic AHB components during high-altitude adaptation, mkm, М±m
|
Параметр Parameter |
Контроль Control |
Сроки эксперимента, сут Experiment duration, days |
||
|
7-е |
15-е |
30-е |
||
|
Толщина ЦО А I типа Thickness of A cytoplasmic processes, Type I |
0,16±0,04 |
0,17±0,006 |
0,26±0,007˟* |
0,18±0,003* |
|
Толщина ЦО эндотелиоцита Thickness of endotheliocyte cytoplasmic processes |
0,19±0,007 |
0,24±0,01˟ |
0,08±0,003˟* |
0,07±0,002˟* |
|
Базальные мембраны Basal membranes |
0,07±0,003 |
0,06±0,003 |
0,10±0,004˟* |
0,06±0,004˟* |
|
Суммарная толщина АГБ Total AHB thickness |
0,42±0,05 |
0,47±0,019 |
0,44±0,014 |
0,31±0,009˟* |
|
Толщина МАП IAS thickness |
3,74±0,06 |
4,30±0,07˟ |
4,28±0,03˟ |
4,76±0,09˟* |
Примечание. Различия достоверны (р<0,05) по сравнению с: ˟ – контролем, * – предыдущим сроком.
Note. AHB – aero-hematic barrier, IAS – interalveolar septum; ˟ – the differences are significant compared to the control (p<0.05); * – the differences are significant compared to the previous term (p<0.05).
Из табл. 1 видно, что толщина ЦО А I типа, эндотелиоцитов, БМ и АГБ достигает максимальных значений в аварийной стадии (7-е сут) адаптации животных в высокогорье. В стабильной фазе адаптации (30-е сут) показатели снижаются по сравнению не только с аварийной фазой, но и с данными контроля. Толщина МАП нарастает независимо от фазы адаптации животных в высокогорье. Следовательно, изменения компонентов АГБ и МАП в
процессе адаптации к высокогорью не совпадают по времени.
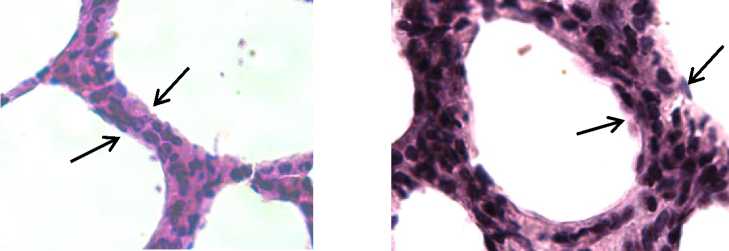
На 7-е сут адаптации за счет гипертрофии и гиперплазии пневмоцитов I–II типов происходит утолщение МАП. Одновременно в отдельных альвеолах отмечаются явления интерстициального отека стенок с поступлением транссудата в их просвет (рис. 1а, б) и образованием «кровяных рек» [13] (рис. 2а, б).
а б
Рис. 1. Межальвеолярная перегородка (черные стрелки): а) контроль, б) на 7-е сут пребывания животных в высокогорье. Утолщение МАП. Окраска гематоксилин-эозином по Майеру. Об. ×40, ок. ×10
Fig. 1. Interalveolar septum (black arrows). a – control, b – Day 7 of animals' life in the highlands. Thickening of the interalveolar septum. Mayer's hematoxylin and eosin staining protocol. Lens ×40, ocular ×10
а
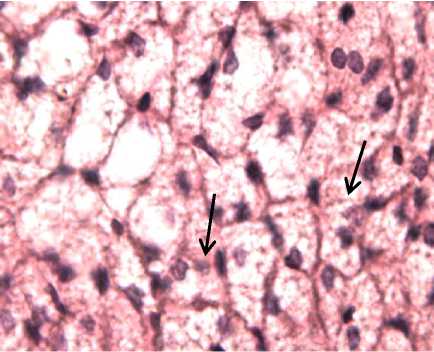
Рис. 2. а) Транссудат в просвете альвеолы (черные стрелки). Окраска гематоксилин-эозином по Майеру. Об. ×40, ок. ×10; б) многорядное расположение эритроцитов в просвете сосуда (белые стрелки). Сканирующая электронная микроскопия на 7-е сут адаптации животных к условиям высокогорья.
СЭМ ×12 000
б
Fig. 2. a) Transudate in the alveoli lumen (black arrows). Mayer's hematoxylin and eosin staining protocol. Lens ×40, ocular ×10; b) multi-row red blood cell arrangement in the vessel lumen (white arrows). Scanning electron microscopy, Day 7 of animals’ adaptation to high-altitudes. SEM ×12 000
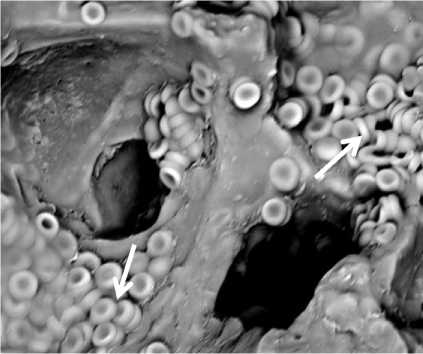
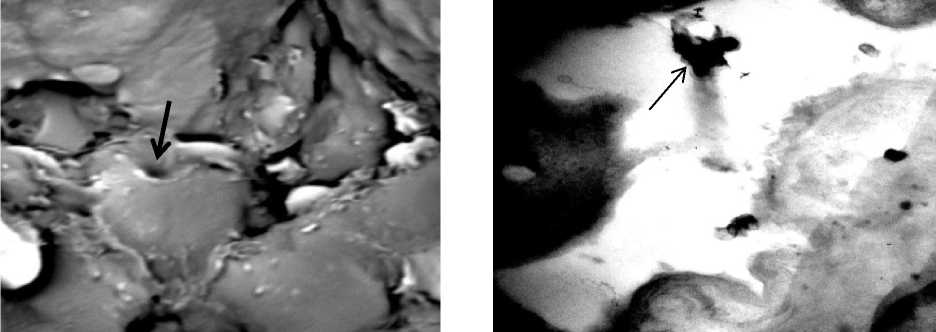
В аварийной фазе адаптации (7-е сут) на электроннограмме отражается разрушение аль-веолоцитов II типа по апокриновому способу
с выходом осмиофильных пластинчатых телец (ОПТ) в просвет альвеол (рис. 3а, б).
б
Рис. 3. а) Альвеолоцит II типа на 7-е сут адаптации к высокогорью. Разрушение клетки по апокриновому способу. СЭМ ×12 000;
б) выход осмиофильных пластинчатых телец в просвет альвеолы (черные стрелки). ТЭМ ×25 000
Fig. 3. a) Type II alveolocyte, Day 7 of adaptation to high-altitudes. Apocrine secretion. SEM ×12 000; b) output of osmiophilic lamellar bodies into alveoli lumen (black arrows). TEM ×25 000
В цитоплазме альвеолоцитов II типа снижается количество молодых осмиофильных пластинчатых и ламеллярных телец с фосфолипидами, что свидетельствует о нарушении
(дистрофии) легочного эпителия [14]. Цистерны гранулярной эндоплазматической сети расширяются, лишаются части рибосом.
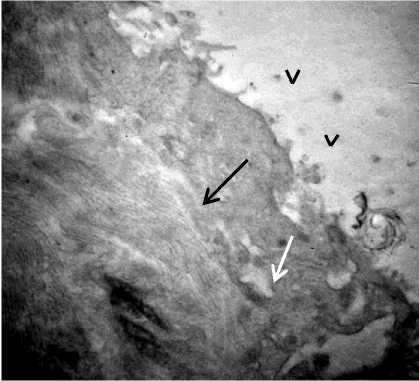
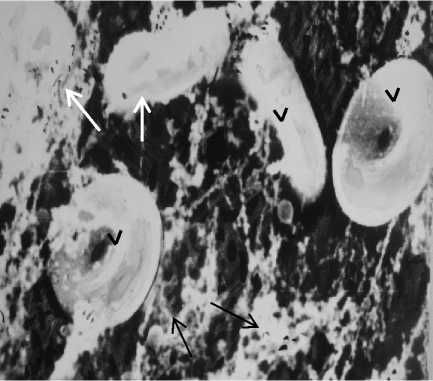
Рис. 4. а) Альвеолоцит II типа на 7-е сут адаптации к высокогорью.
В цитоплазме – расширенная зернистая эндоплазматическая сеть (черная стрелка), мультвезикулярные тельца (белая стрелка), комплекс Гольджи, в просвете альвеолы - микроворсинки ( V ). ТЭМ x25 000;
б) альвеола на 7-е сут адаптации. Видны нитевидные структуры сурфактанта (черная стрелка), макрофаги (белые стрелки) и эритроциты в просвете альвеол ( V ). СЭМ x20 000
б
Fig. 4. a) Type 2 alveolocyte, Day 7 of adaptations to high-altitudes.
In the cytoplasm; expanded granular endoplasmic reticulum (black arrow), multvesicular corpuscles (white arrow), Golgi complex, in the alveoli lumen: microvilli ( V ). TEM x25 000; b) alveolus, Day 7 of adaptation. Surfactant threadlike structure (black arrow), macrophages (white arrows) and erythrocytes are visible in the alveoli lumen ( V ). SEM x20 000
Отдельные альвеолоциты II типа находятся в состоянии повышенной секреторной активности, другие теряют сурфактант за счет выхода ОПТ, встречаются одиночные эритроциты и макрофаги в просвете альвеол (рис. 4а, б).
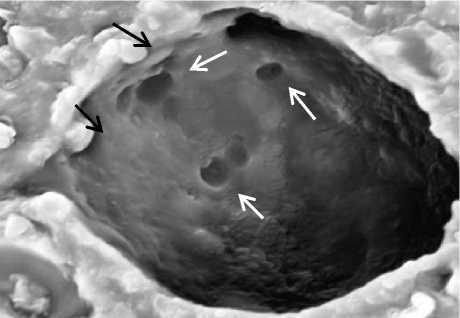
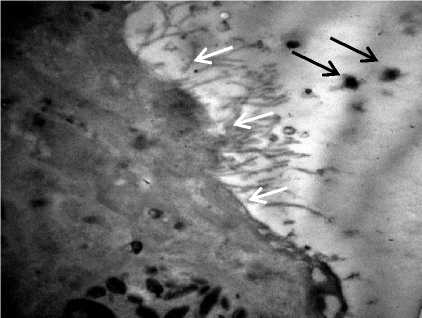
В более поздние сроки пребывания животных в высокогорье в стенке МАП отмечается выбухание альвеолоцитов II типа с многочисленными «отверстиями» – порами Кона (рис. 5а). Апикальная поверхность пневмоци-тов I типа содержит многочисленные цитоплазматические отростки различной длины. В просвете альвеол – разрушенные остатки сурфактанта (рис. 5б).
В контексте проводимого исследования можно выделить факторы взаимодействия: вдыхаемый воздух – легкие – сердце и бронхиальное дерево – кровеносные сосуды – аэрогемати-ческий барьер. Развивается прекапиллярная легочная гипертензия, отражающаяся на функции АГБ, заключающейся в обеспечении нутриентами клеточной популяции МАП [15, 16].
Таким образом, в аварийной фазе (7-е сут) адаптации к высокогорью цитоплазматиче-
ские отростки эндотелиоцитов имеют тенденцию к утолщению, их нутритивная и газообменная функции нарушаются. В стабильной фазе адаптации формируются приспособительные структуры в виде артериол замыкающего типа, артериоло-венулярных анастомозов, регулирующих артериальное давление, наблюдаются дилатация микрососудов в МАП, истончение ЦО эндотелиоцитов по сравнению с контролем (табл. 1).
Мелкие ветви и артериолы легочной артерии в аварийной фазе адаптации к высокогорью повышают сопротивление току крови, при этом наполнение альвеол воздухом с низким парциальным давлением кислорода снижается. Так как строма с залегающими в ней терминальными бронхиолами представлена главным образом ретикулярными и частично коллагеновыми волокнами, менее влияющими на респираторный отдел легких, МАП и ЦО А I типа утолщаются. В этой ситуации нарастает гиперфункция и пролиферация аль-веолоцитов II типа, продуцирующих поверхностно-активные вещества. Структурным суб-
стратом гиперфункции альвеолоцитов II типа выступает снижение числа молодых ОПТ, расширение зернистой эндоплазматической сети, что отражает компенсаторно-приспособительные реакции в ответ на гипоксию. В от-
дельных альвеолах отмечаются зернистая дистрофия эпителия, нарушающая мукоцилиарный транспорт, активация сурфактантной системы легких с последующим развитием респираторного дистресс-синдрома.
а
Рис. 5. а) Межальвеолярная перегородка на 15–30-е сут.
В стенке перегородки – выбухание альвеолоцитов II типа в просвет альвеолы (черные стрелки), многочисленные поры Кона (белые стрелки). СЭМ ×20 000; б) альвеолоцит I типа на 15–30-е сут. Цитоплазматические отростки различной длины с утолщением (белые стрелки).
В просвете альвеол – разрушенный сурфактант (черные стрелки). ТЭМ ×30 000
б
Fig. 5. а) Interalveolar septum, Day 15–30.
In the septum wall: bulging of type II alveolocytes into the alveoli lumen (black arrows), numerous pores of Kohn (white arrows). SEM ×20 000; b) type I alveolocyte, Day 15–30. Cytoplasmic processes of various lengths and thickness (white arrows).
In the alveoli lumen: destroyed surfactant (black arrows) TEM ×30 000
В последующие сроки адаптации к высокогорью толщина ЦО А I типа не отличается от толщины ЦО эндотелиоцитов, БМ и АГБ, при этом толщина МАП превышает контрольные данные. В стенке альвеол увеличивается количество фибробластов, что в условиях гипоксии приводит к расширению и увеличению количества пор Кона, обеспечивая коллатеральное дыхание [2].
Структурные основы адаптации и компенсации изменений функционирования легких в высокогорье охватывают богатый клеточный состав МАП. В альвеолоцитах I типа нарастает внутриклеточная регенерация, аль-веолоциты II типа не только активно секретируют, но и пролиферируют совместно с эндо-телиоцитами и альвеолярными макрофагами. В эти сроки активизируется сурфактантная система за счет клеточной популяции, продуцирующей поверхностно-активное вещество
альвеолоцитами II типа, клетками Клара и альвеолярными макрофагами [17, 18].
Заключение. В результате проведенных исследований установлено, что в ранние сроки адаптации животных к условиям высокогорья отмечается выраженное увеличение основных компонентов АГБ легких (толщины МАП, БМ, ЦО А I типа и эндотелиоцитов капилляров). В просвете альвеол наблюдаются явления транссудата, локальные разрушения альвеоло-цитов II типа в апикальной части по апокриновому способу, вымывание мембран сурфактанта, скопление эритроцитов в стенке альвеол. Активность сурфактантной системы в этот период заключается в гиперплазии и увеличении объема ОПТ, появлении мультвезикулярных пластинчатых телец в цитоплазме альвеолоци-тов II типа и альвеолярных макрофагов, участвующих в поглощении избыточного сурфактанта. В более поздние сроки пребывания жи-
вотных в высокогорье морфометрические показатели АГБ приближаются к конт-рольным величинам, кроме толщины МАП (табл. 1). Активность сурфактантной системы в эти сроки снижается за счет уменьшения выброса ОПТ структур сурфактанта. В стенке альвеол увеличивается количество фибробластов, что в условиях гипоксии приводит к расширению и увеличению количества пор Кона, обеспечивая коллатеральное дыхание [2].
Таким образом, изучение компонентов АГБ у экспериментальных животных (крыс) в разные сроки высокогорной адаптации выявило дистрофические процессы АГБ в МАП, компенсируемые за счет альвеолоцитов I типа, пролиферации альвеолоцитов II типа, что подтверждает адаптивные механизмы ультра-структурной перестройки всех звеньев эпителиального и эндотелиального компонентов легочных альвеол.
Список литературы Ремоделирование компонентов аэрогематического барьера легких в условиях высокогорья
- Айдаралиев A.A., Арабаева А.И., Шатманова Э.К. Устойчивое развитие горных регионов Кыргызстана. Здравоохранение Кыргызстана. 2021; 1: 3-12.
- Шидаков Ю.Х.-М., Балыкин М.В., Каркобатов Х.Д. Горная микроангиология. Бишкек; 2019. 172.
- Матвиенко В.В., Тулекеев Т.М., Матвиенко О.В., ШведскийМ.С. Морфофункциональные изменения сосудистого русла легких в условиях высокогорья. Вестник физической культуры и спорта. Бишкек. 2019; 2: 99-102.
- Иванов К.П. Современные медицинские проблемы микроциркуляции и гипоксического синдрома. Вестник РАМН. 2014; 1-2: 57-63.
- Белов Г.В. Сурфактантная система легких в условиях горного климата. Медицина Кыргызстана. 2014; 5: 19-23.
- Брилль Г.Е., Чеснокова Н.П., Понукалина Е.В. Механизмы компенсации и адаптации к гипоксии. Научное обозрение. Медицинские науки. 2017; 2: 55-57.
- Низамутдинова Р.Р. Влияние неблагоприятных факторов окружающей среды на сурфактантную систему легких и возможности ее спонтанного восстановления. Вестник новых медицинских технологий. 2008; 1: 133-136.
- Lopez-Rodriguez E. Structure-function rela-tionships in pulmonary surfactant membranes: from biophysics to therapy. Biochim. Biophys. Acta. 2014; 6 (6): 1568-1585.
- NematovaR.I. The Introduction of the Laryngeal Mask Airway for Surfactant Administration in Neonates with Respiratory Distress in Azerbaijan. Eurasian Journal of Clinical Sciences. 2019; 1 (1): 63-67.
- Шидаков Ю.Х.-М., Абдумаликова И.А., Матвиенко В.В. Ультраструктурные изменения микроцир-куляторного русла и паренхимы легких при физических нагрузках в условиях высокогорья. Вестник КРСУ. 2016; 7: 191-193.
- Шахбанов Р.К., Асадулаева М.Н., Алиева С.Н., Алимханова А.А. Развитие и функциональное значение системы легочного сурфактанта. Вестник Российского университета дружбы народов. Медицина. 2021; 4: 321-331.
- GhoshM.C. Insulin-like growth factor-I stimulates differentiation of ATII cells to ATI-like cells through activation of Wnta. Am J Physiol Lung Cell Mol. Physiol. 2013; 5 (5): 222-228.
- Gazdhar A. Targeted gene transfer of hepatocyte growth factor to alveolar type II epithelial cells reduces lung fibrosis in rats. Hum Gene Ther. 2013; 24 (24): 105-116.
- Полищук В.В. Функции и действие сурфактанта. Барнаул: Алтайский государственный университет; 2022: 665-666.
- Матвиенко В.В., Шведский М.С., Вагина Д.А. Влияние гипоксии на сурфактантную систему легких. Медико-физиологические проблемы экологии человека. Ульяновск: УлГУ; 2021: 224-226.
- Bouzas V., Haller T., Hobi N., Felder E., Pastoriza-Santos I., Pérez-Gil J. Nontoxic impact of PEG-coated gold nanospheres on functional pulmonary surfactant-secreting alveolar type II cells. Nanotoxicology. 2014: 813.
- CrystalR.G., RandellS. Y., Engelhardt J.F. Airway epithelial cells current concepts and challenges. Proc. Amer. Thorac. Soc. 2008; 5 (5): 772-776.
- Сапаров К.А., Нурмухан Г.С., Султанова А.Ж. Морфологические аспекты респираторного отдела легких при долговременной гипоксической гипоксии. Международный журнал прикладных и фундаментальных исследований. 2015; 12: 677-780


