Репешок аптечный – перспективный сырьевой растительный источник гепатопротекторов
Автор: Васякина Ксения Александровна, Куркина Анна Владимировна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биологические ресурсы: флора
Статья в выпуске: 1-9 т.14, 2012 года.
Бесплатный доступ
Проведено сравнительное изучение содержания флавоноидов в различных образцах травы репешка аптечного (европейского) ( Agrimonia eupatoria L.) с использованием тонкослойной хроматографии и спектрофотометрии. Определено, что преобладающими флавоноидами травы репешка аптечного является изокверцитрин и рутин. Содержание суммы флавоноидов в образцах из различных регионов РФ варьируется в пределах 0,91%-1,32%.
Репешок аптечный (европейский), трава, флавоноиды, гепатопротекторы, лекарственные средства, стандартизация, спектрофотометрия
Короткий адрес: https://sciup.org/148201028
IDR: 148201028 | УДК: 615.32:
Agrimonia eupatoria L. – the perspective raw vegetative source of hepatoprotectors
Comparative studying of flavonoids content in various species of Agrimonia eupatoria L. herbs with thin-layer chromatography and spectophotometery use is made. It is defined that prevailing flavonoids in Agrimonia eupatoria L. herbs is isoquercitrin and rutinum. The maintenance of flavonoids sum in species from various regions of Russian Federation varies within 0,91%-1,32%.
Текст научной статьи Репешок аптечный – перспективный сырьевой растительный источник гепатопротекторов
Флавоноиды как биологически активные соединения обладают широким спектром фармакологического действия и являются уникальным источником желчегонных, гепатопротекторных и антиоксидантных лекарственных средств. Флавоноиды в качестве антиоксидантов играют важную роль в предупреждении нарушений структуры и функции печени при различных патологических состояниях, ускорении регенерации и восстановлении функциональной активности гепатоцитов. Необходимость использования флавоноидов в качестве гепатопротекторов доказана современными исследованиями [3, 4]. Таким образом, лекарственные средства (ЛС) на основе флавоноидов являются перспективными препаратами в комплексной терапии заболеваний гепатобилиарной системы [1, 3, 5].
Одним из перспективных источников желчегонного и гепатопротекторного действия является лекарственное растительное сырье (ЛРС) — трава репешка аптечного (европейского) ( Agrimonia eupatoria L., семейство Розоцветные - Rosaceae ). Репешок аптечный широко применяется в народной медицине при лечении заболеваний печени и желчевыводящих путей, при злокачественных новообразованиях и является перспективным источником желчегонных фитопрепаратов [3, 6, 7]. Однако недостаточная степень изученности химического состава репешка аптечного с точки зрения объяснения многообразия фармакологических свойств препятствует внедрению этого популярного растения в научную медицину. В литературе имеются данные о наличии в надземной части репешка аптечного различных полифенольных веществ, среди которых наибольший интерес представляют флавоноиды, гидроксикоричные кислоты и дубильные вещества [2, 3, 6, 7]. На наш взгляд, одной из потенциальных групп биологически
активных соединений в надземной части репешка аптечного являются флавоноиды, по содержанию которых целесообразно оценивать качество сырья данного растения. По разным литературным источникам [2, 6, 7], флавоноиды репешка аптечного представлены кверцетрином, кемпферолом, лю-теолином, апигенином и их гликозидами.
В настоящее время актуальным вопросом является внедрение природоохранных мероприятий, позволяющих оптимизировать подходы к заготовке ЛРС и созданию фитопрепаратов. Совершенствования методов стандартизации может быть основано только на глубоком изучении химического состава лекарственных растений и фитопрепаратов на их основе.
Цель исследований: разработка методик качественного и количественного анализа травы репешка аптечного в рамках научного обоснования рационального использования растительных ресурсов.
Материалы и методы. В данной работе была исследована трава репешка аптечного (Agrimonia eupatoria L.), собранная в различных регионах РФ: Самарской области, Ульяновской области, Пензенской области, Республики Татарстан, Ставропольского края. Кроме этого, были исследованы также индивидуальные соединения, выделенные из данного ЛРС. Колоночную хроматографию осуществляли с использованием силикагеля L 40/100, полиамида («Woelm»), сефадекса LH-20 (Швеция) и оксида алюминия (II степени активности по Брокману). В качестве элюентных смесей служили смеси воды и этилового спирта, хлороформа и этилового спирта, а также гексана и хлороформа в градиентном режиме (с увеличением степени полярности). 1Н-ЯМР-спектры получали на приборах «Bruker AM 300» (300 МГц), масс-спектры снимали на масс-спектрометре «Kratos MS-30», регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena). Тонкослойную хроматографию (ТСХ) проводили на пластинках «Silufol UV 254» (Чехия) и «Сорбфил ПТСХ-АФ-А-УФ» (Россия) с использованием различных систем растворителей: хлороформ-этанол-вода (26: 16: 3), н-бутанол-ледяная уксусная кислота-вода (4:1:2). Для проявления веществ использовали детекцию в УФ-свете при длине волны 254 и 366 нм, а также обработку хроматограмм растворами диазобензолсульфокислоты (фенольные соединения).
Результаты и обсуждение. По визуальной оценке из хроматограммы видно, что в траве репешка аптечного преобладают два флавоноида, которые нами идентифицированы как изоквер-цетрин (R f =0,54) и рутин (R f =0,47), при этом допускается наличие пятен других действующих веществ (рис. 1).
алюминия хлорида имеет максимум поглощения при 412 нм, в том числе в дифференциальном варианте (рис. 4 и 5). Следовательно, рутин, близкий по своим спектральным характеристикам к флавоноидам травы репешка аптечного, может быть использован в методике анализа в качестве ГСО. Также учитывая доступность рутина и широкое применение данного стандарта в фармацевтическом анализе, считаем целесообразным его использование для целей стандартизации сырья исследуемого растения.
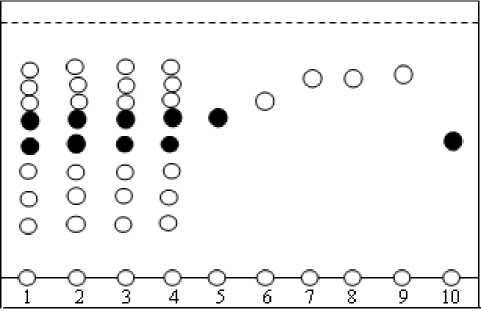
Рис. 1. Хроматографический профиль водноспиртовых извлечений из травы репешка аптечного и некоторых флавоноидов:
1 - Самарская область, с. Царевщина; 2 - Самарская обалсть, пос. Волжский; 3 - Республика Татарстан, с. Соболеново; 4 - Ульяновская область, Радищевский район, близ с. Софьино; 5 - цинарозид; 6 - изокверцитрин; 7 - кверци-тин; 8 - кемпферол; 9 - лютеолин; 10 - рутин
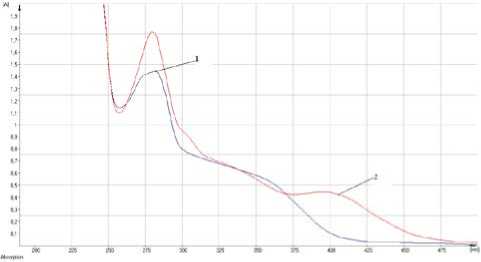
Рис. 2. УФ-спектры растворов водно-спиртового извлечения из травы репешка аптечного: 1 - раствор извлечения из травы репешка аптечного; 2 -раствор извлечения из травы репешка аптечного с добавлением алюминия хлорида
В ходе изучения спектральных характеристик проведено обоснование целесообразности использования метода спектрофотометрии для определения подлинности травы репешка аптечного и количественного определения суммы флавоноидов. Определено, что характер кривой поглощения раствора водно-спиртовых извлечений из травы репешка аптечного обусловлен в основном флавоноидами (рис. 2) [6]. При разработке методики количественного определения суммы флавоноидов использовали реакцию комплексообразования с раствором алюминия хлорида для исключения вклада в значение оптической плотности других групп соединений, в том числе характерных для данного растения гидроксикоричных кислот, имеющих, как правило, основной максимум поглощения в области 326-330 нм [7]. В условиях комплексообразования наблюдается батохромный сдвиг длинноволновой полосы флавоноидов, в частности, флавонов и флавонолов [8], который обнаруживается в УФ-спектре в виде максимума поглощения в области 400-412 нм (рис. 2), что находит подтверждение в условиях дифференциальной спектрофотометрии (рис. 3).
Изучение УФ-спектров ГСО рутина показало, что раствор данного стандарта в присутствии
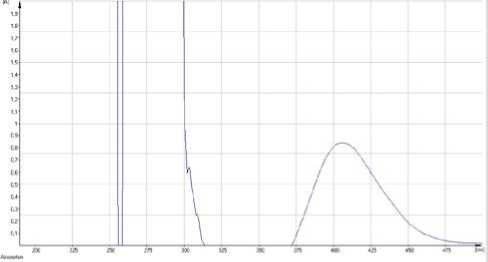
Рис. 3. УФ-спектр раствора водно-спиртового извлечения из травы репешка аптечного (дифференциальный спектр)
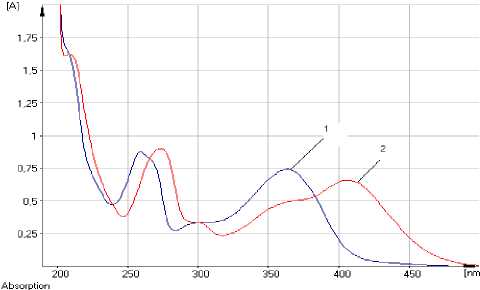
Рис. 4. УФ-спектр спиртового раствора ГСО рутина: 1 - раствор ГСО рутина; 2 - раствор ГСО рутина с добавлением алюминия хлорида
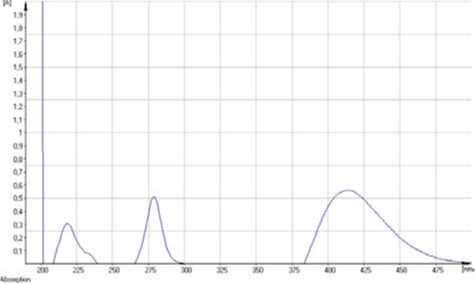
Рис. 5. УФ-спектр раствора ГСО рутина (дифференциальный спектр)
С использованием разработанной методики проанализирован ряд образцов травы репешка аптечного и показано (табл. 1), что содержание суммы флавоноидов в образцах сырья варьирует в пределах от 0,91% до 1,32% (в пересчете на рутин). На наш взгляд, дифференциальная спектрофотометрия позволяет минимизировать вклад сопутствующих веществ в оптическую плотность испытуемого раствора. Следовательно, внедрение данной методики, отвечающей параметрам валидации, позволит объективно оценивать качество сырья репешка аптечного.
Таблица 1. Содержание суммы флавоноидов в различных образцах травы репешка аптечного
|
Характеристика образца сырья |
Содержание суммы флавоноидов в пересчете на рутин (в %) |
|
Самарская область (с. Царевщина), 2009 г. |
1,25±0,03 |
|
Самарская область (пос. Волжский), 2009 г. |
0,91±0,02 |
|
Республик Татарстан (д. Соболеново), 2010 г. |
1,32±0,04 |
|
Ульяновская область, Радищевский район, с. Софьино, 2010 г. |
1,28±0,02 |
Выводы: были разработаны критерии подлинности травы репешка аптечного и определены преобладающие флавоноиды (изокверцетрин и рутин). С учётом того, что трава репешка аптечного широко распространена на территории РФ, в том числе в Самарской области, трава данного растения является перспективным сырьевым растительным источником гепатопротекторов.
Список литературы Репешок аптечный – перспективный сырьевой растительный источник гепатопротекторов
- Гаммерман, А.Ф. Лекарственные растения/А.Ф. Гаммерман, И.Д. Юриевич -Минск: Наука и техника, 1995. 380 с.
- Дрозд, Г.А. Фитохимическое исследование Agrimonia eupatoria/Г.А. Дрозд, С.Ф. Явланская, Т.М. Иноземцева//Химия природных соединений. 1983. № 1. С. 106.
- Егоров, В.А. Гепатопротекторные и иммунотропные лекарственные средства: состояние и перспективы фармацевтического рынка/В.А. Егоров, Л.В. Мошкова, В.А. Куркин, И.К. Петрухина//Монография. -Самара: СамГМУ, 2000. 120 с.
- Куркин, В.А. Основы фитотерапии: Учебное пособие для студентов фармацевтических вузов. -Самара: ООО «Офорт», ГОУ ВПО «СамГМУ Росздрава», 2009. 963 с.
- Куркина, А.В. Фитохимическое исследование сырья и препаратов бессмертника песчаного//Специальный выпуск Известия Самарского научного центра Российской академии наук. 2007. Том 2. С. 177-182.
- Куркина, А.В. Методика количественного определения суммы флавоноидов в траве репешка аптечного//Химико-фармацевтический журнал. 2011. Т. 45. № 1. С. 31-34.
- Растительные ресурсы СССР: Цветковые растения, их химический состав, использование; Семейство Hydrangeaceae -Haloragaceae. -СПб.: Наука, 1987. 326 с.
- Mabry, T.J. The Systematic Identification of Flavonoids./T.J. Mabry, K.R. Markham, M.B. Thomas. -Berlin; Heidelberg; New York, 1970. 354 c.


