Репродуктивные биомаркеры коров - современное состояние исследований и перспективы (обзор)
Автор: Чинаров Р.Ю.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Обзоры, проблемы
Статья в выпуске: 4 т.60, 2025 года.
Бесплатный доступ
Продукция эмбрионов in vitro (IVP-эмбрионы) с использованием ооцитов, извлекаемых посредством аспирации овариальных фолликулов (OPU), - традиционная на сегодняшний день практика в племенном разведении крупного рогатого скота (КРС) (Р.Ю. Чинаров с соавт., 2023; L.B. Ferré с соавт., 2023). Несмотря на существенные успехи, достигнутые в этой области, стоит задача повышения числа пригодных для трансплантации эмбрионов, получаемых за один сеанс OPU, поскольку это напрямую влияет на экономическую эффективность программ трансплантации эмбрионов. Принимая во внимание непосредственное участие в регуляции репродуктивных функций самок половых гормонов, их содержание в крови рассматривается в качестве потенциальных предикторов результативности технологии OPU/IVP (Р.Ю. Чинаров, 2024). Цель настоящего обзора - анализ современного состояния и результатов исследований ассоциаций между содержанием в крови половых гормонов разных классов и эффективностью вспомогательных репродуктивных технологий для определения потенциальных предикторов повышения результативности технологии OPU/IVP у крупного рогатого скота. В исследованиях, проведенных на различных породах европейского (Bos taurus) и зебувидного (Bos indicus) КРС, выявлены связи содержания в фолликулярной жидкости и/или крови прогестерона, эстрадиола-17β, фолликулостимулирующего гормона (ФСГ) и антимюллерова гормона (АМГ) с результативностью OPU. Более высокие концентрации прогестерона в сыворотке крови коров породы Сахивал (Sahiwal) были ассоциированы с более высоким числом фолликулов, пригодных для аспирации (nФ), общим числом извлекаемых ооцит-кумулюсных комплексов (ОКК) и числом жизнеспособных ОКК (M. Nawaz с соавт., 2022). Помеси Bos taurus × Bos indicus , имеющие средние концентрации прогестерона в сыворотке крови, характеризовались более высокой долей развития бластоцист (%БЛ) (L.F.M. Pfeifer с соавт., 2009). Более высокие концентрации эстрадиола-17β в фолликулярной жидкости были ассоциированы с более высокими значениями nФ у помесных мясных телок (F. Mossa с соавт., 2010) и нестельных коров голштинской породы (K. Sakaguchi с соавт., 2019), а также более высоким значением %БЛ у телок-доноров голштинской породы (N. Araki с соавт., 1998). Более высокие значения показателя %БЛ достигались у телок-доноров истобенской породы, имеющих более высокие значения отношения концентрации эстрадиола-17β в сыворотке крови к числу ОКК (Р.Ю. Чинаров с соавт., 2025). Установлены обратные зависимости концентрации ФСГ в сыворотке или плазме крови со значениями nФ у телок и нестельных коров голштинской породы (J.M. Haughian с соавт., 2004; K. Sakaguchi с соавт., 2019), у не лактирующих молочных коров (F. Mossa с соавт., 2010), у телок и лактирующих коров мясного КРС (J.J. Ireland с соавт., 2007; J. Singh с соавт., 2004). Более высокие концентрации АМГ были ассоциированы с более высокими значениями nФ у телок - доноров эмбрионов голштинской породы (B.M. Guerreiro с соавт., 2014; A. Vernunft с соавт., 2015), у высокопродуктивных молочных коров (A.H. Souza с соавт., 2015), у лактирующих коров тагильской породы (Р.Ю. Чинаров с соавт., 2024), у мясного скота Ханву (N. Ghanem с соавт., 2016), японского черного скота (H. Hirayama с соавт., 2019), зебувидного скота породы Nelore (B.M. Guerreiro с соавт., 2014). Таким образом, результаты проведенного анализа показали наличие ряда ассоциаций половых гормонов с эффективностью вспомогательных репродуктивных технологий у различных пород крупного рогатого скота. В этой связи мониторинг концентрации половых гормонов в сыворотке крови самок может стать полезным инструментом отбора доноров для проведения OPU и прогнозирования эффективности получения IVP-эмбрионов у КРС. Целесообразны дальнейшие исследования ассоциаций половых гормонов с результативностью OPU/IVP на различных породах КРС с учетом возраста и физиологического состояния доноров, а также технологических режимов их использования.
Вспомогательные репродуктивные технологии, половые гормоны, аспирация фолликулов, получение эмбрионов in vitro
Короткий адрес: https://sciup.org/142246200
IDR: 142246200 | УДК: 636.018:57.089.3 | DOI: 10.15389/agrobiology.2025.4.581rus
Reproductive biomarkers of cows - current state of research and prospects (review)
Production of in vitro embryos (IVP-embryos) using oocytes retrieved by aspiration of ovarian follicles (OPU) is today a traditional practice in cattle breeding (R.Yu. Chinarov et al., 2023; L.B. Ferré et al., 2023). Despite the significant progress made in this area, the challenge is to increase the number of transferable embryos produced per OPU session, as this directly affects the efficiency of embryo transfer programs. Considering the direct impact of reproductive hormones in the regulation of reproductive functions of females, their contents in the blood is considered as potential predictors of the efficiency of OPU/IVP technology (R.Yu. Chinarov, 2024). The aim of this review is to analyze the current state and research results of the associations between blood content of reproductive hormones of different classes and the efficiency of assisted reproductive technologies to identify potential predictors for improvement of OPU/IVP technology in cattle. Studies conducted on various breeds of European (Bos taurus) and zebu (Bos indicus) cattle have revealed associations between the content of progesterone, estradiol-17β, follicle-stimulating hormone (FSH) and Anti-Mullerian hormone (AMH) in follicular fluid and/or in blood with the efficiency of OPU. Higher concentrations of progesterone in the blood serum of Sahiwal cows were associated with a higher number of follicles suitable for aspiration (nF), the total number of retrieved oocyte-cumulus complexes (OCCs) and the number of viable OCCs (M. Nawaz et al., 2022). Bos taurus × Bos indicus crossbreeds with average progesterone concentrations in blood serum were characterized by a higher blastocyst rate (%BL) (L.F.M. Pfeifer et al., 2009). Higher concentrations of estradiol-17β in the follicular fluid were associated with higher nF values in crossbred beef heifers (F. Mossa et al., 2010) and non-pregnant Holstein cows (K. Sakaguchi et al., 2019), as well as with a higher %BL value in donor heifers of the Holstein breed (N. Araki et al., 1998). Higher values of the %BL indices were achieved in donor heifers of the Istobian breed, which have higher values of the ratio of the concentration of estradiol-17b in blood serum to the number of OCCs (R.Yu. Chinarov et al., 2025). Negative correlations of FSH concentration in blood serum or blood plasma with n F values were observed in heifers and non-pregnant Holstein cows (J.M. Haughian et al., 2004; K. Sakaguchi et al., 2019), in non-lactating dairy cows (F. Mossa et al., 2010), in heifers and lactating cows of beef cattle (J.J. Ireland et al., 2007; J. Singh et al., 2004). Higher concentrations of AMH were associated with higher nF values in donors of the Holstein breed (B.M. Guerreiro et al., 2014; A. Vernunft et al., 2015), in high-productive dairy cows (A.H. Souza et al., 2015), lactating cows of the Tagil breed (R.Yu. Chinarov et al., 2024), Hanwoo beef cattle (N. Ghanem et al., 2016), Japanese black cattle (H. Hirayama et al., 2019), and Nelore zebu cattle (B.M. Guerreiro et al., 2014). Thus, the results of the analysis showed the presence of a number of associations of reproductive hormones with the efficiency of assisted reproductive technologies in different cattle breeds. In this regard, monitoring the concentrations of reproductive hormones in the blood serum of females can be a useful tool for selecting donors for OPU and predicting the efficiency of production of IVP-embryos in cattle. It is advisable to conduct further studies of the associations of reproductive hormones with the efficiency of OPU/IVP in different cattle breeds, considering the age and physiological status of donors, as well as the technological regimens of their use.
Текст обзорной статьи Репродуктивные биомаркеры коров - современное состояние исследований и перспективы (обзор)
Вспомогательные репродуктивные технологии (ВРТ), включая продукцию эмбрионов in vivo (IVD-эмбрионы) и in vitro (IVP-эмбрионы), — традиционная в настоящее время практика в племенном животноводстве
(1-3). Несмотря на существенные успехи, достигнутые в этой области, многие ВРТ все еще требуют усовершенствования. В отношении продукции IVP-эмбрионов одним из ключевых факторов, определяющих результативность технологии, считается получение от одного донора за сеанс или за определенный период времени посредством УЗИ-ассистированной пункции фолликулов яичников (ovum pick-up, OPU) как можно большего числа ооцитов, обладающих хорошими компетенциями к развитию в системе in vitro (3, 4). В этой связи животные, обладающие большей когортой фолликулов, одновременно вступающих в стадию роста и пригодных для аспирации (антральные фолликулы), могут иметь преимущество в отношении результативности OPU, поскольку от них потенциально может быть получено больше ооцитов.
Известно, что в процессе полового цикла у коров под влиянием фолликулостимулирующего гормона в большинстве случаев наблюдается 2-3 волны роста фолликулов с интервалом 7-10 сут (5, 6). Число антральных фолликулов между отдельными животными сильно варьирует (от 8 до 54), но у одних и тех же животных характеризуется высокой повторяемостью между волнами и циклами (7, 8). Для этого признака характерен умеренный уровень наследуемости (0,25-0,31) (9), что превышает значения показателя для большинства репродуктивных признаков, коэффициенты наследуемости которых оцениваются в 5-10 % (10).
Высокая повторяемость в различных сеансах у отдельных коров отмечена и для других количественных и качественных показателей результативности OPU (11-13). Так, у зебувидного скота породы Нелоре (Nelore) повторяемость для числа извлеченных ооцит-кумулюсных комплексов (ОКК) и ОКК хорошего качества, пригодных для культивирования, у индивидуальных доноров в разных сеансах OPU составляла 0,81, для числа полученных бластоцист — 0,79, доли ОКК хорошего качества — 0,55, доли бластоцист — 0,69 (14). В этой связи результативность технологии OPU/IVP может быть повышена посредством отбора доноров, характеризующихся большим размером популяции фолликулов и способных производить больше ооцитов с хорошей компетенцией к развитию в системе in vitro (15). Перспективным подходом считается поиск репродуктивных биомаркеров (16).
В исследованиях, проведенных на мясном скоте, была показана положительная связь размера яичника с числом антральных фолликулов ( r = 0,89, p < 0,001) (12). У коров породы Nelore ( Bos indicus ) наблюдалась достоверная положительная связь (p < 0,0001) числа антральных фолликулов с диаметром и площадью яичников (17). Обнаружены ассоциации клинических показателей крови во время проведения OPU с выходом эмбрионов на стадии бластоцисты (18).
На телках-донорах истобенской породы была установлена достоверная отрицательная связь содержания эритроцитов в крови с числом фолликулов, общим числом полученных ОКК и числом ОКК, пригодных для культивирования (19). У телок этой же породы выявлены ассоциации содержания в крови некоторых метаболитов и ферментов с числом фолликулов, числом полученных ОКК и выходом бластоцист (20). Принимая во внимание непосредственное участие в регуляции репродуктивных функций половых гормонов, их содержание в крови рассматривают в качестве потенциальных предикторов результативности технологии OPU/IVP (3, 16).
Цель настоящего обзора — анализ современного состояния и результатов исследований ассоциаций между содержанием в крови половых 582
гормонов разных классов и эффективностью вспомогательных репродуктивных технологий для определения потенциальных предикторов повышения результативности OPU/IVP у крупного рогатого скота (КРС).
В половом цикле коров различают фолликулярную и лютеальную фазы, регулируемые половыми гормонами, основные из которых — гона-дотропин-рилизинг-гормон (ГнРГ), секретируемый гипоталамусом, фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ) гормоны, синтезируемые передней долей гипофиза, эстрадиол-17 β и прогестерон, основным местом синтеза которых служат яичники и матка, и синтезируемый эндометрием матки простагландин F2 α (ПГF2 α ) (21, 22). В регуляции репродуктивных функций принимают участие целый ряд других гормонов, включая ингибин (23), кисспептин (24-26), антимюллеров гормон (АМГ) (27) и другие, функции которых в аспекте вспомогательных репродуктивных технологий остаются пока менее изученными. При регуляции фаз полового цикла половые гормоны служат химическими посредниками, которые с кровью перемещаются к определенным тканям-мишеням, содержащим рецепторы, специфичные для гормонов. Сочетание секреции половых гормонов и их метаболизма в печени, почках и легких поддерживает оптимальный гормональный баланс во время фолликулярной фазы, эстру-са и лютеальной фазы полового цикла (22).
Краткое описание функций вышеназванных половых гомонов приведено в таблице 1.
-
1. Гормоны, участвующие в регуляции репродуктивной функции коров и их функции (цит. по 21 с дополнениями)
-
2. Связь между содержанием половых гормонов в крови и результативностью вспомогательных репродуктивных технологий у крупного рогатого скота
Порода (группа)
Концентрация гормона I Показатели
Ссылка
Зебувидный молочный скот
Прогестерон
Кск = 2,31±0,059 нг/мл* n Ф = 12,05±0,37*
(29)
Сахивал (Sahiwal)
Помеси Bos taurus ½ Bos indicus
СИ = 54,23 %* n ОКК = 5,31±0,19*** n ОККп = 4,54±0,187*
Кск = 0,32±0,065 нг/мл* n Ф = 10,87±0,40* СИ = 42,53 %* n ОКК = 3,58±0,21*** n ОККп = 3,06±0,199*
К СК = 3,6 нг/мл* % ОККп = 68,4 %
(30)
Голштинская порода израильской
n БЛ = 0,8±0,4 % БЛ = 16,0 %*
К СК = 1,6 нг/мл* % ОККп = 79,4 %
n БЛ = 1,3±0,4 %бл = 28,2 %*
К СК = 0,5 нг/мл* % ОККп = 72,3 %
n БЛ = 0,4±0,4 %бл = 15,0 %*
Эстрадиол 17- β
Бесплодные коровы: n Ф = 7,1
(33)
селекции (лактирующие коровы 2-го и более отелов)
Голштинская порода японской
Кфж = 1854,9 нг/мл СИ = 42,2 %
%др = 57,6 %
%бл = 12,5 %*
Контроль: n Ф = 7,3
Кфж = 1073,6 нг/мл СИ = 44,1 %
% ДР = 63,4 %
%бл = 29,2 %*
Кфж = 1493±186 пг/мл Гомогенная ооплазма
(34)
селекции (телки)
Голштинская порода японской
Кфж = 921±161 пг/мл Гетерогенная ооплазма
Кфж < 100 пг/мл против Меньше
К ФЖ > 100 пг/мл % ДР *, % БЛ * и % БЛв *
Прямая зависимость: n Ф = 13,6±7,6 против
(31)
селекции (нестельные коровы)
Истобенская порода (телки)
Кпл (p < 0,01) n Ф = 59,2±13,1
Кфж (p < 0,05)
ЭД/ПГфж (p < 0,05)
ЭД/ОКК = 0,027±0,03 нг СИ = 66,1 %a,b
(97)
Мясной скот (ангус ½ гере-
% Д = 75,0 %a % БЛ = 39,3 %a,e
ЭД/ОКК = 0,072±0,01 нг СИ = 54,2 %c,d %д = 70,8 %b %бл = 25,0 %b
ЭД/ОКК = 0,149±0,01 нг СИ = 32,4 %a,c % Д = 42,9 % %бл = 14,3 %e
ЭД/ОКК = 0,258±0,013 СИ = 33,3 %b,d
%д = 41,2 %a,b %бл = 0,0 %a,b
Кфж = 588±76 нг/мл** n Ф > 25
(47)
форд ½ шароле, 11-13 мес)
Кфж = 435±59 нг/мл** n Ф < 15
|
Название (химическая структура) |
Место секреции |
Мишень |
Основная функция |
|
ГнРГ (пептид, 10 аминокислот) |
Гипоталамус |
Передняя доля гипофиза |
Стимулирует высвобождение гипофизом ФСГ и ЛГ |
|
Кисспептин (нейропептид, 126 аминокислот) |
Гипоталамус |
Рецепторы на нейронах ГнРГ |
Стимулирует секрецию ГнРГ, усиливая высвобождение гипофизарных и стероидных гормонов |
|
ФСГ (гликопротеин, |
Передняя доля |
Яичник (клетки гранулезы |
Стимулирует развитие фолликулов |
|
> 200 аминокислот) |
гипофиза |
фолликула) |
и синтез эстрадиола |
|
ЛГ (гликопротеин, |
Передняя доля |
Яичник (клетки теки и |
Вызывает созревание фолликулов, |
|
> 200 аминокислот) |
гипофиза |
желтое тело) |
овуляцию; развитие и функцию желтого тела; секрецию прогестерона |
|
Эстрадиол-17 β (стероид) |
Яичник (клетки гранулезы фолликула) и плацента |
Гипоталамус Передняя доля гипофиза Яйцевод, матка, шейка матки, влагалище и вульва |
Индуцирует проявление охоты, стимулирует секрецию ГнРГ перед овуляцией Усиливает секрецию ФСГ и ЛГ Влияет на секрецию слизистых оболочек и стимуляцию мышечной активности полового тракта |
|
Прогестерон, ПГ (стероид) |
Яичник (желтое тело), плацента |
Гипоталамус Эндометрий и миометрий матки, молочная железа |
Снижает высвобождение ГнРГ, тем самым тормозит секрецию ФСГ, созревание доминантных фолликулов Подготавливает эндометрий к имплантации эмбриона; тормозит сокращение мускулатуры матки, обеспечивая сохранение беременности |
|
Простагландин, ПГF2 α |
Матка (эндомет- |
Яичник (желтое тело), |
Вызывает рассасывание желтого |
|
(жирорастворимая кислота) |
рий) |
яйцевод |
тела (лютеолиз); усиливает тонус и сокращение матки |
|
Ингибин (пептид) |
Яичник (клетки гранулезы фолликула) |
Передняя доля гипофиза |
Ингибирует высвобождение ФСГ гипофизом (механизм обратной связи) |
|
Антимюллеров гормон, |
Яичник (клетки |
Яичник (преанртальные |
Ингибирует примордиальный рост |
|
АМГ (пептид) |
гранулезы фолликула) |
и малые антральные фолликулы) |
фолликулов путем ингибирования рецепторов ФСГ в фолликулах |
Примечание. ГнРГ — гонадотропин-рилизинг-гормон, ФСГ — фолликулостимулирующий гормон,
ЛГ — лютеинизирующий гормон.
Участие основных половых гормонов в регуляции полового цикла
схематично представлено на рисунке.
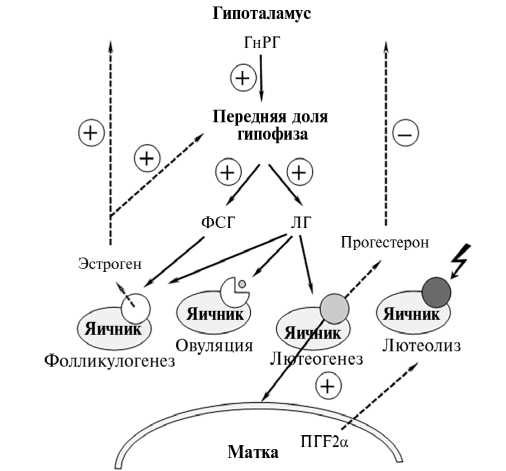
Схема гипоталамо—гипофизарно—гонадной оси у коров: ГнРГ — гонадотропин-рилизинг-гормон; ФСГ — фолликулостимулирующий гормон; ЛГ — лютеинизирующий гормон; ПГF2 α — простагландин F2 α .
По завершении лютеолиза наступает фолликулярная фаза полового цикла. Она начинается с проэструса, когда наблюдается снижение содержания прогестерона, которое приводит к увеличению выбросов ЛГ и повышению количества эстрадиола как в циркулирующей крови, так и в самом фолликуле. В этот период ооцит завершает критические процессы предсозревания. На этой стадии между ооцитами и клетками кумулюса устанавливается двунаправленная связь, что необходимо для осуществления важных метаболических изменений. Сразу после выброса ЛГ взаимодействие между ооцитами и клетками кумулюса прекращается и начинается стадия созревания MII. Внутрифолликулярный гормональный профиль меняется с преимущественного эстрогенного на прогестероновый, что влияет на компетенцию ооцитов к развитию (28).
Результаты экспериментальных исследований на человеке и животных показали наличие ряда зависимостей содержания некоторых половых гормонов в крови и фолликулярной жидкости с числом антральных фолликулов, пригодных для аспирации, количественными и качественными характеристиками получаемых ооцитов и их компетенциями к развитию in vitro до стадии бластоцисты, что позволяет рассматривать их в качестве дополнительного инструмента для повышения эффективности технологии OPU/IVP.
Изучается влияние концентрации прогестерона в сыворотке крови на фолликулярную динамику, количество и качество OPU-ооцитов, а также на их компетенцию к развитию in vitro. M. Nawaz с соавт. (29) изучали влияние концентрации прогестерона на результативность последовательных сеансов OPU у зебувидного молочного скота породы Сахивал (Sahiwal) с гормонально синхронизированным половым циклом. В качестве источника экзогенного прогестерона в опытной группе использовали устройство CIDR для контролируемого внутреннего высвобождения лекарств (controlled internal drug release). Было проведено 4 последовательных сеанса OPU с интервалом 4 сут. Каждые 12 ч проводили сонографические исследования с целью мониторинга паттерна развития фолликулов. Концен- трации прогестерона в опытной и контрольной группах достоверно различались и составили соответственно 2,31±0,059 и 0,32±0,065 нг/мл (p < 0,05). В опытной группе общее число УЗИ-видимых фолликулов было достоверно выше (12,05±0,37 против 10,87±0,40, p < 0,05), в то время как скорость роста фолликулов (мм/сут) была ниже (p > 0,05). В опытной группе по сравнению с контролем оказались более высокие значения степени извлечения ооцитов (54,23 против 42,53 %, p < 0,05), а также общего числа полученных ооцитов (5,31±0,19 против 3,58±0,21, p < 0,0001), числа жизнеспособных ооцитов (4,54±0,187 против 3,06±0,199, p < 0,05) и числа ооцитов категорий I и II (3,37±0,196 против 2,06±0,21, p < 0,05), полученных в среднем за сеанс OPU. Различий в доле созревания, доле дробления и доле развития ооцитов до стадии бластоцисты выявлено не было. Полученные результаты позволили сделать вывод о положительном влиянии повышенного содержания прогестерона в сыворотке крови на степень извлечения и качество ооцитов при отсутствии эффекта на их компетенцию к развитию in vitro.
L.F.M. Pfeifer с соавт. (30) исследовали влияние концентрации прогестерона в крови помесных ( Bos taurus ½ Bos indicus ) коров-доноров на результативность технологии OPU/IVP. Для обеспечения различного содержания прогестерона в крови в 0-е сут коровам группы ПГ внутриваги-нально вводили два новых CIDR (группа с высоким содержанием прогестерона, средняя концентрация прогестерона в дни проведения OPU = 3,6 нг/мл), а животным группы ПГ с — ранее использованный CIDR (группа со средним содержанием прогестерона, 1,6 нг/мл). В контрольной группе (ПГ н ) CIDR не использовали (группа с низким содержанием прогестерона, 0,5 нг/мл). Концентрации прогестерона между группами достоверно различались (p < 0,05). Пункцию фолликулов выполняли с 4-х по 24-е сут с интервалом 4 сут. На 18-е сут проводили отбор образцов с целью оценки характера высвобождения лютеинизирующего гормона. Количество ЛГ в плазме крови оказалось наиболее высоким в группе ПГ с (1,6 нг/мл), имело промежуточное значение в группе ПГ н (1,0 нг/мл) и было самым низким в группе ПГ в (0,8 нг/мл). Больший процент жизнеспособных ооцитов категорий I-III получили в группе ПГ с (79,4 %; 131/165) по сравнению с группой ПГ в (68,4 %; 119/174) (р = 0,07); группа с ПГ н не отличалась от остальных (72,3 %; 60/83). Число и доля развития бластоцист были выше в группе ПГ с (1,3±0,4; 28,2 %), чем в группе ПГ в (0,8±0,4; 16,0 %) или ПГ Н (0,4±0,4; 15,0 %) (p = 0,06 и p = 0,03 соответственно для числа и доли развития бластоцист). На основании полученных результатов авторы сделали вывод, что промежуточные значения концентрации прогестерона в плазме крови, которые обусловливают более высокую циркулирующую концентрацию ЛГ, могут улучшать результативность получения IVP-эмбрионов.
Исследования, проведенные на нестельных коровах голштинской породы, показали более высокие (p < 0,01) концентрации ФСГ в плазме крови в течение полового цикла в группе животных с меньшим (13,6±7,6) по сравнению с группой коров с большим (59,2±13,1) числом антральных фолликулов (31).
Доминирующей формой эстрогена в яичниках коров служит эстра-диол-17β (эстрадиол). Эстрадиол синтезируется гранулезными клетками посредством ароматизации андростендиона в ответ на стимуляцию ФСГ. Важнейшая функция эстрадиола — регуляция секреции гонадотропинов посредством обратной связи. Эстрадиол также играет ключевую роль в фолликулогенезе, в первую очередь на постантральной фолликулярной стадии. Развитие растущего преовуляторного фолликула сопровождается повышением концентрации эстрадиола в крови (32). Для гипоталамо— гипофизарной системы это служит химическим сигналом, указывающим на зрелость растущих фолликулов и индуцирующим преовуляторный выброс ЛГ для вызывания овуляции (23).
Показано, что у бесплодных коров в фолликулярной жидкости преовуляторных фолликулов содержится больше эстрадиола по сравнению с коровами с нормальными воспроизводительными функциями (33). В эксперименте лактирующие коровы были разделены на две категории: контрольная и опытная. Коровы контрольной группы находились на 62133-х сут лактации, нормально циклировали и не были осеменены. Коровы из опытной группы не имели клинически диагностируемых нарушений и не становились стельными не менее чем после четырех осеменений в процессе спонтанной охоты с нормальными интервалами между осеменениями (бесплодные коровы). Коровы были синхронизированы посредством 2-кратной инъекции ПГF2 α с интервалом 14-15 сут. Аспирацию фолликулярной жидкости из преовуляторных фолликулов проводили через 48 ч после второй инъекции ПГF2 α . Различий в диаметре преовуляторных фолликулов между группами выявлено не было. Однако у бесплодных коров концентрация эстрадиола в фолликулярной жидкости была выше по сравнению с контрольной группой: 1854,9 против 1073,6 нг/мл, при этом различий в концентрации андростендиона и прогестерона не обнаружили. Проведение 14 последовательных сеансов OPU с интервалом 3-4 сут не выявило различий между группами в среднем числе фолликулов (соответственно 7,1 и 7,3), степени извлечения ооцитов (42,2 и 44,1 %) и доле по-дробившихся ооцитов (57,6 и 63,4 %), однако доля бластоцист в группе бесплодных коров была достоверно ниже по сравнению с контрольной группой (12,5 и 29,2 %). Авторы делают вывод о том, что воздействие некоторых факторов на ранних стадиях фолликулогенеза вносит вклад в этиологию бесплодия у коров, нарушая компетенцию ооцитов к развитию до стадии бластоцисты (33).
N. Araki c соавт. (34) исследовали влияние концентрации эстрадиола в фолликулярной жидкости отдельных фолликулов и морфологии ОКК на развитие в системе in vitro ооцитов КРС. Средняя концентрация эстрадиола в фолликулах, содержащих гетерогенную ооплазму, оказалась достоверно ниже (p < 0,05) по сравнению с фолликулами, из которых были извлечены ооциты с гомогенной ооплазмой (921 против 1493 пг/мл), в то время как число слоев кумулюсных клеток не зависело от концентрации эстрадиола в фолликулярной жидкости. Вне зависимости от гетерогенности ооплазмы компетенция к развитию in vitro была выше (p < 0,05) у ооцитов, имеющих 4 и более слоев кумулюсных клеток по сравнению с ооцитами с 2-3 слоями кумулюса. Ооциты, полученные из фолликулов с концентрацией эстрадиола менее 100 пг/мл, характеризовались достоверно (p < 0,05) меньшей долей дробления, долей развития бластоцист и долей вылупившихся бластоцист по сравнению с фолликулами с более высокими концентрациями эстрадиола (34).
Биологические свойства эстрадиола позволяют рассматривать его в качестве перспективного биомаркера эффективности вспомогательных репродуктивных технологий.
Многочисленные исследования в этом направлении проводятся на человеке. Например, установлена связь содержания эстрадиола в сыворотке крови в день стимуляции хорионическим гонадотропином (ХГ) с числом получаемых ОКК (35). Более высокие концентрации эстрадиола были 586
ассоциированы с большим числом ОКК, MII-ооцитов, а также числом IVP-эмбрионов хорошего качества (36). Показана положительная связь концентрации эстрадиола на 7-е сут после гиперстимуляции яичников со степенью оплодотворения ооцитов (37). Высокое содержание эстрадиола в день введения чХГ было связано с пониженным выходом бластоцист у человека (38). Была установлена положительная связь между содержанием эстрадиола в крови пациенток в день стимуляции яичников посредством введения лХГ и числом фолликулов ( r = 0,592, p < 0,001), числом извлеченных ооцитов ( r = 0,576, p < 0,001) и числом созревших ооцитов ( r = 0,554, p < 0,001). Соотношение ЭД/ооцит не было ассоциировано с первыми двумя показателями, при этом наблюдалась сильная отрицательная корреляция с числом созревших ооцитов ( r = - 0,280, p < 0,001) (39). Показана значимая взаимосвязь между числом извлеченных ооцитов и соотношением эстрадиола к прогестерону (ЭД/ПГ) на момент индукции овуляции посредством инъекции хорионического гонадотропина человека (чХГ). Среднее число извлеченных ооцитов увеличивалось по мере увеличения квартилей, на которые была разбита исследуемая выборка по соотношению ЭД/ПГ. Ассоциации отношения ЭД/ПГ со степенью извлечения ооцитов, долей созревших ооцитов, процентом беременности и процентом родов выявлено не было (40).
Часто используемым предиктором успешности вспомогательных репродуктивных технологий у человека служит соотношение концентрации эстрадиола в крови в день введения хорионического гонадотропина (ХГ) к числу полученных ОКК (ЭД/ОКК), предложенное E. Loumaye с соавт. (41), а также его аналогичные производные: соотношение ЭД к числу фолликулов (ЭД/ФОЛ) (42) или к числу MII-ооцитов (ЭД/ооцит) (36). Показано, что более низкие значения ЭД/ОКК или ЭД/ооцит ассоциированы с получением большего числа эмбрионов хорошего качества (36, 43). Установлена отрицательная связь показателя ЭД/ооцит с числом ооцитов, долей созревших ооцитов, числом бластоцист хорошего качества (44), числом созревших ооцитов (39, 43). В группе пациенток, имевших значения ЭД/ооцит > 0,204 пг/мл, отмечали более высокие концентрации эстрадиола в крови и меньшее число созревших ооцитов. Значения показателя ЭД/ооцит < 0,204 пг/мл были связаны с более высокой долей оплодотворенных ооцитов, большим числом полученных эмбрионов хорошего качества, процентом беременности и процентом родов (43). Высокие значения ЭД/ооцит (> 400 пг/мл) были ассоциированы с пониженным числом извлеченных ооцитов (в среднем 5,9 ооцитов за сеанс с вариациями от 0 до 15). У пациенток, у которых было получено больше 15 ооцитов за сеанс, высокие значения ЭД/ооцит (> 400 пг/мл) были ассоциированы с более низкими значениями числа ооцитов, доли созревших ооцитов и числа бластоцист хорошего качества. Кроме того, значения ЭД/ооцит > 400 пг/мл в высокой степени коррелировали с наличием нулевых сеансов (сеансы, в которых не было получено ни одного эмбриона) (44). В другом исследовании не выявили связи параметра ЭД/ОКК с результативностью вспомогательных репродуктивных технологий (45).
В настоящее время имеются лишь единичные исследования на сельскохозяйственных животных, посвященные изучению возможности использования эстрадиола в качестве предиктора результативности технологии OPU/IVP. У молочных коров показана связь концентрации эстрадиола в плазме крови с числом яйцеклеток, полученных посредством OPU от животных, находящихся на 3-м мес (72,8±6 сут) лактации, в то время как у коров, находящихся на поздней стадии лактации (263±60 сут), такую связь не обнаружили (46). В исследованиях, проведенных на помесных мясных телках (абердин-ангусская ½ герефорт ½ шароле) в возрасте 1113 мес, установлено, что концентрация эстрадиола в фолликулярной жидкости была ниже у животных с меньшим числом антральных фолликулов (< 15) по сравнению с животными с большим числом антральных фоллку-илов (> 25): 435±59 против 588±76 нг/мл (р < 0,01) (47).
N.R. Kussano с соавт. (48) провели сравнительное исследование содержания эстрадиола и прогестерона, а также отношения концентрации эстрадиола к прогестерону (ЭД/ПГ) в жидкости фолликулов, извлеченные из которых ОКК в системе in vitro развились или, напротив, не развились до стадии бластоцисты (соответственно группы EMB и NEMB). Если концентрации прогестерона в фолликулярной жидкости между группами достоверно не различались (соответственно 164,5 и 152,8 нг/мл), концентрация эстрадиола и значения показателя ЭД/ПГ были достоверно (p < 0,05) выше в группе EMB (соответственно 33,14 и 0,226 нг/мл) по сравнению с группой NEMB (3,73 и 0,024 нг/мл).
В исследованиях K. Sakaguchi с соавт. (31), проведенных на нестельных коровах голштинской породы, показано, что концентрация эстрадиола в плазме крови была достоверно (p < 0,05) ниже в группе животных с меньшим числом антральных фолликулов (13,6±7,6 фолликулов) по сравнению с группой коров с большим числом антральных фолликулов (59,2±13,1), в то время как концентрация эстрадиола и значения показателя ЭД/ПГ в жидкости овулятороных фолликулов оказались выше в группе с большим числом антральных фолликулов (p < 0,05).
В наших исследованиях (49) на телках истобенской породы было показано, что в сеансах OPU, в которых отмечались минимальные значения показателя ЭД/ОКК (0,027±0,03), наблюдалась более высокая доля развития ооцитов до стадии бластоцисты (39,3±9,2 %). Коэффициент корреляции между показателем ЭД/ОКК и долей развития бластоцист составил r = - 0,36 (p < 0,01). В таких сеансах в среднем было получено 2,75±1,03 эмбрионов в стадии бластоцисты, в то время как в сеансах с более высокими значениями показателя ЭД/ОКК (0,258±0,013) стадии бластоцисты не достиг ни один из ооцитов. Полученные результаты показывают целесообразность мониторинга паттерна развития овариальных фолликулов и концентрации эстрадиола в сыворотке крови для отбора телок-доноров истобенской породы для OPU/IVP (49).
В исследованиях на человеке и лабораторных животных было показано, что высокое содержание эстрадиола ухудшает имплантацию бластоцист из-за воздействия на эндометрий. Так, при пересадке эмбрионов, находящихся на стадии первого деления-дробления, содержание эстрадиола в крови пациенток негативно коррелировало со степенью имплантации, процентом клинически подтвержденной беременности, процентом поздних беременностей и процентом рождения потомства. С другой стороны, концентрация эстрадиола в крови не оказывала влияния на результативность пересадки эмбрионов на стадии бластоцисты (50).
На мышах показано, что воздействие высоких концентраций эстрадиола in vitro негативно влияло на имплантацию бластоцист и раннее постимплантационное развитие, главным образом, из-за прямого воздействия эстрадиола на имплантирующиеся бластоцисты. На основании полученных данных сделан вывод, что высокая концентрация эстрадиола в сыворотке крови оказывает влияние не только на эндометрий, но и на бластоцисты непосредственно в период имплантации (51). В группе пациенток с подтвержденной беременностью после пересадки IVP-эмбрионов 588
концентрация эстрадиола в фолликулярной жидкости из самых крупных фолликулов была достоверно ниже, чем в группе не забеременевших пациенток (52). Выявленные закономерности требуют подтверждения на сельскохозяйственных животных.
В качестве потенциального биомаркера для прогнозирования размера популяции фолликулов рассматривается определение концентрации фолликулостимулирующего гормона в сыворотке крови. Содержание ФСГ в сыворотке или плазме находилось в обратной зависимости от числа антральных фолликулов у телок молочного (53) и мясного КРС (8), а также у не лактирующих молочных (31, 54) и лактирующих мясных коров (55). Например, в группе голштинских телок, характеризующихся меньшим числом (5,7±0,4) фолликулов диаметром ≥ 5 мм, отмечены достоверно более высокие пиковые концентрации ФСГ в сыворотке крови по сравнению с группой коров с большим числом (11,0±1,0) фолликулов: 0,41±0,04 против 0,29±0,02 нг/мл (p < 0,05) (53).
В качестве биомаркера овариального резерва, критерием оценки которого служит число антральных фолликулов, рассматривается антимюллеров гормон (АМГ) (27, 56). Известно, что число антральных фолликулов положительно коррелирует с числом извлекаемых ооцитов и полученных эмбрионов в расчете на сеанс OPU (14, 57, 58).
АМГ — член семейства трансформирующих факторов роста бета (TGF- β ) (59). На поздних стадиях эмбрионального развития АМГ секретируется гранулезными клетками яичников самок, включая КРС (27). В исследованиях на человеке было показано, что АМГ выполняет две критически важные функции: ингибирует примордиальный рост фолликулов из пула фолликулов яичника, предотвращая тем самым преждевременное истощение фолликулярных резервов, и снижает чувствительность к ФСГ пре-антральных и небольших антральных фолликулов посредством ингибирования рецепторов ФСГ, модулируя при этом развитие фолликулов (27, 60).
Секреция АМГ инициируется с началом фолликулярных волн, достигает своего пика в примордиальных, первичных и вторичных фолликулах, снижается после селекции доминантного фолликула и отсутствует в атретических фолликулах (27). АМГ контролирует число фолликулов в яичниках и селекцию доминантного фолликула во время фолликулярных волн. На модели мыши показано, что в отсутствие АМГ рекрутирование фолликулов происходит быстрее, однако это приводит к истощению фолликулярных резервов яичников в более молодом возрасте (61). В экспериментах in vivo и in vitro установлено ингибирующее действие АМГ на су-перстимулированный ФСГ рост фолликулов у мышей (62). Экспрессия АМГ резко снижается в крупных фолликулах, что позволяет предположить роль ФСГ и/или эстрадиола в этих изменениях, но лежащие в их основе механизмы остаются гипотетическими (63).
Известно, что концентрация АМГ в сыворотке крови зебувидного скота, характеризующегося большим размером популяции антральных фолликулов, превышает значения показателя у европейских пород скота. Так, средние концентрации АМГ у скота породы Nelore ( B. indicus ) составляли 1,0±0,2 нг/мл против 0,3±0,02 нг/мл у голштинского скота ( B. taurus ) (64). Как у голштинского, так и у зебувидного скота отмечена вариация содержания АМГ в зависимости от физиологического состояния животных. У голштинского скота концентрация АМГ в сыворотке крови у препубертатных телок в возрасте 8-10 мес составляла 0,3±0,04 нг/мл, у циклирующих телок в возрасте 12-14 мес — 0,3±0,03 нг/мл, у лактирую-щих коров — 0,2±0,03 нг/мл, у не лактирующих коров — 0,3±0,03 нг/мл.
У зебувидного скота породы Nelore концентрация АМГ в сыворотке крови у препубертатных телок в возрасте 10-11 мес составляла 0,7±0,1 нг/мл, у препубертатных телок в возрасте 21-23 мес — 1,4±0,3 нг/мл, у циклирующих телок в возрасте 24-26 мес — 1,4±0,4 нг/мл (64). Полагают, что изменения в концентрации АМГ в крови отражают количественные изменения в популяции фолликулов, продуцирующих АМГ (63). В процессе полового цикла содержание АМГ у КРС варьирует незначительно (65). Концентрация АМГ оставалась относительно стабильной в двух различных половых циклах (66), а также при естественных и синхронизированных половых циклах (67).
Ряд работ посвящен изучению связи концентрации АМГ с числом фолликулов у КРС. Установлена высокая корреляция ( r = 0,90, p < 0,05) содержания АМГ с общим числом морфологически полноценных фолликулов (примордиальных, транзиторных, первичных, вторичных и антральных) в яичниках молодняка КРС (12). Среднее значение концентрации АМГ в течение овуляторной фолликулярной волны достоверно коррелировало со средним числом фолликулов в течение двух или трех фолликулярных волн полового цикла (12). Достоверная положительная корреляция между АМГ и числом фолликулов была выявлена как у скота европейского типа (31, 68), так и у зебувидного скота (68-70). Например, в группе голштинских телок с высоким числом антральных фолликулов по сравнению с животными с низким числом антральных фолликулов (34,3±3,12 против 13,4±1,40) отмечали достоверно (p < 0,001) более высокие концентрации АМГ в плазме крови 0,57±0,26 нг/мл против 0,06±0,02 нг/мл (68). Аналогичная закономерность наблюдалась и у зебувидного скота породы Nelore: концентрация АМГ в группе с высоким числом антральных фолликулов (48,1±2,33) по сравнению с группой с низким числом антральных фолликулов (28,4±2,15) оказалась достоверно (p < 0,001) выше — 1,20±0,16 против 0,78±0,16 нг/мл (68). У телок породы Брадфорд (Bradford) были установлены высокая повторяемость и число фолликулов и концентрация АМГ при оценке после отъема и перед началом репродуктивного использования, в связи с чем высокие концентрации АМГ в послеотъемный период могут быть использованы для отбора телок этой породы с более ранним половым созреванием (71). В аналогичном эксперименте на телках герефордской породы выявлена лишь слабая корреляция между показателями в послеотъемный и активный репродуктивный период (71).
Потенциальным преимуществом использования АМГ в качестве репродуктивного биомаркера служит его относительно высокая по сравнению с большинством репродуктивных показателей наследуемость. Коэффициент наследуемости AMГ, рассчитанный по родословной, составлял 0,43±0,07 (72). В масштабном исследовании примерно на 3 тыс. телок голштинской породы, генотипированных по SNP-маркерам, коэффициент геномной наследуемости АМГ составил 0,36±0,03 (72). У голштинских коров канадской селекции значение этого показателя было равно 0,46±0,31 (73).
Относительно стабильные концентрации АМГ в течение полового цикла, позволяющие брать кровь для исследований без учета суток полового цикла, высокая повторяемость между циклами, умеренная наследуемость показателя и его связь с числом антральных фолликулов у ряда пород КРС обусловливают актуальность оценки содержания АМГ в качестве потенциального предиктора результативности вспомогательных репродуктивных технологий, включая число эмбрионов, полученных in vivo после полиовуляции, число ОКК, извлеченных посредством OPU, и число эмбрионов, полученных in vitro.
Так, у высокопродуктивных молочных коровах американской селекции наблюдалась положительная корреляция концентрации АМГ с реакцией на полиовуляцию, оцененной по числу желтых тел на момент вымывания эмбрионов ( r = 0,65; p < 0,01), общим числом вымытых эмбриональных структур ( r = 0,50; p < 0,01) и числом эмбрионов, пригодных для трансплантации ( r = 0,37; p < 0,05) (74). Положительная корреляция содержания АМГ в плазме крови с реакцией на полиовуляцию, числом вымытых эмбрионов и числом эмбрионов, пригодных для трансплантации, была выявлена у японского черного скота (75, 76). Однако у телок голштино-фризской породы не обнаружено связи концентрации АМГ с числом вымытых эмбрионов после полиовуляции (77).
Положительная связь между содержанием АМГ и числом полученных IVP-эмбрионов наблюдалась у голштинского ( r = 0,36, p < 0,001) и зебувидного скота породы Nelore ( r = 0,50, p = 0,003) (64). Для более детального анализа влияния АМГ на результативность технологии OPU/IVP B.M. Guerreiro с соавт. (64) разделили доноров на группы с высоким и низким значением АМГ. Было показано, что в группах с высоким содержанием АМГ в яичниках у самок присутствовало больше УЗИ-видимых аспирированных фолликулов — 20,9±1,5 против 13,6±0,9 (p < 0,0001) у голштинского скота и 54,3±6,1 против 18,6±2,1 (p < 0,0001) у породы Nelore — и было извлечено больше ОКК: соответственно 17,3±1,5 против 9,0±0,9 (p < 0,0001) и 45,3±6,4 против 13,4±1,7 (p < 0,0001). Несмотря на то, что различий в доле полученных бластоцист между группами с высоким и низким содержанием АМГ отмечено не было — 20,6±4,0 против 19,8±4,2 % (p = 0,60) у голштинского скота и 33,7±6,5 против 27,4±5,5 % (p = 0,41) у скота породы Nelore, — в группах с высоким количеством АМГ в среднем за сеанс OPU от одного донора было получено больше эмбрионов по сравнению с группами с низким содержанием АМГ: 3,0±0,7 против 1,2±0,3 (p = 0,04) у голштинского скота и 7,0±1,7 против 2,2±0,5 (p = 0,007) у скота породы Nelore. Авторы пришли к выводу, что содержание АМГ в плазме крови может служить точным эндокринным маркером для прогнозирования выхода IVP-эмбрионов как у европейского B . taurus , так и у зебувидного скота B . indicus . По их мнению, определение концентрации АМГ может служить эффективным приемом повышения общей результативности технологии OPU/IVP в полевых условиях, а также использоваться в качестве критерия для отбора доноров с высокой эмбриональной продуктивностью (64).
A. Vernunft с соавт. (77) выявили положительную корреляцию концентрации АМГ в плазме крови телок-доноров голштино-фризской породы с числом аспирированных фолликулов ( r = 0,45, p < 0,001), числом извлеченных ОКК ( r = 0,43, p < 0,001) и числом полученных IVP-эмбрионов в среднем за сеанс OPU ( r = 0,28, p < 0,02). Более высокие концентрации АМГ в плазме крови были ассоциированы с большим числом аспирированных фолликулов, извлеченных ОКК и полученных IVP-эмбрионов у корейского мясного скота Ханву (Hanwoo) (78).
В наших исследованиях на лактирующих коровах-донорах тагильской породы установлена тенденция к повышению числа УЗИ-видимых фолликулов с увеличением концентрации АМГ в сыворотке крови с 9,20±1,39 в категории с низким содержанием АМГ (0,562±0,011 нг/мл) до 11,67±1,49 в категории с высоким у содержанием АМГ (1,509±0,033 нг/мл). При этом такая тенденция наблюдалась как на не овуляторном, так и на овуляторном яичниках. На уровне тенденции установлено большее число пригодных ОКК и полученных бластоцист в категориях с более высокими концентрациями АМГ по сравнению с категориями с меньшими концентрациями АМГ (79). Приведенные данные подтверждают перспективы использования АМГ в качестве биомаркера для прогнозирования результативности получения как in vivo, так и in vitro эмбрионов у КРС (27).
В качестве потенциального биомаркера для прогнозирования результативности вспомогательных репродуктивных технологий рассматривается кисспептин (25, 80). Кисспептин — это гипоталамический нейропептид, который стимулирует секрецию ГнРГ и регулирует ответ половых стероидов на секрецию ГнРГ (81). Наряду с участием в регуляции гипото-амно—гипофизарно—гонадной оси доказано участие кисспептина в регуляции функции яичников, трофобласта эмбриона и плаценты (82). Показан негативный дозозависимый эффект кисспептина на рост фолликулов, на основании чего было высказано предположение, что кисспептин может подавлять экспрессию рецептора ФСГ (83). Добавление кисспептина в среду для культивирования повышало долю эмбрионов, развившихся до стадии бластоцисты в культуре in vitro (84).
Следует отметить, что большинство данных о влиянии кисспептина на репродуктивные качества КРС получено при экзогенном введении кис-спептин-содержащих препаратов, в то время как изучению ассоциаций концентрации кисспептина с показателями воспроизводства уделяется меньше внимания (25, 80). Так, S. Kaya с соавт. (85) исследовали влияние содержания в крови кисспептина, эстрадиола и прогестерона во время искусственного осеменения на наступление стельности у коров с гормонально синхронизированным половым циклом. Сонографические исследования яичников не выявили различий в размере преовуляторного фолликула во время осеменения у коров, ставших стельными (17,9±0,01 мм), по сравнению с нестельными животными (17,9±0,01 мм). У коров, ставших стельными, содержание кисспептина во время осеменения было достоверно выше по сравнению с нестельными животными (80,58±4,4 против 66,68±2,48 пг/мл, p = 0,003), в то время как различий в концентрации эстрадиола и прогестерона выявлено не было. Обнаружена положительная корреляция между диаметром преовуляторного фолликула и содержанием кисспептина; для эстрадиола и прогестерона такую связь не установили. На основании проведенных исследований был сделан вывод, что концентрация кисспептина в крови во время осеменения может быть использована для прогнозирования успешного наступления стельности.
Ингибины — это димерные белковые гормоны, синтезируемые клетками гранулезы фолликулов в виде субъединиц α и β A/ β B, кодируемых соответственно INHA , INHBA и INHBB (86). Изоформа А ингибина вырабатывается доминантными фолликулами. Полагают, что доминантные фолликулы в течение процесса доминирования до овуляции характеризуются повышенным содержанием ингибина А, который снижается только после овуляции (87). Ингибин B аналогично АМГ обнаруживается на ранних стадиях развития антральных фолликулов (88). Роль ингибина B заключается в передаче химического сигнала от растущих фолликулов в яичнике в переднюю долю гипофиза для снижения секреции ФСГ до уровня, который необходим для поддержания видоспецифического числа овуляций (86).
H. Miura соавт. (89) показали, что процедура OPU обусловливала снижение концентрации ингибина и повышение концентрации ФСГ, в то время как в результате овуляции снижения количества ингибина не происходило. Авторы связывают это с тем, что в контроле концентрации ин-гибина в плазме принимают участие два и более фолликулов, поэтому удаление одного фолликула вследствие овуляции не приводит к снижению концентрации ингибина, в то время как удаление всех видимых фолликулов в результате OPU обусловливает ее уменьшение. Полагают, что именно ингибин служит наиболее важным гормоном, регулирующим специфическое для вида число овуляций у животных как с одной, так и с множественными овуляциями (23).
В ряде исследований показано, что биологическая активность эндогенных ингибинов может быть нейтрализована активной иммунизацией против ингибинов. Это приводит к увеличению секреции гипофизом и, как следствие, к повышению концентрации ФСГ в плазме крови, что стимулирует рост дополнительных или новых фолликулов (86, 90). Так, введение коровам на 12-е сут полового цикла антисыворотки ингибина приводило к достоверному (p < 0,01) повышению концентрации ФСГ и эстрадиола в плазме крови, в то время как влияния на содержание ЛГ или прогестерона не отмечали. Концентрация ФСГ в плазме крови статистически значимо (p < 0,01) возрастала через 8 ч после введения антисыворотки и оставалась высокой в течение 72 ч, снижаясь до контрольного уровня к 84-му ч, что совпадало с резким снижением титра свободных антител к ингибину в плазме крови. Высокие концентрации эстрадиола наблюдались между 36 и 96 ч после обработки антисывороткой (91). Нейтрализация ингибина посредством введения специфической антисыворотки на 5-е сут полового цикла в течение ранней лютеальной фазы обусловливала гиперсекрецию ФСГ с одновременной стимуляцией развития фолликулов яичников коров, что указывает на участие ингибина в негативной регуляции секреции ФСГ в раннюю лютеальную фазу, когда секреция эстрадиола и прогестерона обычно высока (92). Иммунизация коров голштинской породы против ингибина в лютеальной фазе полового цикла приводила к дозозависимому повышению концентрации ФСГ, эстрадиола, активина А и снижению концентрации прогестерона в плазме крови (93).
Для оценки эффективности иммунизации против ингибина в повышении плодовитости КРС и выработки более эффективных рекомендаций по клинической ветеринарной практике L. Ma с соавт. (86) провели мета-анализ данных из научных статей в предметной области исследований. Результаты анализа показали, что иммунизация против ингибина оказывает достоверное (p < 0,0001) влияние на увеличение числа овуляций со средними различиями 0,44 при 95 % доверительном интервале (0,31, 0,56), числа эмбрионов и неоплодотворенных яйцеклеток — 4,51 (2,28, 6,74)), числа фолликулов, доли множественных овуляций (ovulation rate) — 22,50 (8,13, 62,27) и процента стельностей — 2,36 (1,26, 4,40). Кроме того, иммунизация против ингибина оказывала положительное влияние на продукцию эмбрионов: на число эмбрионов 1-, 2- и 3-го класса — соответственно 3,84 (3,54, 4,15); - 0,73 ( - 0,89, - 0,57); - 0,50 ( - 0,75, - 0,25), число дегенерированных эмбрионов — 1,16 ( - 0,51, 2,82), число эмбрионов, пригодных для трансплантации, — 2,67 (2,03, 3,31), число желтых тел — 1,25 (0,79, 1,71). На основании результатов мета-анализа сделан вывод, что иммунизация против ингибина может сделать технологию суперовуляции КРС менее трудоемкой и более эффективной (86).
У человека проводятся исследования потенциального использования ингибина в качестве биомаркера фолликулярной активности и овариального резерва яичников с целью прогнозирования результативности вспомогательных репродуктивных технологий (94). Показана связь концентрации ингибина B в крови пациенток в раннюю фолликулярную фазу с числом извлеченных и оплодотворенных ооцитов (95, 96). В качестве недостатка использования ингибина как маркера фолликулярного резерва рассматривается его большая по сравнению с АМГ и эстрадиолом зависимость от содержания ФСГ, поскольку АМГ секретируется гранулезными клетками не только малых антральных, но и преантральных фолликулов, на которые ФСГ не оказывает влияния (94). Работы по изучению ассоциаций ингибина с результативностью вспомогательных репродуктивных технологий у КРС в доступной литературе отсутствуют.
Данные о связи концентрации половых гормонов с показателями, характеризующими результативность вспомогательных репродуктивных технологий у самок КРС, обобщены в таблице 2. Принимая во внимание выявленные ассоциации, а также существенные индивидуальные различия между донорами в отношении числа получаемых ОКК и их компетенции к развитию in vitro (98-100), мониторинг концентрации половых гормонов в сыворотке крови самок можно использовать в качестве дополнительного критерия при отборе доноров для программ OPU/IVP.
|
Яичники, полученные post mortem Кфж = 33,14 нг/мл* |
EMB фолликулы NEMB фолликулы щий гормон |
(48) |
|
|
Фолл |
ЭД/ПГ = 0,226* Кфж = 3,73 нг/мл* ЭД/ПГ = 0,024* икулостимулирую |
||
|
Голштинская порода (телки) |
Пик концентрации: Кск = 0,29±0,02 нг/мл* Кск = 0,41±0,04 нг/мл* |
d ф > 5 мм: n Ф = 11,0±0,1 n Ф = 5,7±0,2 |
(53) |
|
Голштинская порода японской |
Обратная зависимость |
n Ф = 13,6±7,6 против |
(31) |
|
селекции (нестельные коровы) |
К ПЛ ** |
n Ф = 59,2±13,1 |
|
|
Молочный скот (не лактирующие коровы) |
Обратная зависимость* |
n Ф > 30 |
(54) |
|
Кроссбредные герефорды (лактирующие коровы) |
Обратная зависимость* |
n Ф = 46,2±2,1 n Ф = 18,6±1,1 |
(55) |
|
Мясной скот (телки) |
Обратная зависимость n Ф > 25 (р < 0,03) n Ф < 15 n Ф < 15 Антимюллеров гормон |
(8) |
|
|
Голштинская порода бразильской селекции |
К СК > M К СК < M |
n Ф = 20,9±1,5 **** n ОКК = 17,3±1,5 **** n БЛ = 3,0±0,7 * n Ф = 13,6±0,9 **** n ОКК = 9,0±0,9 **** n БЛ = 1,2±0,3 * |
(64) |
|
Высокопродуктивные молочные коровы |
Кпл = 0,01-374,3 пг/мл Кпл = 44,9±6,9 пг/мл (0,01-82,6 пг/мл) Кпл = 114,1±3,3 пг/мл (91,1-132,5 пг/мл) Кпл = 155,6±3,8 пг/мл (135,3-183,8) пг/мл) Кпл = 243,1±14,3 пг/мл (184,4-374,3 пг/мл) |
n cl: r = 0,65 ** n эмб: r = 0,50 ** n CL = 12,0±1,5 a,b n О + n ЭМБ = 5,0±1,2a,b n ЭМБт = 3,1±0,8 e n CL = 14,7±2,0с n О + n ЭМБ = 5,5±1,3с n ЭМБт = 3,8±1,2 f n CL = 17,2±1,2a,d n О + n ЭМБ = 7,2±1,2a,d n ЭМБт = 4,4±1,1 g n CL = 25,6±2,5 b,c,d n О + n ЭМБ = 14,0±2,3 b,c,d n ЭМБт = 7,2±1,4 e,f,g |
(74) |
|
Голштинская порода немецкой |
Кпл = 0,368±0,028 нг/мл |
n Ф : r = 0,45 *** |
(77) |
|
селекции (телки) |
(0,091-1,391 нг/мл) Кпл ≤ 25 % Кпл = 0,185±0,011 нг/мл 25 % < Кпл < 75 % Кпл = 0,321±0,001 нг/мл Кпл ≥ 75 % Кпл = 0,634±0,073 нг/мл |
n ОКК : r = 0,43 *** n БЛ : r = 0,28 * n Ф = 7,7±0,6 ** n ОКК = 5,7±0,5 ** n БЛ = 1,1±0,3 n ЭМБ = 3,9±1,1 n ЭМБт = 3,3±1,1 n Ф = 9,9±0,8 n ОКК = 7,4±0,6 n БЛ = 1,3±0,2 n ЭМБ = 4,3±0,8 n ЭМБт = 3,0±0,5 n Ф = 11,9±2,0 ** n ОКК = 8,2±0,8 ** n БЛ = 1,4±0.2 n ЭМБ = 5,4±1,3 n ЭМБт = 3,7±0,8 |
|
|
Тагильская порода (лактирующие коровы) |
Кск = 0,562±0,011 нг/мл Кск = 0,796±0,023 нг/мл Кск = 1,170±0,044 нг/мл |
n Ф = 9,20±1,39 СИ = 65,91±21,59 % n ОКК = 5,80±0,86 n БЛ = 1,00±0,32 %бл = 31,25±20,73 % n Ф = 9,42±0,80 СИ = 46,88±9,43 % n ОКК = 4,17±0,58 n БЛ = 1,06±0,44 %бл = 30,51±8,86 % n Ф = 10,75±1,38 |
(98)1 |
СИ = 44,19±24,83 % n ОКК = 4,75±1,32
n БЛ = 1,67±0,88 %бл = 45,45±28,75 %
|
К СК = 1,509±0,033 нг/мл n Ф = 11,67±1,49 СИ = 46,67±16,63 % n ОКК = 5,44±0,90 n БЛ = 1,56±0,52 %бл = 42,42±16,47 % |
|
|
Нелоре (Nelore) |
К СК > M n Ф = 54,3±6,1**** (64) n ОКК = 45,3±6,4**** n БЛ = 7,0±1,7** К СК < M n Ф = 18,6±2,1**** n ОКК = 13,4±1,7**** n БЛ = 2,2±0,5 %** |
|
Мясной скот Ханву (Hanwoo) (коровы) |
К ПЛ < 0,10 нг/мл n Ф = 12,19±2,14e,f (78) n ОКК = 4,77±0,44 e, f n БЛ = 2,2±0,3e,f 0,10 < К ПЛ < 0,25 нг/мл n Ф = 16,91±1,52e n ОКК = 7,38±0,83e n БЛ = 6,9±0,6e К ПЛ 0,25 нг/мл n Ф = 20,40±1,36f n ОКК = 11,46±1,22f n БЛ = 3,9±0,2f |
|
Японский черный скот |
К ПЛ = 0,434±0,376 нг/мл n О + n ЭМБ : p < 0,001 (76) n эмб: p < 0,001 n ЭМБт : p < 0,001 Кисспептин |
|
Голштинская порода турецкой селекции (лактирующие коровы) |
Кск = 80,58±4,4 пг/мл*** Стельные после ИО (85) Кск = 66,68±2,5 пг/мл*** Нестельные после ИО |
Примечание. ИО — искусственное осеменение, Кпл — концентрация гормона в плазме крови,
Кск — концентрация гормона в сыворотке крови, Кфж — концентрация гормона в фолликулярной жидкости, ОКК — ооцит-кумулюсные комплексы, ПГ — прогестерон, СИ — степень извлечения ОКК из фолликулов, ЭД/ОКК — отношение концентрации эстрадиола в сыворотке крови к числу извлеченных ОКК, ЭД/ПГ — отношение концентрации эстрадиола к прогестерону, d ф — диаметр фолликула, EMB/NEMB фолликулы — фолликулы, извлеченные из которых ОКК развились/не развились in vitro до стадии бластоцисты, М — среднее значение; n БЛ — число in vitro эмбрионов, достигших стадии бластоцисты, n окк — число извлеченных ОКК, n ОККп — число пригодных ОКК, n Ф — число фолликулов, n эмб — число вымытых эмбрионов, n ЭМБт — число эмбрионов, пригодных для трансплантации, n CL — число желтых тел; % Д — доля подробившихся зигот; % БЛ — доля полученных бластоцист; % БЛв — доля вылупившихся бластоцист.
-
**** p < 0,0001; *** p < 0,001; ** p < 0,01; * p < 0,05; различия между показателями, маркированными одинаковыми надстрочными буквами, достоверны при a,b,c,d p < 0,01, e,f,g p < 0,05; 1 — приведены расширенные результаты исследований.
Таким образом, проведенный нами анализ источников литературы показал наличие ряда ассоциаций между содержанием половых гормонов и эффективностью вспомогательных репродуктивных технологий, включая технологию OPU/IVP, у разных пород европейского ( Bos taurus ) и зебу-видного ( Bos indicus ) крупного рогатого скота. Установлены связи с результативностью вспомогательных репродуктивных технологий содержания в фолликулярной жидкости и/или крови прогестерона, эстрадиола-17 β , фолликулостимулирующего гормона и антимюллерова гормона. Высокая индивидуальная вариабельность результативности технологии OPU/IVP как в отношении числа извлекаемых ооцит-кумулюсных комплексов, так и их компетенции к эмбриональному развитию в условиях in vitro позволяет рекомендовать проведение мониторинга концентрации половых гормонов в сыворотке крови самок для их отбора в качестве доноров для программ OPU/IVP. Этому должны предшествовать исследования на различных породах крупного рогатого скота с учетом возраста и физиологического состояния доноров, а также технологических режимов их использования.


