Ретроградная трансвенозная абляция этанолом рефрактерных желудочковых аритмий
Автор: Королев С.В., Таварес Л., Вальдеррабано М., Хабазов Р.И., Троицкий А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 2 т.16, 2021 года.
Бесплатный доступ
Описана модифицированная технология ретроградной трансвенозной этанольной абляции при лечении рефрактерных желудочковых аритмий. Данный метод отличается от ранее опубликованного дробным многократным введением этанола с целью создания стойкой редукции аритмогенного миокарда.
Этанольная абляция, катетерная абляция, желудочковые нарушения ритма
Короткий адрес: https://sciup.org/140260116
IDR: 140260116 | DOI: 10.25881/20728255_2021_16_2_93
Retrograde transvenous ethanol ablation of refractory ventricular arrhythmias
The article describes the modified technology of retrograde transvenous ethanol ablation for the treatment of refractory ventricular arrhythmias. This method differs from the previously published fractional repeated administration of ethanol in order to create a stable reduction of arrhythmogenic myocardium.
Текст научной статьи Ретроградная трансвенозная абляция этанолом рефрактерных желудочковых аритмий
Предпосылки и перспективы метода
Радиочастотная катетерная абляция (РЧКА) считается эффективным методом первой линии для лечения рефрактерных желудочковых аритмий (ЖА) [1]. Тем не менее, в долгосрочной перспективе показатель успешной РЧКА, измеренный с точки зрения свободы от любой рецидивирующей ЖА, остается неоптимальным. [2]. Мало что известно о причине рецидива ЖА после острой «успешной» РЧА. Так, продолжающееся ремоделирования левого желудочка может привести к образованию нового субстрата у больных после инфаркта миокарда (ИМ) с желудочковыми тахикардиями (ЖТ). Также возможно, учитывая плохую ее воспроизводимость при индукции, что клинически значимое ЖТ может не проявляться во время электрофизиологического исследования. Известно, что большинство «re-entry» после ИМ являются субэндокардиальными, эффективность РЧ воздействия может быть ограничена наличием субэндокардиального фиброза, а не трансмуральное повреждение способствует возникновению рецидивов того же клинического ЖТ после абляции. Некоторые субстраты ЖТ могут быть интрамиокардиальными или эпикардиальными, ограничивая доставку РЧ энергии катетером только с одной стороны ЛЖ. Кроме того, РЧКА субстрата ЖА, локализованных в непосредственной близости от коронарных артерий, может быть сопряжена с развитием серьезных осложнений [3]. Одним из методов, позволяющих редуцировать аритмогенный субстрат в глубоких слоях миокарда, является химическая абляция этанолом. Изначально был предложен трансартериальный подход доставки этанола, однако он был сопряжен с развитием осложнений, присущим эндоваскулярным операциям на коронарных артериях — диссекция артерий, повреждения коллатералей и пр. [4]. Позднее был предложен ретроградный трансвенозный метод доставки этанола [5]. В этом исследовании показано, что этанол в высоких концентрациях повреждает клеточные мембраны и вызывает нарушения сложных белковых структур, что приводит к немедленному разрушению клеток и элиминации очага аритмии. Однако ряд технических аспектов вопросов, таких как картирование субстрата, доступ и к целевой вене, а так же количество этанола нужного для редукции аритмогенного очага оставалось дискутабельным. Описана модифицированная технология ретроградной трансвенозной этанольной абляции (РТАЭ) в лечении рефрактерных ЖА.
Описание метода
Для обеспечения стабильного доступа к коронарному синусу (КС) проводится интрадьюсер 8F (Preface, Biosense Webster или SL1, Abbott) через правую бедренную вену и позиционируется как можно более дистальнее в

устье КС. Затем, через установленный интрадьюсер проводится многополюсный навигационный катетер через большую вену сердца (БВС), достигая проксимального отдела передней нисходящей вены (ПНВ). Далее приступают к предварительному картированию. Используемые методы для определения оптимальной зоны воздействия включают в себя активационное и стимуляционное картирование, а также их соотношение с 3D электроанато-мической реконструкцией (CARTO, Biosense Webster; или Ensite Precision, Abbot). Многополюсные навигационные катетеры не могут проникать в небольшие коронарные вены, но позволяют обозначить границы той области, внутри которой нужно производить поиск целевой вены, максимально близко подходящей к аритмогенному субстрату миокарда (Рис. 1А и 2B–С).
После предварительного определения участка эктопической желудочковой активности с помощью 3D электроанатомического картирования из области БВС/ПНВ выполняется коронаровенография с целью оценки венозного русла и определения венул, подходящих к аритмогенному субстрату (Рис. 1С и 2F). Для лучшего контрастирования венозного русла можно использовать окклюзирующий баллон. Одним из важных моментов операции является получение лучшей рентгеноскопической проекции интересующей зоны. При локализации субстрата в проксимальном отделе саммита левого желудочка (ЛЖ) в области отхождения диагональных ветвей ПНВ используется левая косая каудальная проекция (Рис. 1D), а при локализации в дистальной части саммита или перегородочной области ЛЖ в области отхождения септальных ветвей ПНВ используется правая косая каудальная проекция (Рис. 2G).
Активационное и стимуляционное картирование, а также селективное канюлирование целевых венул достигаются путем продвижения проводника (Balance Middleweight 0,014 дюйма; Abbott, Santa Clara, CA) в вену по проводниковому катетеру для ангиопластики (JR4, Boston Scientific, Marlborough, MA) (Рис. 2G), который
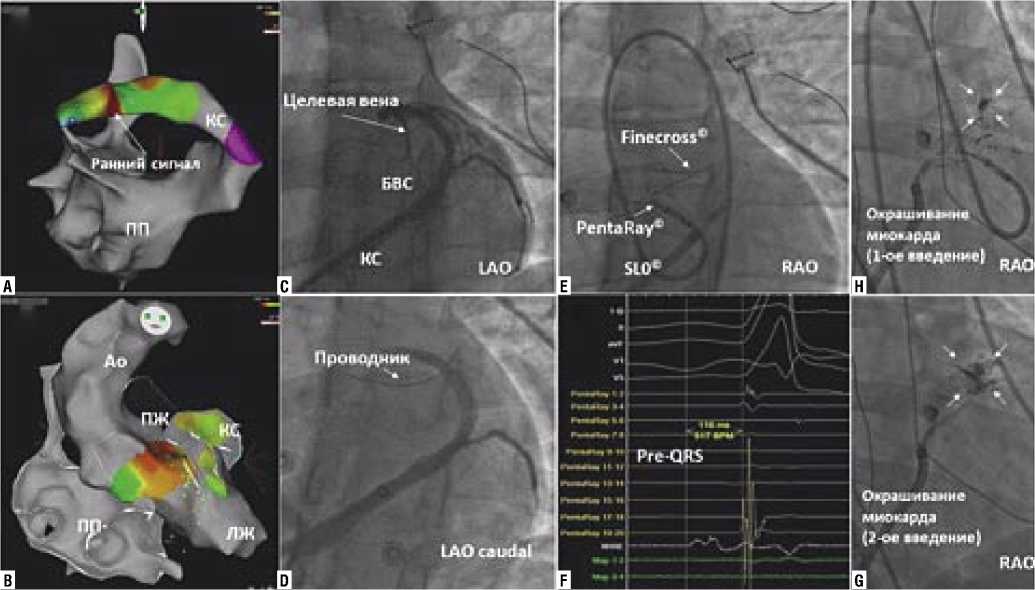
Рис. 1. Успешная ретроградная трансвенозная абляция этанолом эктопии ЖЭС, локализованной в области антеробазальной части ЛЖ (саммит). А: 3D картирование, показывающее наиболее раннее время активации в передней нисходящей вене. B: 3D- картирование полостей сердца, показывающее область ранней активации со стороны эндокарда. C: Венография КС, выполняемая для выявления потенциальных целевых венул, которые могут обеспечить доступ к субстрату ЖЭС в области саммита ЛЖ. D: Определяется потенциальная целевая диагональная венула. Для получения монополярного сигнала в нее проведен проводник. E,F: (E) Рентгеноскопические проекции, показывающие положение многополюсного электрофизиологического катетера (PentaRay) и катетера для ангиопластики внутри венулы (Finecross), а так же (F) соотношение полученных с них электрофизиологических потенциалов. При этом регистрируется самый ранний сигнал, предшествующий комплексу QRS на 116 мс, полученный с проводника (WIRE), который расположен на 3 мм дистальнее кончика катетера Finecross. H: Селективное контрастирование венулы через катетер Finecross после первой инъекции этанола, окрашивание миокарда указывает на достижение этанола целевого участка миокарда. G: Селективное контрастирование венулы через катетер Finecross после второй инъекции этанола, определяется более широкая зона окрашивания миокарда. Ао — аорта, ПЖ — правый желудочек, ПП — правое предсердие, ЖЭС — желудочковая экстрасистолия. ная вена; LAD = левая передняя нисходящая коронарная артерия; LAO = левая передняя косая проекция, RAO = правая передняя косая проекция.

обеспечивает стабильность и управляемость системы «баллон-проводник». Баллон для ангиопластики (рекомендованный размер 6 x 2 мм) продвигают по проводнику таким образом, чтобы дистальный кончик проводника оставался открытым (≈ 3 мм). Ангиографический проводник подключается к электрофизиологической станции с помощью зажима типа «крокодил», и конфигурируется как униполярный электрод. В качестве референтного электрода используется любой электрофизиологический катетер, размещенный в нижней полой вене. Электрофизиологическое подтверждение целевой вены производится с помощью оценки униполярного сигнала с кончика проводника активационным и стимуляционным картированием.
После элетрофизиологического подтверждения оптимально выбранной целевой венулы удаляется проводник, проводится раздувание баллона для ангиопластики и вводится рентгенконтрастное вещество с целью определения размера венулы, наличие коллатералей и степени окрашивания миокарда, что позволяет предварительно оценить объем его химического повреждения. Важно отметить, что венула может признаться не пригодной для химической абляции из-за наличия коллатералей ведущих обратно в КС, минуя миокард. Первоначально вводят 1 мл 95–98% этанола (Alkohol-Konzentrat 95%, Braun (в настоящее время препараты не зарегистрированы на территории РФ). После инфузии этанола баллон для ангиопластики остается раздутым до тех пор, пока не будет оценен эффект на введение. После положительной оценки первого введения (отсутствие активности субстрата) вводят контрастное вещество для определения объема редуцированного миокарда — определяется замедление пассажа контрастного вещества в этой области (Рис. 1H). Далее, повторно трижды медленно (примерно в течение 2 минут) вводят 1 мл этанола с интервалом 3–5 минут между введениями. Повторные инъекции необходимы для закрепления эффекта, поскольку после однократного введения может повреждаться только «венозный компонент» ткани миокарда, тогда как «артериальный компонент» остается неповрежденным. После заключительного введения этанола выполняют контрольное контрастирование, при котором определяется более интенсивное и объемное окрашивание миокарда (Рис. 1G).
Сочетания методов радиочастотной и этанольной абляции
На рисунке 2 представлен пример РТАЭ пациента после неэффективной РЧКА. В этом случае эндокарди-ально выявлено опережение QRS комплекса со стороны ПЖ на 15 мс и отсутствие опережения со стороны ЛЖ. Выполнены РЧ — воздействия в точках максимального pre-QRS ПЖ, однако, элиминации эктопического очага получено не было. При картировании из БВС и ПНВ определяется более ранняя активация эктопической области (Рис. 2B и 2C). При дальнейшем селективном картировании с помощью ангиопластического проводника BMW (Abbott) (Рис. 2G) выявлена ветвь ПНВ с
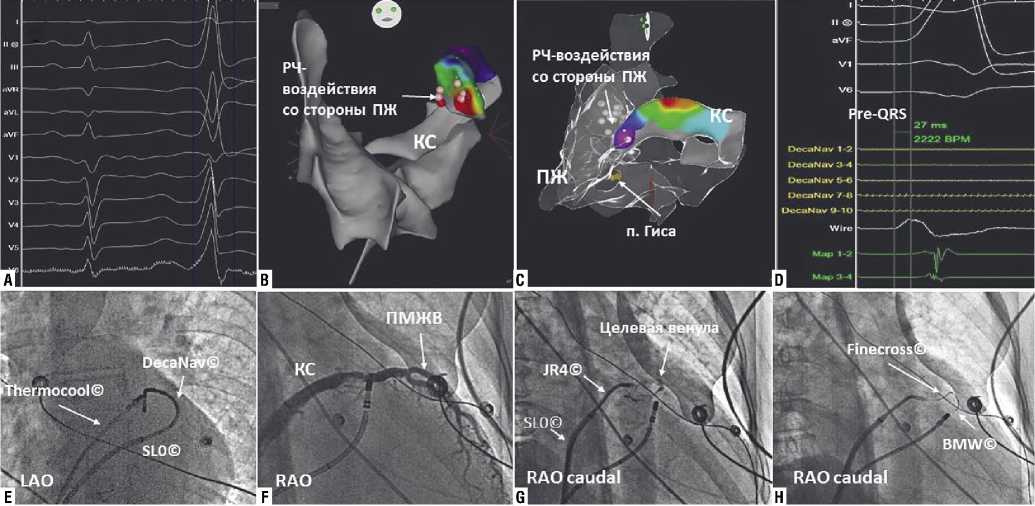
Рис. 2. Пример гибридной операции. Успешная венозная абляция этанолом ЖЭС через септальную ветвь ПНВ (объяснения в тексте) после неэффективных РЧ-воздействий. A: ЭКГ с эктопической с желудочковой активностью. B, C: 3D реконструкция, показывающая самое раннее время активации в ПНВ и нанесенные ранее РЧ-воздействия со стороны эндокарда ПЖ. D: Наиболее ранняя активация ЖЭС (pre-QRS-30 мс) определенная в целевой вене (Wire). E: Рентгеноскопическая проекция, на которой показано положение многополярного картирующего электрофизиологического катетера в месте ранней активации. F: Этап коронаровенографии, выполненной для оценки венозного русла и определения целевых ветвей. G: Селективное контрастирование потенциальной целевой ветви, выявляется венула, исходящая из ПНВ (септальная ветвь). H: Позиционирование авгиопласти-ческого катетера (Finecross) в целевой вене для выполнения химической абляции.
сигналом опережающим комплекс QRS на 30 мс (Рис. 2D) с последующим введением в нее этанола (Рис. 2F) и купированием эктопической активности.
Преимущества и недостатки метода
Ранее были опубликованы данные мультицентрового исследования с подробным описанием характеристик пациентов [5]. По данному методу в различных медицинских учреждениях прооперировано 63 пациента с ЖА, резистентной к медикаментозной терапии и РЧКА. Проведение операции РТАЭ для каждого пациента было одобрено местным этическим комитетом. Все пациенты дали согласие на абляцию этанолом. РТАЭ применялось только у пациентов, у которых определялось оптимальное опережение pre-QRS эктопического сигнала в коронарных венах. Интраоперационная эффективность оценивалась как положительная в случае полного прекращения ЖА, у пациентов у которых не наступала элиминация ЖА процедура признавалась неэффективной. После завершения РТАЭ пациенты наблюдались в операционной на предмет возможного рецидива не менее 30 минут. Общее время наблюдения за пациентами после лечения составило 12 месяцев, оценка эффективности операции производилась ежемесячно на основании субъективных жалоб пациента, анализа ЭКГ и суточного ХМ-ЭКГ. Эффективность в «остром» периоде достигнута у 56 больных (98%). Отсутствие ЖА после РТАЭ через год наблюдалось у 43 пациентов (78%) (Рис. 3). В 5% случаев (3 пациента) наблюдалось осложнение в виде развития гемоперикарда из-за повреждения вен инструментами при манипуляциях. Осложнений, связанных с введением этанола, не отмечалось.
Недостатком этого метода является вариация анатомии коронарных вен. Электрофизиологическая цель операции может быть достигнута только в том случае, если подходящая вена располагается в непосредственной близости от эктопического очага. Кроме того, наличие вено-венозных коллатералей так же может повлиять
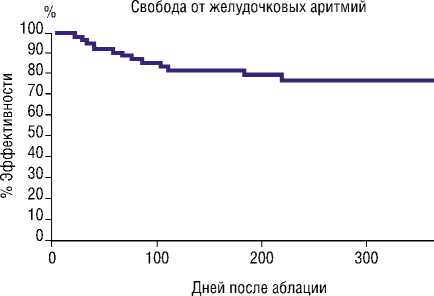
Рис. 3. (Адаптировано из Tavares L et al. JACC. 2020) Оценка эффективности операции по методу Каплана-Мейера. Эффективность операции после 12 месяцев наблюдения составила 78%.
на успех операции, так как в этом случае происходит сброс этанола в обход целевого участка миокарда. Важным аспектом является размер вены, в случае наличия интрамуральных вен крупного диаметра, оптимальное опережение комплекса QRS может регистрироваться в проксимальной ее части, что делает невозможным окклюзию вены для введения этанола. Осложнением, непосредственно связанным с этим методом абляции, может являться развитие гемоперикарда в следствии дис-секциии вены сердца при манипуляциях инструментами. Так же от хирурга требуется умение владеть навыками в области рентгенэндоваскулярной хирургии включающие выполнение венографии КС, селективное канюлирование вен и инфляцию баллонов для ангиопластики.
Обсуждение
Наиболее часто используемым методом абляции различных желудочковых аритмий остается РЧКА. Доказано, что эффективность РЧКА составляет 81% при лечении ЖТ в «остром» периоде [6], и около 49% в течение среднесрочного наблюдения [7]. К другим методам, набирающим популярность в этом отношении, относятся криоаблация, лазерная абляция и сфокусированный ультразвук высокой интенсивности [8–15]. Все эти вмешательства, как и РЧКА, требуют непосредственного контакта аблационного катетера с миокардом для устранения аритмий. Однако, аритмогенный субстрат при желудочковых аритмиях может быть локализован со стороны эндокарда [16]. Хотя доступ к эпикарду достаточно широко применяется с помощью субксифоидной техники, но он может быть затруднен в следствии развития спаечного процесса у пациентов после кардохирургических операций [16]. Кроме того, не редко субстрат желудочковых аритмий располагается в интрамуральном слое миокарда, что затрудняет его редукцию с помощью «контактных» катетеров. [17–19]. Аритмии, возникающие из области саммита ЛЖ, являются особенно сложными для РЧКА, обуславливается это тем, что их источник не только может располагаться интрамурально но и граничить с коронарными артериями, что не позволяет безопасно выполнить РЧКА через эпикардиальный доступ [20–22]. Одной из перспективных технологий, обеспечивающих редукцию целевого участка миокарда, является химическая аблация через сосуды сердца. Использование этанола для абляции предшествовало развитие РЧКА [23–26]. Первая успешная трансартериальная этанольная абляция описана Brugada et al. в 1989 г. у троих больных с ЖТ [27].
Kay et al. [26] сообщили о трансартериальной абляции этанолом у 10 пациентов с эффективностью 90% в остром периоде. Однако при таком подходе часто развивались серьезные осложнения такие как полная атриовентрикулярная блокада, перикадит, диссекция коронарных артерий, повреждение не целевого миокарда, приводящего к инфаркту [24–26]. Кроме того, у больных с ишемической болезнью сердца данная методика ограничена трудностью доставки этанола к миокарду из-за
стенозов коронарных артерий [23]. Чтобы нивелировать осложнения связанные с трансартериальной методикой и упростить операцию был предложен ретроградный доступ через вены сердца эффективность и безопасность которого была доказана на животных [28]. По нашему опыту, РТАЭ доказала свою высокую эффективность в лечении желудочковых аритмий.
Заключение
РТАЭ является практически осуществимым методом, и его можно будет рассмотреть как один из вариантов лечения рефрактерных к лекарственной терапии и РЧКА желудочковых аритмий после регистрации необходимых компонентов для ее выполнения на территории РФ.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
doi: 10.1016/j.hrthm.2015.08.030.
Список литературы Ретроградная трансвенозная абляция этанолом рефрактерных желудочковых аритмий
- Cronin E, Bogun F, Maury P, et al. 2019 HRS/EHRA/APHRS/LAHRS expert consensus statement on catheter ablation of ventricular arrhythmias. EP Europace. 2019; 21(8): 1143-1144. doi:10.1093/europace/ euz132.
- Kuck KH, Schaumann A, Eckardt L, et al, VTACH study group (2010) Catheter ablation of stable ventricular tachycardia before defibrillator implantation in patients with coronary heart disease (VTACH): a multicentre randomised controlled trial. Lancet. 375: 31-34.
- Baher A, Shah DJ, Valderrabano M, et al. Coronary venous ethanol infusion for the treatment of refractory ventricular tachycardia. Heart Rhythm. 2012; 9: 1637-1639, doi: 10.1161/CIRCEP.116.004352.
- Schurmann P, Penalver J, Valderrabano M, et al. Ethanol for the treatment of cardiac arrhythmias. Curr Opin Cardiol 2015, 30333-343, doi:10.1161/ CIRCEP.116.004352.
- Tavares L, Valderrabano M. Retrograde venous ethanol ablation for ventricular tachycardia. Heart rhythm. 2018; 16: 478-483. doi: 10.1016/j.hrt-hm.2018.09.010.
- Tavares L, Lador A, Fuentes S, et al. Intramural Venous Ethanol Infusion for Refractory Ventricular Arrhythmias: Outcomes of a Multicenter Experience. JACC: Clinical Electrophysiology. 2020; 6. doi:10.1016/j.jacep.2020.07.023.
- Haqqani HM, Roberts-Thomson KC. Radiofrequency catheter ablation for ventricular tachycardia. Heart Lung Circ. 2012; 21: 402-412. doi: 10.1016/ j.hlc.2011.10.015.
- Stevenson WG, Wilber DJ, Natale A, et al. Irrigated radiofrequency catheter ablation guided by electroanatomic mapping for recurrent ventricular tachycardia after myocardial infarction: The multicenter thermocool ventricular tachycardia ablation trial. Circulation. 2008, 118: 2773-2782. doi: 10.1161/ CIRCULATI0NAHA.108.788604.
- Koruth JS, Dukkipati S, Carrillo RG, et al. Safety and efficacy of high-intensity focused ultrasound atop coronary arteries during epicardial catheter ablation. J Cardiovasc Electrophysiol. 2011, 22: 1274-1280. doi: 10.1111/ j.1540-8167.2011.02084.x.
- Vincent GM, Fox J, Benedick BA et al. Laser catheter ablation of simulated ventricular tachycardia. Lasers Surg Med. 1987, 7: 421-425. doi: 10.1002/ lsm.1900070508.
- Nakano H, Koyanagi H, Endo M, et al. laser ablation in the treatment of ventricular tachycardia: Problems in the clinical case. Kyobu Geka. 1990, 43: 24-30. Available at: https://pubmed.ncbi.nlm.nih.gov/2304295.
- Saksena S, Gielchinsky I, Tullo NG. Argon laser ablation of malignant ventricular tachycardia associated with coronary artery disease. Am J Cardiol. 1989, 64: 1298-1304. doi: 10.1016/0002-9149(89)90571-7.
- Choi EK, Nagashima K, Lin KY, et al. Surgical cryoablation for ventricular tachyarrhythmia arising from the left ventricular outflow tract region. Heart Rhythm. 2015, 12: 1128-1136. doi: 10.1016/j.hrthm.2015.02.016.
- Di Biase L, Al-Ahamad A, Santangeli P, et al. Safety and outcomes of cryoablation for ventricular tachyarrhythmias: Results from a multicenter experience. Heart Rhythm. 2011, 8: 968-974. doi: 10.1016/j.hrthm.2011.02.038.
- Kumar S, Barbhaiya CR, Sobieszczyk P, et al. Role of alternative intervent-ional procedures when endo- and epicardial catheter ablation attempts for ventricular arrhythmias fail. Circ Arrhythm Electrophysiol. 2015, 8: 606615. doi: 10.1161/CIRCEP.114.002522.
- Uppu SC, Tuzcu V. Cryoablation of ventricular tachycardia arising from the left-coronary sinus cusp. Pediatr Cardiol. 2013, 34: 725-728. doi: 10.1007/ s00246-012-0331-7.
- Izquierdo M, Sanchez-Gomez JM, Ferrero de Loma-Osorio A et al. Endo-epicardial versus only-endocardial ablation as a first line strategy for the treatment of ventricular tachycardia in patients with ischemic heart disease. Circ Arrhythm Electrophysiol. 2015, 8: 882-889. doi: 10.1161/ CIRCEP.115.002827.
- Chen H, Shehata M, Swerdlow C, et al. Intramural outflow tract ventricular tachycardia: Anatomy, mapping, and ablation. Circ Arrhythm Electrophysiol. 2014, 7: 978-981. doi: 10.1161/CIRCEP.114.001744.
- Abdel Wahab A, Stevenson W, Thompson K, et al. Intramural ventricular recording and pacing in patients with refractory ventricular tachycardia: Initial findings and feasibility with a retractable needle catheter. Circ Arrhythm Electrophysiol. 2015, 8: 1181-1188. doi: 10.1161/CIRCEP.115.002940.
- Yamada T, Maddox WR, McElderry HT, et al. Radiofrequency catheter ablation of idiopathic ventricular arrhythmias originating from intramural foci in the left ventricular outflow tract: Efficacy of sequential versus simultaneous unipolar catheter ablation. Circ Arrhythm Electrophysiol. 2015, 8: 344-352. doi: 10.1161/CIRCEP.114.002259.
- Baldinger SH, Kumar S, Barbhaiya CR et al. Epicardial radiofrequency ablation failure during ablation procedures for ventricular arrhythmias: Reasons and implications for outcomes. Circ Arrhythm Electrophysiol. 2015, 8: 1422-1432. doi: 10.1161/CIRCEP.115.003202.
- Lin CY, Chung FP, Lin YJ, et al. Radiofrequency catheter ablation of ventricular arrhythmias originating from the continuum between the aortic sinus of valsalva and the left ventricular summit: Electrocardiographic characteristics and correlative anatomy. Heart Rhythm. 2015, 13: 111-121. doi: 10.1016/j.hrthm.2015.08.030.
- Hutchinson MD, Garcia FC. An organized approach to the localization, mapping, and ablation of outflow tract ventricular arrhythmias. J Cardiovasc Electrophysiol. 2013, 24: 1189-1197. doi: 10.1111/jce.12237.
- Delacretaz E, Seiler J, Tanner H, et al. Ablation of ventricular tachycardia: Neither inside nor out, thus back to alcohol. Heart Rhythm. 2006, 3: 1230-1231. doi: 10.1016/j.hrthm.2006.06.014.
- Haines DE, Whayne JG, DiMarco JP. Intracoronary ethanol ablation in swine: Effects of ethanol concentration on lesion formation and response to programmed ventricular stimulation. J Cardiovasc Electrophysiol. 1994, 5: 422-431. doi: 10.1111/j.1540-8167.1994.tb01181.x.
- Inoue H. Can chemical ablation of ventricular myocardium with ethanol surpass radiofrequency catheter ablation? J Cardiovasc Electrophysiol. 1998, 9: 985-987. doi: 10.1111/j.1540-8167.1998.tb00139.x.
- Kay GN, Epstein AE, Bubien RS, et al. Intracoronary ethanol ablation for the treatment of recurrent sustained ventricular tachycardia. J Am Coll Cardiol. 1992, 19: 159-168. doi: 10.1016/0735-1097(92)90068-x.
- Brugada P, de Swart H, Smeets JL, et al. Transcoronary chemical ablation of ventricular tachycardia. Circulation. 1989, 79: 475-482. doi: 10.1161/01. cir.79.3.475.
- Wright KN, Morley T, Bicknell J, et al. Retrograde coronary venous infusion of ethanol for ablation of canine ventricular myocardium. J Cardiovasc Electrophysiol. 1998, 9: 976-984. doi: 10.1111/j.1540-8167.1998.tb00138.x.


