Ретроспективный анализ по сравнению эффективности химиотерапии и таргетной терапии метастатической феохромоцитомы
Автор: Жуликов Я.А., Коваленко Е.И., Галанова К.Н., Тятюшкина А.Н., Евдокимова Е.В., Маркович А.А., Бохян В.Ю., Рослякова А.А., Мартынова О.А., Делекторская В.В., Перегородиева С.С., Тамразова М.Р., Артамонова Е.В.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.14, 2024 года.
Бесплатный доступ
Введение: Феохромоцитома (ФХ) и параганглиома (ПГ) относятся к группе редких опухолей нейроэндокринной природы, источником которых служат хромаффинные клетки. Основные опции лекарственной терапии ФХ/ПГ — химиотерапия (ХТ) на основе алкилирующих препаратов и таргетная терапия сунитинибом. Сравнительных данных по эффективности этих опций нет, что и стало целью данного исследования. Материалы и методы: В данное ретроспективное одноцентровое исследование включены пациенты старше 18 лет, получившие ХТ или таргетную терапию в первой линии лечения метастатической ФХ/ПГ с сентября 2015 по август 2023. Результаты: В исследование включено 33 пациента, которые были разделены на две группы — ХТ (N = 18, 54,5%) и таргетной терапии (N = 15, 45,5 %). В группе ХТ 12 пациентов (66,7%) получили терапию по схеме CVD, 6 (33,3%) — темозоломид. В группе таргетной терапии сунитиниб получили 10 пациентов (66,7%), пазопаниб — 4 (26,7%), эверолимус — 1 (6,7%). Конкурентная терапия аналогами соматостатина в группах ХТ и таргетной терапии проводилась 12 (66,7%) и 10 (66,7%) пациентам. Группы были сопоставимы по всем основным характеристикам. Объективный ответ был достигнут у 11,11% (N = 2) и 6,67% (N = 1) [р=0,99], контроль болезни > 6 мес. — 61,11% и 60% (р = 0,99), биохимический ответ — 36,36% и 30% (р = 0,9) в группах ХТ и таргетной терапии соответственно. Медиана ВБП составила 12,7 мес. (2,9-22,3) в группе ХТ против 12,9 мес. (2,3-26,5) в группе таргетной терапии (р = 0,55). Медиана общей выживаемости не была достигнута ни в одной из групп. Обсуждение: Учитывая сопоставимую эффективность обеих лекарственных опций, индолентное течение болезни, большинство пациентов не нуждаются в назначении ХТ в 1 линии. При выборе терапии у пациентов в первую очередь необходимо учитывать профиль безопасности препаратов.
Феохромоцитома, параганглиома, сунитиниб, нейроэндокринные опухоли, химиотерапия
Короткий адрес: https://sciup.org/140310088
IDR: 140310088 | DOI: 10.18027/2224-5057-2024-016
Efficacy of chemotherapy and targeted therapy for metastatic pheochromocytoma / paraganglioma: retrospective analysis
Introduction: Pheochromocytoma (PC) and paraganglioma (PG) are rare neuroendocrine tumors derived from adrenal chromaffin cells. The main options of systemic therapy for PC / PG are alkylating agent-based chemotherapy (ChT) and targeted therapy with sunitinib. There are no comparative data on the efficacy of these options, which became the purpose of this study.Materials and methods: This retrospective single-center study included patients over 18 y. o. who received ChT or targeted therapy for the first line treatment for metastatic PC / PG from September 2015 to August 2023.Results: The study included 33 patients (pts) who were divided into two groups — ChT (N = 18, 54.5 %) and targeted therapy (N = 15, 45.5%). In the ChT group, 12 pts (66.7%) received CVD regimen, 6 (33.3%) — temozolomide. In the targeted therapy group, 10 pts (66.7%) received sunitinib, 4 (26.7%) — pazopanib, and 1 (6.7%) — everolimus. Concurrent somatostatin analogues therapy was prescribed in 12 (66.7%) and 10 (66.7%) pts in the ChT and targeted therapy groups, respectively. Both groups were comparable by all main characteristics. Objective response was achieved in 11.11 % (N = 2) and 6.67 % (N = 1) [p=0.99], disease control > 6 months — 61.11 % and 60% (p = 0.99), biochemical response — 36.36% and 30% (p = 0.9) in the ChT and targeted therapy groups, respectively. Median PFS was 12.7 (2.9-22.3) in the ChT versus 12.9 months (2.3-26.5) in the targeted therapy group (p = 0.55). Median overall survival was not reached in both groups.Discussion: According to comparable efficacy of both treatment options and the indolent course of PC / PG, most patients do not require ChT in the 1st line of treatment. While choosing the 1st line therapy it is necessary firstly to take into account the safety profile of the drugs.
Текст научной статьи Ретроспективный анализ по сравнению эффективности химиотерапии и таргетной терапии метастатической феохромоцитомы
Феохромоцитомы (ФХ) и параганглиомы (ПГ) относятся к группе редких опухолей нейроэндокринной природы, источником которых служат хромаффинные клетки [1]. Согласно классификации эндокринных опухолей ВОЗ 2017 г. (4 пересмотр), к ФХ относятся опухоли, исходящие из хромаффинных клеток мозгового слоя надпочечников, к ПГ — опухоли из пара- или симпатических ганглиев вненадпочеч-никовой локализации [2]. В зависимости от вида параганглия вегетативной нервной системы ПГ делят на симпатические и парасимпатические. По данным отдельных небольших популяционных исследований, частота ФХ/ПГ в популяции составляет от 2 до 8 случаев на 1 млн человек в год [3–6]. Однако, согласно различным аутопсийным данным, ФХ обнаруживаются в 0,05–0,13% случаев [7,8]. Около 30–45% случаев ФХ/ПГ связано с наследственными синдромами, для детской популяции этот показатель достигает 70 % [9–13]. Большинство ФХ и ПГ характеризуются индолетным течением, частота рецидива заболевания после радикального хирургического лечения составляет 10–15% при ФХ и достигает 30–35% при ПГ [13–14]. Самым неблагоприятным прогнозом с высоким риском метастазирования (до 40%) отличается мутация SDHB [15–16].
Арсенал системной терапии метастатической ФХ/ПГ состоит из аналогов соматостатина (данные экстраполированы из клинических рекомендаций по лечению нейроэндокринных опухолей), PRRT (пептидная рецепторная радиотерапия), таргетная терапия (сунитиниб) и химиотерапия на основе алкилирующих агентов (темозоломид или CVD — дакарбазин 600 мг/м2 в 1–2 дни, циклофосф- амид 750 мг/м2 в 1 день, винкристин 1,5 мг/м2 в 1 день, цикл 21 день) [17]. Исследований, напрямую сравнивающих эффективность данных подходов, нет, что обусловлено редкостью патологии. Европейские эксперты предлагают следующую последовательность терапии метастатической ФХ/ПГ: при индолентном течении — пептидная рецепторная радионуклидная терапия (PRRT) + аналоги соматостатина, сунитиниб, химиотерапия. При агрессивном течении приоритетной опцией лечения является назначение химиотерапии [18]. Молекулярно-генетических маркеров, позволяющих индивидуализировать лечение, также нет. Наличие герминальных мутаций SDHB, которые встречаются у 40–50 % пациентов с метастатической ФХ / ПГ, ассоциировано с неблагоприятным прогнозом, однако данные опухоли более чувствительны ко всем описанным выше вариантам терапии. Так, наличие мутаций в гене SDHB ассоциировано с метилированием MGMT и более высокой чувствительностью к химиотерапии, частота объективных ответов (ЧОО) в этой популяции достигает 50% (N = 5/10) против 0% в подгруппе SDHB wild type (wt) [19]. Потеря функции SDHB способствует накоплению сукцината, что приводит к псевдогипоксическому состоянию, гиперметилированию, неоангиогенезу и определяет потенциальную чувствительность к ингибиторам тирозинкиназ [18,20]. Подгрупповой анализ рандомизированного исследования FIRSTMAPPP, сравнивавшего эффективность сунитиниба по сравнению с плацебо, показал, что ЧОО в подгруппе с наличием герминальной мутации в гене SDHB составляет 50% (N = 6/12) против 22% при SDHB wt [21,22].
Кроме того, сравнительно недавно арсенал лечебных опций при диссеминированной ФХ/ПГ пополнился следую- щими таргетными препаратами: белзутифан у пациентов с наличием герминальных мутаций в гене VHL (также его эффективность изучается в когорте пациентов с VHLwt); селперкатиниб при герминальных/соматических мутациях в гене RET [23–25].
Учитывая отсутствие сравнительных данных по эффективности химиотерапии и таргетной терапии метастатической ФХ/ПГ, актуальной проблемой является выбор оптимального варианта терапии 1 линии, что и стало целью данного исследования.
МАТЕРИАЛЫ И МЕТОДЫ
В данное ретроспективное одноцентровое исследование включены пациенты старше 18 лет, получившие химиотерапию или таргетную терапию в первой линии лечения метастатической ФХ/ПГ с сентября 2015 по август 2023. Все блоки были пересмотрены в НМИЦ онкологии им. Н.Н. Блохина. У 16 пациентов (48,5%) был определен статус SDHB, из них методом иммуногистохимического исследования (ИГХ) у 13 и секвенирования нового поколения (NGS) — у 3.
Всем пациентам перед началом лечения выполнялось комплексное обследование — компьютерная томография (КТ) органов грудной клетки, брюшной полости и малого таза с внутривенным контрастом или позитронно-эмиссионная томография с фтордезоксиглюкозой или 68 Ga-DOTATATE. Всем пациентам перед началом терапии были определены фракционированные метане-фрин и норметанефрин суточной мочи (для сбора использовалась емкость с консервантом — лимонная кислота) или крови, хромогранин А крови. При превышении верхней границы нормы этих показателей далее продолжался контроль этих показателей каждые 2 месяца. Оценка эффективности терапии проводилась по критериям RECIST 1.1, также нами был оценен маркерный ответ, который был определен как снижение норметанефрина и метанефрина на ≥ 50%.
Все расчеты были выполнены в программе IBM SPSS Statistics Professional 26.0. Достоверность различий между количественными показателями вычисляли с помощью непараметрических критериев Манна–Уитни. Различия считали значимыми при р < 0,05. Для оценки показателей выживаемости без прогрессирования (ВБП) и общей выживаемости (ОВ) использовался метод Каплана–Майера.
РЕЗУЛЬТАТЫ
В исследование включено 33 пациента, которые были разделены на две группы — химиотерапии (ХТ: n = 18, 54,5%) и таргетной терапии (n = 15, 45,5%) в качестве первой линии лечения. В группе ХТ12 пациентов (66,7%) получили лечение по схеме CVD дакарбазин 600 мг/м2 в 1–2 дни, циклофосфамид 750 мг/м2 в 1 день, винкристин 1,5 мг/м2 в 1 день, цикл 21 день), 6 (33,3%) — темозоломид в метрономном режиме по 75 мг/м2 внутрь 1–21 дни, цикл 28 дней. В группе таргетной терапии сунитиниб в дозе 37,5 мг внутрь ежедневно получили 10 пациентов (66,7%), пазопаниб 800 мг в сутки — 4 (26,7%), эверолимус 10 мг в сутки — 1 (6,7 %). Конкурентная терапия аналогами соматостатина в группах химио- и таргетной терапии проводилась 12 (66,7%) и 10 (66,7%) пациентам соответственно (табл. 1).
Таблица 1. Режимы терапии
Table 1. Therapy regimens
|
Химиотерапия (n= 18) |
Таргетная терапия (n= 15) |
|||
|
n |
% |
n |
% |
|
|
Темозоломид |
6 |
33,33 |
||
|
CVD |
12 |
66,67 |
||
|
Сунитиниб |
10 |
66,67 |
||
|
Пазопаниб |
4 |
26,67 |
||
|
Эверолимус |
1 |
6,67 |
||
|
Конкурентная терапия аналогами соматостатина |
||||
|
Да |
12 |
66,67 |
10 |
66,67 |
|
Нет |
6 |
33,33 |
5 |
33,33 |
Характеристики пациентов представлены в таблице 2. Группы были сопоставимы по основным факторам. Большей части пациентов в анамнезе выполнялось удаление первичной опухоли — 88,89% (n = 16) в группе ХТ и 73,33% (n = 11) в группе таргетной терапии. Средний возраст составил 52,3 и 49,6 лет соответственно. В группе химиотерапии преобладали ФХ — 61,1 %, в группе таргетной терапии ПГ — 60 % (p < 0,05). Большая часть пациентов были женского пола — 66,7 и 73,3% в группах химио- и таргетной терапии. В группе ХТ наблюдалась тенденция к более высокому уровню индексу пролиферации ki67, среднее значение которого составило 14,8 и 9,6% соответственно (р = 0,4). Повышенная секреция катехоламинов наблюдалась у 61,1 % (n = 11) и 66,7% (n = 10) в группах химио- и тар-гетной терапии, эти пациенты были включены в анализ маркерного ответа на терапию. Секреция норметанефрина наблюдалась у 44,4 % (n = 8) и 46,7% (n = 7), метанефрина 16,67% (n = 3) и 20 % (n = 3) пациентов соответственно. В группе химиотерапии чаще наблюдалось метастатическое поражение костей — 50% против 26,67%. У половины пациентов был определен статус SDHB — 44,5 и 53,3 % пациентов в группах химиотерапии и таргетной терапии. Частота мутаций в гене SDHB составила 62,5 % (n = 5 / 8) против 25% (n = 2/8) соответственно (p = 0,31). При ПГ и ФХ частота мутаций в гене SDHB была несколько выше — 62,5% (n = 5/8) против 25 % (n = 2 / 8), хотя различия не достигли статистической значимости (p = 0,31).
Объективный ответ был достигнут у 11,11 % (n = 2) и 6,67 % (n = 1) в группах химио- и таргетной терапии (р = 0,99), в том числе у 1 пациента был достигнут пол-
Таблица 2. Характеристики пациентов
Table 2. Patient characteristics
Таблица 3. Ответ на терапию
Table 3. Response to therapy
|
Наилучший ответ |
Хим иотерапия (n=18) |
Таргетная терапия (n=15) |
p |
||
|
n |
% |
n |
% |
||
|
Прогрессирование |
6 |
33,33 |
3 |
20,00 |
|
|
Стабилизация |
9 |
50,00 |
10 |
66,67 |
|
|
Частичный ответ |
1 |
5,56 |
1 |
6,67 |
|
|
Полный ответ |
1 |
5,56 |
0 |
0,00 |
|
|
Объективный ответ |
2 |
11,11 |
1 |
6,67 |
0,99 |
|
Не оценен |
1 |
5,56 |
1 |
6,67 |
0,99 |
|
Контроль болезни ≥6 мес. |
11 |
61,11 |
9 |
60,00 |
0,99 |
|
Уменьшение метанефрина/ норметанефрина ≥50% |
4 |
36,36 |
3 |
30,00 |
0,9 |
При медиане наблюдения 15,1 мес. в группе химиотерапии и 13,4 мес. в группе таргетной терапии не наблюдалось различий в ВБП, медиана которой составила 12,7 (2,9–22,3) и 12,9 мес. (2,3–26,5) соответственно (р = 0,55, рис. 1). Медиана общей выживаемости не была достигнута ни в одной из групп (р = 0,42, рис. 2).
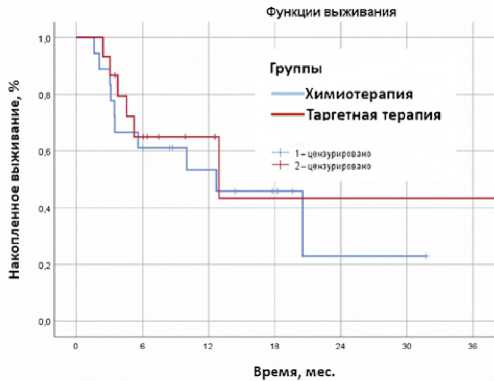
Рисунок 1. Выживаемость без прогрессирования
-
Figure 1. Progression-free survival
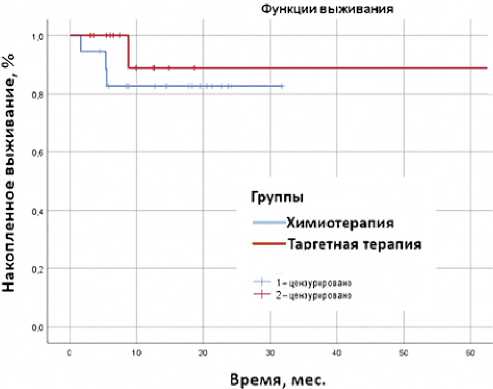
Рисунок 2. Общая выживаемость
-
Figure 2. Overall survival
ОБСУЖДЕНИЕ
В данном ретроспективном исследовании впервые проведено сравнение эффективности химио- и таргетной терапии в 1 линии лечения метастатической ФХ/ПГ. Частота объективного ответа была невысокой, существенно не различалась в группах химио- и таргетной терапии — 11,11% и 6,67% соответственно, у большей части пациентов наилучшим эффектом была стабилизация. Частота контроля болезни ≥ 6 мес. и биохимического ответа также не различались; медиана ВБП в обеих группах составила 12 мес. Большая часть пациентов в группе таргетной терапии полу- чали сунитиниб, данные по ВБП в нашем исследовании были несколько выше, чем в предыдущих работах, посвященных эффективности сунитиниба — 8,9 мес. в исследовании FIRSTMAPPP (21,22,26). Выживаемость пациентов в группе химиотерапии сопоставима с литературными данными (18,19). Медиана общей выживаемости при медиане наблюдения 15,1 и 13,4 мес. в обеих группах не была достигнута.
Существенными ограничениями данной работы являлись небольшой объем выборки, что обусловлено редкостью патологии, значимые различия между характеристиками групп — локализация первичной опухоли (ФХ/ПГ), неизвестный статус мутации SDHB у половины пациентов. Однако основные характеристики пациентов в обеих группах были сопоставимы, что позволило провести сравнительный анализ эффективности химио- и таргетной терапии и сделать вывод о эквивалентности двух видов лечения в 1 линии метастатической ФХ / ПГ.
ЗАКЛЮЧЕНИЕ
Учитывая сопоставимую эффективность обеих лекарственных опций и индолентное течение болезни, большинство пациентов не нуждаются в назначении ХТ в 1 линии. Следует принять во внимание, что при выборе терапии в первую очередь необходимо учитывать профиль безопасности препаратов. Так, таргетная терапия сунити-нибом может быть выбрана исключительно у пациентов с контролируемой артериальной гипертензией. В случаях, когда на фоне комплексной антигипертензивной терапии с включением α-адреноблокаторов не удается достичь целевых цифр артериального давления (< 140/90 мм. рт. ст.), предпочтение следует отдавать ХТ.


